جلد 22، شماره 2 - ( تابستان 1404 )
جلد 22 شماره 2 صفحات 136-123 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Rahimi Sabet Z, Ghobeh M, Khorshidfar M, Deyhim M R. Comparative Analysis of Oxidative Damage and Metabolic Parameters in Red Blood Cells Stored in CPDA1 and CPD+SAGM. bloodj 2025; 22 (2) :123-136
URL: http://bloodjournal.ir/article-1-1578-fa.html
URL: http://bloodjournal.ir/article-1-1578-fa.html
رحیمی ثابت زهرا، قبه مریم، خورشیدفر مونا، دیهیم محمدرضا. بررسی مقایسهای پارامترهای آسیب اکسیداتیو و متابولیزم فرآورده گلبول قرمز در دو محیط CPDA1 و CPD+SAGM در طول مدت ذخیرهسازی. فصلنامه پژوهشی خون. 1404; 22 (2) :123-136
استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون
متن کامل [PDF 948 kb]
(517 دریافت)
| چکیده (HTML) (1418 مشاهده)
مقدمه
امروزه تحقیقات مرتبط با فرآوردههای خونی و ارتقاء سلامت خون یکی از موضوعات اصلی تحقیق در حوزه طب انتقال خون میباشد. در این رابطه، حفظ و سلامت فرآورده گلبول قرمز به عنوان یکی از پرمصرفترین فرآوردههای خونی از اهمیت ویژهای برخوردار است (1).
هدف اولیه از تزریق گلبول قرمز، افزایش حمل اکسیژن به بافتها و اندامهایی است که به علت کم خونی، ظرفیت حمل اکسیژن توسط گلبولهای قرمز در آنها کاهش یافته است (3، 2). گلبولهای قرمز تهیه شده در مراکز انتقال خون میتوانند برای 35 الی 42 روز در دمای 2 تا 6 درجه سانتیگراد در بانکهای خون بیمارستانی نگهداری شوند (5، 4). بـا توجه به پیشرفتهایی که امروزه در حفظ و نگهداری گلبولهای قرمز رخ داده است، مانند ارتقاء کیفیت کیسههای نگهداری خون، طرز تهیه فرآورده گلبول قرمز، انتقال و توزیع آن با حفظ زنجیره سرد و همچنین چرخـه نگهـداری آن، اما کماکان گلبولهای قرمز در طـی فرآیندهـای ذکر شده به خصوص در طی دوران ذخیرهسازی، دچار یک سری تغییرات مورفولوژیک، عملکردی و بیوشیمیایی شده که میتواند سبب کاهش بقاء، کاهش عملکرد و همچنین کاهش کیفیت آن قبل از تزریق به بیماران گردد که اصطلاحاً به مجموعه این تغییرات آسیب ذخیره گلبول قرمز گفته میشود (2).
این تغییرات، شامل یکسری تغییرات متابولیزم مثل افزایش گلیکولیز و مصرف گلوکز است که موجب افزایش غلظت لاکتات بـه عنوان محصول گلیکولیز شده و می تواند سبب اسیدی شدن محیط گلبول قرمز و در نتیجه سبب کاهش pH گردد که با تغییـرات مورفولوژی گلبول قرمز ارتباط مستقیم دارد. کاهش غلظت آدنوزین تریفسفات (ATP)، کـاهش غلظت دیفسفوگلیسرات (DPG) و افزایش غلظت یون پتاسیم از دیگر تغییرات بیوشیمیایی است که در طول مدت ذخیرهسازی گلبول قرمز رخ داده و میتوانند سبب کاهش بقاء گلبولهای قرمز در طی ذخیرهسازی و افزایش بروز عوارض ناشی از تزریق خون گردد (13-7، 6، 4).
سایر تغییرات مرتبط با آسیب ذخیره گلبول قرمز، بروز آسیبهای اکسیداتیو میباشد. در طول ذخیرهسازی گلبول قرمز بـا تولید بیش از حد اکسیدانها، تعادل سیستم اکسیدان-آنتیاکسیدانی گلبول قرمز مختل شده و ظرفیت آنتیاکسیدانی گلبول قرمز دیگر توانایی مهار این شدت از اکسیدانها را ندارد. در نتیجه آن سطح اکسیدانهایی مثل رادیکالهای آزاد اکسیژن و افزایش سطح رادیکاهای هیدروکسیل در گلبول قرمز افزایش یـافته که میتوانند با صدمه به پروتئینهای غشاء، سبب تخریب غشاء گلبول قرمز گردند. این صدمات در بسیاری از مواقع بسیار جدی بوده و به صورت برگشتناپذیر میباشند که میتوانند سبب لیزگلبولهای قرمز شوند (5-3).
اگر چه تـاثیر آسیب ذخیره گلبول قرمز و جنبههای بالینی آن هنوز به طور کامل شناخته شده نیست، به همین علت در رابطه با تـأثیر آسیبهای ذخیره بر کارآیی و کیفیت گلبولهای قرمز، مطالعههای زیـادی در حال انجام میباشد.
امروزه در طی جمعآوری خون کـامل و تهیه گلبول قرمز از ماده سیترات- فسفات- دکستروز-آدنین (CPDA1) به عنوان ضد انعقاد در کیسههای نگهداری خون استفاده میشود. در مواردی هم که نیاز به استفاده از گلبولهای قرمز کم لکوسیت باشد، پس از فیلتراسیون لکوسیتها، به کیسههای نگهداری محلول سالین-آدنین-گلوکز-مانیتول (SAGM) اضافه میگردد کـه برای مصارف خاص مانند بیماران مبتلا به لوسمـی و یـا تالاسمــی به کار میرود (6).
با توجه به اهمیت آسیب ذخیره گلبول قرمز و تـاثیر مخرب آن بر کیفیت این فرآورده خونی و از طرفی معرفی تغییرات متابولیزم و آسیبهای اکسیداتیو به عنوان عوامل اصلی در بروز آسیب ذخیره گلبول قرمز، هدف مطالعه حاضر، بررسی آسیب ذخیره گلبول قرمز از طریق ارزیابی پارامترهای متابولیزم و اکسیداتیو در دو محیط CPDA1 و CPD+SAGM به صورت جداگانه در طول مدت ذخیرهسازی این فرآورده تا 42 روز در شرایط بانک خون بود.
مواد و روشها
در این مطالعه تجربی که در مرکز تحقیقات سازمان انتقال خون ایران در سال 1400 انجام شد، 10 کیسه خون حاوی گلبول قرمز متراکم که به صورت تصادفی ساده، بـدون در نظر گرفتن سن و نوع گروه خونی اهداکنندگان انتخاب شده بود مورد بررسی قرار گرفت. 5 کیسه خون حاوی CPDA1 و 5 کیسه خون نیز دارای نگهدارنده CPD+ SAGM بودند. کلیه اهداکننـدگان خون در این مطالعه مرد بودند. معیار ورود اهداکنندگان خون به مطالعه، افراد سالمی بودند که توسط معیارهایی که از طرف سازمان انتقال
خون برای انتخاب اهداکننده سالم تدوین شده است توسط پزشک اهدا انتخاب شده بودند. افرادی که دارای این شرایط نبودند از مطالعه خارج میشدند. تعداد نمونه نیز با توجه به حجم نمونه در مطالعههای مشابه تعیین شد (11).
فرآورده گلبول قرمز تهیه شده طبق دستورالعمل حمل خون و فرآوردههای خونی سازمان انتقال خون ایران با حفظ زنجیره سرد و پایش دما توسط دیتا لاگر از پایگاه انتقال خون استان تهران به آزمایشگاه مرکز تحقیقات سازمان انتقال خون آورده شد و سریعاً به یخچالهای استاندارد بـانـک خـون در دمای 2-6 درجه سانتیگراد منتقل گردیـد.
در این مطالعه، پارامترهـای متابولیزم، هماتولوژیک و آسیب اکسیداتیو گلبول قرمز در دوگروه گلبول قرمز حاوی CPDA1 و گلبـول قرمز حاوی CPD SAGM+ در طول مدت نگهداری این فرآورده به ترتیب در روزهای صفر (روز تهیـه گلبول قرمز) 2، 7، 14، 21، 28، 35 و 42 مورد ارزیابی قرار گرفت. برای ارزیابی آسیب اکسیداتیو گلبول قرمز از شاخصهـایی نظیر اندازهگیری مالون دی آلدئید (MDA) که شاخص پراکسیداسیون لیپیدی بود، اندازهگیری اکسیدانهای کل (total oxidant) و اندازهگیری آنزیمهای آنتیاکسیدان گلوتاتیون پراکسیداز (GPX) و سوپراکسیددیسموتاز (SOD) استفاده شد. برای ارزیابی وضعیت متابولیزم گلبول قرمز نیز از شاخصهای متابولیزم که شامل اندازهگیری غلظت گلوکز، انـدازهگیری غلظت لاکتات و اندازهگیری pH بود استفاده گردید. در این مطالعه، اندازهگیری فعالیت آنزیم لاکتات دهیدروژناز (LDH) و میزان همولیز گلبولهای قرمز نیز بـه عنوان شاخصهای آسیب سلولی مورد سنجش قرار گرفت. همچنین پـارامترهای هماتولوژیک گلبول قرمز که شامل اندازهگیری تعداد شمارش گلبول قرمز، میزان هماتوکریت (Hct)، غلظت هموگلوبین (Hb) و اندکسهای MCV ، MCH وMCHC بـود نیز انجام شد.
نمونـهگیری از کیسهها در شرایط کاملاً استریل در زیر هود لامینار کلاس 2 انجام شد و ارزیـابی پارامترها نیز به صورت دوتـایی انجام گرفت. مراحل کنترل کیفی، جهت اطمینان از دقت و صحت آزمایشها قبل از شروع به کار با هر دستگـــاه، بــا استفـاده از کنتـرلهـای تجـاری معتبـر
TuruLab (پارس آزمون - ایران) صورت گرفت.
الف ـ پارامترهای هماتولوژیک
شمارش گلبول قرمز و اندکسهای گلبول قرمز:
شمارش گلبولهای قرمز روشی برای ارزیابی کیفیت، تعداد و حجم گلبولهای قرمز است. شمارش تعداد گلبولهای قرمز در هر دو گروه بـا استفاده از دستگاه اتومـاتیک شمارشگر سلولهای خونی (ژاپن، 1000 Sysmex K-) انجام گردید. نمونهها به میزان 1:5 با فسفات بافر سالین (PBS) رقیق شدند و توسط دستگاه شمارشگر سلولی، تعداد گلبولهای قرمز (RBC) و شاخصهای آن که شامل غلظت هموگلوبین (Hb)، میزان هماتوکریـت (Hct)، میانگیـن حجم گلبول قرمز (MCV)، MCH و MCHC بود اندازهگیری شد.
ب ـ بررسی و ارزیابی پارامترهای متابولیزم گلبول قرمز
در این بخش ابتدا 5 میلیلیتر از فرآورده گلبول قرمز در شرایط کاملاً استریل از طریق کورد کیسه به داخل لوله آزمایش منتقل گردید، سپس نمونه در g 3700 به مدت 10 دقیقه سانتریفیوژ شد و پلاسما از گلبول قرمز جدا گردید. پلاسما جهت بررسی و ارزیابی پارامترهای متابولیزم که شامل اندازهگیری غلظت گلوکز، اندازهگیری غلظت لاکتات و اندازهگیری pH بود با استفاده از دستگاه اتوآنالایزر شیمی (ژاپن، هیتاچی 911) اندازهگیری شد.
1- اندازهگیری غلظت گلوکز:
غلظت گلوکز با استفاده از روش آنزیمی گلوکزاکسیداز )شرکت دارواش - ایران(، به صورت واکنش رنگسنجی انجام شد. جذب نوری رنگ ایجاد شده در مقابل استاندارد در طول موج 500 نـانومتر قرائت گردید که شدت آن متناسب با غلظت گلوکز در نمونه بود.
2- اندازهگیری غلظت لاکتات:
اندازهگیری غلظت لاکتات بـا استفاده از روش آنزیمی (شرکت پارس آزمون- ایران) انجام شد. در این آزمایش لاکتـات در حضور NAD در مجاورت آنزیم لاکتات دهیدروژنـاز بـه پیروات تبدیل میگردد. میزان NADH تولید شده در این واکنش با مقدار لاکتات در نمونـه رابطه مستقیم داشت.
3- اندازهگیری pH :
در این روش، ابتدا دستگاه pH متر (Metler,UK) ، بـا محلولهای استاندارد کالیبره شد و سپس pH خارج سلولی اندازهگیری گردید.
ج- بررسی شاخصهای آسیب سلولی
1- اندازهگیری فعالیت آنزیم لاکتات دهیدروژناز (LDH) :
اندازهگیری فعالیت آنزیم LDH پلاسما بر اساس تبدیل پیروات به لاکتات است کـه توسط آنزیم LDH کاتالیز میگردد (کیت شرکت پارس آزمون- ایران). در این واکنش آنزیمی که در آن + NADH به +NAD تبدیـل میشود، تغییرات جذب نوری در واحد زمان و در طول موج 340 نانومتر محاسبه گردید که متناسب با فعالیت آنزیم بود که بر اساس واحد IU/L گزارش شد.
2- بررسی شاخص همولیز در گلبولهای قرمز:
فاکتور همـولیز یکی از مهمترین پـارامترهای کنترل کیفیت در گلبولهای قرمز طی مدت ذخیرهسازی آن میباشد. در این روش میزان هموگلوبین آزاد در پلاسما ارزیابی میگردد. ابتدا 100 میکرولیتر از پلاسمای نمونهها به لوله آزمایش منتقل شده و سپس 1 میلیلیتر سدیم کربنات به تمامی لولهها اضافه گشته و میزان جذب نوری هر نمونه با استفاده از دستگاه اسپکتروفتومتر (Cecil 7200,UK) در طول موجهای 415، 450 و 700 نانومتر قرائت شد. سپس با استفاده از فرمول زیر، شاخص همولیز محاسبه گردید (12). این روش ارزیابی، طبق دستورالعمل سازمان انتقال خون ایران انجام شد.
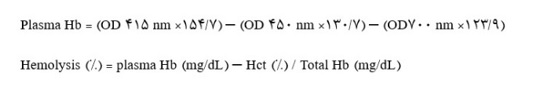
د- شاخصهای آسیب اکسیداتیو
1- اندازهگیری غلظت مالون دی دآلدئید (MDA) :
روش تیوباربیتوریک اسید یکی از روشهای استاندارد جهت اندازهگیری MDA (محصول نهایی پراکسیداسیون لیپیدها) میباشد. در این روش که بر اساس واکنش MDA با تیوباربیتوریک اسید در دمای جوش میبـاشد، جذب نوری کمپلکس ایجاد شده که به رنگ صورتی بود در طول موج 532 نانومتر توسط اسپکتروفتومترخوانده شد و بر اساس منحنی استاندارد که از قبل تهیه شده بود، غلظـــت
MDA در واحد میکرومول محاسبه گردید (13).
2- اندازهگیری غلظت اکسیدانهای تام (Total oxidant):
به منظور اندازهگیری غلظت اکسیدانها از کیت کمپانی (زلبیو - آلمان) استفاده شد. انـدازهگیری به روش رنـگسنجی و بر مبنای واکنشاکسیداسیون و احیاء میباشد. جذب نوری محصول به دست آمده در طول موج 560 نانومتر خوانده شد و بر اساس منحنی استاندارد که از قبل تهیه شده بود، غلظت اکسیدانها در واحد میلیمول محاسبه گردید.
3- انـدازهگیری فعالیت آنزیم سوپراکسید دیسموتاز (SOD):
برای انـدازهگیری فعالیت آنزیم آنتیاکسیدان SOD، از کیت کمپانی (زلبیو - آلمان) استفاده شد. در این روش از آنیون سوپراکسید برای تبدیل هیدروژن پراکسید و اکسیژن تحت شرایط آنزیماتیکی استفاده میشود. در نهایت با اضافه کردن کروموژن به محیط واکنش، کمپلکس رنگی ایجاد شده و میزان جذب نوری آن در صفر و 2 دقیقه در طول موج 420 نانومتر قرائت گردید و سپس با استفاده از فرمول زیر، فعالیت آنزیم SOD از طریق فرمول و بر اساس IU/mL محاسبه شد.

4- اندازهگیری فعالیت آنزیم گلوتاتیون پراکسیداز (GPX):
برای انـدازهگیری فعالیت آنزیم آنتیاکسیدان GPX از کیت کمپانی (زلبیو - آلمان) استفاده شد. این آنزیم گلوتـاتیون را بـه عنوان اهداکننده الکترون نهایی برای احیای سلنوسیستئین از طریق افزودن GSH استفاده میکند. گلوتاتیون پراکسیداز آن را به GSSG تبدیل کرده و GSH بـاقیمانده توسط DTNB ، کمپلکس زرد رنگی را ایجاد مینماید. فعالیت این آنزیم، بـه طور غیر مستقیم در ارتباط با تشکیل کمپلکس زرد رنگ توسط احیا DTNB میباشد. جذب نوری این کمپلکس در طول موج 412 نـانومتر قرائت شد و نهایتاً فعالیـت آنزیم از طریق فرمــول زیر بر اساس IU/mL محاسبه گردید.

هـ - آنالیز آماری:
تمامی دادههـا وارد نـرمافزار SPSS نسخـه 22 گردیـد و
قبل از شروع آزمونهای آماری روی دادهها، طبیعی بودن توزیع متغیرهای مورد تحقیق توسط آزمون شاپیرو ویلک بررسی شد. متغیرهای تحقیق، بین گروهها و نیز بین دفعات اندازهگیری مختلف توسط آنالیز واریانس با اندازههای تکراری (Repeated measure Anova) مقایسه گردید. جهت مقایسه زوجی دادهها نیز با توجه به توزیع پارامتریک یا غیر پارامتریک متغیرها در هر نوبت اندازهگیری، از آزمون آماری تی مستقل (independent paired T-test) و یـا از آزمون آماری من ویتنی (Mann-Whitney) استفاده شد و مقادیر متغیرها در هر نوبت اندازهگیری بین گروهها مقایسه گردید. مقادیر 05/0 p< از نظر آماری معنادار در نظر گرفته شد.
یافتهها
الف- پارامترهای هماتولوژیک
نتایج آنـالیز واریانس نشان میداد که تعداد گلبولهای قرمز در روزهای مختلف اندازهگیری با یکدیگر تفاوت معناداری نـداشتند. همچنین نوبت اندازهگیری و گروه با یکدیگر اثر متقابـل نداشت. یعنی تأثیر نوبت اندازهگیری (زمان) روی میزان RBC وابسته به گروهها نبوده و مستقل از آن بود. بر اساس این نتایج غلظت Hb در روزهای مختلف اندازهگیری با یکدیگر تفاوت معناداری داشت (015/0 p=). همچنین نوبـت اندازهگیری و گروه با یکدیگـر اثر متقابل نداشت یعنی تأثیر نوبت اندازهگیری (زمان) روی غلظت Hb وابسته به گروهها نبوده و مستقل از آن بود. میزان Hct نیز در روزهای مختلف اندازهگیری با یکدیگر تفاوت معناداری داشت (001/0 p=) ولی نوبت اندازهگیری و گروه با یکدیگر اثر متقابل نـداشت یعنی تأثیر نوبت اندازهگیری (زمان) روی میزان HCT وابسته به گروهها نبوده و مستقل از آن میباشد. همچنین، نتایج آزمون واریانس نشان میداد که میزان MCV در روزهای مختلف اندازهگیری با یکدیگر تفاوت معناداری داشت (001/0 p=). MCV یک روند افزایشی را در طول زمان در هر دو گروه نشان میداد و نوبت انـدازهگیری و گروه با یکدیگر اثر متقابل نداشت، یعنی تـأثیر نوبت اندازهگیری (زمان) روی میزان MCV وابسته به گروهها نبوده و مستقل از آن بود. بر اساس این نتایج، میزان MCH در روزهای مختلف اندازهگیری با یکدیگر تفاوت معناداری نداشت. همچنین نوبت اندازهگیری و گروه با یکدیگر اثر متقابل را نشان نداد، یعنی تأثیر نوبت اندازهگیری (زمان) روی میزان MCH وابسته به گروهها نبوده و مستقل از آن بود. همچنین نتایج آنـالیز واریانس نشان داد که میزان MCHC در روزهای مختلف انـدازهگیری بـا یکدیگر تفاوت معناداری داشت (001/0 p=). MCHC یـک روند کاهشی را در هر دو گروه CPDA1 و SAGM + CPD در طول زمان نشان میداد. نوبت اندازهگیری و گروه با یکدیگر اثر متقابل نـداشت. یعنی تأثیر نوبت اندازهگیری (زمان) روی میزان MCHC وابسته به گروهها نبوده و مستقل از آن بود. بـا توجه به نتایج آنالیز واریانس، میزان همـولیز گلبول قرمز در روزهای مختلف اندازهگیری بـا یکدیگر تفاوت داشت و یک روند افزایشی را نشان میداد (045/0 p=). مقایسه مقادیر همولیز در گروههای مطالعه به تفکیک هر یک از نوبتهای اندازهگیری انجام شد و بر طبق آن، نـوبت اندازهگیری و گروه با یکدیگر اثر متقابل نداشت یعنی تأثیر نوبت اندازهگیری (زمان) روی میزان همولیز وابسته به گروه نبود و مستقل از آن بود.
در مرحله بعدی آنالیز آماری، مقایسه تمامی پارامترهای هماتولوژیـک در گروههای CPDA1 و SAGM + CPD به تفکیک روزهای اندازهگیری انجام شد. به دلیل این که کلیه دادهها دارای توزیع غیر طبیعی (non-parametric) بودند بـدین منظور، از آزمون غیر پارامتریک من ویتنی استفاده شد (05/0 p<). بر طبق نتایج به دست آمده از آزمایش غیر پـارامتریـک منویتنی مشخص شد که تعداد RBC در روزهای 0، 2، 7، 14، 21، 28 و 35 نگهداری گلبول قرمز در گروه CPD+SAGM بـه مراتب کمتر از تعداد گلبولهای قرمز در گروه CPDA1 بود که این تغییرات از نظر آماری معنادار بود. نتایج نشان میداد کـه غلظت هموگلوبین در کیسههای حاوی CPD+SAGM در روزهای صفر 2، 14، 21، 28 و 42 نگهداری نسبت بـه گروه CPDA1 به مراتب افزایش کمتری را نشان میداد که این تغییرات از نظر آماری معنادار بود. میزان هماتوکریـت نیز در کیسههای حاوی CPD+SAGM در تمامی روزهای نگهداری گلبول قرمز نسبت بـه گروه CPDA1 به مراتب کمتر بود و این تغییرات نیز از نظر آماری معنادار بود (جدول 1). بر طبق نتایج به دست آمده از آنـالیز من ویتنی هیچگونه اختلاف معناداری در تغییرات میانگین MCV، MCHو MCHCدردو گروه در مقایسه دو بـه دو در روزهای مختلف نگهداری گلبول قرمز مشاهده نشد. بر طبق این نتایج با وجود این که
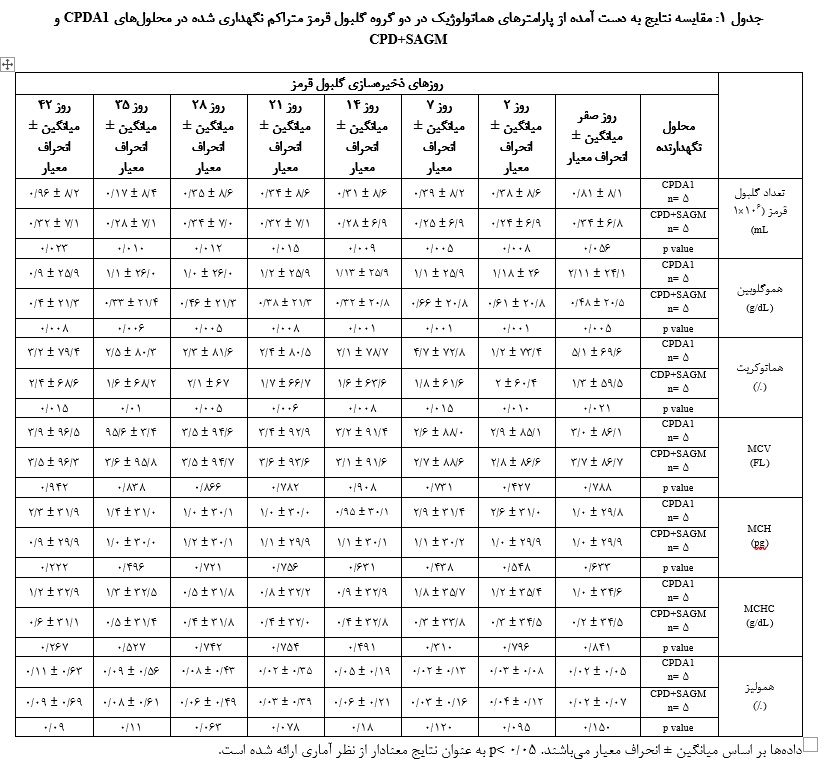
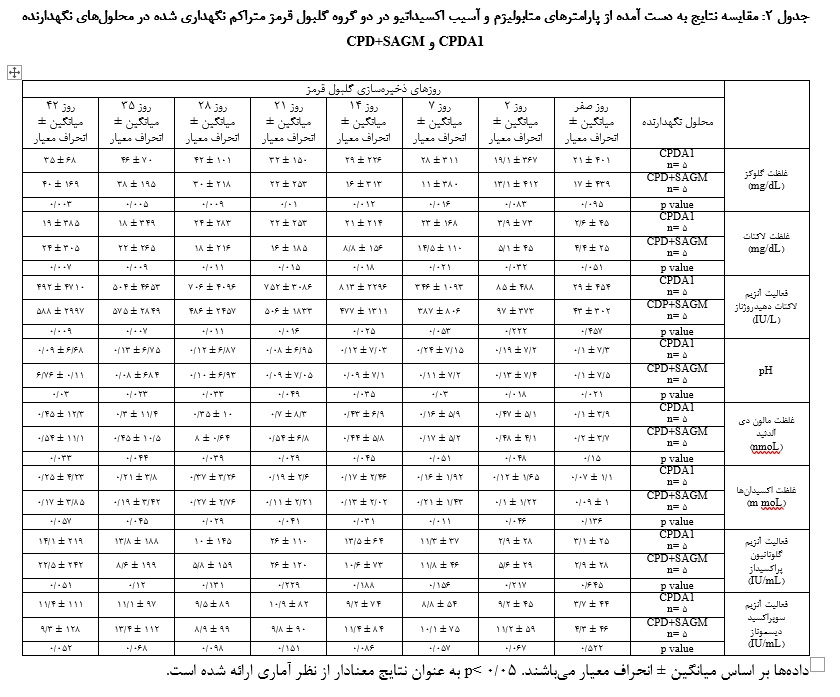
دادهها بر اساس میانگین ± انحراف معیار میباشند. 05/0 p< به عنوان نتایج معنادار از نظر آماری ارائه شده است.
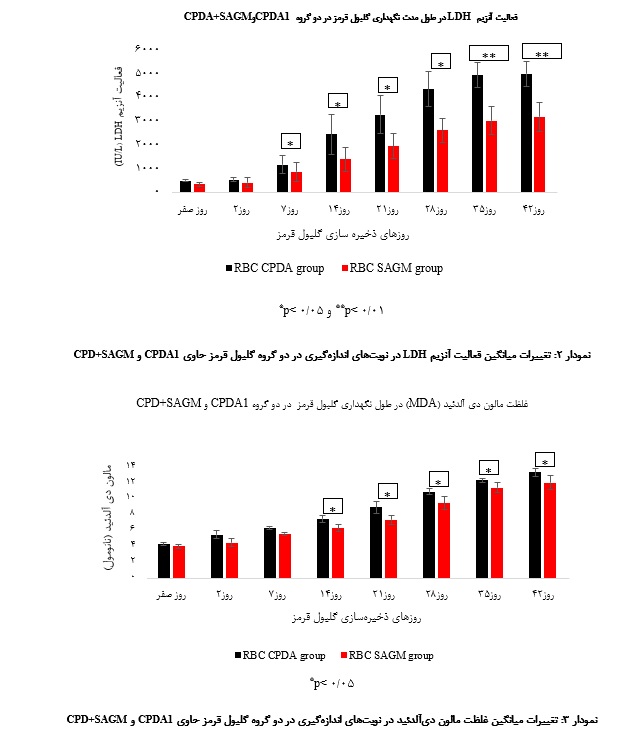
گروه CPD+SAGM بـه مـراتب افزایش کمتری را نسبت بــه گـروه CPDA1 نشان مـیداد که این تغییرات از نظر آماری معنادار بود (نمودار 3، جدول 2). از نظر میزان اکسیـدان تام در روزهای 2، 7، 14 ذخیرهسازی گلبـول قرمز، بیـن گروههـای CPDA1 و CPD+SAGM اختــلاف معناداری وجود داشت و در گروه CPD+SAGM ، غلظت اکسیدانها در روزهای ذکر شده به مراتب افزایش کمتری را نشان میداد (جدول 2). بر طبق نتایج به دست آمـده از آزمایـش پارامتریـک T-test، اگر چه در اغلب روزهای نگهداری گلبول قرمز در گروه CPD+SAGM فعالیت بیشتری از آنزیم GPX نسبت به گروه CPDA1 مشاهده میشد، ولی این اختلاف از نظر آماری معنادار نبود (جـدول 2). بر طبق این نتایج، در اغلب روزهای نـگهداری گلبول قرمز در گروه CPD+SAGM فعالیت بیشتری از آنزیم SOD نسبت بـه گروه CPDA1 مشاهده میشد ولی این اختلاف از نظر آماری معنادار نبود (جدول 2).
بحث
آسیب ذخیره گلبول قرمز میتواند باعث کاهش عملکرد، کاهش بقا و کاهش کیفیت فرآورده گلبول قرمز قبل از تزریق آن به بیماران گردد. آسیبهای اکسیداتیو و تغییرات متابولیزم گلبول قرمز که در طی ذخیرهسازی این فرآورده رخ میدهد، از دلایل اصلی آسیب ذخیره گلبول قرمز به شمار میآیند (11). آسیب اکسیداتیو، نتیجه صدماتی است که از طرف رادیکالهای آزاد اکسیژن به گلبول قرمز در طی ذخیرهسازی وارد شده و در بسیاری از مواقع این آسیبها به صورت برگشتناپذیر بوده کـه میتوانند منجر به لیز گلبولهای قرمز گردنـد (15، 14). تأثیر آسیب ذخیره در گلبولهای قرمز و جنبههای بالینی آن هنوز بـه طور کامل شناخته شده نیست و به همین علت در رابطه با تأثیر آن بر کـارآیی و کیفیت گلبولهای قرمز در شرایط in-vitro و in-vivo مطالعههای زیادی در حال انجام میباشد.
با توجه به اهمیت آسیب ذخیره گلبول قرمز و تـأثیر مخرب آن بر کیفیت این فرآورده خونی، در این مطالعه بـه بررسی و ارزیابی تغییرات اکسیداتیو و متابولیزم گلبول قرمز در دو محیط CPDA1 و CPD+SAGM در طول مدت ذخیرهسازی این فرآورده تا 42 روز پرداختیم.
یکی از متغیرهای تحقیق در این مطالعه، اندازهگیری غلظت گلوکز در کیسههای حاوی گلبول قرمز بود. گلوکز به عنوان یکی از منابع اصلی تولید آدنوزین تریفسفات (ATP) انرژی سلول را تـأمین میکند ولی منابع گلوکز محدود بوده و در طول مدت ذخیرهسازی گلبول قرمز مصرف میشود و بـه همین دلیل غلظت گلوکز کاهش یافته که میتوانـد سبب کاهش سطح ATP به عنوان منبع اصلی انرژی سلول گردد. بـدین ترتیب، عدم تعادلی که بین مصرف گلوکز و کـاهش سطح ATP در طول مدت ذخیرهسازی به وجود میآید میتواند سبب کاهش زندهمانی گلبول قرمز در طی ذخیرهسازی آن گردد (16).
بر طبق نتایج به دست آمده مشخص شد که غلظت گلوکز در طی مدت نگهداری گلبول قرمز تا 42 روز در هر دو گروه گلبول قرمز به صورت معناداری کاهش یافته و این کاهش از روز 14 به بعد با میزان بیشتری میباشد. از طرف دیگر مشاهده شد که غلظت گلوکز در گروه گلبول قرمز دارای CPD+SAGM به مراتب کاهش کمتری را نسبت به گروه CPDA1 در تمامی روزهای ذخیرهسازی داشت و بـه نظر میرسد، گلوکز به عنوان منبع انرژی سلول، در گروه CPD+SAGM بهتر حفظ شده که میتواند منجـر بـه کاهـش کمتـر ATP و در نتیجـــه زنـــدهمانی
بیشترگلبول قرمز در طی دوران ذخیرهسازی گردد.
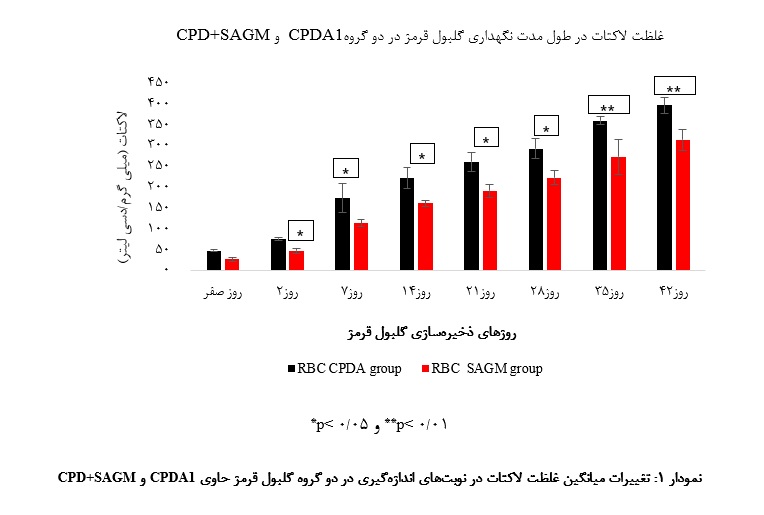
بررسی غلظت لاکتات در فرآورده گلبول قرمز، یکی دیگر از متغیرهای این مطالعه بود. گلبولهای قرمز به دلیل فقدان میتوکندری برای تـأمین انرژی وابسته به مسیر بیهوازی گلیکولیز میباشند و همزمان با مصرف گلوکز در طی فرآیند گلیکولیز، تولید لاکتات نیز بـه عنوان یکی از محصولات گلیکولیز افزایش مییابد. بر طبق نتایج به دست آمده، غلظت لاکتات در هر دو گروه گلبول قرمز افزایش یافته بود ولی در گلبولهای قرمز حاوی CPD+SAGM نسبت به گروه CPDA1 این افزایش کمتر بود. بدین ترتیب گلبولهای قرمز دارای SAGM، بـا توجه به مقدار گلوکزی که در این ترکیب بوده توانسته است ذخیره بیشتری از گلوکز را برای تأمین انرژی سلول فراهم سازد و با تأثیر خود بر گلیکولیز منجر بـه کاهش تولید لاکتات نسبت به گروه CPDA1 گردد.
بر اساس نتایج به دست آمده از این مطالعه، میزان pH ، همزمان بـا تولید لاکتات در هر دو گروه کاهش یافته بود ولی این کاهش در گروه SAGM با توجه به تولید کمتر لاکتات، نسبت به گروه CPDA1 کمتر بود و حاکی از حفظ بهتر pH در این گروه بود. همان طور که قبلاً نیز گفته شد، کاهش pH یکی از عوامل اصلی است که میتواند سبب تغییرات مورفولوژیـک و در نتیجه کاهش بقاء و زندهمانی فرآورده گلبول قرمز در طی ذخیرهسازی آن گردد (17، 5-3). این رونـد تغییرات متابولیزم در هر دو گروه گلبول قرمز بـا نتایج مطالعه امیدخـدا ، ماخاراجی و قاجار همخوانی داشت (19، 18، 5). بر اساس نتایج مطالعهای که انگوئن و همکارانش در سال 2024 انجـام دادند، به این نکته اشاره داشتند که SAGM با حفظ فشار اسمزی و ممانعت از کاهش بیش از حد ATP و pH در طول مدت نگهداری گلبول قرمز میتواند آسیب ذخیره گلبول قرمز را تـا حد زیادی کاهش داده و سبب زندهمانی بیشتر سلول و در نتیجـه حفظ کیفیت فرآورده گلبول قرمز در طول مدت ذخیرهسازی آن گردد (17). نتایج مطالعه حاضر نیز حاکی از این بود که تغییرات متابولیکی که میتواند منجر به آسیب ذخیره گلبول قرمز گردد در گروه SAGM نسبت به CPDA1 کمتر بود.
یکی دیگر از متغیرهای تحقیق، فعالیت آنزیم LDH بود که در این مطالعه به آن پرداخته شد. بر اساس نتایج به دست آمده فعالیت آنزیم LDH در طی ذخیرهسازی گلبول قرمز در هر دو گروه دارای CPDA1 و CPD+SAGM یک روند افزایشی را نشان میداد ولی این روند در گروه SAGM بـه مراتـب کمتر از CPDA1 بود. افزایش فعالیت آنزیم LDH در گلبولهای قرمز یکی از شاخصهای مهم در ارزیـابی آسیب غشاء سلول میباشد (20، 12). در مطالعههای زیـادی نشان داده شده که با افزایش زمان ذخیرهسازی گلبول قرمز، فعالیت آنزیم LDH به صورت چشمگیری افزایش مییـابد، در دو مطالعه جداگانه که توسط مرجانی و قزلباش نیز انجام شده به این مسأله اشاره کردهاند (20، 12). در مطالعهای که توسط ورما بر روی 30 اهداکننده انجام شد، پارامترهای بیوشیمیایی گلبول قرمز مورد پایش قرار گرفت. نتیجه این مطالعه حاکی از این بود که، گلبولهای قرمز در طی مدت ذخیرهسازی ممکن است تحت همـولیز خود به خودی قرار گیرند و خواص بیوشیمیایی و مکانیکی آنها تغییر کند. نتایج این تحقیق همچنین نشان میداد کـه تغییرات قابل توجهی در میزان فسفر، پروتئین، pH و سطوح فعالیت آنزیم LDH و آنزیم آسپارتـات آمینو ترانسفراز (SGOT) ایجاد میگردد (7). شاستری و همکاران در سال 2019 در مطالعهای دیگر به بررسی تغییرات بیوشیمیایی و متابولیکی گلبولهای قرمز در طی دوران ذخیرهسازی پرداختند و بر طبق نتایج بـه دست آمده مشخص شد که غلظت پتاسیم و فعالیت آنزیم LDH از هفته اول ذخیرهسازی به شدت افزایش یافته و این افزایش در گلبولهای قرمز دارای SAGM بـه مراتـب کمتر از CPDA1 بود. به گفته این محققین یکی از دلائل آن میتوانـد بسته بـه میزان مانیتولی باشد که در ترکیب SAGM وجود دارد و این خود میتواند سبب حفظ و پایداری بیشتر غشاء سلول گردد (6). بنابراین، بـا توجه به نتایج به دست آمده از مطالعه حاضر به نظر میرسد که غشاء گلبولهای قرمز دارای SAGM نسبت به گروه CPDA1 دچار آسیب کمتری در طول زمان ذخیرهسازی بوده و SAGM توانسته است سبب حفـظ و پایـداری بیشتـر غشـا و همچنیـــن حفظ بیشتر
متابولیزم در این فرآورده خونی شده باشد.
در این مطالعه، همچنین به بررسی میزان اکسیدانها و پراکسیداسیون لیپیدی که یکی از شاخصههای مهم آسیب اکسیداتیو سلولی است پرداخته شد. بر اساس نتایج به دست آمده، میزان اکسیدانها و پراکسیداسیون لیپیدی در هر دو گروه گلبول قرمز، رونـد افزایشی را در طول مدت ذخیرهسازی نشان میداد، این روند از روز 14 به بعد تا روز 42 بیشتر بود. این نتایج همچنین نشان میداد که غلظت اکسیدانها و غلظت MDA (شاخص پراکسیداسیون لیپیدی) در گروه CPD+SAGM نسبت به CPDA1 از افزایش کمتری برخوردار بوده است. همچنین، مقایسه زوجی دادهها از روز 14 نگهداری بـه بعد اختلاف معناداری بین میانگین MDA در دو گروه را نشان میداد. نتایج مطالعههای زیادی حاکی از تولید اکسیدانها و پراکسیداسیون لیپیدی در طول مدت ذخیرهسازی گلبول قرمز میباشد که این امر سبب افزایش استرس و آسیب اکسیداتیو و همچنین افزایش شکنندگی اسمزی در گلبولهای قرمز شده و منجر بـه لیز سلولها میگردد (21-25، 9، 2).
در تحقیقی که توسط ون ویجک و همکارانش در سال 2019 انجام شد، شکنندگی اسمزی گلبولهای قرمزحاوی CPDA2 مورد بررسی قرار گرفـت و مشخص شد که گلبولهای قرمز غشاء خود را به مرور زمان در طی ذخیرهسازی از دست داده و شکننده میشوند. بخش عمده این افزایش شکنندگی مربوط به تجمع و خروج لاکتات از درون گلبول قرمز است و افزایش لاکتات در شکنندگی اسمزی گلبول قرمز تأثیر زیادی را خواهد داشت. نتیجه این پژوهش نشان میداد کـه هرچه به روزهای آخر ذخیرهسازی گلبولهای قرمز نزدیکتر میشویم، شکنندگی و تغییر شکل و عدم قابلیت زنـده بودن گلبولهای قرمز بیشتر خواهد شد (10).
با توجه به نتایج بـه دست آمده به نظر میرسد که گلبولهای قرمز دارای SAGM با حفظ متابولیزم و حفظ ظرفیت آنتیاکسیدانی، آسیب کمتری به غشاء گلبول قرمز وارد شده و پایداری غشاء در مقابل آسیبهای اکسیداتیو بیشتر میباشد و در نتیجه تغییرات متابولیزم و اکسیداتیوی که میتوانند سبب بروز آسیب ذخیره گلبول قرمز گردند در گلبولهای قرمز حـاوی SAGM به مراتب کمتر از گلبولهای قرمز حاوی CPDA1 است.
نتیجهگیری
یافتههای این مطالعه نشان میداد که SAGM توانسته است با کاهش تغییرات متابولیکی و اکسیداتیو سبب کاهش آسیب ذخیره گلبول قرمز گردد که میتواند منجر بـه بهبود عملکرد و افزایش بقاء گلبول قرمز در طی دوران ذخیرهسـازی ایـن فـرآورده شـود کـه البتــه نیاز به انجام
مطالعههای تکمیلی در سطوح In vitro و In vivo میباشد.
حمایت مالی
مطالعه فوق بدون حمایت مالی ارگان و نهاد خـاصی انجام شده است.
عدم تعارض منافع
نویسندگان اظهار میکنند هیچگونه تعارض منافعی در این مطالعه وجود نداشته است.
نقش نویسندگان
زهرا رحیمـی ثـابت: همکاری در طراحی اولیه پروژه، همکاری در جمعآوری و بررسی مقالات مرتبط با پروژه، راهاندازی و انجام آزمایشهای تحقیق، همکاری در جمعآوری دادههای تحقیق، همچنین در نگارش نسخه اولیه مقاله شرکت داشته است.
دکتر مریم قبه: به عنوان استاد مشاور در تفسیر نتایج پروژه و در نگارش و ویرایش مقاله شرکت داشته است.
دکتر موناخورشیدفر: به عنوان مشاور علمی و همکاری در آمادهسازی نسخه نهایی مقاله شرکت داشته است.
دکتر محمدرضا دیهیم: به عنوان استاد راهنما، شرکت در انتخاب موضوع تحقیق و طراحی اولیه پروژه، همکاری در راهاندازی آزمایشهای تحقیق و نظارت بر انجام صحیح آنها، نظارت بر تفسیر دقیق نتایج و تجزیه و تحلیل دادهها، همکاری در نگارش مقاله و همچنین نظارت بر ویرایش نسخه نهایی مقاله شرکت داشته است.
تشکر و قدردانی
این پروژه بخشی از پایاننامه کارشناسی ارشد می باشد که در تاریخ 20/10/1399 در شورای پژوهشی دانشگاه آزاد اسلامی به تصویب رسیده است. از معاونت آموزشی و پژوهشی مؤسسه آموزش عالی طب انتقال خون و همکاران محترم در پـایگاه انتقال خون استان تهران که همکاری لازم را جهت اجرای این پـروژه داشتهاند و هم چنین از همکاران شاغل در آزمایشگاههای بیوشیمی، هماتولوژی و مرکز نوآوری سازمان انتقال خون نهایت تشکر و قدردانی به عمل میآید.
متن کامل: (294 مشاهده)
بررسی مقایسهای پارامترهای آسیب اکسیداتیو و متابولیزم فرآورده گلبول قرمز در دو محیط CPDA1 و CPD+SAGM در طول مدت ذخیرهسازی
زهرا رحیمی ثابت1، مریم قبه2 ، مونا خورشیدفر3 ، محمدرضا دیهیم4
1- کارشناس ارشد بیوشیمی ـ دانشکده علوم پایه دانشگاه آزاد اسلامی واحد علوم و تحقیقات ـ تهران ـ ایران
2- PhD تخصصی بیوشیمی ـ استادیار گروه زیستشناسی ـ دانشکده علوم پایه دانشگاه آزاد اسلامی واحد علوم و تحقیقات ـ تهران ـ ایران
3- PhD تخصصی هماتولوژی و بانک خون آزمایشگاهی ـ مرکز تحقیقات قلب و ریه دانشکده پزشکی بریتیش کلمبیا ـ ونکوور ـ کانادا
4- PhD تخصصی بیوشیمی بالینی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
1- کارشناس ارشد بیوشیمی ـ دانشکده علوم پایه دانشگاه آزاد اسلامی واحد علوم و تحقیقات ـ تهران ـ ایران
2- PhD تخصصی بیوشیمی ـ استادیار گروه زیستشناسی ـ دانشکده علوم پایه دانشگاه آزاد اسلامی واحد علوم و تحقیقات ـ تهران ـ ایران
3- PhD تخصصی هماتولوژی و بانک خون آزمایشگاهی ـ مرکز تحقیقات قلب و ریه دانشکده پزشکی بریتیش کلمبیا ـ ونکوور ـ کانادا
4- PhD تخصصی بیوشیمی بالینی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
https://doi.org/10.18502/avr.v34i2.18052 Citation: Rahimi Sabet Z, Ghobeh M, Khorshidfar M, Deyhim M.R. Comparative Analysis of Oxidative Damage and Metabolic Parameters in Red Blood Cells Stored in CPDA1 and CPD+SAGM. J Iran Blood Transfuse. 2025: 22 (2): 123-136 نویسنده مسئول: محمدرضا دیهیم. استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون، تهران ـ ایران صندوق پستی: 1157-14665 E-mail: m.deyhim@tmi.ac.ir |
چکیده سابقه و هدف گلبولهای قرمز در طول مدت نگهداری دچار یکسری تغییرات مورفولوژیک و عملکردی شده که میتواند سبب کاهش بقا و کاهش عملکرد آن گردد که اصطلاحاً به آسیب ذخیره گلبول قرمز معروف میباشد. آسیبهای اکسیداتیو و تغییرات متابولیکی گلبول قرمز در طی نگهداری از دلایل اصلی این آسیبها میباشند. در این تحقیق به بررسی آسیب ذخیره گلبول قرمز با استفاده از پارامترهای آسیب اکسیداتیو و متابولیزم در دو گروه گلبول قرمز حاوی CPDA1و گلبول قرمز حاوی CPD+SAGM پرداخته شد. مواد و روشها در این مطالعه تجربی که در سال 1400 در مرکز تحقیقات سازمان انتقال خون انجام گردید، 5 فرآورده گلبول قرمز دارای CPDA1 و 5 فرآورده دیگر حاوی CPD+SAGM ، به صورت تصادفی ساده انتخاب شد و به ارزیابی پارامترهای آسیب اکسیداتیو و متابولیزم تا 42 روز نگهداری در فواصل زمانی روزهای صفر، 2، 7، 14، 21، 28، 35 و 42 پرداخته شد. در هر بار نمونهبرداری، انـدازهگیری پارامترها به صورت 2 بار تکرار انجام گردید. برای مقایسه متغیرها در هر نوبـت اندازهگیری بین گروهها از آزمونهای آماری تی- مستقل و من ویتنی و برای ارزیابی روند تغییرات داخل گروهی از آزمون واریانس دو طرفه با اندازهگیری تکراری استفاده شد. یافتهها فعالیت آنزیم لاکتات دهیدروژناز (LDH) و غلظت لاکتات در گروه CPD+SAGM بـه مراتب افزایش کمتری را نسبت به گروه CPDA1 نشان داد (05/0 p<). همچنین غلظت گلوکز و میزان pH نیز در گروه CPD+SAGM نسبت به گروه CPDA1 کاهش کمتری را نشان می داد (05/0 p<). در مقایسه دو به دو گروهها ، غلظت مالون دیآلـدئید (MDA) و غلظت توتال اکسیدان در روزهای مختلف نگهداری گلبول قرمز به خصوص از روز هفتم به بعد در گروه CPD+SAGM نسبت به گروه CPDA1 افزایش کمتری را نشان داد (05/0 p<). نتیجه گیری به نظر میرسد که SAGM توانسته بود با حفظ متابولیزم و کاهش آسیب اکسیداتیو سبب کاهش آسیب ذخیره گلبول قرمز نسبت به گروه CPDA1 شود که میتواند منجر به حفظ بهتر بقا و ارتقاء کیفیت این فرآورده در طول مدت ذخیرهسازی گردد. البتـه نیـاز بـه انجام مطالعههای تکمیلی بیشتری در سطوح In vitro و In vivo میباشد. کلمات کلیدی: گلبولهای قرمز، بانک خون، آسیب اکسیداتیو |
مقدمه
امروزه تحقیقات مرتبط با فرآوردههای خونی و ارتقاء سلامت خون یکی از موضوعات اصلی تحقیق در حوزه طب انتقال خون میباشد. در این رابطه، حفظ و سلامت فرآورده گلبول قرمز به عنوان یکی از پرمصرفترین فرآوردههای خونی از اهمیت ویژهای برخوردار است (1).
هدف اولیه از تزریق گلبول قرمز، افزایش حمل اکسیژن به بافتها و اندامهایی است که به علت کم خونی، ظرفیت حمل اکسیژن توسط گلبولهای قرمز در آنها کاهش یافته است (3، 2). گلبولهای قرمز تهیه شده در مراکز انتقال خون میتوانند برای 35 الی 42 روز در دمای 2 تا 6 درجه سانتیگراد در بانکهای خون بیمارستانی نگهداری شوند (5، 4). بـا توجه به پیشرفتهایی که امروزه در حفظ و نگهداری گلبولهای قرمز رخ داده است، مانند ارتقاء کیفیت کیسههای نگهداری خون، طرز تهیه فرآورده گلبول قرمز، انتقال و توزیع آن با حفظ زنجیره سرد و همچنین چرخـه نگهـداری آن، اما کماکان گلبولهای قرمز در طـی فرآیندهـای ذکر شده به خصوص در طی دوران ذخیرهسازی، دچار یک سری تغییرات مورفولوژیک، عملکردی و بیوشیمیایی شده که میتواند سبب کاهش بقاء، کاهش عملکرد و همچنین کاهش کیفیت آن قبل از تزریق به بیماران گردد که اصطلاحاً به مجموعه این تغییرات آسیب ذخیره گلبول قرمز گفته میشود (2).
این تغییرات، شامل یکسری تغییرات متابولیزم مثل افزایش گلیکولیز و مصرف گلوکز است که موجب افزایش غلظت لاکتات بـه عنوان محصول گلیکولیز شده و می تواند سبب اسیدی شدن محیط گلبول قرمز و در نتیجه سبب کاهش pH گردد که با تغییـرات مورفولوژی گلبول قرمز ارتباط مستقیم دارد. کاهش غلظت آدنوزین تریفسفات (ATP)، کـاهش غلظت دیفسفوگلیسرات (DPG) و افزایش غلظت یون پتاسیم از دیگر تغییرات بیوشیمیایی است که در طول مدت ذخیرهسازی گلبول قرمز رخ داده و میتوانند سبب کاهش بقاء گلبولهای قرمز در طی ذخیرهسازی و افزایش بروز عوارض ناشی از تزریق خون گردد (13-7، 6، 4).
سایر تغییرات مرتبط با آسیب ذخیره گلبول قرمز، بروز آسیبهای اکسیداتیو میباشد. در طول ذخیرهسازی گلبول قرمز بـا تولید بیش از حد اکسیدانها، تعادل سیستم اکسیدان-آنتیاکسیدانی گلبول قرمز مختل شده و ظرفیت آنتیاکسیدانی گلبول قرمز دیگر توانایی مهار این شدت از اکسیدانها را ندارد. در نتیجه آن سطح اکسیدانهایی مثل رادیکالهای آزاد اکسیژن و افزایش سطح رادیکاهای هیدروکسیل در گلبول قرمز افزایش یـافته که میتوانند با صدمه به پروتئینهای غشاء، سبب تخریب غشاء گلبول قرمز گردند. این صدمات در بسیاری از مواقع بسیار جدی بوده و به صورت برگشتناپذیر میباشند که میتوانند سبب لیزگلبولهای قرمز شوند (5-3).
اگر چه تـاثیر آسیب ذخیره گلبول قرمز و جنبههای بالینی آن هنوز به طور کامل شناخته شده نیست، به همین علت در رابطه با تـأثیر آسیبهای ذخیره بر کارآیی و کیفیت گلبولهای قرمز، مطالعههای زیـادی در حال انجام میباشد.
امروزه در طی جمعآوری خون کـامل و تهیه گلبول قرمز از ماده سیترات- فسفات- دکستروز-آدنین (CPDA1) به عنوان ضد انعقاد در کیسههای نگهداری خون استفاده میشود. در مواردی هم که نیاز به استفاده از گلبولهای قرمز کم لکوسیت باشد، پس از فیلتراسیون لکوسیتها، به کیسههای نگهداری محلول سالین-آدنین-گلوکز-مانیتول (SAGM) اضافه میگردد کـه برای مصارف خاص مانند بیماران مبتلا به لوسمـی و یـا تالاسمــی به کار میرود (6).
با توجه به اهمیت آسیب ذخیره گلبول قرمز و تـاثیر مخرب آن بر کیفیت این فرآورده خونی و از طرفی معرفی تغییرات متابولیزم و آسیبهای اکسیداتیو به عنوان عوامل اصلی در بروز آسیب ذخیره گلبول قرمز، هدف مطالعه حاضر، بررسی آسیب ذخیره گلبول قرمز از طریق ارزیابی پارامترهای متابولیزم و اکسیداتیو در دو محیط CPDA1 و CPD+SAGM به صورت جداگانه در طول مدت ذخیرهسازی این فرآورده تا 42 روز در شرایط بانک خون بود.
مواد و روشها
در این مطالعه تجربی که در مرکز تحقیقات سازمان انتقال خون ایران در سال 1400 انجام شد، 10 کیسه خون حاوی گلبول قرمز متراکم که به صورت تصادفی ساده، بـدون در نظر گرفتن سن و نوع گروه خونی اهداکنندگان انتخاب شده بود مورد بررسی قرار گرفت. 5 کیسه خون حاوی CPDA1 و 5 کیسه خون نیز دارای نگهدارنده CPD+ SAGM بودند. کلیه اهداکننـدگان خون در این مطالعه مرد بودند. معیار ورود اهداکنندگان خون به مطالعه، افراد سالمی بودند که توسط معیارهایی که از طرف سازمان انتقال
خون برای انتخاب اهداکننده سالم تدوین شده است توسط پزشک اهدا انتخاب شده بودند. افرادی که دارای این شرایط نبودند از مطالعه خارج میشدند. تعداد نمونه نیز با توجه به حجم نمونه در مطالعههای مشابه تعیین شد (11).
فرآورده گلبول قرمز تهیه شده طبق دستورالعمل حمل خون و فرآوردههای خونی سازمان انتقال خون ایران با حفظ زنجیره سرد و پایش دما توسط دیتا لاگر از پایگاه انتقال خون استان تهران به آزمایشگاه مرکز تحقیقات سازمان انتقال خون آورده شد و سریعاً به یخچالهای استاندارد بـانـک خـون در دمای 2-6 درجه سانتیگراد منتقل گردیـد.
در این مطالعه، پارامترهـای متابولیزم، هماتولوژیک و آسیب اکسیداتیو گلبول قرمز در دوگروه گلبول قرمز حاوی CPDA1 و گلبـول قرمز حاوی CPD SAGM+ در طول مدت نگهداری این فرآورده به ترتیب در روزهای صفر (روز تهیـه گلبول قرمز) 2، 7، 14، 21، 28، 35 و 42 مورد ارزیابی قرار گرفت. برای ارزیابی آسیب اکسیداتیو گلبول قرمز از شاخصهـایی نظیر اندازهگیری مالون دی آلدئید (MDA) که شاخص پراکسیداسیون لیپیدی بود، اندازهگیری اکسیدانهای کل (total oxidant) و اندازهگیری آنزیمهای آنتیاکسیدان گلوتاتیون پراکسیداز (GPX) و سوپراکسیددیسموتاز (SOD) استفاده شد. برای ارزیابی وضعیت متابولیزم گلبول قرمز نیز از شاخصهای متابولیزم که شامل اندازهگیری غلظت گلوکز، انـدازهگیری غلظت لاکتات و اندازهگیری pH بود استفاده گردید. در این مطالعه، اندازهگیری فعالیت آنزیم لاکتات دهیدروژناز (LDH) و میزان همولیز گلبولهای قرمز نیز بـه عنوان شاخصهای آسیب سلولی مورد سنجش قرار گرفت. همچنین پـارامترهای هماتولوژیک گلبول قرمز که شامل اندازهگیری تعداد شمارش گلبول قرمز، میزان هماتوکریت (Hct)، غلظت هموگلوبین (Hb) و اندکسهای MCV ، MCH وMCHC بـود نیز انجام شد.
نمونـهگیری از کیسهها در شرایط کاملاً استریل در زیر هود لامینار کلاس 2 انجام شد و ارزیـابی پارامترها نیز به صورت دوتـایی انجام گرفت. مراحل کنترل کیفی، جهت اطمینان از دقت و صحت آزمایشها قبل از شروع به کار با هر دستگـــاه، بــا استفـاده از کنتـرلهـای تجـاری معتبـر
TuruLab (پارس آزمون - ایران) صورت گرفت.
الف ـ پارامترهای هماتولوژیک
شمارش گلبول قرمز و اندکسهای گلبول قرمز:
شمارش گلبولهای قرمز روشی برای ارزیابی کیفیت، تعداد و حجم گلبولهای قرمز است. شمارش تعداد گلبولهای قرمز در هر دو گروه بـا استفاده از دستگاه اتومـاتیک شمارشگر سلولهای خونی (ژاپن، 1000 Sysmex K-) انجام گردید. نمونهها به میزان 1:5 با فسفات بافر سالین (PBS) رقیق شدند و توسط دستگاه شمارشگر سلولی، تعداد گلبولهای قرمز (RBC) و شاخصهای آن که شامل غلظت هموگلوبین (Hb)، میزان هماتوکریـت (Hct)، میانگیـن حجم گلبول قرمز (MCV)، MCH و MCHC بود اندازهگیری شد.
ب ـ بررسی و ارزیابی پارامترهای متابولیزم گلبول قرمز
در این بخش ابتدا 5 میلیلیتر از فرآورده گلبول قرمز در شرایط کاملاً استریل از طریق کورد کیسه به داخل لوله آزمایش منتقل گردید، سپس نمونه در g 3700 به مدت 10 دقیقه سانتریفیوژ شد و پلاسما از گلبول قرمز جدا گردید. پلاسما جهت بررسی و ارزیابی پارامترهای متابولیزم که شامل اندازهگیری غلظت گلوکز، اندازهگیری غلظت لاکتات و اندازهگیری pH بود با استفاده از دستگاه اتوآنالایزر شیمی (ژاپن، هیتاچی 911) اندازهگیری شد.
1- اندازهگیری غلظت گلوکز:
غلظت گلوکز با استفاده از روش آنزیمی گلوکزاکسیداز )شرکت دارواش - ایران(، به صورت واکنش رنگسنجی انجام شد. جذب نوری رنگ ایجاد شده در مقابل استاندارد در طول موج 500 نـانومتر قرائت گردید که شدت آن متناسب با غلظت گلوکز در نمونه بود.
2- اندازهگیری غلظت لاکتات:
اندازهگیری غلظت لاکتات بـا استفاده از روش آنزیمی (شرکت پارس آزمون- ایران) انجام شد. در این آزمایش لاکتـات در حضور NAD در مجاورت آنزیم لاکتات دهیدروژنـاز بـه پیروات تبدیل میگردد. میزان NADH تولید شده در این واکنش با مقدار لاکتات در نمونـه رابطه مستقیم داشت.
3- اندازهگیری pH :
در این روش، ابتدا دستگاه pH متر (Metler,UK) ، بـا محلولهای استاندارد کالیبره شد و سپس pH خارج سلولی اندازهگیری گردید.
ج- بررسی شاخصهای آسیب سلولی
1- اندازهگیری فعالیت آنزیم لاکتات دهیدروژناز (LDH) :
اندازهگیری فعالیت آنزیم LDH پلاسما بر اساس تبدیل پیروات به لاکتات است کـه توسط آنزیم LDH کاتالیز میگردد (کیت شرکت پارس آزمون- ایران). در این واکنش آنزیمی که در آن + NADH به +NAD تبدیـل میشود، تغییرات جذب نوری در واحد زمان و در طول موج 340 نانومتر محاسبه گردید که متناسب با فعالیت آنزیم بود که بر اساس واحد IU/L گزارش شد.
2- بررسی شاخص همولیز در گلبولهای قرمز:
فاکتور همـولیز یکی از مهمترین پـارامترهای کنترل کیفیت در گلبولهای قرمز طی مدت ذخیرهسازی آن میباشد. در این روش میزان هموگلوبین آزاد در پلاسما ارزیابی میگردد. ابتدا 100 میکرولیتر از پلاسمای نمونهها به لوله آزمایش منتقل شده و سپس 1 میلیلیتر سدیم کربنات به تمامی لولهها اضافه گشته و میزان جذب نوری هر نمونه با استفاده از دستگاه اسپکتروفتومتر (Cecil 7200,UK) در طول موجهای 415، 450 و 700 نانومتر قرائت شد. سپس با استفاده از فرمول زیر، شاخص همولیز محاسبه گردید (12). این روش ارزیابی، طبق دستورالعمل سازمان انتقال خون ایران انجام شد.
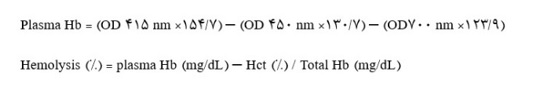
د- شاخصهای آسیب اکسیداتیو
1- اندازهگیری غلظت مالون دی دآلدئید (MDA) :
روش تیوباربیتوریک اسید یکی از روشهای استاندارد جهت اندازهگیری MDA (محصول نهایی پراکسیداسیون لیپیدها) میباشد. در این روش که بر اساس واکنش MDA با تیوباربیتوریک اسید در دمای جوش میبـاشد، جذب نوری کمپلکس ایجاد شده که به رنگ صورتی بود در طول موج 532 نانومتر توسط اسپکتروفتومترخوانده شد و بر اساس منحنی استاندارد که از قبل تهیه شده بود، غلظـــت
MDA در واحد میکرومول محاسبه گردید (13).
2- اندازهگیری غلظت اکسیدانهای تام (Total oxidant):
به منظور اندازهگیری غلظت اکسیدانها از کیت کمپانی (زلبیو - آلمان) استفاده شد. انـدازهگیری به روش رنـگسنجی و بر مبنای واکنشاکسیداسیون و احیاء میباشد. جذب نوری محصول به دست آمده در طول موج 560 نانومتر خوانده شد و بر اساس منحنی استاندارد که از قبل تهیه شده بود، غلظت اکسیدانها در واحد میلیمول محاسبه گردید.
3- انـدازهگیری فعالیت آنزیم سوپراکسید دیسموتاز (SOD):
برای انـدازهگیری فعالیت آنزیم آنتیاکسیدان SOD، از کیت کمپانی (زلبیو - آلمان) استفاده شد. در این روش از آنیون سوپراکسید برای تبدیل هیدروژن پراکسید و اکسیژن تحت شرایط آنزیماتیکی استفاده میشود. در نهایت با اضافه کردن کروموژن به محیط واکنش، کمپلکس رنگی ایجاد شده و میزان جذب نوری آن در صفر و 2 دقیقه در طول موج 420 نانومتر قرائت گردید و سپس با استفاده از فرمول زیر، فعالیت آنزیم SOD از طریق فرمول و بر اساس IU/mL محاسبه شد.

4- اندازهگیری فعالیت آنزیم گلوتاتیون پراکسیداز (GPX):
برای انـدازهگیری فعالیت آنزیم آنتیاکسیدان GPX از کیت کمپانی (زلبیو - آلمان) استفاده شد. این آنزیم گلوتـاتیون را بـه عنوان اهداکننده الکترون نهایی برای احیای سلنوسیستئین از طریق افزودن GSH استفاده میکند. گلوتاتیون پراکسیداز آن را به GSSG تبدیل کرده و GSH بـاقیمانده توسط DTNB ، کمپلکس زرد رنگی را ایجاد مینماید. فعالیت این آنزیم، بـه طور غیر مستقیم در ارتباط با تشکیل کمپلکس زرد رنگ توسط احیا DTNB میباشد. جذب نوری این کمپلکس در طول موج 412 نـانومتر قرائت شد و نهایتاً فعالیـت آنزیم از طریق فرمــول زیر بر اساس IU/mL محاسبه گردید.

هـ - آنالیز آماری:
تمامی دادههـا وارد نـرمافزار SPSS نسخـه 22 گردیـد و
قبل از شروع آزمونهای آماری روی دادهها، طبیعی بودن توزیع متغیرهای مورد تحقیق توسط آزمون شاپیرو ویلک بررسی شد. متغیرهای تحقیق، بین گروهها و نیز بین دفعات اندازهگیری مختلف توسط آنالیز واریانس با اندازههای تکراری (Repeated measure Anova) مقایسه گردید. جهت مقایسه زوجی دادهها نیز با توجه به توزیع پارامتریک یا غیر پارامتریک متغیرها در هر نوبت اندازهگیری، از آزمون آماری تی مستقل (independent paired T-test) و یـا از آزمون آماری من ویتنی (Mann-Whitney) استفاده شد و مقادیر متغیرها در هر نوبت اندازهگیری بین گروهها مقایسه گردید. مقادیر 05/0 p< از نظر آماری معنادار در نظر گرفته شد.
یافتهها
الف- پارامترهای هماتولوژیک
نتایج آنـالیز واریانس نشان میداد که تعداد گلبولهای قرمز در روزهای مختلف اندازهگیری با یکدیگر تفاوت معناداری نـداشتند. همچنین نوبت اندازهگیری و گروه با یکدیگر اثر متقابـل نداشت. یعنی تأثیر نوبت اندازهگیری (زمان) روی میزان RBC وابسته به گروهها نبوده و مستقل از آن بود. بر اساس این نتایج غلظت Hb در روزهای مختلف اندازهگیری با یکدیگر تفاوت معناداری داشت (015/0 p=). همچنین نوبـت اندازهگیری و گروه با یکدیگـر اثر متقابل نداشت یعنی تأثیر نوبت اندازهگیری (زمان) روی غلظت Hb وابسته به گروهها نبوده و مستقل از آن بود. میزان Hct نیز در روزهای مختلف اندازهگیری با یکدیگر تفاوت معناداری داشت (001/0 p=) ولی نوبت اندازهگیری و گروه با یکدیگر اثر متقابل نـداشت یعنی تأثیر نوبت اندازهگیری (زمان) روی میزان HCT وابسته به گروهها نبوده و مستقل از آن میباشد. همچنین، نتایج آزمون واریانس نشان میداد که میزان MCV در روزهای مختلف اندازهگیری با یکدیگر تفاوت معناداری داشت (001/0 p=). MCV یک روند افزایشی را در طول زمان در هر دو گروه نشان میداد و نوبت انـدازهگیری و گروه با یکدیگر اثر متقابل نداشت، یعنی تـأثیر نوبت اندازهگیری (زمان) روی میزان MCV وابسته به گروهها نبوده و مستقل از آن بود. بر اساس این نتایج، میزان MCH در روزهای مختلف اندازهگیری با یکدیگر تفاوت معناداری نداشت. همچنین نوبت اندازهگیری و گروه با یکدیگر اثر متقابل را نشان نداد، یعنی تأثیر نوبت اندازهگیری (زمان) روی میزان MCH وابسته به گروهها نبوده و مستقل از آن بود. همچنین نتایج آنـالیز واریانس نشان داد که میزان MCHC در روزهای مختلف انـدازهگیری بـا یکدیگر تفاوت معناداری داشت (001/0 p=). MCHC یـک روند کاهشی را در هر دو گروه CPDA1 و SAGM + CPD در طول زمان نشان میداد. نوبت اندازهگیری و گروه با یکدیگر اثر متقابل نـداشت. یعنی تأثیر نوبت اندازهگیری (زمان) روی میزان MCHC وابسته به گروهها نبوده و مستقل از آن بود. بـا توجه به نتایج آنالیز واریانس، میزان همـولیز گلبول قرمز در روزهای مختلف اندازهگیری بـا یکدیگر تفاوت داشت و یک روند افزایشی را نشان میداد (045/0 p=). مقایسه مقادیر همولیز در گروههای مطالعه به تفکیک هر یک از نوبتهای اندازهگیری انجام شد و بر طبق آن، نـوبت اندازهگیری و گروه با یکدیگر اثر متقابل نداشت یعنی تأثیر نوبت اندازهگیری (زمان) روی میزان همولیز وابسته به گروه نبود و مستقل از آن بود.
در مرحله بعدی آنالیز آماری، مقایسه تمامی پارامترهای هماتولوژیـک در گروههای CPDA1 و SAGM + CPD به تفکیک روزهای اندازهگیری انجام شد. به دلیل این که کلیه دادهها دارای توزیع غیر طبیعی (non-parametric) بودند بـدین منظور، از آزمون غیر پارامتریک من ویتنی استفاده شد (05/0 p<). بر طبق نتایج به دست آمده از آزمایش غیر پـارامتریـک منویتنی مشخص شد که تعداد RBC در روزهای 0، 2، 7، 14، 21، 28 و 35 نگهداری گلبول قرمز در گروه CPD+SAGM بـه مراتب کمتر از تعداد گلبولهای قرمز در گروه CPDA1 بود که این تغییرات از نظر آماری معنادار بود. نتایج نشان میداد کـه غلظت هموگلوبین در کیسههای حاوی CPD+SAGM در روزهای صفر 2، 14، 21، 28 و 42 نگهداری نسبت بـه گروه CPDA1 به مراتب افزایش کمتری را نشان میداد که این تغییرات از نظر آماری معنادار بود. میزان هماتوکریـت نیز در کیسههای حاوی CPD+SAGM در تمامی روزهای نگهداری گلبول قرمز نسبت بـه گروه CPDA1 به مراتب کمتر بود و این تغییرات نیز از نظر آماری معنادار بود (جدول 1). بر طبق نتایج به دست آمده از آنـالیز من ویتنی هیچگونه اختلاف معناداری در تغییرات میانگین MCV، MCHو MCHCدردو گروه در مقایسه دو بـه دو در روزهای مختلف نگهداری گلبول قرمز مشاهده نشد. بر طبق این نتایج با وجود این که

میزان همولیز در روزهای 2، 7، 28 و 42 نگهداری گلبول قرمز در گروه SAGM+CPD افزایش کمتـری را نسبت به گـروه CPDA1 نشان میداد ولی این تغییرات از نظر آماری معنادار نبود (جدول 1).
ب ـ پارامترهای متابولیزم
بر طبق نتایج بـه دست آمده از آنالیز واریانس، غلظت گلوکز در روزهای مختلف اندازهگیری با یکدیگر تفاوت معنادارداشت (05/0 p<). همچنین نوبت اندازهگیری و گروه بـا یکدیگر اثر متقابل را نشان داد (02/0 p=) یعنی تأثیر نوبت اندازهگیری (زمان) روی غلظت گلوکز وابسته به گروهها بود. میانگین غلظت گلوکز بـا گذشت زمان از روز اول تا روز 42 به طور متوالی در هر دو گروه +SAGM CPD وCPDA1 کاهش یافته بود ولی این کاهش در گروه CPDA1 بـه مراتب بیشتر از گروه + SAGM CPD بود. بر طبق ایـن نتایج، غلظت لاکتات در روزهای مختلف اندازهگیری بـا یکدیگر تفاوت معنادار را نشان داد (001/0 p<). همچنین نوبت اندازهگیری و گروه با یکدیگر اثر متقابل داشت (001/0 p=)، یعنی تـأثیر نوبت اندازهگیری (زمان) روی میزان لاکتات وابسته بـه گروه بود. با توجه به نتایج به دست آمده، به طور کلی گروه CPDA1 در مقایسه با گـروه CPD+SAGM ، از افزایش لاکتات بیشتری برخوردار بود. بر طبق این نتایج، میزان pH در روزهای مختلف اندازهگیری بـا یکدیگر تفاوت معناداری داشت (001/0 p<)(نمودار 1). بـا گذشت زمان، میزان pH در هر دو گروه CPDA1 و CPD+SAGM کاهش یـافت و به طور کلی میزان pH درگروه CPD+SAGM در مقایسه با گروهCPDA1 اندکی بیشتر بود. مقایسه مقادیر pH در گروههای مطالعه بـه تفکیک هر یک از نوبتهای انـدازهگیری انجام شد و بر طبق آن، نوبت انـدازهگیری و گروه با یکدیگر اثر متقابل داشت (011/0 p=)، یعنی تأثیر نوبت اندازهگیری (زمان) روی میزان pH وابسته به گروه بود. میزان فعالیت آنزیم LDH در روزهای مختلف انـدازهگیری با یکدیگر تفاوت معنادار را نشان می داد (001/0 p<). در هر دو گروه میانگین LDH بـا گذشت زمان افزایش یافت و در همه روزهای اندازهگیری، میانگین فعالیت LDH در گروه +SAGM CPD افزایش کمتری را نسبت به گروه CPDA1 نشان میداد. همچنین نوبـت انـدازهگیری و گروه با یکدیگر اثر متقابل داشت (002/0 p=)، یعنی تأثیر نوبت اندازهگیری (زمان) روی میزان فعالیت آنزیم LDH وابسته به گروه بوده و مستقل از آن نبود. مقایسه تمامی پـارامترهای متابولیزم در دو گروه به تفکیک روزهای اندازهگیری انجام شد و به دلیل این کـه کلیه دادهها بـا توجه به آنالیز شاپیرو، دارای توزیع غیر طبیعی (non-parametric) بودنـد، از آزمون غیر پارامتریک منویتنی استفاده شد، به جز گلوکز که دارای توزیع طبیعی (parametric) بود و از آزمون پارامتریک T-test استفاده شد.
نتایج مقایسه زوجی که با استفاده از T-test به دست آمد، نشان داد که میانگین غلظت گلوکز در روزهای 7، 21، 14، 28، 35 و 42 اختلاف معناداری را بین دو گروه نشان میداد و میانگین غلظت گلوکز در گروه CPDA1 بـه مراتب نسبت به گروه CPD+SAGM کمتر بود (جدول 2).
بر طبق همین نتایج، مشخص شد که غلظت لاکتات نیز در روزهای 0، 2، 7، 14، 21، 28، 35 و 42 در گروه CPD+SAGM به مراتب افزایش کمتری را نسبت گروه CPDA1 نشان داد کـه این تغییرات از نظر آماری معنادار بود (05/0 p<).
میزان pH نیز بـه دنبال افزایش لاکتات، در روزهای 2، 7، 14، 28 و 42 در گروه CPDA1 نسبت به CPD+SAGM به مراتب کاهش بیشتری را نشان میداد، این تغییرات از نظر آماری معنادار بود (05/0 p<).
بر طبق نتایج به دست آمده از آزمـایش غیر پارامتریک من ویتنی مشخص شد کـه میزان فعالیت آنزیم LDH در روزهای 2، 21، 28، 35 و 42 در گروه CPD+SAGM بـه مراتب افزایش کمتری را نسبت بـه گروه CPDA1 نشان مـیداد کـه ایـن تغییـرات نیـز از نظـر آماری معنادار بود
(05/0 p<)(نمودار 2)(جدول 2).
ج ـ پارامترهای آسیب اکسیداتیو
نتایـج به دست آمده از آنالیز واریانس نشان مـیداد کـه نوبتهای مختلف اندازهگیری از لحاظ غلظت MDA با یکدیگر تفاوت معناداری داشتند (001/0 p=). یعنی با افزایش زمان نگهداری گلبول قرمز، در هر دو گروه غلظت MDA افزایش یـافته بود، ولی بین نوبت اندازهگیری و گروه اثر متقابـل وجود نداشت، یعنی تأثیر نوبت انـدازهگیری (زمان) روی میزان MDA وابسته به گروهها نبوده و مستقل از آن بود. در ارتباط با غلظت اکسیدانها هم بـه همین ترتیب، نوبـتهای مختلف اندازهگیری از لحاظ میزان اکسیدانها با یکدیگر تفاوت معناداری داشت (001/0 p=)، یعنی بـا افزایش زمان نگهداری گلبول قرمز، در هر دو گروه غلظت اکسیدانها افزایش یافته بود، اما بین نوبت اندازهگیری و گروه اثر متقابل وجود نـداشت یعنی تأثیر نوبت انـدازهگیری (زمان) روی میزان اکسیدانها وابسته به گروهها نبوده و مستقل از آن بود. نتایج به دست آمده از آنـالیز واریانس نشان میدادکه نوبتهای مختلف انـدازهگیری از لحاظ فعالیت آنزیم GPX با یکدیگر تفاوت معناداری دارنـد (001/0 p=). یعنی بـا افزایش زمان نگهداری گلبول قرمز، در هر دو گروه فعالیت آنزیم افزایش یـافته بود. همچنین نتایج نشان میداد که بین نوبت انـدازهگیری و گروه اثر متقابل وجود نداشت یعنی تأثیر نوبت اندازهگیری (زمان) روی فعالیت آنزیم وابسته بـه گروهها نبوده و مستقل از آن بود. همچنین، نوبـتهای مختلف اندازهگیری از لحاظ فعالیت آنزیم SOD بـا یکدیگر تفاوت معناداری را نشان میداد (001/0 p=). یعنی بـا افزایش زمان نگهداری گلبول قرمز، در هر دو گروه فعالیت آنزیم افزایش یـافته بود ولی بین نوبت اندازهگیری و گروه اثر متقابل وجود نداشت، یعنی تـأثیر نوبت اندازهگیری (زمان) روی فعالیت آنزیم وابسته به گروهها نبوده و مستقل از آن بود.
در مقایسه زوجی دادهها به تفکیک روزهای اندازهگیری، با توجه به توزیع دادهها، برای MDA و SOD از آزمایش غیر پارامتریک منویتنی و برای مقایسه اکسیدان تام و GPX از آزمون T-test استفاده شد. بر طبق نتایج به دست آمده از آزمایش غیرپارامتریک منویتنی مشخص شد که غلظـت MDA در روزهــای 7، 14، 21، 28، 35 و 42 در
ب ـ پارامترهای متابولیزم
بر طبق نتایج بـه دست آمده از آنالیز واریانس، غلظت گلوکز در روزهای مختلف اندازهگیری با یکدیگر تفاوت معنادارداشت (05/0 p<). همچنین نوبت اندازهگیری و گروه بـا یکدیگر اثر متقابل را نشان داد (02/0 p=) یعنی تأثیر نوبت اندازهگیری (زمان) روی غلظت گلوکز وابسته به گروهها بود. میانگین غلظت گلوکز بـا گذشت زمان از روز اول تا روز 42 به طور متوالی در هر دو گروه +SAGM CPD وCPDA1 کاهش یافته بود ولی این کاهش در گروه CPDA1 بـه مراتب بیشتر از گروه + SAGM CPD بود. بر طبق ایـن نتایج، غلظت لاکتات در روزهای مختلف اندازهگیری بـا یکدیگر تفاوت معنادار را نشان داد (001/0 p<). همچنین نوبت اندازهگیری و گروه با یکدیگر اثر متقابل داشت (001/0 p=)، یعنی تـأثیر نوبت اندازهگیری (زمان) روی میزان لاکتات وابسته بـه گروه بود. با توجه به نتایج به دست آمده، به طور کلی گروه CPDA1 در مقایسه با گـروه CPD+SAGM ، از افزایش لاکتات بیشتری برخوردار بود. بر طبق این نتایج، میزان pH در روزهای مختلف اندازهگیری بـا یکدیگر تفاوت معناداری داشت (001/0 p<)(نمودار 1). بـا گذشت زمان، میزان pH در هر دو گروه CPDA1 و CPD+SAGM کاهش یـافت و به طور کلی میزان pH درگروه CPD+SAGM در مقایسه با گروهCPDA1 اندکی بیشتر بود. مقایسه مقادیر pH در گروههای مطالعه بـه تفکیک هر یک از نوبتهای انـدازهگیری انجام شد و بر طبق آن، نوبت انـدازهگیری و گروه با یکدیگر اثر متقابل داشت (011/0 p=)، یعنی تأثیر نوبت اندازهگیری (زمان) روی میزان pH وابسته به گروه بود. میزان فعالیت آنزیم LDH در روزهای مختلف انـدازهگیری با یکدیگر تفاوت معنادار را نشان می داد (001/0 p<). در هر دو گروه میانگین LDH بـا گذشت زمان افزایش یافت و در همه روزهای اندازهگیری، میانگین فعالیت LDH در گروه +SAGM CPD افزایش کمتری را نسبت به گروه CPDA1 نشان میداد. همچنین نوبـت انـدازهگیری و گروه با یکدیگر اثر متقابل داشت (002/0 p=)، یعنی تأثیر نوبت اندازهگیری (زمان) روی میزان فعالیت آنزیم LDH وابسته به گروه بوده و مستقل از آن نبود. مقایسه تمامی پـارامترهای متابولیزم در دو گروه به تفکیک روزهای اندازهگیری انجام شد و به دلیل این کـه کلیه دادهها بـا توجه به آنالیز شاپیرو، دارای توزیع غیر طبیعی (non-parametric) بودنـد، از آزمون غیر پارامتریک منویتنی استفاده شد، به جز گلوکز که دارای توزیع طبیعی (parametric) بود و از آزمون پارامتریک T-test استفاده شد.
نتایج مقایسه زوجی که با استفاده از T-test به دست آمد، نشان داد که میانگین غلظت گلوکز در روزهای 7، 21، 14، 28، 35 و 42 اختلاف معناداری را بین دو گروه نشان میداد و میانگین غلظت گلوکز در گروه CPDA1 بـه مراتب نسبت به گروه CPD+SAGM کمتر بود (جدول 2).
بر طبق همین نتایج، مشخص شد که غلظت لاکتات نیز در روزهای 0، 2، 7، 14، 21، 28، 35 و 42 در گروه CPD+SAGM به مراتب افزایش کمتری را نسبت گروه CPDA1 نشان داد کـه این تغییرات از نظر آماری معنادار بود (05/0 p<).
میزان pH نیز بـه دنبال افزایش لاکتات، در روزهای 2، 7، 14، 28 و 42 در گروه CPDA1 نسبت به CPD+SAGM به مراتب کاهش بیشتری را نشان میداد، این تغییرات از نظر آماری معنادار بود (05/0 p<).
بر طبق نتایج به دست آمده از آزمـایش غیر پارامتریک من ویتنی مشخص شد کـه میزان فعالیت آنزیم LDH در روزهای 2، 21، 28، 35 و 42 در گروه CPD+SAGM بـه مراتب افزایش کمتری را نسبت بـه گروه CPDA1 نشان مـیداد کـه ایـن تغییـرات نیـز از نظـر آماری معنادار بود
(05/0 p<)(نمودار 2)(جدول 2).
ج ـ پارامترهای آسیب اکسیداتیو
نتایـج به دست آمده از آنالیز واریانس نشان مـیداد کـه نوبتهای مختلف اندازهگیری از لحاظ غلظت MDA با یکدیگر تفاوت معناداری داشتند (001/0 p=). یعنی با افزایش زمان نگهداری گلبول قرمز، در هر دو گروه غلظت MDA افزایش یـافته بود، ولی بین نوبت اندازهگیری و گروه اثر متقابـل وجود نداشت، یعنی تأثیر نوبت انـدازهگیری (زمان) روی میزان MDA وابسته به گروهها نبوده و مستقل از آن بود. در ارتباط با غلظت اکسیدانها هم بـه همین ترتیب، نوبـتهای مختلف اندازهگیری از لحاظ میزان اکسیدانها با یکدیگر تفاوت معناداری داشت (001/0 p=)، یعنی بـا افزایش زمان نگهداری گلبول قرمز، در هر دو گروه غلظت اکسیدانها افزایش یافته بود، اما بین نوبت اندازهگیری و گروه اثر متقابل وجود نـداشت یعنی تأثیر نوبت انـدازهگیری (زمان) روی میزان اکسیدانها وابسته به گروهها نبوده و مستقل از آن بود. نتایج به دست آمده از آنـالیز واریانس نشان میدادکه نوبتهای مختلف انـدازهگیری از لحاظ فعالیت آنزیم GPX با یکدیگر تفاوت معناداری دارنـد (001/0 p=). یعنی بـا افزایش زمان نگهداری گلبول قرمز، در هر دو گروه فعالیت آنزیم افزایش یـافته بود. همچنین نتایج نشان میداد که بین نوبت انـدازهگیری و گروه اثر متقابل وجود نداشت یعنی تأثیر نوبت اندازهگیری (زمان) روی فعالیت آنزیم وابسته بـه گروهها نبوده و مستقل از آن بود. همچنین، نوبـتهای مختلف اندازهگیری از لحاظ فعالیت آنزیم SOD بـا یکدیگر تفاوت معناداری را نشان میداد (001/0 p=). یعنی بـا افزایش زمان نگهداری گلبول قرمز، در هر دو گروه فعالیت آنزیم افزایش یـافته بود ولی بین نوبت اندازهگیری و گروه اثر متقابل وجود نداشت، یعنی تـأثیر نوبت اندازهگیری (زمان) روی فعالیت آنزیم وابسته به گروهها نبوده و مستقل از آن بود.
در مقایسه زوجی دادهها به تفکیک روزهای اندازهگیری، با توجه به توزیع دادهها، برای MDA و SOD از آزمایش غیر پارامتریک منویتنی و برای مقایسه اکسیدان تام و GPX از آزمون T-test استفاده شد. بر طبق نتایج به دست آمده از آزمایش غیرپارامتریک منویتنی مشخص شد که غلظـت MDA در روزهــای 7، 14، 21، 28، 35 و 42 در

دادهها بر اساس میانگین ± انحراف معیار میباشند. 05/0 p< به عنوان نتایج معنادار از نظر آماری ارائه شده است.


بحث
آسیب ذخیره گلبول قرمز میتواند باعث کاهش عملکرد، کاهش بقا و کاهش کیفیت فرآورده گلبول قرمز قبل از تزریق آن به بیماران گردد. آسیبهای اکسیداتیو و تغییرات متابولیزم گلبول قرمز که در طی ذخیرهسازی این فرآورده رخ میدهد، از دلایل اصلی آسیب ذخیره گلبول قرمز به شمار میآیند (11). آسیب اکسیداتیو، نتیجه صدماتی است که از طرف رادیکالهای آزاد اکسیژن به گلبول قرمز در طی ذخیرهسازی وارد شده و در بسیاری از مواقع این آسیبها به صورت برگشتناپذیر بوده کـه میتوانند منجر به لیز گلبولهای قرمز گردنـد (15، 14). تأثیر آسیب ذخیره در گلبولهای قرمز و جنبههای بالینی آن هنوز بـه طور کامل شناخته شده نیست و به همین علت در رابطه با تأثیر آن بر کـارآیی و کیفیت گلبولهای قرمز در شرایط in-vitro و in-vivo مطالعههای زیادی در حال انجام میباشد.
با توجه به اهمیت آسیب ذخیره گلبول قرمز و تـأثیر مخرب آن بر کیفیت این فرآورده خونی، در این مطالعه بـه بررسی و ارزیابی تغییرات اکسیداتیو و متابولیزم گلبول قرمز در دو محیط CPDA1 و CPD+SAGM در طول مدت ذخیرهسازی این فرآورده تا 42 روز پرداختیم.
یکی از متغیرهای تحقیق در این مطالعه، اندازهگیری غلظت گلوکز در کیسههای حاوی گلبول قرمز بود. گلوکز به عنوان یکی از منابع اصلی تولید آدنوزین تریفسفات (ATP) انرژی سلول را تـأمین میکند ولی منابع گلوکز محدود بوده و در طول مدت ذخیرهسازی گلبول قرمز مصرف میشود و بـه همین دلیل غلظت گلوکز کاهش یافته که میتوانـد سبب کاهش سطح ATP به عنوان منبع اصلی انرژی سلول گردد. بـدین ترتیب، عدم تعادلی که بین مصرف گلوکز و کـاهش سطح ATP در طول مدت ذخیرهسازی به وجود میآید میتواند سبب کاهش زندهمانی گلبول قرمز در طی ذخیرهسازی آن گردد (16).
بر طبق نتایج به دست آمده مشخص شد که غلظت گلوکز در طی مدت نگهداری گلبول قرمز تا 42 روز در هر دو گروه گلبول قرمز به صورت معناداری کاهش یافته و این کاهش از روز 14 به بعد با میزان بیشتری میباشد. از طرف دیگر مشاهده شد که غلظت گلوکز در گروه گلبول قرمز دارای CPD+SAGM به مراتب کاهش کمتری را نسبت به گروه CPDA1 در تمامی روزهای ذخیرهسازی داشت و بـه نظر میرسد، گلوکز به عنوان منبع انرژی سلول، در گروه CPD+SAGM بهتر حفظ شده که میتواند منجـر بـه کاهـش کمتـر ATP و در نتیجـــه زنـــدهمانی
بیشترگلبول قرمز در طی دوران ذخیرهسازی گردد.
بررسی غلظت لاکتات در فرآورده گلبول قرمز، یکی دیگر از متغیرهای این مطالعه بود. گلبولهای قرمز به دلیل فقدان میتوکندری برای تـأمین انرژی وابسته به مسیر بیهوازی گلیکولیز میباشند و همزمان با مصرف گلوکز در طی فرآیند گلیکولیز، تولید لاکتات نیز بـه عنوان یکی از محصولات گلیکولیز افزایش مییابد. بر طبق نتایج به دست آمده، غلظت لاکتات در هر دو گروه گلبول قرمز افزایش یافته بود ولی در گلبولهای قرمز حاوی CPD+SAGM نسبت به گروه CPDA1 این افزایش کمتر بود. بدین ترتیب گلبولهای قرمز دارای SAGM، بـا توجه به مقدار گلوکزی که در این ترکیب بوده توانسته است ذخیره بیشتری از گلوکز را برای تأمین انرژی سلول فراهم سازد و با تأثیر خود بر گلیکولیز منجر بـه کاهش تولید لاکتات نسبت به گروه CPDA1 گردد.
بر اساس نتایج به دست آمده از این مطالعه، میزان pH ، همزمان بـا تولید لاکتات در هر دو گروه کاهش یافته بود ولی این کاهش در گروه SAGM با توجه به تولید کمتر لاکتات، نسبت به گروه CPDA1 کمتر بود و حاکی از حفظ بهتر pH در این گروه بود. همان طور که قبلاً نیز گفته شد، کاهش pH یکی از عوامل اصلی است که میتواند سبب تغییرات مورفولوژیـک و در نتیجه کاهش بقاء و زندهمانی فرآورده گلبول قرمز در طی ذخیرهسازی آن گردد (17، 5-3). این رونـد تغییرات متابولیزم در هر دو گروه گلبول قرمز بـا نتایج مطالعه امیدخـدا ، ماخاراجی و قاجار همخوانی داشت (19، 18، 5). بر اساس نتایج مطالعهای که انگوئن و همکارانش در سال 2024 انجـام دادند، به این نکته اشاره داشتند که SAGM با حفظ فشار اسمزی و ممانعت از کاهش بیش از حد ATP و pH در طول مدت نگهداری گلبول قرمز میتواند آسیب ذخیره گلبول قرمز را تـا حد زیادی کاهش داده و سبب زندهمانی بیشتر سلول و در نتیجـه حفظ کیفیت فرآورده گلبول قرمز در طول مدت ذخیرهسازی آن گردد (17). نتایج مطالعه حاضر نیز حاکی از این بود که تغییرات متابولیکی که میتواند منجر به آسیب ذخیره گلبول قرمز گردد در گروه SAGM نسبت به CPDA1 کمتر بود.
یکی دیگر از متغیرهای تحقیق، فعالیت آنزیم LDH بود که در این مطالعه به آن پرداخته شد. بر اساس نتایج به دست آمده فعالیت آنزیم LDH در طی ذخیرهسازی گلبول قرمز در هر دو گروه دارای CPDA1 و CPD+SAGM یک روند افزایشی را نشان میداد ولی این روند در گروه SAGM بـه مراتـب کمتر از CPDA1 بود. افزایش فعالیت آنزیم LDH در گلبولهای قرمز یکی از شاخصهای مهم در ارزیـابی آسیب غشاء سلول میباشد (20، 12). در مطالعههای زیـادی نشان داده شده که با افزایش زمان ذخیرهسازی گلبول قرمز، فعالیت آنزیم LDH به صورت چشمگیری افزایش مییـابد، در دو مطالعه جداگانه که توسط مرجانی و قزلباش نیز انجام شده به این مسأله اشاره کردهاند (20، 12). در مطالعهای که توسط ورما بر روی 30 اهداکننده انجام شد، پارامترهای بیوشیمیایی گلبول قرمز مورد پایش قرار گرفت. نتیجه این مطالعه حاکی از این بود که، گلبولهای قرمز در طی مدت ذخیرهسازی ممکن است تحت همـولیز خود به خودی قرار گیرند و خواص بیوشیمیایی و مکانیکی آنها تغییر کند. نتایج این تحقیق همچنین نشان میداد کـه تغییرات قابل توجهی در میزان فسفر، پروتئین، pH و سطوح فعالیت آنزیم LDH و آنزیم آسپارتـات آمینو ترانسفراز (SGOT) ایجاد میگردد (7). شاستری و همکاران در سال 2019 در مطالعهای دیگر به بررسی تغییرات بیوشیمیایی و متابولیکی گلبولهای قرمز در طی دوران ذخیرهسازی پرداختند و بر طبق نتایج بـه دست آمده مشخص شد که غلظت پتاسیم و فعالیت آنزیم LDH از هفته اول ذخیرهسازی به شدت افزایش یافته و این افزایش در گلبولهای قرمز دارای SAGM بـه مراتـب کمتر از CPDA1 بود. به گفته این محققین یکی از دلائل آن میتوانـد بسته بـه میزان مانیتولی باشد که در ترکیب SAGM وجود دارد و این خود میتواند سبب حفظ و پایداری بیشتر غشاء سلول گردد (6). بنابراین، بـا توجه به نتایج به دست آمده از مطالعه حاضر به نظر میرسد که غشاء گلبولهای قرمز دارای SAGM نسبت به گروه CPDA1 دچار آسیب کمتری در طول زمان ذخیرهسازی بوده و SAGM توانسته است سبب حفـظ و پایـداری بیشتـر غشـا و همچنیـــن حفظ بیشتر
متابولیزم در این فرآورده خونی شده باشد.
در این مطالعه، همچنین به بررسی میزان اکسیدانها و پراکسیداسیون لیپیدی که یکی از شاخصههای مهم آسیب اکسیداتیو سلولی است پرداخته شد. بر اساس نتایج به دست آمده، میزان اکسیدانها و پراکسیداسیون لیپیدی در هر دو گروه گلبول قرمز، رونـد افزایشی را در طول مدت ذخیرهسازی نشان میداد، این روند از روز 14 به بعد تا روز 42 بیشتر بود. این نتایج همچنین نشان میداد که غلظت اکسیدانها و غلظت MDA (شاخص پراکسیداسیون لیپیدی) در گروه CPD+SAGM نسبت به CPDA1 از افزایش کمتری برخوردار بوده است. همچنین، مقایسه زوجی دادهها از روز 14 نگهداری بـه بعد اختلاف معناداری بین میانگین MDA در دو گروه را نشان میداد. نتایج مطالعههای زیادی حاکی از تولید اکسیدانها و پراکسیداسیون لیپیدی در طول مدت ذخیرهسازی گلبول قرمز میباشد که این امر سبب افزایش استرس و آسیب اکسیداتیو و همچنین افزایش شکنندگی اسمزی در گلبولهای قرمز شده و منجر بـه لیز سلولها میگردد (21-25، 9، 2).
در تحقیقی که توسط ون ویجک و همکارانش در سال 2019 انجام شد، شکنندگی اسمزی گلبولهای قرمزحاوی CPDA2 مورد بررسی قرار گرفـت و مشخص شد که گلبولهای قرمز غشاء خود را به مرور زمان در طی ذخیرهسازی از دست داده و شکننده میشوند. بخش عمده این افزایش شکنندگی مربوط به تجمع و خروج لاکتات از درون گلبول قرمز است و افزایش لاکتات در شکنندگی اسمزی گلبول قرمز تأثیر زیادی را خواهد داشت. نتیجه این پژوهش نشان میداد کـه هرچه به روزهای آخر ذخیرهسازی گلبولهای قرمز نزدیکتر میشویم، شکنندگی و تغییر شکل و عدم قابلیت زنـده بودن گلبولهای قرمز بیشتر خواهد شد (10).
با توجه به نتایج بـه دست آمده به نظر میرسد که گلبولهای قرمز دارای SAGM با حفظ متابولیزم و حفظ ظرفیت آنتیاکسیدانی، آسیب کمتری به غشاء گلبول قرمز وارد شده و پایداری غشاء در مقابل آسیبهای اکسیداتیو بیشتر میباشد و در نتیجه تغییرات متابولیزم و اکسیداتیوی که میتوانند سبب بروز آسیب ذخیره گلبول قرمز گردند در گلبولهای قرمز حـاوی SAGM به مراتب کمتر از گلبولهای قرمز حاوی CPDA1 است.
نتیجهگیری
یافتههای این مطالعه نشان میداد که SAGM توانسته است با کاهش تغییرات متابولیکی و اکسیداتیو سبب کاهش آسیب ذخیره گلبول قرمز گردد که میتواند منجر بـه بهبود عملکرد و افزایش بقاء گلبول قرمز در طی دوران ذخیرهسـازی ایـن فـرآورده شـود کـه البتــه نیاز به انجام
مطالعههای تکمیلی در سطوح In vitro و In vivo میباشد.
حمایت مالی
مطالعه فوق بدون حمایت مالی ارگان و نهاد خـاصی انجام شده است.
عدم تعارض منافع
نویسندگان اظهار میکنند هیچگونه تعارض منافعی در این مطالعه وجود نداشته است.
نقش نویسندگان
زهرا رحیمـی ثـابت: همکاری در طراحی اولیه پروژه، همکاری در جمعآوری و بررسی مقالات مرتبط با پروژه، راهاندازی و انجام آزمایشهای تحقیق، همکاری در جمعآوری دادههای تحقیق، همچنین در نگارش نسخه اولیه مقاله شرکت داشته است.
دکتر مریم قبه: به عنوان استاد مشاور در تفسیر نتایج پروژه و در نگارش و ویرایش مقاله شرکت داشته است.
دکتر موناخورشیدفر: به عنوان مشاور علمی و همکاری در آمادهسازی نسخه نهایی مقاله شرکت داشته است.
دکتر محمدرضا دیهیم: به عنوان استاد راهنما، شرکت در انتخاب موضوع تحقیق و طراحی اولیه پروژه، همکاری در راهاندازی آزمایشهای تحقیق و نظارت بر انجام صحیح آنها، نظارت بر تفسیر دقیق نتایج و تجزیه و تحلیل دادهها، همکاری در نگارش مقاله و همچنین نظارت بر ویرایش نسخه نهایی مقاله شرکت داشته است.
تشکر و قدردانی
این پروژه بخشی از پایاننامه کارشناسی ارشد می باشد که در تاریخ 20/10/1399 در شورای پژوهشی دانشگاه آزاد اسلامی به تصویب رسیده است. از معاونت آموزشی و پژوهشی مؤسسه آموزش عالی طب انتقال خون و همکاران محترم در پـایگاه انتقال خون استان تهران که همکاری لازم را جهت اجرای این پـروژه داشتهاند و هم چنین از همکاران شاغل در آزمایشگاههای بیوشیمی، هماتولوژی و مرکز نوآوری سازمان انتقال خون نهایت تشکر و قدردانی به عمل میآید.
فهرست منابع
1. Tinmouth A, Chin-Yee I. The clinical consequences of the red cell storage lesion. Transfus Med Rev 2001; 15(2): 91-107.
https://doi.org/10.1053/tm.2001.22613 [DOI:10.1053/tmrv.2001.22613]
2. Chaudhary R, Katharia R. Oxidative injury as contributory factor for red cells storage lesion during twenty eight days of storage. Blood Transfus 2012; 10(1): 59-62
3. Olechnowicz J, Tinkov A, Skalny A, Suliburska J. Zinc status is associated with inflammation, oxidative stress, lipid, and glucose metabolism. J Physiol Sci 2018; 68(1): 19-31. [DOI:10.1007/s12576-017-0571-7] [PMID] []
4. Hashemi Tayer A, Amirizadeh N, Mghsodlu M, Nikogoftar M, Deyhim MR, Ahmadinejad M. Evaluation of Blood Storage Lesions in Leuko-depleted Red Blood Cell Units. Iran J Ped Hematol Oncol 2017; 7 (3):171-9. [Article in Farsi]
5. Jahanshahi Ghajar S, Deyhim MR, Sotoudehnejad Nematollahi F, Rafiei MH. Red blood cells storage lesion: the effect of blood donation time on biochemical parameters. Sci J Iran Blood Transfus Organ 2019; 16 (3): 161-71. [ Article in Farsi]
6. Shastry S, Shivhare A, Murugesan M, Baliga PB. Red cell storage lesion and the effect of buffy-coat reduction on the biochemical parameters. Transfus Apher Sci 2019; 58(2): 179-82. [DOI:10.1016/j.transci.2019.01.003] [PMID]
7. Verma M, Dahiya K, Malik D, Sehgal P, Devi R, Soni A, et al. Effect of blood storage on complete biochemistry. J Blood Disord Transfus 2015; 6(6): 1-4. [DOI:10.4172/2155-9864.1000329]
8. Charles AT, Bungudu UG, Osaro E, Tosan E. Effect of Storage on Osmotic Fragility in CPDA-1 Stored Blood in Sokoto, Northwestern Nigeria. Advances in Hematology and Oncology Research 2018; 1(1): 1-6. [DOI:10.33140/AHOR.01.01.02]
9. Reval D , Sharma R, Lodha S, Prakash S. Biochemical Changes in the Stored Whole Blood Assessd at the Pediatric Intervalsin CPDA1 Anticoagulant Containing Blood Bags. Asian J Pharm Clin Res 2023; 16(2): 113-5. [DOI:10.22159/ajpcr.2023.v16i2.47220]
10. Van Wijk R, Van Solinge WW. The energy-less red blood cell is lost: erythrocyte enzyme abnormalities of glycolysis. Blood 2005; 106(13): 4034-42. [DOI:10.1182/blood-2005-04-1622] [PMID]
11. Danehpash S, Shirkhanloo H, Azami K, Deyhim MR. Evaluation of Lipid Peroxidation, Antioxidant Status and Trace Elements in Red Blood Cell Concentrates during Storage. Iranian Jurnal of Blood and Cancer 2021; 13(3): 85-91
12. Ghezelbash B, Azarkeivan A, Pourfathollah AA, Deyhim M, Hajati E, Goodarzi A. Comparative Evaluation of Biochemical and Hematological Parameters of Pre-Storage Leukoreduction during RBC Storage. Int J Hematol Oncol Stem Cell Res 2018; 12(1): 35-42.
13. Mustafa I, Al Marwani A, Mamdouh Nasr K, Abdulla Kano N, Hadwan T. Time dependent assessment of morphological changes: leukodepleted packed red blood cells stored in SAGM. Biomed Res Int 2016; 2016: 4529434. [DOI:10.1155/2016/4529434] [PMID] []
14. Orlov D, Karkouti K. The pathophysiology and consequences of red blood cell storage. Anaesthesia 2015; 70(1): 29-37. [DOI:10.1111/anae.12891] [PMID]
15. Kücükakin B, Kocak V, Lykkesfeldt J, Nielsen HJ, Magnussen K, Rosenberg J, et al. Storage-induced increase in biomarkers of oxidative stress and inflammation in red blood cell components. Scand J Clin Lab Invest 2011; 71(4): 299-303. [DOI:10.3109/00365513.2011.563789] [PMID]
16. Aggarwal G, Tiwari AK, Pabbi S, Bhardwaj G, Rawat G, Harith AK, et al. Storage Lesions in Red Blood Cell‐Saline Adenine Glucose Mannitol: In-vitro and In-vivo Analysis over 42 Days and its Implications in Routine Transfusion Practice. Global Journal of Transfusion Medicine 2022; 7(1): 12-7. [DOI:10.4103/gjtm.gjtm_113_20]
17. Nguyen T , Fernández C, Pastora J. Impact of Different Red Blood Cell Storage Solutions and Conditions on Cell Function and Viability: A Systematic Review. Biomolecule 2024; 14(813): 1-28 [DOI:10.3390/biom14070813] [PMID] []
18. Omidkhoda A, Hedayati B, Kafi-Abad SA. The effect of whole blood storage time on quality of RBCs. Scientific Journal of Iranian Blood Transfusion Organization. Sci J Iran Blood Transfus Organ 2015, 11(1): 56-63. [Article in Farsi]
19. Mukherjee S, Marwaha N, Prasad R, Sharma RR, Thakral B. Serial assessment of biochemical parameters of red cell preparations to evaluate safety for neonatal transfusions. Indian J Med Res 2010; 132: 715-20.
20. Marjani A, Abolvahab Moradi A, Araz Berdie Ghourcaie A.B. Alterations in Plasma Lipid Peroxidation and Erythrocyte Superoxide Dismutase and Glutathione Peroxidase Enzyme Activities During Storage of Blood. Asian Journal of Biochemistry 2007; 2(2): 118-23. [DOI:10.3923/ajb.2007.118.123]
21. Deyhim MR, Nabavi Z, Jalili MA, Maghsoudloo M, Khoshnaghsh F. Alternation in Erythrocyte Enzyme Antioxidant Activity during Blood Storage. Iranian Journal of Blood and Cancer 2014; 6(2): 69-74.
22. Wilking M, Ndiaye M, Mukhtar H, Ahmad N. Circadian Rhythm Connections to Oxidative Stress: Implications for Human Health. Antioxid Redox Signal 2013; 19(2): 192-208. [DOI:10.1089/ars.2012.4889] [PMID] []
23. Barzegar S, Nadali F, Pourfatollah A.A, Abbaspour A.R, Farokhinia S, Shiravand Y. Oxidative stress changes in blood bags in consecutive weeks after donation. Sci J Iran Blood Transfus Organ 2016, 13(1): 11-8. [Article in Farsi]
24. Saeideh Hajizamani, Kamran Atarodi, Mohammad Reza Deyhim, Fahimeh Ranjbar Kermani, Kamran Mousavi Hosseini. Antioxidative effects of α‑tocopherol on stored human red blood cell units. Asian J Transfus Sci 2024; 18(1): 102-7. [DOI:10.4103/ajts.ajts_130_22] [PMID] []
25. Mehrdadi N, Deyhim M.R, Hekmat A. The effect of N-acetyl-cysteine (NAC) on RBC oxidative damage and RBC metabolism during storage of red blood cell product in blood bank condition. Medical Journal of Tabriz University of Medical Sciences and Health Services 2021; 42(6): 667-76. [Article in Farsi] [DOI:10.34172/mj.2021.007]
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







