جلد 22، شماره 2 - ( تابستان 1404 )
جلد 22 شماره 2 صفحات 159-150 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Ashouri kafshgar E, Chegini A, Samiee S, Zadsar M. The Evaluation of Quality Parameters of Platelet Apheresis Products Obtained from the Fresenius COM.TEC Device during Storage. bloodj 2025; 22 (2) :150-159
URL: http://bloodjournal.ir/article-1-1563-fa.html
URL: http://bloodjournal.ir/article-1-1563-fa.html
آشوری کفشگر الهه، چگینی آزیتا، سمیعی شهرام، زادسر مریم. بررسی پارامترهای کیفی پلاکت در فرآورده پلاکت فرزیس حاصل از دستگاه Fresenius COM.TEC در طی روزهای ذخیره سازی. فصلنامه پژوهشی خون. 1404; 22 (2) :150-159
استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون
متن کامل [PDF 669 kb]
(476 دریافت)
| چکیده (HTML) (1260 مشاهده)
مقدمه
پلاکتها سلولهای کوچک بدون هستهای هستند که قطری حدود 5-2 میکرون دارنـد و از سلولهای بزرگی تحت عنوان مگـاکاریوسیتها در مغز استخوان منشا میگیرنـد (1). این سلولها در حالت استراحت به دلیل شبکههایی از رشتههای اکتین و میکروتوبولهای درونشان دارای شکلی دیسکویید میباشند. تعداد طبیعی پلاکتها در خون حدود 150 تا 400 هزار در هر میکرولیتر است (3، 2). پلاکتها نقش مهمی در هموستاز و فعالیتهای انعقادی دارنـد، به طوری که تزریق آنها برای بیماران با ترمبوسیتوپنی نجاتدهنده بوده و یکی از راههای افزایش پلاکت بیماران، تزریق پلاکتهای اهدایی تهیه شده با روشهای مختلف میباشد (4، 1). فرآوردههای پلاکتی با سه روش متفاوتPRP (Platelets rich plasma)،Buffy coat و Apheresis تهیه میشوند (4). روش آفرزیس را میتوان روشی ایمن برای تولید مؤثرتر پلاکت به دلیل تماس بیماران بـا اهداکنندگان کمتر در نظر گرفت (5). اساس جداسازی پلاکت در روش آفرزیس ورود خون اهداکننده به دستگاه آفرزیس و جداسازی پلاکت و بازگشت باقی اجزای خون به بدن اهدا کننده است. این دستگاهها با سیستم فیلتراسیون یـا سانتریفیوژ یا ترکیبی از این دو قادر به جداسازی اجزای خون هستند (6). Haemonetics MCS و Trima Accel و COBE Spectra و Fresenius و ... دستگاههای جداسازی پلاکت به روش سانتریفیوژ میباشند (8، 7). مطالعههای اخیر به بررسی دستگاههای مختلف از نظر ارزیـابی هر چه دقیقتر عملکرد دستگاهها و کیفیت فرآورده حـاصل از آنها همانند تعداد پلاکتها و تغییرات pH, Glucose, ،LDH ، میزان فعال شدن پلاکتها و همچنین میکروپارتیکلهای پلاکتی پرداختهاند (9).
یکی از دستگاههای تهیـه پلاکت آفرزیس، Fresenius COM.TEC است. این دستگاه بر اساس سانتریفیوژ جریان متناوب (IFC) به جداسازی پلاکت از سایر اجزای خونی میپـردازد، در این روش خون پس از تکمیل فرآیند جداسازی بـه بدن اهداکننده باز میگردد. خون در فرآیند جداسازی با استفاده از پمپهای مختلف نظیر پمپ خون، پمپ ضد انعقاد، پمپ وریـد و پمپ جمعآوری در ست دستگاه به جریان میافتد. پس از سانتریفیوژ، پلاکتها جدا شده و در نهایت فرآورده پلاکتی حاصل در کیسه پلاکت جمعآوری میگردد و سایر سلولها به همراه پلاسما به بدن اهداکننده بازگردانده میشود. لذا در این مطالعه به بررسی تعداد پلاکتها، MTT ، LDH و pH در پلاکتهای تهیه شده توسط دستگاه Fresenius COM.TEC در طول مدت ذخیرهسازی پلاکتها پرداخته شد.
مواد و روشها
در ایـن مطالعـه تجربی، از واحدهای پلاکت آفرزیس حاصل ازدستگاه Fresenius COM.TEC که در اداره کل انتقال خون استان تهران در بخش اهدا تهیه شده بود، استفاده گردید. از اهداکنندگان داوطلب، رضـایتنامه آگاهانـه جهـت استفاده از محصول نهایی پلاکت آفرزیس در کار تحقیقاتی گرفته شد. معیار ورود اهداکنندگان به این مطالعه، افراد کـاملاً سالم با هموگلوبین بیش از 5/12 گرم در دسیلیتر، وزن اهداکننده بیش از ۵۰ کیلـوگرم، هماتوکریـت بیش از 38%، آزمایشهای منفی HIV، HBsAg ،HCV و RPR ، گـذشت حداقل ۳ ماه پس از اهدای خون کامل و حداقل ۳ روز پس از آخرین اهدای پلاکت و دسترسی کافی به وریدهای اهداکننده با رعایت دستورالعملهای سازمان انتقال خون ایران بودند.
معیارهای خروج شامل مصرف داروهای ضد التهاب غیر استروئیدی (NSAIDs) مانـند آسپرین، ایبوپروفن، نـاپروکسن، دیکلوفناک و غیره و ابتلا به بیماری زمینهای بودنـد. نمونهگیری از فرآورده پلاکتی حاصل ازدستگاه Fresenius COM.TEC (Fresenius HemoCare GmbH آلمان) صورت گرفت.
پارامترهای تنظیم شده در دستگاه Fresenius COM.TEC شامل: جریان خون کامـل 75-50 میلیلیتر در دقیقه، نقطه تنظیم رابط 33 و ضد انعقاد خون به کـل خون 1: 9 بود. اطلاعات زیر شامل وزن اهداکننده، جنس، قد، سطح هموگلوبین و میزان پلاکت قبل از آفرزیس به دستگاه داده میشد. میزان برداشت هدف پلاکت (Target PLT yield) به میزان (1011 ×5-3) تعیین شد.
در هر آفرزیس ،دو کیسه فرآورده پلاکت آفرزیس تهیه میگردید که یک کیسه با حجم250 میلیلیتر جهت تزریق به بیمار به بیمارستان ارسال میشد. کیسه دیگر برای بررسی و انجام آزمایشهای مطالعه، بـا حجم حدود 50 میلیلیتر تهیه گردید. همه کیسههای دریافت شده با حجم حـدود 50 میلیلیتر جهت انجام آزمایشها به مرکز تحقیقات انتقال خون منتقل شد. به هرکدام ازکیسههای آفرزیس تهیه شده ابتدا لیبل خاصی چسبانیده و سپس در شیـکر انکوباتور در آزمایشگاه مرکز تحقیقات سازمان انتقال خون با دمای مشخص 2 ± 22 درجه سانتیگراد با حرکت دورانی ملایم rpm 60 نگهداری شدند و در روزهای 1،3،5 کیسههای پلاکت آفرزیس از نظر ظاهری و swirling مورد بررسی قرار گرفتند. Swirling(یـا چرخش) با بررسی کیسههای حاوی پلاکت در برابر نور ارزیابی و به صورت زیر امتیازدهی شد:
امتیاز ۰: همگن کدر است و با فشار تغییر نمیکند.
امتیاز ۱: همگن فقط در قسمتی از کیسه میچرخد و شفاف نیست.
امتیاز ۲: چرخش همگن واضح در تمام قسمتهای کیسه.
امتیاز ۳: چرخش همگن بسیار واضح در تمام قسمتهای کیسه (10). پس از تـایید سلامت و طبیعی بودن رنگ و swirling، برای انجـام آزمـایشهای مورد نظر در روزهای 1،3،5 ذخیرهسازی ، حدود 10 میلیلیتر از فرآورده از طریق کورد کیسه، به لوله فالکون استریل منتقل شد. فرآوردههای منتقل شده به فالکون جهت بررسی از نظر شمارش پلاکت، نمونهها با PBS به نسبت 1 به 5 رقیق شده و سپس، به دستگاه سل کانتر KX1000 SYSMEX داده شد تا از نظر تعداد پلاکت شمارش شوند. سپس الکترودهای دستگاه pH متر (Herisau ، pH lab 827 Metrohm سوئیس) با استفاده از آب دیونیزه شسته و با گاز استریل آبگیری شد و در نهایـت در محلول pH خنثی (7 pH=) کالیبره گردید و بعد از اطمینان از صحت دستگاه و خوانش درست، pH نمونهها با دستگاه pH متر در هر سه روز ذخیرهسازی اندازهگیری شد. برای بررسی و تشخیص آسیب سلولی و تعیین میزان آن، آزمایش لاکتات دهیدروژناز (LDH) برای کیسهها انجام شد. 500 میکرولیتر از نمونه پلاکتی از فالکون استریل به میکروتیوب منتقل و سپس با دور rpm 4000 به مدت 10 دقیقه سانتریفیوژ شد. در هر سه روز 1، 3 و 5 ، فعالیت آنزیم LDH با استفاده از کیت شرکت دلتا درمان پارس بر اساس واکنش تبدیـل لاکتـات بـه پیـروات که توسط آنزیم LDH کاتـالیز میشود، توسط دستگاه کوباس ECL COBAS E411 اندازهگیری گردیـد. برای بررسی زندهمانی سلولها، از روش 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl-2H-tetrazolium bromide (MTT) استفاده شــد.
در ایـن روش، ابتدا حـدود 107× 1سلول در 100 میکرولیتر پلاکـت آماده شد و به چاهکهای پلیت منتقل گردیـد و سپس 10 میکرولیتر از محلول فرمازون (Sigma-Aldrich,USA) به هر چاهک اضافه شد و به مدت 4 ساعت در انکوباتور CO2 انکوبه گردید. پس از طی مدت انـکوبـاسیون، معرف DMSO (دی متیل سولفوکسید)(مرک، آلمان) را به مقدار 100 میکرولیتر بـه نمونهها اضافه کرده و سپس 10 دقیقه در انکوباتور CO2 انکوبـه شد. بعد از طی مدت زمان انکوباسیون، نمونهها در طول موج 570 نـانومتر توسط الایزا ریـدر (کارخانجات تولیدی نورهان فجر Elisa reader multiskan-thermo fisher scientific ، آمریکا) خوانده شد.
آزمون آماری:
به منظور محاسبه حجم نمونـه در این طرح از نرمافزار G*power استفاده شد. در این نرمافزار با در نظر گرفتن آزمون repeated measure تحت فرض سطح معناداری 05/0 و توان ۸۰ درصد و یـک اندازه اثر (effect size f=0.17) ، حداقل حجم نمونه برابر ۲۵ محاسبه گردید.
بـا توجه به توزیع طبیعی، دادههای حاصل از آزمایشها در نرمافزار R وارد و میانگین و انحراف معیار و p-value بـا مدلLinear regression در روزهای مختلف ذخیرهسازی (1،3،5) محاسبه گردید. p-value کمتر از 05/0 معنادار در نظر گرفته شد.
یافتهها
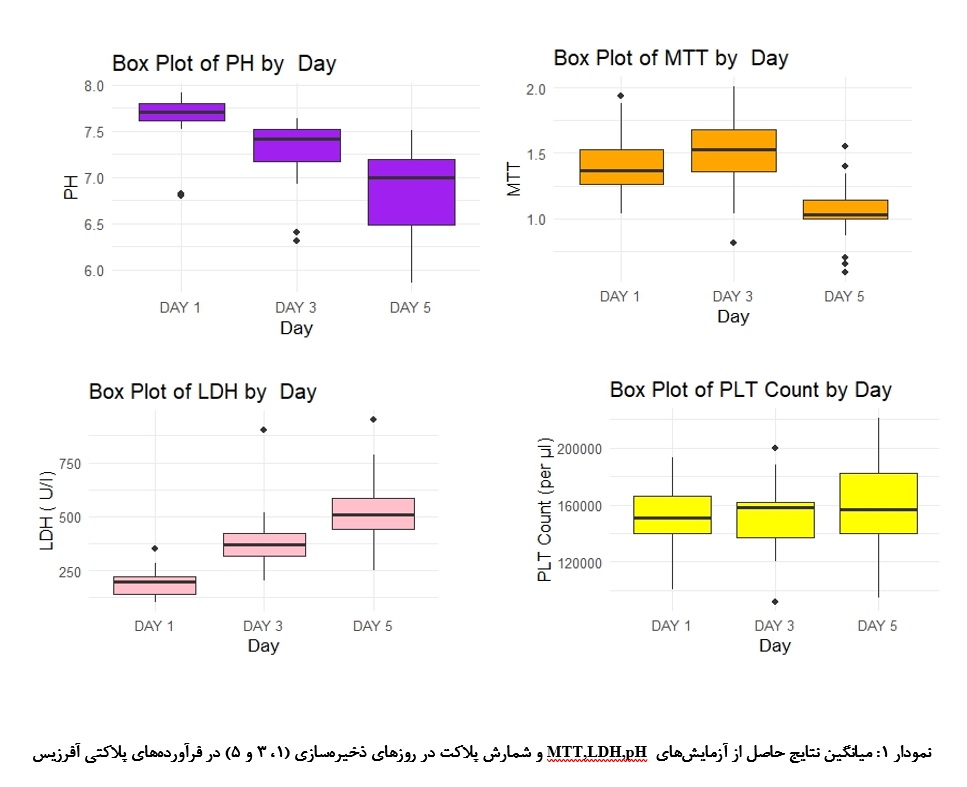
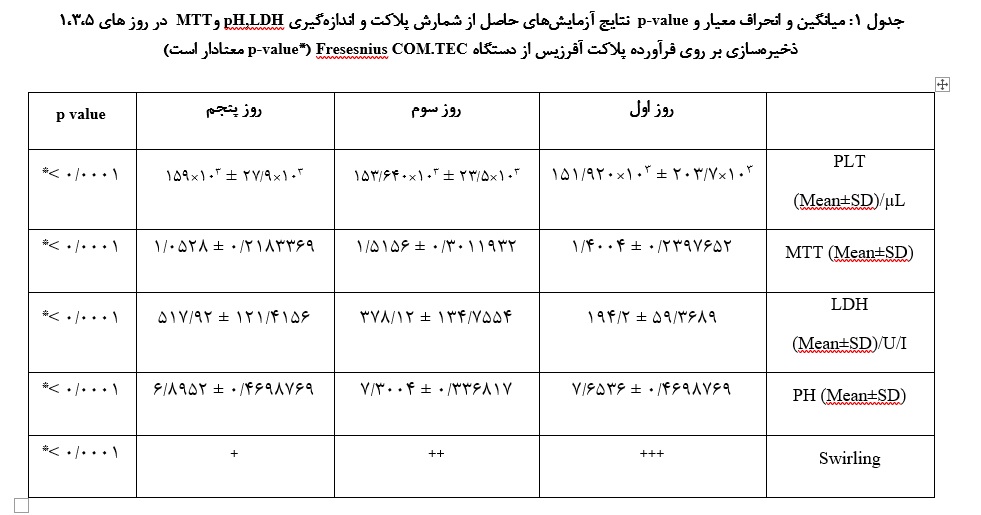
25 فرآورده پلاکت حاصل از دستگاه Fresesnius COM.TEC در روزهای ذخیرهسازی (1،3،5) بررسی گردید. پلاکتهای آفرزیس از نظر ظاهری و swirling در روزهای ذخیرهسازی اول و سوم امتیاز 2 و 3 را گرفتند. میانگین نتایج شمارش پلاکت در روز 1 ذخیرهسازی فرآوردههای پلاکت آفرزیس حاصل از دستگاه Fresesnius ، COM.TEC /µL103×920/151 و در روز 3 ذخیرهسازی /µL103×640/153 و همچنین در روز پنجم /µL103 ×159 بود. تفاوت معناداری از روز اول تا پنجم در تعداد پلاکت مشاهده نشد. تغییرات pH در روز 1 ذخیرهسازی 63/7 و در روز 3 ، 30/7 و در روز 5، 89/6 دیده شد (0001/0 p<) (نمودار 1)(جدول 1).
میانگین زنـدهمانی پلاکتها با آزمایـش MTT در روز 1
ذخیرهســـازی40/1 در روز 3، 51/1 و در روز 5، 05/1 بود
(0001/0 p<). میــانگیـن میـزان LDH نیـــــز در روز 1،
Unit/L 2/194 ، در روز 3، Unit/L 12/378 و در روز 5،
Unit/L 92/517 به دست آمد (0001/0 p<).
بحث
در این مطالعه پلاکتهای آفرزیس حاصل از دستگاه Fresenius COM.TEC از نظرظاهری و swirling در روزهای ذخیرهسازی امتیاز 2 و 3 و سپس 1 را گرفتند. در شمارش PLt این فرآوردههای پلاکت فرزیس تفاوت معناداری در روزهای 1 ، 3 و 5 ذخیرهسازی مشاهده نشد، اما نتایج آزمـایشهای pH ، LDH و MTT در روزهای ذخیرهسازی معنادار بود (0001/0 p<).
Swirling و ارزیابی چرخش یک روش ساده و غیر تهاجمی برای بررسی پلاکتها است که به صورت بصری انجام میشود و برای کنترل کیفی معمول هر پلاکـت و در مقیاس بزرگ مفید است. بررسی بصری swirling بـا مورفولوژی پلاکـت مرتبط است؛ وجود آن نشاندهنده مورفولوژی دیسکوئید و عدم وجود آن نشاندهنده مورفولوژی کروی پلاکتها است (10). سینگ و همکـاران نمره 3 swirling را در 7/79%، 9/83% و 90% از واحدهای پلاکـت مشاهده کردند، در حالی که امتیاز 2 به ترتیب به 3/20 %، 1/16 % و 10% از واحـدهای PRP-PC ، BC-PC و apheresisPC داده شد. آنها در هیچ واحدی امتیاز یک را در روز اول تهیه مشاهده نکردند (10). برتولینی و همکاران در مطالعه خود گزارش کردند که پلاکتهای تـازه در 83% از واحـدها swirling مثبت و تنها در 2% منفی بوده و بقیه swirling متوسط داشتند. پس از ۵ روز نگهداری، میزان swirling پلاکتهای مثبت 65% کاهش یافت و برتولینی نتیجه گرفت که این کاهش میتوانـد به دلیل آسیبهایی باشد که در طول نگهداری پلاکـتها رخ میدهند (11). در مطالعه ما واحـدهای پلاکت در روز اول امتیاز 3 داشتند که در روز پنجم امتیاز هیچکدام به 0 نرسید.
فعالیت متابولیک فرآوردههای پلاکت فرزیس عمدتاً بـا pH ، pCO2 ، pO2 ، بیکربنات، گلوکز و لاکتات بررسی میشود. متابولیسم پلاکتها در خارج از بـدن و حین نگهداری در دمای ˚C2±22 تغییر میکند و سبب تغییراتی در pHمیشود (12). اگر pH به کمتر از 8/6 نرسد، حجم پلاکت در طول سه روز تقریباً 10% کاهش مییـابد. در میزان pH کمتر از 8/6 تورم سلولها شروع میشود و در 0/6pH= به حداکثر خود میرسد. اگر pH از این سطح پـایینتر بیاید، افزایش تدریجی حجم پلاکـت و کاهش چگالی دیده میشود که نشاندهنده تورم بـه دلیل ورود مایع خارج سلولی است. در 0/6pH= ، حجم پلاکت تقریباً دو برابر شده و سرعت تبدیل دیسک به کره افزایش مییابد. بـه طوری که اگر pH به 7/5 تا 9/5 برسد، فقط کرههای متورم دیده میشوند. اگر pH بالاتر از 1/6 بمانـد، این تغییرات تقریباً به طور کامل برگشتپذیر هستند، اما اگر pH به زیر 1/6 برسد، قابل برگشت نیستند. گلبولهای سفید خون در محیط کشت PC اثر مخربی دارند و منجر بـه کاهش قابل توجه pH، افزایش مصرف گلوکز، تولید اسید لاکتیک و آزادسازی LDH در طول نگهداری میشوند. pH در طول ذخیرهسازی بسته به محلولهای موجود در کیسههای پلاستیکی نگهداری پلاکت و شرایط ذخیرهسازی کـاهش مییابد. افزایش گلیکولیز پلاکت منجر بـه کاهش pH به سطوح نزدیک به 0/6 در پلاکتهای ذخیره شده در پلاسما میشود و با از دست دادن قابل توجه قابلیت حیات پلاکـتها همراه است (10). در مطالعه ما تغییرات میانگین pH در روز 1 ذخیرهسازی 63/7 و در روز 3 ، 30/7 و در روز 5، 89/6 دیـده شد که به کمتر از 8/6 نرسید (0001/0 p<).
آزمایش دیگری که برروی فرآوردههای پلاکت انجام شد LDH بود که افزایش آن را در روزهای نگهداری (1،3،5) مشاهده کردیم. پروچازکوا و همکاران بر روی دو دستگاه Trima و MCS مطالعهای انجـام دادند. آنها نیز افزایش LDH را در طی روزهای ذخیرهسازی (1،3،5) در هر دو دستگاه مشاهده نمودند که با میزان pH رابطه عکس داشت. آنها افزایش LDH را در روز 5 در فرآورده حاصل از دستگاهMCS به طور معناداری بیشتر گزارش کردنـد. سرکوب چرخه کربس در میتوکندری و انباشت اسید کربنیک در سیتوپلاسم حاصل از چرخه گلیکولیز سبب کاهش pH میشود و افزایش LDH هم میتوانـد به دلیل ادامه روند گلیکولیز در سیتوپلاسم سلولهای پلاکت باشد (13). ما نیز کاهش میزان pH و افزایش میانگین LDH در روزهای نگهداری پلاکت را مشاهده کردیم (0001/0 p<).
ماچر و همکاران در سال 2010 به بررسی فرآوردههای حاصل از دستگاهها Amicus وTrima پرداختند، آنها نیز افزایش LDH و کاهش pH در روزهای ذخیرهسازی را همانند مطالعه ما و تحقیق پروچازکوا گزارش نمودنـد و این موضوع را متأثر از جنس کیسه و تبادل مناسب اکسیژن دانستند (14). بر اساس نتایج حاصل از مطالعه اکسیا و همکاران، ازدست دادن میزان زنده ماندن سلولها (cellular viability) بـا افزایش LDH و لاکتات در کیسه، کـاهش pH و طیف وسیعی از پدیدههای متابولیکی دیگر مرتبط است. این تغییرات همراه بـا تغییرات مورفولوژیکی در پلاکتها رخ میدهد کـه پارامترهای متابولیکی را بدتر میکند (15). برای معکوس کردن این تغییرات از کیسههایی که امکان تبادل بهتر و مؤثرتر گاز در هنگام ذخیرهسازی در دمای 22 تا 24 درجه سانتیگراد را فراهم میکنند و از ضد انعقادهای بهتر برای کـاهش میزان فعال شدن پلاکت در خـارج از بدن استفاده کردهاند (15). اکسیا و همکاران برای بررسی فعالیت متابولیک سلولها از آزمایشهای MTT و LDH بـا روش اسپکتروفتومتریـک استفاده کردند. آنها فعالیت متابولیکی پنج جفت پلاکـت را با استفاده از روش MTT در فواصل زمانی مختلف سنجیدند و به یکی از آنها PEG-rHuMGDF برای بررسی تأثیر TPOبر زندهمانی پلاکتها اضافـه کردند. پلاکتها فعالیت متابولیکی طبیعی خود را برای 6 روز اول ذخیرهسازی حفظ کردند و سپس در طول مدت ذخیرهسازی بعدی، کاهش تدریجی و خطی در فعالیت متابولیکی داشتند. بـا این حال، در هیچ زمانی هیچ تـأثیری از وجود PEG-rHuMGDF مشاهده نشد. تغییرات MTS و MTT در کیسههای پلاکت در طول ذخیرهسازی بـه موازات تغییرات pH و LDH بود (15). در مطالعه ما نیز آزمایش MTT در روز 5 نسبت بـه روز 1 کاهش داشت. این کاهش در نتایج حاصل از MTT میتواند نشانهای از مرگ بیشتر پلاکتها در روز 5 ذخیرهسازی نسبت به روز اول باشد. ولی در روز سوم افزایش در میزان آزمایش دیده شد که میبایستی عوامل مخدوشکننده این آزمایش را درنظر گرفت. علیرغم کـاربردهای گسترده این آزمایش در طی چهار دهـه گذشته، روش MTT اغلب بدون توجه به مکانیسمهای اساسی و محدودیتها آن، تفسیر و استفاده میشود. مکانیسم بنیادی آزمایش MTT ، ]3-(4،5-دی متیل تـیازول-2-ایـل)-2،5-دی فنیل-2H-تترازولیوم برومایـد[ یک نمک مونو تترازولیوم است که از یک هسته حلقه تترازول چهارتایی با بار مثبت حاوی چهار اتم نیتروژن احاطه شده توسط سه حلقه آروماتیک شامل دو بخش فنیل و یک حلقه تیازولیل تشکیل شده است. احیای MTT منجر به اختلال در حلقه تترازول مرکزی و تشکیل یک مولکول نامحلول در آب به رنگ آبی- بنفش به نام فورمازان میشود. معرف MTT میتواند از غشای سلولی و همچنین غشای داخلی میتوکندری سلولهـای زنده (احتمالاً به دلیل بار مثبت آن و همچنین ساختار لیپوفیلی آن) عبور کند و توسط سلولهای فعال متابولیکی به فورمازان احیا شود. این سنجش به عنوان یک سنجش فعالیت متابولیک سلولی کاربرد گستردهای دارد. بـا این حال، کاربرد آن به طور فزآیندهای برای استنباط فرآیندهای ثـانویه یا حالتهای سلولها، مانند زندهمانی، که اغلب بیاساس است، به کار گرفته شده است. محل تشکیل فورمازان و انتقال درون سلولی آن همچنان بحثبرانگیز است. مطالعههای بیوشیمیایی و میکروسکوپی، فورمازان را در اندامکهای مختلف درون سلولی (در شبکه آنـدوپلاسمی، قطرات لیپیدی سیتوزولی، غشاهای پلاسما، هسته و میکروزومها) پیدا کردهاند. مطالعههای متعدد محدودیـتهای سنجش MTT و عـوامل مخدوشکننده مختلفی را آشکار کردهاند. برخی از متغیرهای مخدوشکنندهای که معمولاً نادیده گرفته میشوند شامل تعداد سلولهای کشتشده، غلظت معرف، MTT اضافه شده به سلولها، زمان انکوباسیون سلولها بـا MTT ، نوع محیط کشت، حـذف مایع رویی سلولها پس از انکوباسیون MTT و طول موجی کـه در آن چگالی نوری اندازهگیری میشود، هستند. افزایش تعداد سلولها، سطح کل فورمازان تولید شده توسط جمعیت سلولی و در نتیجه OD اندازهگیری شده را افزایش میدهد. برای ارزیابی زندهماندن سلولها، بـاید آزمایشهای کنترلی دقیقی به عنوان وسیلهای برای تعیین چگونگی تـأثیر پارامترهای ذکر شده بر رابطه بین OD اندازهگیری شده و تعداد سلولها انجام شود. سطح OD صرفاً یـک نمایش ساده از یک پارامتر مانند زندهماندن سلول، تکثیر سلولی یا فعالیت متابولیک نیست، بلکه مجموعهای از عوامل بسیاری در سطح تک سلول و جمعیت سلولی و همچنین سایر عوامل سلولی مانند فاز رشد سلولی و میزان جذب MTT و خروج فورمازان است که همگی میتوانند به طور بالقوه آزمایش/محیط کشت را تحت تاثیر قرار دهد. این پیچیدگی حتی میتوانـد باعث نتایج مثبت کاذب در هنگام آزمایش بـا استفاده از سنجش MTT شود (16). بنابراین با توجه به آن که تعداد سلول/تراکم و غلظت MTT بر میزان تشکیل فرمازان تـأثیر میگذارد، بهینهسازی دقیق شرایط سنجش متناسب با ردههای سلولهای خاص و استفاده از کنترلهای مناسب همانند بررسی اگریگومتری، فلوسیتومتری و نشانگرهای آپوپتوز از محدودیتهای مطالعه ما به شمار میرود.
حسین و همکـاران در سـال 2015 بــه بررسی تغییرات
شمارش پلاکتی در روزهای 1، 3، 5 و 7 ذخیرهسازی پرداختند. آنها فرآوردههای پلاکتی محصول دستگاه Cobe spectra را بررسی کردند. در مطالعه آنها 16 نفر، به تعداد 9 مرد و 6 زن پلاکت اهدا کردند. در مطالعه آنها شمارش پلاکـت در روزهای ذخیرهسازی رونـد کاهشی داشت (17). اما برخلاف تحقیق حسین و همکاران، نتایج حاصل از مطالعه ما تغییرات چشمگیر و معناداری در شمارش پلاکت در روزهای ذخیرهسازی نشان نداد که میتواند به این دلیل بـاشد که آنها روز 7 را نیز در مطالعه خود گنجانیده بودند و ما تا روز 5 میزان پلاکـتها را بررسی کردیم. در مطالعه تین گارد و همکاران در سال 2008 که به بررسی تفاوت فرآوردههای حاصل از دو دستگاه cobe Spectra و Trima Accel بر روی 20 پلاکت آفرزیس (از هر دستگاه 10 فرآورده پلاکـت آفرزیس) در روز های 0، 1، 3، 5 و 7 پرداختند، نیز مشاهده شد. در نتایج حاصل از این مطالعه گزارش کردنـد که تغییرات تعداد پلاکت در هر دو دستگاه در طی روزهای ذخیرهسازی ثـابت بود ولی میانگین حجم پلاکت MPV( mean platelet volume) در روز 1 نسبت به روز 0 روند کاهشی داشت، ولی در سایر روزها در این پارامتر هم تغییراتی دیـده نشد. آنها نتیجهگیری کردند که کیفیت پلاکـت پس از ذخیرهسازی به مدت ۷ روز به خوبی حفظ شده بود، اگر چـه فعالشدن پلاکتهـا را در طول ذخیرهسازی، توسط آزمایشهای pCO2 ، pO2 و pH در گازهای خون، و مارکرهـای سطح پلاکـت GPIb (CD42b) and P-selectin (CD62P) در فلوسیتومتری مشاهده کردند و هیچ تفاوتی در کیفیت پلاکـت بین PCهای تولید شده توسط دو دستگاه Spectra و Trima گزارش نکردند (18). در مطالعه ما تفاوت معناداری در شمارش پلاکت فرآوردههای پلاکت فرزیس حاصل از دستگاه Fresenius COM.TEC در روزهای 1، 3 و 5 ذخیرهسازی مشاهده نشد. اگر چه تین گارد و همـکاران متغیرهای مختلف متابولیک همانند میزان قند، لاکتات، گـازهای خونی، میزان Soluble P-selectin در پلاسما، مارکرهای سطح پلاکت ،Clotting time and coagulum G و hypotonic shock response (HSR) را نیز بررسی کردند.
گلبولهای سفید خون در فرآورده پلاکت اثر مخربی بر محیط ذخیرهسازی دارند و منجر به کاهش قابل توجه pH، افزایش مصرف گلوکز، تولید اسید لاکتیک و آزادسازی LDH در طول ذخیرهسازی میشوند. در نتیجه، در فرآورده پلاکتی کـه غلظت بالایی از لکوسیتها دارند، وضعیت پلاکتهـا تا روز 5 ذخیرهسازی نیز به طور قابل توجهی تحت تـأثیر قرار میگیرد که با دفع بالای β-TG، از دست دادن نوکلئوتیدهای پلاکتی، کـاهش توانایی ترکیب آدنوزین 3 فسفات و مورفولوژی ضعیف پلاکتها نشان داده میشود (19).
در مطالعه تورا و همکاران میزان pH در فرآوردههای آفرزیس در روز 5 نگهداری 16/0 ± 89/6 گزارش شده بـود و در مطالعه ما نیز pH در روز 5 ، 46/0 ± 89/6 بـه دست آمد. آنها بر روی ۶۶۹ فرآورده پلاکتی آفرزیس مطالعه کردنـد که از این تعداد ۴۶۰ واحد آفرزیس تحت بررسی آزمایشگاهی و کنترل کیفیت قرار گرفت. نتایج حاصل از pH در مطالعه آنها نشان داد که بر اساس جنس کیسهها و شرایط نگهداری، میزان pH کاهش مییابد که این کـاهش متأثر از شرایط نامناسب فیزیولوژیک در اثر افزایش ذخیرهسازی برای پلاکتهای تهیه شده در هر سه روش رندوم دنور، آفرزیس و بافیکوت بود (19).
محدودیتهای مطالعه حاضر، عدم بررسی تمامی موارد کنترل کیفی و بررسی روشهــای پیشــرفتهتــر ارزیــابی کیفیـت پلاکت، آزمـایشهـایی از قبیـل انـدازهگیـری فعالیـت آنها بـه وسـیله بیـان مارکرهـایp62 CD و 63CD با روش فلوسیتومتری واگریگومتری، بهینهسازی دقیق شرایط سنجش MTT بر روی فرآورده پلاکت آفرزیس حاصل از دستگاه Fresenius COM.TEC است و بهتر بود سایر موارد کنترل کیفی همانند حجم واحد آفرزیس، تعداد WBC، تعداد RBC و استریلیتی، هم بررسی و همچنین مقایسهای بین دستگاههای مختلف آفرزیس با هم انجام میشد.
نتیجهگیری
بررسیهای آزمایشگاهی برروی فرآوردههای حاصل از دستگاه آفرزیـس Fresesnius COM.TEC در روزهای ذخیرهسازی نشان داد که میتوان از این دستگاه تهیه پلاکت نیز استفاده کرد. برای تفسیر نتایج MTT محدودیتهای آن را بایستی در نظر گرفت و از کنترلهای مناسب دیگر نیز بهره برد.
حمایت مالی
این پروژه توسط مرکز تحقیقات انتقال خون، مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ایران تأمین مالی شده است.
ملاحظات اخلاقی
مطالعه حاضر دارای کد اخلاق IR.TMI.REC.1402.009 از کمیته اخلاق مؤسسه عالی آموزشی و پژوهشی طب انتقال خون تهران ، ایران است.
عدم تعارض منافع
نویسندگان اظهار میکنند هیچگونه تعارض منافعــی در
این مطالعه وجود نداشته است.
نقش نویسندگان
اله آشوری کفشگر: انجام مراحل عملی، تجزیه و تحلیل و تفسیر نتایج، تهیه پیشنویس مقاله
دکتر آزیتا چگینی: مدیریت و طراحی مطالعه، تفسیر نتایج و بازبینی، تهیه و اصلاح پیشنویس مقاله
شهرام سمیعی: طراحی مطالعه، انجام مراحل عملی و تهیه پیشنویس مطالعه
دکتر مریم زادسر: تجزیه و تحلیل، تفسیر نتایج، تهیه پیشنویس مقاله
تشکر و قدردانی
این مقاله نتیجه پایاننامه دانشجویی کارشناسی ارشد رشته زیست فناوری پزشکی مرکز تحقیقات مؤسسه عالی آموزشی و پژوهشی طب انتقال خون میبـاشد. تهیه فرآورده از پایگاه انتقال خون تهران و مراحل پروژه در آزمایشگـاه مرکز تحقیقات انجام گردیـد. بدین وسیله از پرسنل زحمتکش اداره کل انتقال خون تهران و مرکز تحقیقات تشکر و قدردانی بـه عمل میآید.
متن کامل: (257 مشاهده)
بررسی پارامترهای کیفی پلاکت در فرآورده پلاکت فرزیس حاصل از دستگاه Fresenius COM.TEC در طی روزهای ذخیرهسازی
الهه آشوری کفشگر1، آزیتا چگینی2 ، شهرام سمیعی3 ، مریم زادسر4
1- دانشجوی کارشناسی ارشد هماتولوژی و بانک خون ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- متخصص بیهوشی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
3- کارشناس ارشد بیوشیمی ـ مربی مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
4- متخصص بیماریهای عفونی ـ دانشیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
1- دانشجوی کارشناسی ارشد هماتولوژی و بانک خون ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- متخصص بیهوشی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
3- کارشناس ارشد بیوشیمی ـ مربی مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
4- متخصص بیماریهای عفونی ـ دانشیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
 http://dx.doi.org/10.61186/bloodj.21.4.296 Citation: Ashouri kafshgar E, Chegini A, samiee Sh, Zadsar M. The Evaluation of Quality Parameters of Platelet Apheresis Products Obtained from the Fresenius COM.TEC Device during Storage. J Iran Blood Transfuse. 2025: 22 (2): 150-159 نویسنده مسئول: دکتر آزیتا چگینی. استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران صندوق پستی: 1157-14665 E-mail: a.chegini@
کد اخلاق: IR.TMI.REC.1402.009 |
چکیده سابقه و هدف پلاکتها سلولهای کوچک و بدون هستهای هستند که برای انواع مداخلات درمانی حیاتی میباشند. اطمینان از کیفیت پلاکتهای تزریق شده برای دستیابی به نتایج مطلوب برای بیمار بسیار مهم است. دستگاههای مختلفی برای جداسازی محصولات پلاکتی از خون کامل وجود دارند که هر کدام ویژگیهای منحصر به فردی دارند. این مطالعه با هدف ارزیابی دستگاه آفرزیس پلاکت Fresenius COM.TEC با تجزیه و تحلیل تغییرات pH، تعداد پلاکت، سطح لاکتات دهیدروژناز و زندهمانی پلاکت (MTT) در روزهای نگهداری 1، 3 و 5 انجام شد. مواد و روشها در این مطالعه تجربی، 25 واحد آفرزیس پلاکت به صورت تصادفی از اهداکنندگان مرد در مرکز انتقال خون تهران با استفاده از دستگاه Fresenius COM.TEC جمعآوری شد. فرآوردههای پلاکتی در دمای 24-20 درجه سانتیگراد در شیکر انکوباتور نگهداری شدند. نمونهها در روزهای نگهداری 1، 3 و 5 برای ارزیابی pH، LDH، تعداد و زندهمانی پلاکت جمعآوری شدند. تمام آزمایشها در آزمایشگاه مرکز تحقیقات انتقال خون انجام شد. تجزیـه و تحلیـل دادهها با استفاده از نرمافزار R انجام شـد و مقادیـر 05/0 p< از نظر آماری معنادار در نظر گرفته شدند. یافتهها سطح LDH در روز 5 به بالاترین حد خود رسید و در طول دوره نگهداری افزایش معناداری نشان داد و تفاوت آماری معناداری بین روزهای نگهداری وجود داشت. کاهش مداوم pHنیز در طول زمان مشاهده شد. نتایج سنجش MTT افزایشی گذرا در روز 3 و به دنبال آن کاهش در روز 5 را نشان داد که از نظر آماری معنادار بود (0001/0 p<). در مقابل، تعداد پلاکتها هیچ تغییر معناداری را در تمام روزهای نگهداری نشان نداد. نتیجه گیری هیچ تغییر قابل توجهی در تعداد پلاکتها در فرآوردههای آفرزیس جمعآوری شده از طریق دستگاه Fresenius COM.TEC در طول مدت نگهداری مشاهده نشد. با این حال، کاهش pH و افزایش LDH در روزهای 1، 3 و 5 مشاهده شد که با روندهای گزارششده در مطالعههای مشابه مطابقت دارد. تفسیر نتایج سنجش MTT به دلیل محدودیتهای آن باید با احتیاط انجام شود و بر لزوم کنترلهای دقیق تأکید میگردد. کلمات کلیدی: پلاکت فرزیس، کنترل کیفی، پلاکتهای خون، انتقال پلاکت |
مقدمه
پلاکتها سلولهای کوچک بدون هستهای هستند که قطری حدود 5-2 میکرون دارنـد و از سلولهای بزرگی تحت عنوان مگـاکاریوسیتها در مغز استخوان منشا میگیرنـد (1). این سلولها در حالت استراحت به دلیل شبکههایی از رشتههای اکتین و میکروتوبولهای درونشان دارای شکلی دیسکویید میباشند. تعداد طبیعی پلاکتها در خون حدود 150 تا 400 هزار در هر میکرولیتر است (3، 2). پلاکتها نقش مهمی در هموستاز و فعالیتهای انعقادی دارنـد، به طوری که تزریق آنها برای بیماران با ترمبوسیتوپنی نجاتدهنده بوده و یکی از راههای افزایش پلاکت بیماران، تزریق پلاکتهای اهدایی تهیه شده با روشهای مختلف میباشد (4، 1). فرآوردههای پلاکتی با سه روش متفاوتPRP (Platelets rich plasma)،Buffy coat و Apheresis تهیه میشوند (4). روش آفرزیس را میتوان روشی ایمن برای تولید مؤثرتر پلاکت به دلیل تماس بیماران بـا اهداکنندگان کمتر در نظر گرفت (5). اساس جداسازی پلاکت در روش آفرزیس ورود خون اهداکننده به دستگاه آفرزیس و جداسازی پلاکت و بازگشت باقی اجزای خون به بدن اهدا کننده است. این دستگاهها با سیستم فیلتراسیون یـا سانتریفیوژ یا ترکیبی از این دو قادر به جداسازی اجزای خون هستند (6). Haemonetics MCS و Trima Accel و COBE Spectra و Fresenius و ... دستگاههای جداسازی پلاکت به روش سانتریفیوژ میباشند (8، 7). مطالعههای اخیر به بررسی دستگاههای مختلف از نظر ارزیـابی هر چه دقیقتر عملکرد دستگاهها و کیفیت فرآورده حـاصل از آنها همانند تعداد پلاکتها و تغییرات pH, Glucose, ،LDH ، میزان فعال شدن پلاکتها و همچنین میکروپارتیکلهای پلاکتی پرداختهاند (9).
یکی از دستگاههای تهیـه پلاکت آفرزیس، Fresenius COM.TEC است. این دستگاه بر اساس سانتریفیوژ جریان متناوب (IFC) به جداسازی پلاکت از سایر اجزای خونی میپـردازد، در این روش خون پس از تکمیل فرآیند جداسازی بـه بدن اهداکننده باز میگردد. خون در فرآیند جداسازی با استفاده از پمپهای مختلف نظیر پمپ خون، پمپ ضد انعقاد، پمپ وریـد و پمپ جمعآوری در ست دستگاه به جریان میافتد. پس از سانتریفیوژ، پلاکتها جدا شده و در نهایت فرآورده پلاکتی حاصل در کیسه پلاکت جمعآوری میگردد و سایر سلولها به همراه پلاسما به بدن اهداکننده بازگردانده میشود. لذا در این مطالعه به بررسی تعداد پلاکتها، MTT ، LDH و pH در پلاکتهای تهیه شده توسط دستگاه Fresenius COM.TEC در طول مدت ذخیرهسازی پلاکتها پرداخته شد.
مواد و روشها
در ایـن مطالعـه تجربی، از واحدهای پلاکت آفرزیس حاصل ازدستگاه Fresenius COM.TEC که در اداره کل انتقال خون استان تهران در بخش اهدا تهیه شده بود، استفاده گردید. از اهداکنندگان داوطلب، رضـایتنامه آگاهانـه جهـت استفاده از محصول نهایی پلاکت آفرزیس در کار تحقیقاتی گرفته شد. معیار ورود اهداکنندگان به این مطالعه، افراد کـاملاً سالم با هموگلوبین بیش از 5/12 گرم در دسیلیتر، وزن اهداکننده بیش از ۵۰ کیلـوگرم، هماتوکریـت بیش از 38%، آزمایشهای منفی HIV، HBsAg ،HCV و RPR ، گـذشت حداقل ۳ ماه پس از اهدای خون کامل و حداقل ۳ روز پس از آخرین اهدای پلاکت و دسترسی کافی به وریدهای اهداکننده با رعایت دستورالعملهای سازمان انتقال خون ایران بودند.
معیارهای خروج شامل مصرف داروهای ضد التهاب غیر استروئیدی (NSAIDs) مانـند آسپرین، ایبوپروفن، نـاپروکسن، دیکلوفناک و غیره و ابتلا به بیماری زمینهای بودنـد. نمونهگیری از فرآورده پلاکتی حاصل ازدستگاه Fresenius COM.TEC (Fresenius HemoCare GmbH آلمان) صورت گرفت.
پارامترهای تنظیم شده در دستگاه Fresenius COM.TEC شامل: جریان خون کامـل 75-50 میلیلیتر در دقیقه، نقطه تنظیم رابط 33 و ضد انعقاد خون به کـل خون 1: 9 بود. اطلاعات زیر شامل وزن اهداکننده، جنس، قد، سطح هموگلوبین و میزان پلاکت قبل از آفرزیس به دستگاه داده میشد. میزان برداشت هدف پلاکت (Target PLT yield) به میزان (1011 ×5-3) تعیین شد.
در هر آفرزیس ،دو کیسه فرآورده پلاکت آفرزیس تهیه میگردید که یک کیسه با حجم250 میلیلیتر جهت تزریق به بیمار به بیمارستان ارسال میشد. کیسه دیگر برای بررسی و انجام آزمایشهای مطالعه، بـا حجم حدود 50 میلیلیتر تهیه گردید. همه کیسههای دریافت شده با حجم حـدود 50 میلیلیتر جهت انجام آزمایشها به مرکز تحقیقات انتقال خون منتقل شد. به هرکدام ازکیسههای آفرزیس تهیه شده ابتدا لیبل خاصی چسبانیده و سپس در شیـکر انکوباتور در آزمایشگاه مرکز تحقیقات سازمان انتقال خون با دمای مشخص 2 ± 22 درجه سانتیگراد با حرکت دورانی ملایم rpm 60 نگهداری شدند و در روزهای 1،3،5 کیسههای پلاکت آفرزیس از نظر ظاهری و swirling مورد بررسی قرار گرفتند. Swirling(یـا چرخش) با بررسی کیسههای حاوی پلاکت در برابر نور ارزیابی و به صورت زیر امتیازدهی شد:
امتیاز ۰: همگن کدر است و با فشار تغییر نمیکند.
امتیاز ۱: همگن فقط در قسمتی از کیسه میچرخد و شفاف نیست.
امتیاز ۲: چرخش همگن واضح در تمام قسمتهای کیسه.
امتیاز ۳: چرخش همگن بسیار واضح در تمام قسمتهای کیسه (10). پس از تـایید سلامت و طبیعی بودن رنگ و swirling، برای انجـام آزمـایشهای مورد نظر در روزهای 1،3،5 ذخیرهسازی ، حدود 10 میلیلیتر از فرآورده از طریق کورد کیسه، به لوله فالکون استریل منتقل شد. فرآوردههای منتقل شده به فالکون جهت بررسی از نظر شمارش پلاکت، نمونهها با PBS به نسبت 1 به 5 رقیق شده و سپس، به دستگاه سل کانتر KX1000 SYSMEX داده شد تا از نظر تعداد پلاکت شمارش شوند. سپس الکترودهای دستگاه pH متر (Herisau ، pH lab 827 Metrohm سوئیس) با استفاده از آب دیونیزه شسته و با گاز استریل آبگیری شد و در نهایـت در محلول pH خنثی (7 pH=) کالیبره گردید و بعد از اطمینان از صحت دستگاه و خوانش درست، pH نمونهها با دستگاه pH متر در هر سه روز ذخیرهسازی اندازهگیری شد. برای بررسی و تشخیص آسیب سلولی و تعیین میزان آن، آزمایش لاکتات دهیدروژناز (LDH) برای کیسهها انجام شد. 500 میکرولیتر از نمونه پلاکتی از فالکون استریل به میکروتیوب منتقل و سپس با دور rpm 4000 به مدت 10 دقیقه سانتریفیوژ شد. در هر سه روز 1، 3 و 5 ، فعالیت آنزیم LDH با استفاده از کیت شرکت دلتا درمان پارس بر اساس واکنش تبدیـل لاکتـات بـه پیـروات که توسط آنزیم LDH کاتـالیز میشود، توسط دستگاه کوباس ECL COBAS E411 اندازهگیری گردیـد. برای بررسی زندهمانی سلولها، از روش 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl-2H-tetrazolium bromide (MTT) استفاده شــد.
در ایـن روش، ابتدا حـدود 107× 1سلول در 100 میکرولیتر پلاکـت آماده شد و به چاهکهای پلیت منتقل گردیـد و سپس 10 میکرولیتر از محلول فرمازون (Sigma-Aldrich,USA) به هر چاهک اضافه شد و به مدت 4 ساعت در انکوباتور CO2 انکوبه گردید. پس از طی مدت انـکوبـاسیون، معرف DMSO (دی متیل سولفوکسید)(مرک، آلمان) را به مقدار 100 میکرولیتر بـه نمونهها اضافه کرده و سپس 10 دقیقه در انکوباتور CO2 انکوبـه شد. بعد از طی مدت زمان انکوباسیون، نمونهها در طول موج 570 نـانومتر توسط الایزا ریـدر (کارخانجات تولیدی نورهان فجر Elisa reader multiskan-thermo fisher scientific ، آمریکا) خوانده شد.
آزمون آماری:
به منظور محاسبه حجم نمونـه در این طرح از نرمافزار G*power استفاده شد. در این نرمافزار با در نظر گرفتن آزمون repeated measure تحت فرض سطح معناداری 05/0 و توان ۸۰ درصد و یـک اندازه اثر (effect size f=0.17) ، حداقل حجم نمونه برابر ۲۵ محاسبه گردید.
بـا توجه به توزیع طبیعی، دادههای حاصل از آزمایشها در نرمافزار R وارد و میانگین و انحراف معیار و p-value بـا مدلLinear regression در روزهای مختلف ذخیرهسازی (1،3،5) محاسبه گردید. p-value کمتر از 05/0 معنادار در نظر گرفته شد.
یافتهها
25 فرآورده پلاکت حاصل از دستگاه Fresesnius COM.TEC در روزهای ذخیرهسازی (1،3،5) بررسی گردید. پلاکتهای آفرزیس از نظر ظاهری و swirling در روزهای ذخیرهسازی اول و سوم امتیاز 2 و 3 را گرفتند. میانگین نتایج شمارش پلاکت در روز 1 ذخیرهسازی فرآوردههای پلاکت آفرزیس حاصل از دستگاه Fresesnius ، COM.TEC /µL103×920/151 و در روز 3 ذخیرهسازی /µL103×640/153 و همچنین در روز پنجم /µL103 ×159 بود. تفاوت معناداری از روز اول تا پنجم در تعداد پلاکت مشاهده نشد. تغییرات pH در روز 1 ذخیرهسازی 63/7 و در روز 3 ، 30/7 و در روز 5، 89/6 دیده شد (0001/0 p<) (نمودار 1)(جدول 1).
میانگین زنـدهمانی پلاکتها با آزمایـش MTT در روز 1
ذخیرهســـازی40/1 در روز 3، 51/1 و در روز 5، 05/1 بود
(0001/0 p<). میــانگیـن میـزان LDH نیـــــز در روز 1،
Unit/L 2/194 ، در روز 3، Unit/L 12/378 و در روز 5،
Unit/L 92/517 به دست آمد (0001/0 p<).


در این مطالعه پلاکتهای آفرزیس حاصل از دستگاه Fresenius COM.TEC از نظرظاهری و swirling در روزهای ذخیرهسازی امتیاز 2 و 3 و سپس 1 را گرفتند. در شمارش PLt این فرآوردههای پلاکت فرزیس تفاوت معناداری در روزهای 1 ، 3 و 5 ذخیرهسازی مشاهده نشد، اما نتایج آزمـایشهای pH ، LDH و MTT در روزهای ذخیرهسازی معنادار بود (0001/0 p<).
Swirling و ارزیابی چرخش یک روش ساده و غیر تهاجمی برای بررسی پلاکتها است که به صورت بصری انجام میشود و برای کنترل کیفی معمول هر پلاکـت و در مقیاس بزرگ مفید است. بررسی بصری swirling بـا مورفولوژی پلاکـت مرتبط است؛ وجود آن نشاندهنده مورفولوژی دیسکوئید و عدم وجود آن نشاندهنده مورفولوژی کروی پلاکتها است (10). سینگ و همکـاران نمره 3 swirling را در 7/79%، 9/83% و 90% از واحدهای پلاکـت مشاهده کردند، در حالی که امتیاز 2 به ترتیب به 3/20 %، 1/16 % و 10% از واحـدهای PRP-PC ، BC-PC و apheresisPC داده شد. آنها در هیچ واحدی امتیاز یک را در روز اول تهیه مشاهده نکردند (10). برتولینی و همکاران در مطالعه خود گزارش کردند که پلاکتهای تـازه در 83% از واحـدها swirling مثبت و تنها در 2% منفی بوده و بقیه swirling متوسط داشتند. پس از ۵ روز نگهداری، میزان swirling پلاکتهای مثبت 65% کاهش یافت و برتولینی نتیجه گرفت که این کاهش میتوانـد به دلیل آسیبهایی باشد که در طول نگهداری پلاکـتها رخ میدهند (11). در مطالعه ما واحـدهای پلاکت در روز اول امتیاز 3 داشتند که در روز پنجم امتیاز هیچکدام به 0 نرسید.
فعالیت متابولیک فرآوردههای پلاکت فرزیس عمدتاً بـا pH ، pCO2 ، pO2 ، بیکربنات، گلوکز و لاکتات بررسی میشود. متابولیسم پلاکتها در خارج از بـدن و حین نگهداری در دمای ˚C2±22 تغییر میکند و سبب تغییراتی در pHمیشود (12). اگر pH به کمتر از 8/6 نرسد، حجم پلاکت در طول سه روز تقریباً 10% کاهش مییـابد. در میزان pH کمتر از 8/6 تورم سلولها شروع میشود و در 0/6pH= به حداکثر خود میرسد. اگر pH از این سطح پـایینتر بیاید، افزایش تدریجی حجم پلاکـت و کاهش چگالی دیده میشود که نشاندهنده تورم بـه دلیل ورود مایع خارج سلولی است. در 0/6pH= ، حجم پلاکت تقریباً دو برابر شده و سرعت تبدیل دیسک به کره افزایش مییابد. بـه طوری که اگر pH به 7/5 تا 9/5 برسد، فقط کرههای متورم دیده میشوند. اگر pH بالاتر از 1/6 بمانـد، این تغییرات تقریباً به طور کامل برگشتپذیر هستند، اما اگر pH به زیر 1/6 برسد، قابل برگشت نیستند. گلبولهای سفید خون در محیط کشت PC اثر مخربی دارند و منجر بـه کاهش قابل توجه pH، افزایش مصرف گلوکز، تولید اسید لاکتیک و آزادسازی LDH در طول نگهداری میشوند. pH در طول ذخیرهسازی بسته به محلولهای موجود در کیسههای پلاستیکی نگهداری پلاکت و شرایط ذخیرهسازی کـاهش مییابد. افزایش گلیکولیز پلاکت منجر بـه کاهش pH به سطوح نزدیک به 0/6 در پلاکتهای ذخیره شده در پلاسما میشود و با از دست دادن قابل توجه قابلیت حیات پلاکـتها همراه است (10). در مطالعه ما تغییرات میانگین pH در روز 1 ذخیرهسازی 63/7 و در روز 3 ، 30/7 و در روز 5، 89/6 دیـده شد که به کمتر از 8/6 نرسید (0001/0 p<).
آزمایش دیگری که برروی فرآوردههای پلاکت انجام شد LDH بود که افزایش آن را در روزهای نگهداری (1،3،5) مشاهده کردیم. پروچازکوا و همکاران بر روی دو دستگاه Trima و MCS مطالعهای انجـام دادند. آنها نیز افزایش LDH را در طی روزهای ذخیرهسازی (1،3،5) در هر دو دستگاه مشاهده نمودند که با میزان pH رابطه عکس داشت. آنها افزایش LDH را در روز 5 در فرآورده حاصل از دستگاهMCS به طور معناداری بیشتر گزارش کردنـد. سرکوب چرخه کربس در میتوکندری و انباشت اسید کربنیک در سیتوپلاسم حاصل از چرخه گلیکولیز سبب کاهش pH میشود و افزایش LDH هم میتوانـد به دلیل ادامه روند گلیکولیز در سیتوپلاسم سلولهای پلاکت باشد (13). ما نیز کاهش میزان pH و افزایش میانگین LDH در روزهای نگهداری پلاکت را مشاهده کردیم (0001/0 p<).
ماچر و همکاران در سال 2010 به بررسی فرآوردههای حاصل از دستگاهها Amicus وTrima پرداختند، آنها نیز افزایش LDH و کاهش pH در روزهای ذخیرهسازی را همانند مطالعه ما و تحقیق پروچازکوا گزارش نمودنـد و این موضوع را متأثر از جنس کیسه و تبادل مناسب اکسیژن دانستند (14). بر اساس نتایج حاصل از مطالعه اکسیا و همکاران، ازدست دادن میزان زنده ماندن سلولها (cellular viability) بـا افزایش LDH و لاکتات در کیسه، کـاهش pH و طیف وسیعی از پدیدههای متابولیکی دیگر مرتبط است. این تغییرات همراه بـا تغییرات مورفولوژیکی در پلاکتها رخ میدهد کـه پارامترهای متابولیکی را بدتر میکند (15). برای معکوس کردن این تغییرات از کیسههایی که امکان تبادل بهتر و مؤثرتر گاز در هنگام ذخیرهسازی در دمای 22 تا 24 درجه سانتیگراد را فراهم میکنند و از ضد انعقادهای بهتر برای کـاهش میزان فعال شدن پلاکت در خـارج از بدن استفاده کردهاند (15). اکسیا و همکاران برای بررسی فعالیت متابولیک سلولها از آزمایشهای MTT و LDH بـا روش اسپکتروفتومتریـک استفاده کردند. آنها فعالیت متابولیکی پنج جفت پلاکـت را با استفاده از روش MTT در فواصل زمانی مختلف سنجیدند و به یکی از آنها PEG-rHuMGDF برای بررسی تأثیر TPOبر زندهمانی پلاکتها اضافـه کردند. پلاکتها فعالیت متابولیکی طبیعی خود را برای 6 روز اول ذخیرهسازی حفظ کردند و سپس در طول مدت ذخیرهسازی بعدی، کاهش تدریجی و خطی در فعالیت متابولیکی داشتند. بـا این حال، در هیچ زمانی هیچ تـأثیری از وجود PEG-rHuMGDF مشاهده نشد. تغییرات MTS و MTT در کیسههای پلاکت در طول ذخیرهسازی بـه موازات تغییرات pH و LDH بود (15). در مطالعه ما نیز آزمایش MTT در روز 5 نسبت بـه روز 1 کاهش داشت. این کاهش در نتایج حاصل از MTT میتواند نشانهای از مرگ بیشتر پلاکتها در روز 5 ذخیرهسازی نسبت به روز اول باشد. ولی در روز سوم افزایش در میزان آزمایش دیده شد که میبایستی عوامل مخدوشکننده این آزمایش را درنظر گرفت. علیرغم کـاربردهای گسترده این آزمایش در طی چهار دهـه گذشته، روش MTT اغلب بدون توجه به مکانیسمهای اساسی و محدودیتها آن، تفسیر و استفاده میشود. مکانیسم بنیادی آزمایش MTT ، ]3-(4،5-دی متیل تـیازول-2-ایـل)-2،5-دی فنیل-2H-تترازولیوم برومایـد[ یک نمک مونو تترازولیوم است که از یک هسته حلقه تترازول چهارتایی با بار مثبت حاوی چهار اتم نیتروژن احاطه شده توسط سه حلقه آروماتیک شامل دو بخش فنیل و یک حلقه تیازولیل تشکیل شده است. احیای MTT منجر به اختلال در حلقه تترازول مرکزی و تشکیل یک مولکول نامحلول در آب به رنگ آبی- بنفش به نام فورمازان میشود. معرف MTT میتواند از غشای سلولی و همچنین غشای داخلی میتوکندری سلولهـای زنده (احتمالاً به دلیل بار مثبت آن و همچنین ساختار لیپوفیلی آن) عبور کند و توسط سلولهای فعال متابولیکی به فورمازان احیا شود. این سنجش به عنوان یک سنجش فعالیت متابولیک سلولی کاربرد گستردهای دارد. بـا این حال، کاربرد آن به طور فزآیندهای برای استنباط فرآیندهای ثـانویه یا حالتهای سلولها، مانند زندهمانی، که اغلب بیاساس است، به کار گرفته شده است. محل تشکیل فورمازان و انتقال درون سلولی آن همچنان بحثبرانگیز است. مطالعههای بیوشیمیایی و میکروسکوپی، فورمازان را در اندامکهای مختلف درون سلولی (در شبکه آنـدوپلاسمی، قطرات لیپیدی سیتوزولی، غشاهای پلاسما، هسته و میکروزومها) پیدا کردهاند. مطالعههای متعدد محدودیـتهای سنجش MTT و عـوامل مخدوشکننده مختلفی را آشکار کردهاند. برخی از متغیرهای مخدوشکنندهای که معمولاً نادیده گرفته میشوند شامل تعداد سلولهای کشتشده، غلظت معرف، MTT اضافه شده به سلولها، زمان انکوباسیون سلولها بـا MTT ، نوع محیط کشت، حـذف مایع رویی سلولها پس از انکوباسیون MTT و طول موجی کـه در آن چگالی نوری اندازهگیری میشود، هستند. افزایش تعداد سلولها، سطح کل فورمازان تولید شده توسط جمعیت سلولی و در نتیجه OD اندازهگیری شده را افزایش میدهد. برای ارزیابی زندهماندن سلولها، بـاید آزمایشهای کنترلی دقیقی به عنوان وسیلهای برای تعیین چگونگی تـأثیر پارامترهای ذکر شده بر رابطه بین OD اندازهگیری شده و تعداد سلولها انجام شود. سطح OD صرفاً یـک نمایش ساده از یک پارامتر مانند زندهماندن سلول، تکثیر سلولی یا فعالیت متابولیک نیست، بلکه مجموعهای از عوامل بسیاری در سطح تک سلول و جمعیت سلولی و همچنین سایر عوامل سلولی مانند فاز رشد سلولی و میزان جذب MTT و خروج فورمازان است که همگی میتوانند به طور بالقوه آزمایش/محیط کشت را تحت تاثیر قرار دهد. این پیچیدگی حتی میتوانـد باعث نتایج مثبت کاذب در هنگام آزمایش بـا استفاده از سنجش MTT شود (16). بنابراین با توجه به آن که تعداد سلول/تراکم و غلظت MTT بر میزان تشکیل فرمازان تـأثیر میگذارد، بهینهسازی دقیق شرایط سنجش متناسب با ردههای سلولهای خاص و استفاده از کنترلهای مناسب همانند بررسی اگریگومتری، فلوسیتومتری و نشانگرهای آپوپتوز از محدودیتهای مطالعه ما به شمار میرود.
حسین و همکـاران در سـال 2015 بــه بررسی تغییرات
شمارش پلاکتی در روزهای 1، 3، 5 و 7 ذخیرهسازی پرداختند. آنها فرآوردههای پلاکتی محصول دستگاه Cobe spectra را بررسی کردند. در مطالعه آنها 16 نفر، به تعداد 9 مرد و 6 زن پلاکت اهدا کردند. در مطالعه آنها شمارش پلاکـت در روزهای ذخیرهسازی رونـد کاهشی داشت (17). اما برخلاف تحقیق حسین و همکاران، نتایج حاصل از مطالعه ما تغییرات چشمگیر و معناداری در شمارش پلاکت در روزهای ذخیرهسازی نشان نداد که میتواند به این دلیل بـاشد که آنها روز 7 را نیز در مطالعه خود گنجانیده بودند و ما تا روز 5 میزان پلاکـتها را بررسی کردیم. در مطالعه تین گارد و همکاران در سال 2008 که به بررسی تفاوت فرآوردههای حاصل از دو دستگاه cobe Spectra و Trima Accel بر روی 20 پلاکت آفرزیس (از هر دستگاه 10 فرآورده پلاکـت آفرزیس) در روز های 0، 1، 3، 5 و 7 پرداختند، نیز مشاهده شد. در نتایج حاصل از این مطالعه گزارش کردنـد که تغییرات تعداد پلاکت در هر دو دستگاه در طی روزهای ذخیرهسازی ثـابت بود ولی میانگین حجم پلاکت MPV( mean platelet volume) در روز 1 نسبت به روز 0 روند کاهشی داشت، ولی در سایر روزها در این پارامتر هم تغییراتی دیـده نشد. آنها نتیجهگیری کردند که کیفیت پلاکـت پس از ذخیرهسازی به مدت ۷ روز به خوبی حفظ شده بود، اگر چـه فعالشدن پلاکتهـا را در طول ذخیرهسازی، توسط آزمایشهای pCO2 ، pO2 و pH در گازهای خون، و مارکرهـای سطح پلاکـت GPIb (CD42b) and P-selectin (CD62P) در فلوسیتومتری مشاهده کردند و هیچ تفاوتی در کیفیت پلاکـت بین PCهای تولید شده توسط دو دستگاه Spectra و Trima گزارش نکردند (18). در مطالعه ما تفاوت معناداری در شمارش پلاکت فرآوردههای پلاکت فرزیس حاصل از دستگاه Fresenius COM.TEC در روزهای 1، 3 و 5 ذخیرهسازی مشاهده نشد. اگر چه تین گارد و همـکاران متغیرهای مختلف متابولیک همانند میزان قند، لاکتات، گـازهای خونی، میزان Soluble P-selectin در پلاسما، مارکرهای سطح پلاکت ،Clotting time and coagulum G و hypotonic shock response (HSR) را نیز بررسی کردند.
گلبولهای سفید خون در فرآورده پلاکت اثر مخربی بر محیط ذخیرهسازی دارند و منجر به کاهش قابل توجه pH، افزایش مصرف گلوکز، تولید اسید لاکتیک و آزادسازی LDH در طول ذخیرهسازی میشوند. در نتیجه، در فرآورده پلاکتی کـه غلظت بالایی از لکوسیتها دارند، وضعیت پلاکتهـا تا روز 5 ذخیرهسازی نیز به طور قابل توجهی تحت تـأثیر قرار میگیرد که با دفع بالای β-TG، از دست دادن نوکلئوتیدهای پلاکتی، کـاهش توانایی ترکیب آدنوزین 3 فسفات و مورفولوژی ضعیف پلاکتها نشان داده میشود (19).
در مطالعه تورا و همکاران میزان pH در فرآوردههای آفرزیس در روز 5 نگهداری 16/0 ± 89/6 گزارش شده بـود و در مطالعه ما نیز pH در روز 5 ، 46/0 ± 89/6 بـه دست آمد. آنها بر روی ۶۶۹ فرآورده پلاکتی آفرزیس مطالعه کردنـد که از این تعداد ۴۶۰ واحد آفرزیس تحت بررسی آزمایشگاهی و کنترل کیفیت قرار گرفت. نتایج حاصل از pH در مطالعه آنها نشان داد که بر اساس جنس کیسهها و شرایط نگهداری، میزان pH کاهش مییابد که این کـاهش متأثر از شرایط نامناسب فیزیولوژیک در اثر افزایش ذخیرهسازی برای پلاکتهای تهیه شده در هر سه روش رندوم دنور، آفرزیس و بافیکوت بود (19).
محدودیتهای مطالعه حاضر، عدم بررسی تمامی موارد کنترل کیفی و بررسی روشهــای پیشــرفتهتــر ارزیــابی کیفیـت پلاکت، آزمـایشهـایی از قبیـل انـدازهگیـری فعالیـت آنها بـه وسـیله بیـان مارکرهـایp62 CD و 63CD با روش فلوسیتومتری واگریگومتری، بهینهسازی دقیق شرایط سنجش MTT بر روی فرآورده پلاکت آفرزیس حاصل از دستگاه Fresenius COM.TEC است و بهتر بود سایر موارد کنترل کیفی همانند حجم واحد آفرزیس، تعداد WBC، تعداد RBC و استریلیتی، هم بررسی و همچنین مقایسهای بین دستگاههای مختلف آفرزیس با هم انجام میشد.
نتیجهگیری
بررسیهای آزمایشگاهی برروی فرآوردههای حاصل از دستگاه آفرزیـس Fresesnius COM.TEC در روزهای ذخیرهسازی نشان داد که میتوان از این دستگاه تهیه پلاکت نیز استفاده کرد. برای تفسیر نتایج MTT محدودیتهای آن را بایستی در نظر گرفت و از کنترلهای مناسب دیگر نیز بهره برد.
حمایت مالی
این پروژه توسط مرکز تحقیقات انتقال خون، مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ایران تأمین مالی شده است.
ملاحظات اخلاقی
مطالعه حاضر دارای کد اخلاق IR.TMI.REC.1402.009 از کمیته اخلاق مؤسسه عالی آموزشی و پژوهشی طب انتقال خون تهران ، ایران است.
عدم تعارض منافع
نویسندگان اظهار میکنند هیچگونه تعارض منافعــی در
این مطالعه وجود نداشته است.
نقش نویسندگان
اله آشوری کفشگر: انجام مراحل عملی، تجزیه و تحلیل و تفسیر نتایج، تهیه پیشنویس مقاله
دکتر آزیتا چگینی: مدیریت و طراحی مطالعه، تفسیر نتایج و بازبینی، تهیه و اصلاح پیشنویس مقاله
شهرام سمیعی: طراحی مطالعه، انجام مراحل عملی و تهیه پیشنویس مطالعه
دکتر مریم زادسر: تجزیه و تحلیل، تفسیر نتایج، تهیه پیشنویس مقاله
تشکر و قدردانی
این مقاله نتیجه پایاننامه دانشجویی کارشناسی ارشد رشته زیست فناوری پزشکی مرکز تحقیقات مؤسسه عالی آموزشی و پژوهشی طب انتقال خون میبـاشد. تهیه فرآورده از پایگاه انتقال خون تهران و مراحل پروژه در آزمایشگـاه مرکز تحقیقات انجام گردیـد. بدین وسیله از پرسنل زحمتکش اداره کل انتقال خون تهران و مرکز تحقیقات تشکر و قدردانی بـه عمل میآید.
نوع مطالعه: پژوهشي |
موضوع مقاله:
بيوتكنولوژي
فهرست منابع
1. Rinder HM, Tomer A. Platelet production, kinetics , and hemostasis. In: Simon TL, Snyder EL, Solheim BG, Stowell ChP, Strauss RG, Petrides M. Rossi's Principles of Transfusion Medicine. 4th ed. USA: Blackwell Publishing; 2009. p. 149-67. [DOI:10.1002/9781444303513.ch10]
2. Rinder HM, Tomer A. Platelet production, kinetics, and hemostasis. Rossi's Principles of Transfusion Medicine. 2009 Jan 9:149-67. [DOI:10.1002/9781444303513.ch10]
3. Ribatti D, Crivellato E. Giulio Bizzozero and the discovery of platelets. Leuk Res 2007; 31(10): 1339-41. [DOI:10.1016/j.leukres.2007.02.008] [PMID]
4. Javadzadeh Shahshahani H, Akhavan Tafti F, Amini Kafi‐abad S. An overview of three methods used to prepare the platelet components from whole blood and apheresis method. Sci J Iran Blood Transfus Organ 2023; 20(3): 236-54. [Article in Farsi]
5. Hillyer CD, Silberstein LE, Ness PM, Anderson KC, Roback JD. Blood Banking and Transfusion Medicine: Basic Principle and Practice. 2nd ed. USA: Churchill Livingstone; 2007. p.735-6.
6. McLeod BC, Weinstein R, Winters JL, Szczepiorkowski ZM. Apheresis: Principles and Practice. 3rd ed. USA: AABB; 2010. p. 2-23.
7. Smith J, Burgstaler E. Blood component collection by apheresis. In: Roback JD, Combs MR, Grossman BJ, Hillyer ChD. Technical Manual. 17th ed. USA: AABB; 2008. p. 227-38.
8. Chegini A, Mirrezaie M, Poorreza M, Rezaie A, Anbardan A. Assessment of plateletphersis donation in Tehran Blood Center. Sci J Iran Blood Transfus Organ 2013; 10(2): 140-6. [Article in Farsi]
9. Sadeghi Neysiyani S , Amini-Kafiabad S. The effect of different types of plateletpheresis devices on the quality parameters of the produced platelet units. Sci J Iran Blood Transfus Organ 2024; 21(2): 169-84. [Article in Farsi]
10. Singh RP, Marwaha N, Malhotra P, Dash S. Quality assessment of platelet concentrates prepared by platelet rich plasma-platelet concentrate, buffy coat poor-platelet concentrate (BC-PC) and apheresis-PC methods. Asian J Transfus Sci 2009; 3(2): 86-94 [DOI:10.4103/0973-6247.53882] [PMID] []
11. Bertolini F, Rebulla P, Riccardi D, Cortellaro M, Ranzi ML, Sirchia G. Evaluation of platelet concentrates prepared from buffy coats and stored in a glucose‐free crystalloid medium. Transfusion 1989; 29(7): 605-9. [DOI:10.1046/j.1537-2995.1989.29789369678.x] [PMID]
12. Sadeghi Neysiyani S, Amini Kafi-Abad S. The effect of different types of plateletpheresis devices on the quality parameters of the produced platelet units. Sci J Iran Blood Transfus Organ 2024; 21(2): 169-84. [Article in Farsi]
13. Procházková R, Andrýs C, Hubáčková L, Krejsek J. Markers of platelet activation and apoptosis in platelet concentrates collected by apheresis. Transfus Apher Sci 2007; 37(2): 115-23. [DOI:10.1016/j.transci.2007.03.015] [PMID]
14. Macher S, Sipurzynski‐Budrass S, Rosskopf K, Rohde E, Griesbacher A, Groselj‐Strele A, et al. Function and activation state of platelets in vitro depend on apheresis modality. Vox Sang 2010; 99(4): 332-40. [DOI:10.1111/j.1423-0410.2010.01353.x] [PMID]
15. Xia Y, Li J, Bertino A, Kuter D. Thrombopoietin and the TPO receptorduring platelet storage. Transfusion 2000; 40(8): 976-87. [DOI:10.1046/j.1537-2995.2000.40080976.x] [PMID]
16. Ghasemi M, Turnbull T, Sebastian S, Kempson I. The MTT assay: utility, limitations, pitfalls, and interpretation in bulk and single-cell analysis. Int J Mol Sci 2021; 22(23): 12827. [DOI:10.3390/ijms222312827] [PMID] []
17. Hussein E. Clinical and quality evaluation of apheresis vs random‐donor platelet concentrates stored for 7 days. Transfus Med 2015; 25(1): 20-6. [DOI:10.1111/tme.12187] [PMID]
18. Tynngård N, Lindahl TL, Trinks M, Studer M, Berlin G. The quality of platelet concentrates produced by COBE Spectra and Trima Accel cell separators during storage for 7 days as assessed by in vitro methods. Transfusion 2008; 48(4): 715-22. [DOI:10.1111/j.1537-2995.2007.01610.x] [PMID]
19. Toora E, Kulkarni RG, Manivannan P, Sastry AS, Basavarajegowda A, Sahoo D. Quality assessment of platelet concentrates prepared by platelet-rich plasma, buffy-coat, and apheresis methods in a tertiary care hospital in South India: A cross-sectional study. Asian J Transfus Sci 2023; 17(2): 239-45. [DOI:10.4103/ajts.ajts_73_22] [PMID] []
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







