جلد 22، شماره 4 - ( زمستان 1404 )
جلد 22 شماره 4 صفحات 326-316 |
برگشت به فهرست نسخه ها
Ethics code: (IR.YUMS.REC.1404.116)
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Sabz G, Rad F, Saraei A. The Relationship of Serum Ferritin Levels and Age with Hearing Disorders in Patients with Beta-Thalassemia Major. bloodj 2025; 22 (4) :316-326
URL: http://bloodjournal.ir/article-1-1600-fa.html
URL: http://bloodjournal.ir/article-1-1600-fa.html
سبز غلام عباس، راد فریبا، سرائی عاطفه. ارتباط بین سطح فریتین سرم و سن در بیماران بتا تالاسمی ماژور شهر یاسوج با اختلالات شنوایی. فصلنامه پژوهشی خون. 1404; 22 (4) :316-326
دانشیار گروه علوم پایه دانشکده پزشکی دانشگاه علوم پزشکی یاسوج
متن کامل [PDF 626 kb]
(91 دریافت)
| چکیده (HTML) (180 مشاهده)
مقدمه
تالاسمی ماژور یک اختلال هماتولوژیک ارثی است که با بروز کمخونی شدید تظاهر مییابد. در حال حاضر، درمان استانـدارد حمایتی برای این بیماری، انتقال خون منظم است که با تغییر سیر بیماری از یک وضعیت کشنده در دوران کودکی بـه یک بیماری مزمن، سبب افزایش قابل توجه امید به زندگی بیماران شده است. با این حال، این درمان نجاتبخش، به دنبال تجمع پیشرونده آهن در بدن و عدم وجود مکانیسم فیزیولوژیک کارآمد برای دفع آن، منجر بـه بروز چالش عمدهای در مدیریت بیماران تحت عنوان افزایش بار آهن گردیده است (2، 1).
در شرایط گرانباری آهن، آهن اضافی در اندامهای حیاتی مختلف از قبیل قلب، کبد، غدد درونریز و سیستم عصبی رسوب کرده و موجب ایجاد آسیبهای جدی در عملکرد این اندامها میشود. برای پایش بار آهن در این بیماران، از فریتین سرم به عنوان معیار استاندارد استفاده میگردد که سطح مطلوب آن معمولاً کمتر از ۱۰۰۰ نانوگرم بر دسیلیتر توصیه میشود (3، 2).
به منظور مقابله با این چالش، درمان با شلاتورهای آهن (Iron Chelators) از حدود شش دهه پیش آغاز شده است. اگر چه داروهای شلاتور در دو نسل قدیم (مانند دسفرال یا دفروکسامین) و جـدید (مانند دفریپرون و دفرازیروکس) نقش حیاتی در افزایش طول عمر بیماران ایفا کردهاند، اما با طیف وسیعی از عوارض جانبی بالقوه همراه هستند. یکی از عوارض مهم و نسبتاً شایع این داروها که تأثیر مستقیمی بر کیفیت زنـدگی بیماران دارد، اختلال در عملکرد شنوایی است (4).
کاهش شنوایی (که کاهش حساسیت سیستم ادراک صوتی تعریف میشود) در بیماران مبتلا به تالاسمی ماژور یک عارضه چند عاملی محسوب میشود (5). بر اساس پاتوفیزیولوژی و محل وقوع آسیب در مسیر شنوایی، به انواع مختلفی تقسیمبندی میگردد که عبارتند از: کاهش شنوایی حسی- عصبی (Sensorineural Hearing Loss - SNHL) که ناشی از آسیب به سلولهای مویی حساس در حلزون گوش داخلی یا اعصاب مرتبط با مسیر شنوایی است و معمولاً دائمی و غیر قابل بازگشت میباشد. این نوع کاهش شنوایی به طور خاص با سمیت نـاشی از شلاتورهای آهن، به ویژه دفروکسامین (که معمـولاً بـه صـورت SNHL دو طرفـه در فرکـانسهای بالا بروز میکند) و همچنین با تجمع آهن در
سیستم عصبی مرتبط دانسته شده است. اگرچه شلاتورهای خوراکی نسل جدید مانند دفریپرون و دفرازیروکس ایمنتر به نظر میرسند، اما همچنان نیاز به پایش منظم شنوایی دارند (6، 5). کاهش شنوایی انتقالی (Conductive Hearing Loss - CHL) بـه دنبال موانع موجود در انتقال صوت از مجرای گوش خارجی به گوش داخلی رخ میدهد که میتواند ناشی از آسیب بـه پرده گوش، استخوانچههای گوش میانی یا عملکرد نادرست شیپور استاش باشد. همچنین نوع سوم تحـت عنوان کاهش شنوایی مختلط (Mixed Hearing Loss) شناخته میشود که ترکیبی از هر دو نوع حسی-عصبی و انتقالی است (6، 5). مطالعهها گزارش دادند که کاهش شنوایی در بیماران بتا تالاسمی ماژور در مقایسه با جمعیت عمومی بالاتر است. به عنوان مثال، در داخل ایران، میانگین کاهش شنوایی در این بیماران حدود 20% گزارش شده است، در حالی که این رقم در جمعیت کلی حدود 10%-7% برآورد میشود. یک مطالعه متا آنالیز اختلالات شنوایی در بیماران تالاسمی را حدود 3/20 % گزارش کرده است که این رقم اهمیت موضوع را به وضوح نشان میدهد (8، 7).
اگر چه برخی مطالعهها ارتباط معناداری بین سطح فریتین سرم و شدت SNHL گزارش کردهاند، اما سایر پژوهشها چنین رابطهای را به صورت قطعی تأیید نکردهاند (10، 9). علاوه بر سمیت دارویی و بار آهن، عوامل دیگری مانند کمکاری تیروئید، دیابت و کمخونی مزمن نیز میتوانند در بروز اختلال شنوایی در این بیماران نقش داشته باشند (12، 11). مطالعههای تصویربرداری پیشرفته مانند PET هایپوپرفیوژن (کاهش خونرسانی) در قشر شنوایی بیماران تالاسمی را نشان دادهاند که میتواند به عنوان یک نشانگر متابولیک مطرح باشد و ارتباط بین تجمع آهن و اختلال عملکرد عروقی مغز را تأیید کند (14-9).
مطالعهها گزارش دادند که کاهش شنوایی در بیماران بتا تالاسمی ماژور در مقایسه با جمعیت عمومی بالاتر است (8، 7). با وجود درمانهای مدرن، خطر آسیب شنوایی به طور کامل رفع نشده و نیاز به تحقیقات بیشتر در این زمینه وجود دارد. سه شکاف اصلی دانش شامل مکانیسم دقیق آسیب شنوایی، نقش شلاتورها در پیشگیری یا بهبود آن و ارتبـاط کمـی بیـن سطـح فریتیـن و شدت کاهش شنوایی
هستند (14، 13، 10، 9).
ایـن پـژوهش بـا هدف بررسی ارتباط بین سطح فریتین
سرم و سن با نوع و شدت اختلالات شنوایی در بیماران تالاسمی ماژور طراحی شده است. همچنین، تأثیر رژیمهای مختلف شلاتهکنندگی آهن بر سلامت شنوایی به عنوان هدف فرعی بررسی خواهد شد. نتایج این مطالعه میتواند به استفاده از فریتین بـه عنوان یک نشانگر زیستی برای پیـشبینی خطر اختلال شنوایی و در نهایـت، بهبود راهبردهای مدیریتی و کیفیت زندگی بیماران مبتلا به تالاسمی ماژور کمک کند.
مواد و روشها
در این مطالعه مقطعی توصیفی- تحلیلی در کلیه بیماران مبتلا به تالاسمی ماژور شهر یاسوج که در 6 ماهه اول سال 1404 برای انتقال خون به بیمارستان شهید بهشتی یاسوج مراجعه میکردند، به صورت نمونهگیری تمام شماری و پس از اخذ رضایت آگاهانه، وارد مطالعه شدند. داشتن بتا تالاسمی ماژور از معیارهای ورود به مطالعه بود، ضمن این که کلیه بیماران به طور منظم از شلاتورهای آهن استفاده میکردند و به عنوان یکی از معیارهای اصلی ورود بیماران بـه مطالعه در نظر گرفته شد.
بیماران بـا سابقه ابتلا به عوامل تأثیرگذار بر شنوایی مانند بیماریهای عفونی ویروسی و بـاکتریایی، ضربات مکانیکی به سر و صورت، سابقه ترومای صوتی، کاهش شنوایی ژنتیکی، مصرف داروهای اتوتوکسیک و بیماریهای مغزی عروقی بر اساس چک لیست تهیه شده اطلاعات دموگرافیک شامل سن، جنس، نوع آهنزدای مصرفی و زمان شروع انتقال خون ثبت شد. قبل از تزریق خون، 5 میلیلیتر خون از بیماران داوطلب جهت تعیین میزان هموگلوبین و فریتین پلاسما - توسط کیتهای شرکت زیست شیمی - در آزمایشگاه بیمارستان شهید بهشتی گرفته شد. پس از تکمیل چـک لیست و بررسیهای آزمایشگاهی بیماران بر اساس سن و نوع آهنزدای مصرفی و فریتین گروهبندی شدند.
بر اساس سن، بیماران به دو گروه سنی بالای 20 و زیر 20 سال طبقهبندی شدند.
بر اساس نوع آهن زدای مصرفی به 5 گــروه طبقهبنـدی
شدند که عبارتند از: گروه اول بیمارانی که تنها دفروکسامین
مصرف میکردنـد. گـروه دوم بیمارانـی که دفرازیروکس بـه
تنهایی مصرف میکردند. گروه سوم بیمارانی که دفریپرون به تنهایی مصرف میکردند. گروه چهارم بیمارانی که دفروکسامین و دفرازیروکس را هم زمان مصرف میکردند. گروه پنجم بیمارانی که دفروکسامین و دفریپرون را همزمان مصرف میکردند.
بر اساس میانگین سطح فریتین اندازهگیری شده با روش الایزا (دیـازیست - ایران) به دو گروه بالای 1000 و کمتر مساوی 1000 نانوگرم در دسیلیتر گروهبندی شدند. همچنین به منظور بررسی اختلالات شنوایی، بیماران توسط اودیولوژیست، شنوایی سنجی شدند. ادیومتری به وسیله دستگاه در 6 فرکانس 250 هرتز، 500 هرتز، 2000 هرتز، 4000 هرتـز و 8000 هرتز انجام شد. پس از بررسیهای انجام شده بیماران بر اساس اختلالات شنوایی و شدت بیماری گروهبندی شدند. بر اساس اختلالات شنوایی بیماران مطالعه ما به 3 گروه طبقهبندی شدند: گروهی با اختلالات شنوایی حسی- عصبی (Sensorineural Hearing Loss)، گروهی بـا اختلالات شنوایی انتقالی (Conductive Hearing Loss) و گـروهی با اختلالات مختلط (Mixed Hearing Loss). همچنین بیماران بر اساس شدت بیماری به سه گروه خفیف، متوسط و شدید طبقهبندی شدند. بیمارانی که در شدت 0 تا 25 دسیبـل جواب دادند از شنوایی طبیعی، 25 تا 40 دسیبل کاهش شنوایی خفیف ، 40 تا 60 دسیبل کاهش شنوایی متوسط و 70 تا 90 دسیبل از کاهش شنوایی شدید برخوردار بودند.
روشهای تجزیه و تحلیل دادهها :
متغیرهای کمی بـا محاسبه میانگین و انحراف معیار توصیف شدند. برای بررسی طبیعی بودن متغیرهای کمی از آزمون کولموگروف اسمیرنوف استفاده شد. متغیرهای کیفی با استفاده از جداول توزیع فراوانی و ترسیم نمودار توصیف شدند. ارتباط متغیرهای کمی - کیفی بـا آزمون کایدو و آزمون independent T test سنجیده شد. برای مقایسه دادههـای non parametric از آزمونهای یو مانویتنی (مقایسه دو گروه) و کروسکال والیس (مقایسه چند گروه) با نرم افزار SPSS ویرایش 27 استفاده شد. سطح معناداری کمتر از 05/0 لحاظ شد.
یافتهها
ایـن مطالعه بـر روی 113 بیمار تـالاسمی ماژور مراجعه
کننده به بیمارستان شهید بهشتی شهر یاسوج انجام شد. تمامی این بیماران دارای بیماری تالاسمی تایید شده بودند و جهت تزریق خون در بازه زمانی مشخص شده مراجعه میکردند. از میان 113 مورد بیمار بتا تالاسمی ماژور، 96 بیمار به مطالعه وارد شدند (سایر بیماران در مراحل میانی کار به دلیل عدم مراجعه به مرکز شنوایی سنجی از مطالعه
خارج شدند).
در مطالعه حاضر میانگین سن بیماران 25/9 ± 25/27 سال گزارش شد و 6/40 درصد (39 n=) بیماران را مردان و 4/59 درصد (57 n=) را زنان تشکیل دادند (جدول 1).
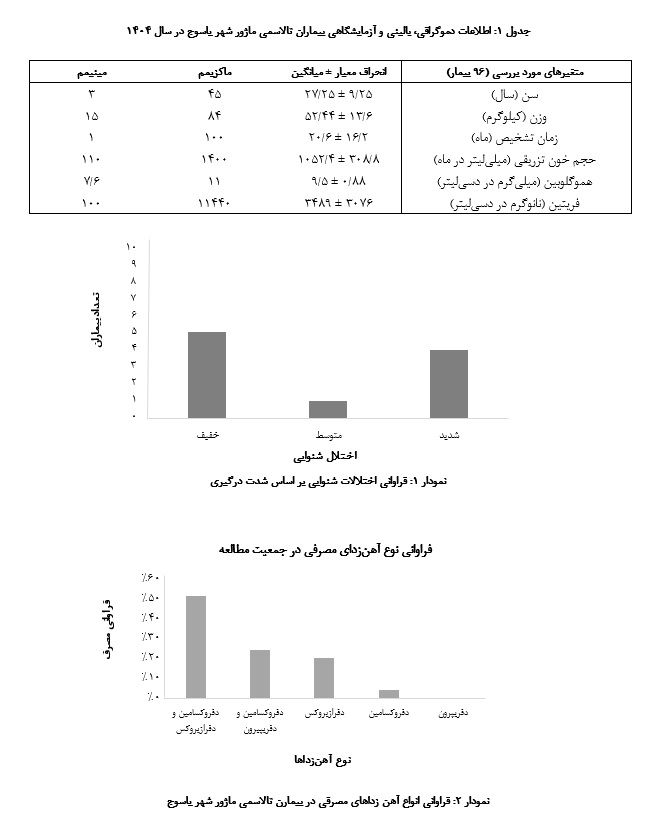
 از مجموع 96 بیمار بررسی شده، تنها 2/10درصد (10 n=) از بیماران از اختلالات شنوایی رنج میبردنـد و 6/89 درصد (86 (n= طبیعی بودند. از میان 10 بیمار تالاسمی ماژور با اختلالات شنوایی، فراوانی اختلال حسی عصبی 90 درصد (9 n=)، نوع انتقالی صفر درصد و نوع مختلط 10 درصد (1 n=) بود. درگیری یک طرفه در بیماران با اختلالات شنوایی 40 درصد (4 n=) و درگیری دو طرفه در این جمعیت 60 درصد(6 n=) بود. نتایج بررسیهای مـا نشان داد که 50 درصد (5 n=) بیماران مطالعه حاضر دارای اختلال خفیف شنوایی، 10 درصد (1 n=) دارای اختلال متوسط و 40 درصد اختلال شدید شنوایی (4 n=) دارند (نمودار 1).
از مجموع 96 بیمار بررسی شده، تنها 2/10درصد (10 n=) از بیماران از اختلالات شنوایی رنج میبردنـد و 6/89 درصد (86 (n= طبیعی بودند. از میان 10 بیمار تالاسمی ماژور با اختلالات شنوایی، فراوانی اختلال حسی عصبی 90 درصد (9 n=)، نوع انتقالی صفر درصد و نوع مختلط 10 درصد (1 n=) بود. درگیری یک طرفه در بیماران با اختلالات شنوایی 40 درصد (4 n=) و درگیری دو طرفه در این جمعیت 60 درصد(6 n=) بود. نتایج بررسیهای مـا نشان داد که 50 درصد (5 n=) بیماران مطالعه حاضر دارای اختلال خفیف شنوایی، 10 درصد (1 n=) دارای اختلال متوسط و 40 درصد اختلال شدید شنوایی (4 n=) دارند (نمودار 1).
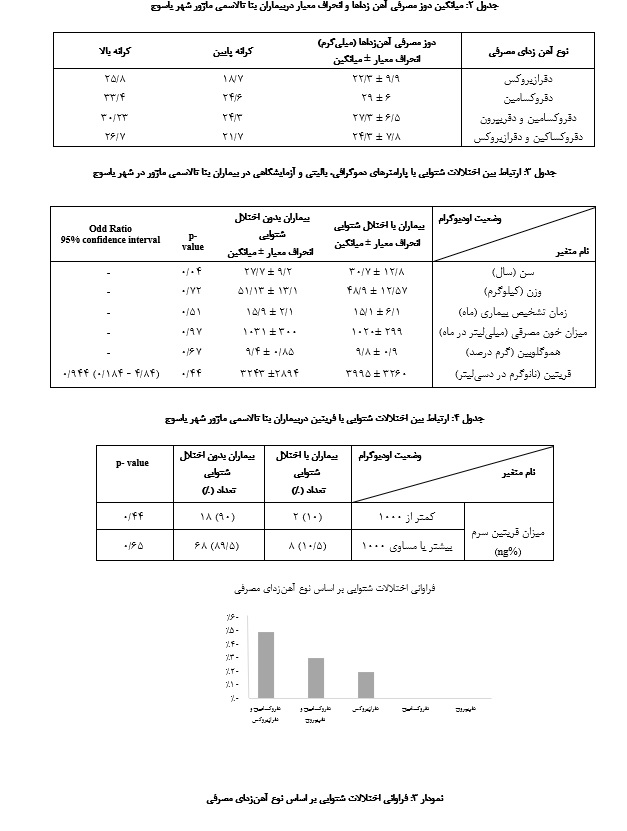
بر اساس نوع آهنزدای مصرفی بیماران بـه 5 گروه طبقهبندی شدند. بیشترین بیماران در گروه چهارم (دفروکسامین و دفرازیروکس) قرار داشتند و هیچ یک از بیماران دفریپرون به تنهایی مصرف نمیکردند (نمودار 2). میانگین دوز مصرفی آهنزداها و انحراف معیار آنها در جدول نشان داده شده است (جدول 2).
بررسی ارتباط بین اختلالات شنوایی بـا پارامترهای دموگرافی، بالینی و آزمایشگاهی در بیماران بتا تالاسمی ماژور شهر یاسوج :
به منظور بررسی ارتباط بین اختلالات شنوایی با پـارامترهای دموگرافی، بالینی و آزمایشگاهی دربیماران بتاتالاسمی ماژور شهر یاسوج ابتدا بیماران به دو گروه با اختلال شنوایی و بدون اختلال شنوایی طبقهبندی شدنـد. نتایج ما نشان داد که بین اختلالات شنوایی و سن ارتباط معناداری وجود دارد (04/0 p=). در بیماران بـالای 20 سال شانس ابتلا به اختلال شنوایی17/1 برابر گروه زیر 20 سال بود(82/4-28/0 :%95CI).
در مطالعه حاضر بین اختلالات شنوایی و سطح فریتین ارتباط معناداری وجود نداشت. همچنین نتایج حاضر نشان داد که بین اختلالات شنوایی با جنس ارتباط معناداری مشاهده نشد. بـه علاوه بررسیهای آماری نشان داد که بین اختلالات شنوایی و متغیرهای وزن، زمان تشخیص بیماری، میزان مصرف خون و هموگلوبین ارتباط معناداری وجود ندارد (جداول 3 و 4).
ارتباط بین اختلالات شنوایی با نوع آهنزدای مصرفی در بیماران بتا تالاسمی ماژور شهر یاسوج مورد بررسی قرار گرفت. نتایج نشان داد کـه اگر چه در بیمارانی که به طور همزمان دفروکسامین و دفرازیروکس مصرف میکردند اختلال شنوایی بیشتر دیده شد (50% ، 5 n=) اما از نظر آماری رابطه معناداری در این رابطه دیده نشد (نمودار 3).
بحث
این مطالعه مقطعی توصیفی - تحلیلی با هدف بررسی ارتباط بین سطح فریتین سرم و اختلالات شنوایی در ۱۱۳ بیمار مبتلا به بتا تالاسمی ماژور در شهر یاسوج انجام شد. شیوع اختلالات شنوایی در این جمعیت ۴۲/۱۰ درصد بود. شایعترین نوع اختلال، حسی-عصبی با ۹۰ درصد و الگوی درگیری بیشتر دوطرفه (۶۰ درصد) گزارش شد. نکته قابل توجه، درجه شدید اختلال در ۴۰ درصد بیماران مبتلا بود. در تحلیل ارتباطات، بین افزایش سن و اختلال شنوایی رابطه معنادار مثبت مشاهده شد، اما برخلاف انتظار، بین سطح فریتین سرم و اختلال شنوایی ارتباط آماری معناداری یافت نشد و همچنین ارتباطی با نوع داروی آهنزدا (شلاتور) دیده نشد.
یافتههای این مطالعه از نظر شیوع اختلالات شنوایی با نتایج چندین پژوهش قبلی همسو است. ازجمله در مطالعه انجام شده توسط رئیسی و همکاران، کاهش شنوایی 3/10 درصد گزارش شد (15).
برخلاف مطالعه ما، مطالعههای انجام شده توسط کمپانی و همکاران و چهکندی و همکاران شیوع بالاتری از اختلالات شنوایی را گزارش می دهند (بـه ترتیب 9/30 درصد و 20درصد) (17، 16).
همچنین، در متـاآنالیز انجام شده توسط بادفر و همکاران، شیوع کلی کم شنوایی در بیماران تالاسمی ماژور تحت درمان با دفروکسامین را 3/27 درصد گزارش کرد کـه بـالاتر از میزان گزارش شده در مطالعه حاضر (42/10 درصد) بود (13). این تفاوت ممکن است ناشی از تفاوت در روشهای ارزیـابی شنوایی، ویژگیهای جمعیت شناختی بیماران یا دستورالعملهای درمانی باشد.
یافته اصلی این مطالعه نشاندهنده ارتباط معنادار بین افزایش سن و شیوع اختلالات شنوایی در بیماران مبتلا به بتا تالاسمی ماژور است. این ارتباط را میتوان با مکانیسم مواجهه تجمعی و پیری فیزیولوژیک توضیح داد. سن بالاتر بـه منزله مواجهه طولانی مدت تر با دو عامل آسیبزای اصلی یعنی گرانباری آهن و درمان طولانی مدت با شلاتورهای آهن است. این مواجهه تجمعی، احتمال رسیدن بـه یک آستانه آسیب را که پس از آن اختلال عملکرد شنوایی آشکار میشود، به شدت افزایش میدهد. بنابراین، در بیماران مسنتر، اثرات پیری و سمیت ناشی از درمان بر یکدیگر اثر همافزایی داشته و منجر بـه بروز زودرس و شدیدتر اختلالات شنوایی میشوند.
هم راستا بـا مطالعه ما، مطالعه آلده و همکاران بر روی بیماران ایتالیایی (با پیگیری بیش از ۲۰ سال) نشان داد که بیماران مبتلا به سمیت گوشی، میانگین سنی بالاتری داشتند و مدت زمان طولانیتری تحت درمان شلاتهکننده قرار گرفته بودند (10). همچنین تارتاگلیـون و همکاران در مرور سیستماتیک خود خاطر نشان کردند که اگر چه مطالعهها نتایج متناقضی را در رابطه بـا فریتین گزارش کردهانـد، اما سن به طور ثابتتری به عنوان یک عامل پیشبینی کننده کاهش شنوایی ظاهر شده است. به علاوه مطالعه فرانوش و همکاران که بر روی یـک کوهورت بزرگ ایرانی (۱۰۱۰ بیمار) انجام شده بود، نیز همبستگی مثبت و معناداری بین سن و اختلالات شنوایی را گزارش کرد (18).
ذکر این نکته ضروری است که برخی مطالعهها در تضاد بـا نتایج ما میباشند. برای مثال بـادفر و همکاران در متاآنالیز خود ارتباط معناداری بین سن و کاهش شنوایی پیدا نکردهاند (13). این ناهمخوانی ظاهری میتوانـد ناشی از عوامل زیر باشد: ساختار سنی جمعیت مورد مطالعه، تأثیر قویتر عوامل مخدوشگر ماننـد عدم پایبندی به درمان شلاتهکننده یا کنترل ضعیف بار آهن میتواند چنان تأثیر مخرب و سریعی داشته باشد که حتی در سنین پایین نیز منجر به عوارض شود.
در مطالعه حاضر بین نوع آهنزدا و اختلالات شنوایی ارتباط معناداری مشاهده نشد. در حالی که برخلاف نتایج ما در مطالعه اشرفی و همکاران گزارش شد کـه بین میزان مصرف دفروکسامین و بروز کاهش شنوایی ارتباط معناداری وجود دارد (8). این یـافتهها تـأیید میکند که اگر چه شلاتورهای آهن برای پیشگیری از عوارض ناشی از بار آهن ضروری هستند، اما خود میتوانند عوارض جانبی مهمی از جمله اتوتوکسیسیتی ایجاد کنند.
در مقابل، مطالعه پوشش دوست و همکـاران، رئیسـی و
همکاران و کمپانی و همکاران همراستا با مطالعه ما گزارش دادند که ارتباط معناداری بین مصرف دفرازیروکس و اختلالات شنوایی وجود ندارد (19، 17، 15). این ناهمخوانی ممکن است ناشی از تفاوت در پروفایل ایمنی شلاتورهای مختلف باشد. دفرازیروکس به عنوان یک شلاتور نسل جدید، احتمالاً پروفایل ایمنی بهتری از نظر عوارض شنوایی دارد. هنوز در این مورد اختلاف نظر وجود دارد و لازم است مطالعههای وسیعتر و به صورت کوهورت انجام شود تا این مسأله با دقت بیشتری مورد بررسی قرار گیرد.
مطالعه طولی آلـده و همکاران نشان داد که درمان طولانی مدت بـا شلاتورهای آهن ممکن است منجر به سمیت گوش شود (10). این یافته اهمیت پایش منظم شنوایی در بیماران تحـت درمان با شلاتورهای آهن را برجسته میسازد.
در مطالعه حاضر غلبه اختلالات شنوایی از نوع حسی-عصبی شایعترین اختلال گزارش شد که بـا بیشتر مطالعههای قبلی مشابـه است. به عنوان مثال، مطالعه تارتاگلیون و همکاران در مرور سیستماتیک خود، شیوع بیشتر کمشنوایی حسی- عصبی را در بیماران تالاسمی گزارش کردند (4). همچنین کمپانی و همکاران نشان دادند که اختلالات عصبی در مقابل اختلالات انتقالی شایعتر است (17).
در مطالعه انجام شده توسط رئیسی و همکاران برخلاف مطالعه ما اختلالات شنوایی انتقالی بیشتر از نوع حسی-عصبی گزارش شده است (15). یافتههای این مطالعه نشان داد کـه 40% از بیماران مبتلا به اختلال شنوایی، درجـه شدید این عارضه را تجربه میکنند. این رقم در مقایسه با مطالعههای پیشین، نگرانکننده و قابـل تأمل است.
مطالعه آلده و همکاران کـه بر روی بیماران با سابقه طولانی درمان شلاتهکننده انجام شد، اغلب موارد کاهش شنوایی را در محدوده خفیف تا متوسط گزارش کرد و موارد شدید عمدتاً در بیماران با سابقه مصرف طولانی مدت و با دوز بالا دفروکسامین دیده شد (10).
مطالعه تیوانا و همکاران نیز که به بررسی دفرازیروکس پرداخت، شیوع بسیار پائینی از کاهش شنوایی بالینی گزارش کرد و اکثر موارد گزارش شده توسط ادیومتری، در مرز تشخیـص و در محدوده خفیف قرار داشتند (20).
این تقابل نشان میدهد اگر چه ممکن است شیوع کلی اختلال در جمعیت مورد مطالعـه ما پایینتر باشد، ولی بار بیماری (Disease Burden) برای آن دسته از بیمارانی کـه درگیر میشوند، به طور قابل توجهی سنگینتر است. این یافته میتوانـد زنـگ خطری برای سیستم بهداشتی منطقه
باشد که نیاز به پیگیری و مداخله قویتر دارد.
فرضیه میتواند توضیح دهنده شدت بالای آسیب در این
جمعیت باشد:
تأخیر در تشخیص و شروع درمان شلاتهکننده، مدت
زمان مواجهه بافتهای حساس مانند حلزون گوش با سطوح بسیار بالای آهن آزاد طولانیتر شده است. این مواجهه طولانی مدت میتواند منجر به آسیب اکسیداتیو غیر قابل برگشت و در نتیجه شدت بیشتر اختلال شود. الگوی مصرف شلاتورها همان طور که در یافتهها ذکر شد، الگوی ترکیبی مصرف شلاتور (به ویژه دفروکسامین و دفرازیروکس) در این جمعیت شایع بود. اگر چـه از نظر آماری ارتباط معناداری پیدا نشد، اما اثر سینرژیستیک (همافزایی) سمیت این دو دارو بر روی سلولهای مویی گوش نمیتواند به طور کامل رد شود. این پدیده در مطالعههای آزمایشگاهی مورد بحث قرار گرفته است.
عوامل محیطی، تغذیهای یا شیوع بالاتر برخی همابتلاییها (مانند کمبود ویتامینهای آنتیاکسیدان مانند A و E که نقش محافظتی در برابر استرس اکسیداتیو دارند) میتوانـد جمعیت را نسبت به سمیت ناشی از آهن یا شلاتورها آسیبپذیرتر کند و شدت عوارض را افزایش دهد.
یافته مربوط به عدم ارتباط فریتین سرم با اختلال شنوایی، اگر چه ممکن است در نگاه اول غیر منتظره به نظر برسد، اما بـا یافتههای برخی مطالعههای معتبر دیگر همخوانی دارد و از منظر پاتوفیزیولوژیک قابل تفسیر است (4). به طور کلی، فریتین سرم یک شاخص غیر مستقیم و گاهی نـاقص برای ارزیـابی بار آهن در بافتهای خاص مانند حلزون گوش محسوب میشود. ممکن است آسیب به سلولهای حساس شنوایی بیش از آن که تحت تأثیر مستقیم سطح کلی آهن خون باشد، ناشی از سمیت اختصاصی برخی شلاتورهای آهن (به ویژه دفروکسامین)، تجمع موضعی آهن در بافت گوش، یا حساسیت فردی و زمینه ژنتیکی باشد. به عنوان مثال، مرور سیستماتیک تارتاگلیون و همکاران (۲۰۲۰) نیز بر عدم وجود ارتباط ثابت بین فریتین و کاهش شنوایی تأکید کرده و نقش مستقل عوامل دیگری مانند اتوتوکسیسیتی دارویی را برجسته نموده است (4).
این موضوع نشان میدهد که مکانیسم آسیب شنوایی در بیماران تالاسمی چند عاملی و پیچیده است و نمیتوان آن را صرفاً به یک شاخص آزمایشگاهی مانند فریتین سرم تقلیل داد. بنابراین، این یـافته بر اهمیت پایش منظم و مستقیم شنوایی با ادیومتری در تمامی بیماران، صرف نظر از عدد فریتین سرم، به عنوان یک جزء ضروری از برنامه مراقبت جامع این بیماران تاکید میکند. برای روشن شدن دقیقتر این مکـانیسمها، انجام مطالعههای طولی مدت که همزمان مارکرهای دقیقتر بـار آهن بافتی و شاخصهای استرس اکسیداتیو را اندازهگیری کنند، پیشنهاد مــــیشود.
محدودیتهای مطالعه:
طراحی مقطعی مطالعه امکـان استنباط رابطه علّی را فراهم نمیکند. از طرفی، حجم نمونـه محـدود، به ویژه تعداد کم بیماران دارای اختلال شنوایی (10 n=)، ممکن است قدرت آماری را برای شناسایی برخی ارتباطات کاهش داده باشد.
نتیجهگیری
اگر چه این مطالعه ارتباط مستقیمی بین سطح فریتین سرم و اختلالات شنوایی در بیماران بتا تالاسمی ماژور نشان نـداد، اما اهمیت پایش منظم شنوایی و مدیریت بهینه بار آهن را بـه ویژه در بیماران مسنتر برجسته میسازد. همچنین همکاری بین هماتولوژیستها، ادیولوژیستها، متخصصان گوش و حلق و بینی و پزشکان داخلی برای حفظ کیفیت زندگی این بیماران ضروری است. از طرفی ارتباط معنادار بین سن و اختلال شنوایی در مطالعه حاضر، یـک پیام بالینی واضح دارد که بیماران مسنتر مبتلا به تالاسمی ماژور یک گروه پرخطر برای اختلالات شنوایی هستند. این موضوع لزوم اجرای یک دستورالعمل پایش منظم و مادامالعمر شنوایی را که با افزایش سن بیماران تکرار و تشدید میشود، ایجاب میکند.
این رویکرد پیشگیرانـه نه تنها میتواند به تشخیص زود هنگام کمک کند، بلکه امکان تعدیل رژیم درمانی (ماننـد بررسی دوز شلاتورها) را قبل از بروز آسیب غیر قابـل برگشت فراهم میآورد و در نهایت به حفظ کیفیت زندگی این بیماران کـه به لطف پیشرفتهای درمانی، به سنین میانسالی و بالاتر میرسند، کمک شایانی میکند.
حمایت مالی
ایـن پـروژه با حمایت مالی دانشگاه علوم پزشکی یاسوج
انجام شده است.
ملاحظات اخلاقی
ایـن پـژوهش منتـج از پایاننامـه دانشجویـــی با عنوان
بررسی ارتباط سطح فریتین با اختلالات شنوایی در بیماران تـالاسمی ماژور شهر یاسوج بـا کد اخـلاق IR.YUMS.REC.1404.116 به تصویب رسیـده است.
عدم تعارض منافع
نویسندگان اظهار میکنند هیچگونه تعارض منافعی در
این مطالعه وجود نداشته است.
نقش نویسندگان
دکتر غلامعباس سبز: همکاری در طراحی موضوع و مشاوره
بالینی و کمک در تفسیر نتایج، نوشتن مقاله
دکتر فریبا راد: طراحی موضوع، مدیریت پروژه، ادیت مقاله و پاسخ به مجله
عاطفه سرائی: انجام آزمایشها و جمعآوری دادهها
تشکر و قدردانی
بدینوسیله نویسندگان از کارکنان محترم بیمارستان شهید بهشتی یاسوج تشکر و قدردانی مینمایند.
متن کامل: (14 مشاهده)
ارتباط بین سطح فریتین سرم و سن در بیماران بتا تالاسمی ماژور شهر یاسوج با
اختلالات شنوایی
غلامعباس سبز1 ، فریبا راد2 ، عاطفه سرائی3
1- متخصص جراحی گوش و حلق و بینی ـ دانشیار گروه جراحی دانشکده پزشکی دانشگاه علوم پزشکی یاسوج ـ یاسوج ـ ایران
2- دکترای هماتولوژی و بانک خون آزمایشگاهی ـ دانشیار گروه علوم پایه دانشکده پزشکی دانشگاه علوم پزشکی یاسوج - یاسوج - ایران
3- دانشجوی پزشکی ـ مرکـز تحقیقـات سـلولی مولکـولی دانشـگاه علـوم پزشـکی یاسـوج ـ یاسـوج ـ ایران
اختلالات شنوایی
1- متخصص جراحی گوش و حلق و بینی ـ دانشیار گروه جراحی دانشکده پزشکی دانشگاه علوم پزشکی یاسوج ـ یاسوج ـ ایران
2- دکترای هماتولوژی و بانک خون آزمایشگاهی ـ دانشیار گروه علوم پایه دانشکده پزشکی دانشگاه علوم پزشکی یاسوج - یاسوج - ایران
3- دانشجوی پزشکی ـ مرکـز تحقیقـات سـلولی مولکـولی دانشـگاه علـوم پزشـکی یاسـوج ـ یاسـوج ـ ایران
  http://dx.doi.org/10.61882/bloodj.22.2.160 Citation: Sabz Gh, Rad F, Saraei A. The Relationship of Serum Ferritin Levels and Age with Hearing Disorders in Patients with Beta-Thalassemia Major. J Iran Blood Transfus. 2025: 22 (4): 316-326 نویسنده مسئول: دکتر فریبا راد. دانشیار گروه علوم پایه دانشکده پزشکی دانشگاه علوم پزشکی یاسوج ـ یاسوج ـ ایران کدپستی: 7591741417 E-mail fariba.rad89@gmail.com
کد اخلاق: IR.YUMS.REC.1404.116 |
چکیده سابقه و هدف یکی از عوارضی که میتواند به دنبال تجمع و رسوب آهن در سیستم عصبی به واسطه تزریق خون مکرر در بیماران مبتلا به تالاسمی ماژور رخ دهد، اختلال در میزان شنوایی این افراد میباشد. به این دلیل در این مطالعه سعی شده است که به بررسی ارتباط بین سطح فریتین سرم و سن با اختلالات شنوایی در بیماران بتا تالاسمی ماژور شهر یاسوج پرداخته شود. مواد و روشها در این مطالعه مقطعی توصیفی - تحلیلی، 96 بیمار مبتلا به بتا تالاسمی ماژور شهر یاسوج طی سالهای 1404-1403 از نظر مشکلات شنوایی بررسـی شـدند. پس از جمعآوری اطلاعات دموگرافی، آزمایشگاهی و ادیومتری بیماران، نتایج با استفاده از نرمافزار آماری 27 SPSS و استفاده از آزمونهای آماری کایدو ، t-test ، منویتنی و کروسکال والیس در سطح معنادار 05/0 p< مورد تجریه و تحلیل قرار گرفت. یافتهها در این مطالعه، میانگین سنی بیماران 25/9 ± 27/25 سال بود و فراوانی اختلالات شنوایی در آنها 42/10درصد (10 n=) به دست آمد. فراوانی اختلال حسی عصبی 90 درصد (9 n=) و نوع آمیخته 10 درصد (1 n=) بود. 50 درصد (5 n=) بیماران دارای اختلال خفیف، 10 درصد (1 n=) دارای اختلال متوسط و 40 درصد اختلال شدید (4 n=) داشتند. 51% بیماران دفروکسامین و دفرازیروکس را به طور همزمان مصرف میکردند. نتایج نشان داد که بین سن و اختلالات شنوایی ارتباط معناداری وجود دارد (04/0 p=) ولی بین اختلالات شنوایی با سطح فریتین ارتباط معناداری دیده نشد. نتیجه گیری ارتباط سن و اختلال شنوایی حاوی پیام بالینی مهمی است که بیماران مسنتر مبتلا به تالاسمی ماژور یک گروه پرخطر برای اختلالات شنوایی هستند. این موضوع لزوم اجرای یک دستورالعمل پایش منظم و مادامالعمر شنوایی را که با افزایش سن بیماران تکرار و تشدید میشود، ایجاب میکند. کلمات کلیدی: بتا تالاسمی ماژور، شلاتورهای آهن، اختلالات شنوایی |
|
1- Acridine Orange
|
|
1- Biological safety cabinet
|
|
1- Platelet Concentrate
2- Food and Drug Administration 3- Normal Skin Flora 4- Platelet Rich Plasma-Platelet Concentrate 5- Eosin-Methylene blue 6- Thioglycolate |
|
1- Acridine Orange
|
|
1- Biological safety cabinet
|
|
1- Platelet Concentrate
2- Food and Drug Administration 3- Normal Skin Flora 4- Platelet Rich Plasma-Platelet Concentrate 5- Eosin-Methylene blue 6- Thioglycolate |
مقدمه
تالاسمی ماژور یک اختلال هماتولوژیک ارثی است که با بروز کمخونی شدید تظاهر مییابد. در حال حاضر، درمان استانـدارد حمایتی برای این بیماری، انتقال خون منظم است که با تغییر سیر بیماری از یک وضعیت کشنده در دوران کودکی بـه یک بیماری مزمن، سبب افزایش قابل توجه امید به زندگی بیماران شده است. با این حال، این درمان نجاتبخش، به دنبال تجمع پیشرونده آهن در بدن و عدم وجود مکانیسم فیزیولوژیک کارآمد برای دفع آن، منجر بـه بروز چالش عمدهای در مدیریت بیماران تحت عنوان افزایش بار آهن گردیده است (2، 1).
در شرایط گرانباری آهن، آهن اضافی در اندامهای حیاتی مختلف از قبیل قلب، کبد، غدد درونریز و سیستم عصبی رسوب کرده و موجب ایجاد آسیبهای جدی در عملکرد این اندامها میشود. برای پایش بار آهن در این بیماران، از فریتین سرم به عنوان معیار استاندارد استفاده میگردد که سطح مطلوب آن معمولاً کمتر از ۱۰۰۰ نانوگرم بر دسیلیتر توصیه میشود (3، 2).
به منظور مقابله با این چالش، درمان با شلاتورهای آهن (Iron Chelators) از حدود شش دهه پیش آغاز شده است. اگر چه داروهای شلاتور در دو نسل قدیم (مانند دسفرال یا دفروکسامین) و جـدید (مانند دفریپرون و دفرازیروکس) نقش حیاتی در افزایش طول عمر بیماران ایفا کردهاند، اما با طیف وسیعی از عوارض جانبی بالقوه همراه هستند. یکی از عوارض مهم و نسبتاً شایع این داروها که تأثیر مستقیمی بر کیفیت زنـدگی بیماران دارد، اختلال در عملکرد شنوایی است (4).
کاهش شنوایی (که کاهش حساسیت سیستم ادراک صوتی تعریف میشود) در بیماران مبتلا به تالاسمی ماژور یک عارضه چند عاملی محسوب میشود (5). بر اساس پاتوفیزیولوژی و محل وقوع آسیب در مسیر شنوایی، به انواع مختلفی تقسیمبندی میگردد که عبارتند از: کاهش شنوایی حسی- عصبی (Sensorineural Hearing Loss - SNHL) که ناشی از آسیب به سلولهای مویی حساس در حلزون گوش داخلی یا اعصاب مرتبط با مسیر شنوایی است و معمولاً دائمی و غیر قابل بازگشت میباشد. این نوع کاهش شنوایی به طور خاص با سمیت نـاشی از شلاتورهای آهن، به ویژه دفروکسامین (که معمـولاً بـه صـورت SNHL دو طرفـه در فرکـانسهای بالا بروز میکند) و همچنین با تجمع آهن در
سیستم عصبی مرتبط دانسته شده است. اگرچه شلاتورهای خوراکی نسل جدید مانند دفریپرون و دفرازیروکس ایمنتر به نظر میرسند، اما همچنان نیاز به پایش منظم شنوایی دارند (6، 5). کاهش شنوایی انتقالی (Conductive Hearing Loss - CHL) بـه دنبال موانع موجود در انتقال صوت از مجرای گوش خارجی به گوش داخلی رخ میدهد که میتواند ناشی از آسیب بـه پرده گوش، استخوانچههای گوش میانی یا عملکرد نادرست شیپور استاش باشد. همچنین نوع سوم تحـت عنوان کاهش شنوایی مختلط (Mixed Hearing Loss) شناخته میشود که ترکیبی از هر دو نوع حسی-عصبی و انتقالی است (6، 5). مطالعهها گزارش دادند که کاهش شنوایی در بیماران بتا تالاسمی ماژور در مقایسه با جمعیت عمومی بالاتر است. به عنوان مثال، در داخل ایران، میانگین کاهش شنوایی در این بیماران حدود 20% گزارش شده است، در حالی که این رقم در جمعیت کلی حدود 10%-7% برآورد میشود. یک مطالعه متا آنالیز اختلالات شنوایی در بیماران تالاسمی را حدود 3/20 % گزارش کرده است که این رقم اهمیت موضوع را به وضوح نشان میدهد (8، 7).
اگر چه برخی مطالعهها ارتباط معناداری بین سطح فریتین سرم و شدت SNHL گزارش کردهاند، اما سایر پژوهشها چنین رابطهای را به صورت قطعی تأیید نکردهاند (10، 9). علاوه بر سمیت دارویی و بار آهن، عوامل دیگری مانند کمکاری تیروئید، دیابت و کمخونی مزمن نیز میتوانند در بروز اختلال شنوایی در این بیماران نقش داشته باشند (12، 11). مطالعههای تصویربرداری پیشرفته مانند PET هایپوپرفیوژن (کاهش خونرسانی) در قشر شنوایی بیماران تالاسمی را نشان دادهاند که میتواند به عنوان یک نشانگر متابولیک مطرح باشد و ارتباط بین تجمع آهن و اختلال عملکرد عروقی مغز را تأیید کند (14-9).
مطالعهها گزارش دادند که کاهش شنوایی در بیماران بتا تالاسمی ماژور در مقایسه با جمعیت عمومی بالاتر است (8، 7). با وجود درمانهای مدرن، خطر آسیب شنوایی به طور کامل رفع نشده و نیاز به تحقیقات بیشتر در این زمینه وجود دارد. سه شکاف اصلی دانش شامل مکانیسم دقیق آسیب شنوایی، نقش شلاتورها در پیشگیری یا بهبود آن و ارتبـاط کمـی بیـن سطـح فریتیـن و شدت کاهش شنوایی
هستند (14، 13، 10، 9).
ایـن پـژوهش بـا هدف بررسی ارتباط بین سطح فریتین
سرم و سن با نوع و شدت اختلالات شنوایی در بیماران تالاسمی ماژور طراحی شده است. همچنین، تأثیر رژیمهای مختلف شلاتهکنندگی آهن بر سلامت شنوایی به عنوان هدف فرعی بررسی خواهد شد. نتایج این مطالعه میتواند به استفاده از فریتین بـه عنوان یک نشانگر زیستی برای پیـشبینی خطر اختلال شنوایی و در نهایـت، بهبود راهبردهای مدیریتی و کیفیت زندگی بیماران مبتلا به تالاسمی ماژور کمک کند.
مواد و روشها
در این مطالعه مقطعی توصیفی- تحلیلی در کلیه بیماران مبتلا به تالاسمی ماژور شهر یاسوج که در 6 ماهه اول سال 1404 برای انتقال خون به بیمارستان شهید بهشتی یاسوج مراجعه میکردند، به صورت نمونهگیری تمام شماری و پس از اخذ رضایت آگاهانه، وارد مطالعه شدند. داشتن بتا تالاسمی ماژور از معیارهای ورود به مطالعه بود، ضمن این که کلیه بیماران به طور منظم از شلاتورهای آهن استفاده میکردند و به عنوان یکی از معیارهای اصلی ورود بیماران بـه مطالعه در نظر گرفته شد.
بیماران بـا سابقه ابتلا به عوامل تأثیرگذار بر شنوایی مانند بیماریهای عفونی ویروسی و بـاکتریایی، ضربات مکانیکی به سر و صورت، سابقه ترومای صوتی، کاهش شنوایی ژنتیکی، مصرف داروهای اتوتوکسیک و بیماریهای مغزی عروقی بر اساس چک لیست تهیه شده اطلاعات دموگرافیک شامل سن، جنس، نوع آهنزدای مصرفی و زمان شروع انتقال خون ثبت شد. قبل از تزریق خون، 5 میلیلیتر خون از بیماران داوطلب جهت تعیین میزان هموگلوبین و فریتین پلاسما - توسط کیتهای شرکت زیست شیمی - در آزمایشگاه بیمارستان شهید بهشتی گرفته شد. پس از تکمیل چـک لیست و بررسیهای آزمایشگاهی بیماران بر اساس سن و نوع آهنزدای مصرفی و فریتین گروهبندی شدند.
بر اساس سن، بیماران به دو گروه سنی بالای 20 و زیر 20 سال طبقهبندی شدند.
بر اساس نوع آهن زدای مصرفی به 5 گــروه طبقهبنـدی
شدند که عبارتند از: گروه اول بیمارانی که تنها دفروکسامین
مصرف میکردنـد. گـروه دوم بیمارانـی که دفرازیروکس بـه
تنهایی مصرف میکردند. گروه سوم بیمارانی که دفریپرون به تنهایی مصرف میکردند. گروه چهارم بیمارانی که دفروکسامین و دفرازیروکس را هم زمان مصرف میکردند. گروه پنجم بیمارانی که دفروکسامین و دفریپرون را همزمان مصرف میکردند.
بر اساس میانگین سطح فریتین اندازهگیری شده با روش الایزا (دیـازیست - ایران) به دو گروه بالای 1000 و کمتر مساوی 1000 نانوگرم در دسیلیتر گروهبندی شدند. همچنین به منظور بررسی اختلالات شنوایی، بیماران توسط اودیولوژیست، شنوایی سنجی شدند. ادیومتری به وسیله دستگاه در 6 فرکانس 250 هرتز، 500 هرتز، 2000 هرتز، 4000 هرتـز و 8000 هرتز انجام شد. پس از بررسیهای انجام شده بیماران بر اساس اختلالات شنوایی و شدت بیماری گروهبندی شدند. بر اساس اختلالات شنوایی بیماران مطالعه ما به 3 گروه طبقهبندی شدند: گروهی با اختلالات شنوایی حسی- عصبی (Sensorineural Hearing Loss)، گروهی بـا اختلالات شنوایی انتقالی (Conductive Hearing Loss) و گـروهی با اختلالات مختلط (Mixed Hearing Loss). همچنین بیماران بر اساس شدت بیماری به سه گروه خفیف، متوسط و شدید طبقهبندی شدند. بیمارانی که در شدت 0 تا 25 دسیبـل جواب دادند از شنوایی طبیعی، 25 تا 40 دسیبل کاهش شنوایی خفیف ، 40 تا 60 دسیبل کاهش شنوایی متوسط و 70 تا 90 دسیبل از کاهش شنوایی شدید برخوردار بودند.
روشهای تجزیه و تحلیل دادهها :
متغیرهای کمی بـا محاسبه میانگین و انحراف معیار توصیف شدند. برای بررسی طبیعی بودن متغیرهای کمی از آزمون کولموگروف اسمیرنوف استفاده شد. متغیرهای کیفی با استفاده از جداول توزیع فراوانی و ترسیم نمودار توصیف شدند. ارتباط متغیرهای کمی - کیفی بـا آزمون کایدو و آزمون independent T test سنجیده شد. برای مقایسه دادههـای non parametric از آزمونهای یو مانویتنی (مقایسه دو گروه) و کروسکال والیس (مقایسه چند گروه) با نرم افزار SPSS ویرایش 27 استفاده شد. سطح معناداری کمتر از 05/0 لحاظ شد.
یافتهها
ایـن مطالعه بـر روی 113 بیمار تـالاسمی ماژور مراجعه
کننده به بیمارستان شهید بهشتی شهر یاسوج انجام شد. تمامی این بیماران دارای بیماری تالاسمی تایید شده بودند و جهت تزریق خون در بازه زمانی مشخص شده مراجعه میکردند. از میان 113 مورد بیمار بتا تالاسمی ماژور، 96 بیمار به مطالعه وارد شدند (سایر بیماران در مراحل میانی کار به دلیل عدم مراجعه به مرکز شنوایی سنجی از مطالعه
خارج شدند).
در مطالعه حاضر میانگین سن بیماران 25/9 ± 25/27 سال گزارش شد و 6/40 درصد (39 n=) بیماران را مردان و 4/59 درصد (57 n=) را زنان تشکیل دادند (جدول 1).


بر اساس نوع آهنزدای مصرفی بیماران بـه 5 گروه طبقهبندی شدند. بیشترین بیماران در گروه چهارم (دفروکسامین و دفرازیروکس) قرار داشتند و هیچ یک از بیماران دفریپرون به تنهایی مصرف نمیکردند (نمودار 2). میانگین دوز مصرفی آهنزداها و انحراف معیار آنها در جدول نشان داده شده است (جدول 2).
بررسی ارتباط بین اختلالات شنوایی بـا پارامترهای دموگرافی، بالینی و آزمایشگاهی در بیماران بتا تالاسمی ماژور شهر یاسوج :
به منظور بررسی ارتباط بین اختلالات شنوایی با پـارامترهای دموگرافی، بالینی و آزمایشگاهی دربیماران بتاتالاسمی ماژور شهر یاسوج ابتدا بیماران به دو گروه با اختلال شنوایی و بدون اختلال شنوایی طبقهبندی شدنـد. نتایج ما نشان داد که بین اختلالات شنوایی و سن ارتباط معناداری وجود دارد (04/0 p=). در بیماران بـالای 20 سال شانس ابتلا به اختلال شنوایی17/1 برابر گروه زیر 20 سال بود(82/4-28/0 :%95CI).
در مطالعه حاضر بین اختلالات شنوایی و سطح فریتین ارتباط معناداری وجود نداشت. همچنین نتایج حاضر نشان داد که بین اختلالات شنوایی با جنس ارتباط معناداری مشاهده نشد. بـه علاوه بررسیهای آماری نشان داد که بین اختلالات شنوایی و متغیرهای وزن، زمان تشخیص بیماری، میزان مصرف خون و هموگلوبین ارتباط معناداری وجود ندارد (جداول 3 و 4).
ارتباط بین اختلالات شنوایی با نوع آهنزدای مصرفی در بیماران بتا تالاسمی ماژور شهر یاسوج مورد بررسی قرار گرفت. نتایج نشان داد کـه اگر چه در بیمارانی که به طور همزمان دفروکسامین و دفرازیروکس مصرف میکردند اختلال شنوایی بیشتر دیده شد (50% ، 5 n=) اما از نظر آماری رابطه معناداری در این رابطه دیده نشد (نمودار 3).
بحث
این مطالعه مقطعی توصیفی - تحلیلی با هدف بررسی ارتباط بین سطح فریتین سرم و اختلالات شنوایی در ۱۱۳ بیمار مبتلا به بتا تالاسمی ماژور در شهر یاسوج انجام شد. شیوع اختلالات شنوایی در این جمعیت ۴۲/۱۰ درصد بود. شایعترین نوع اختلال، حسی-عصبی با ۹۰ درصد و الگوی درگیری بیشتر دوطرفه (۶۰ درصد) گزارش شد. نکته قابل توجه، درجه شدید اختلال در ۴۰ درصد بیماران مبتلا بود. در تحلیل ارتباطات، بین افزایش سن و اختلال شنوایی رابطه معنادار مثبت مشاهده شد، اما برخلاف انتظار، بین سطح فریتین سرم و اختلال شنوایی ارتباط آماری معناداری یافت نشد و همچنین ارتباطی با نوع داروی آهنزدا (شلاتور) دیده نشد.
یافتههای این مطالعه از نظر شیوع اختلالات شنوایی با نتایج چندین پژوهش قبلی همسو است. ازجمله در مطالعه انجام شده توسط رئیسی و همکاران، کاهش شنوایی 3/10 درصد گزارش شد (15).
برخلاف مطالعه ما، مطالعههای انجام شده توسط کمپانی و همکاران و چهکندی و همکاران شیوع بالاتری از اختلالات شنوایی را گزارش می دهند (بـه ترتیب 9/30 درصد و 20درصد) (17، 16).
همچنین، در متـاآنالیز انجام شده توسط بادفر و همکاران، شیوع کلی کم شنوایی در بیماران تالاسمی ماژور تحت درمان با دفروکسامین را 3/27 درصد گزارش کرد کـه بـالاتر از میزان گزارش شده در مطالعه حاضر (42/10 درصد) بود (13). این تفاوت ممکن است ناشی از تفاوت در روشهای ارزیـابی شنوایی، ویژگیهای جمعیت شناختی بیماران یا دستورالعملهای درمانی باشد.
یافته اصلی این مطالعه نشاندهنده ارتباط معنادار بین افزایش سن و شیوع اختلالات شنوایی در بیماران مبتلا به بتا تالاسمی ماژور است. این ارتباط را میتوان با مکانیسم مواجهه تجمعی و پیری فیزیولوژیک توضیح داد. سن بالاتر بـه منزله مواجهه طولانی مدت تر با دو عامل آسیبزای اصلی یعنی گرانباری آهن و درمان طولانی مدت با شلاتورهای آهن است. این مواجهه تجمعی، احتمال رسیدن بـه یک آستانه آسیب را که پس از آن اختلال عملکرد شنوایی آشکار میشود، به شدت افزایش میدهد. بنابراین، در بیماران مسنتر، اثرات پیری و سمیت ناشی از درمان بر یکدیگر اثر همافزایی داشته و منجر بـه بروز زودرس و شدیدتر اختلالات شنوایی میشوند.
هم راستا بـا مطالعه ما، مطالعه آلده و همکاران بر روی بیماران ایتالیایی (با پیگیری بیش از ۲۰ سال) نشان داد که بیماران مبتلا به سمیت گوشی، میانگین سنی بالاتری داشتند و مدت زمان طولانیتری تحت درمان شلاتهکننده قرار گرفته بودند (10). همچنین تارتاگلیـون و همکاران در مرور سیستماتیک خود خاطر نشان کردند که اگر چه مطالعهها نتایج متناقضی را در رابطه بـا فریتین گزارش کردهانـد، اما سن به طور ثابتتری به عنوان یک عامل پیشبینی کننده کاهش شنوایی ظاهر شده است. به علاوه مطالعه فرانوش و همکاران که بر روی یـک کوهورت بزرگ ایرانی (۱۰۱۰ بیمار) انجام شده بود، نیز همبستگی مثبت و معناداری بین سن و اختلالات شنوایی را گزارش کرد (18).
ذکر این نکته ضروری است که برخی مطالعهها در تضاد بـا نتایج ما میباشند. برای مثال بـادفر و همکاران در متاآنالیز خود ارتباط معناداری بین سن و کاهش شنوایی پیدا نکردهاند (13). این ناهمخوانی ظاهری میتوانـد ناشی از عوامل زیر باشد: ساختار سنی جمعیت مورد مطالعه، تأثیر قویتر عوامل مخدوشگر ماننـد عدم پایبندی به درمان شلاتهکننده یا کنترل ضعیف بار آهن میتواند چنان تأثیر مخرب و سریعی داشته باشد که حتی در سنین پایین نیز منجر به عوارض شود.
در مطالعه حاضر بین نوع آهنزدا و اختلالات شنوایی ارتباط معناداری مشاهده نشد. در حالی که برخلاف نتایج ما در مطالعه اشرفی و همکاران گزارش شد کـه بین میزان مصرف دفروکسامین و بروز کاهش شنوایی ارتباط معناداری وجود دارد (8). این یـافتهها تـأیید میکند که اگر چه شلاتورهای آهن برای پیشگیری از عوارض ناشی از بار آهن ضروری هستند، اما خود میتوانند عوارض جانبی مهمی از جمله اتوتوکسیسیتی ایجاد کنند.
در مقابل، مطالعه پوشش دوست و همکـاران، رئیسـی و
همکاران و کمپانی و همکاران همراستا با مطالعه ما گزارش دادند که ارتباط معناداری بین مصرف دفرازیروکس و اختلالات شنوایی وجود ندارد (19، 17، 15). این ناهمخوانی ممکن است ناشی از تفاوت در پروفایل ایمنی شلاتورهای مختلف باشد. دفرازیروکس به عنوان یک شلاتور نسل جدید، احتمالاً پروفایل ایمنی بهتری از نظر عوارض شنوایی دارد. هنوز در این مورد اختلاف نظر وجود دارد و لازم است مطالعههای وسیعتر و به صورت کوهورت انجام شود تا این مسأله با دقت بیشتری مورد بررسی قرار گیرد.
مطالعه طولی آلـده و همکاران نشان داد که درمان طولانی مدت بـا شلاتورهای آهن ممکن است منجر به سمیت گوش شود (10). این یافته اهمیت پایش منظم شنوایی در بیماران تحـت درمان با شلاتورهای آهن را برجسته میسازد.
در مطالعه حاضر غلبه اختلالات شنوایی از نوع حسی-عصبی شایعترین اختلال گزارش شد که بـا بیشتر مطالعههای قبلی مشابـه است. به عنوان مثال، مطالعه تارتاگلیون و همکاران در مرور سیستماتیک خود، شیوع بیشتر کمشنوایی حسی- عصبی را در بیماران تالاسمی گزارش کردند (4). همچنین کمپانی و همکاران نشان دادند که اختلالات عصبی در مقابل اختلالات انتقالی شایعتر است (17).
در مطالعه انجام شده توسط رئیسی و همکاران برخلاف مطالعه ما اختلالات شنوایی انتقالی بیشتر از نوع حسی-عصبی گزارش شده است (15). یافتههای این مطالعه نشان داد کـه 40% از بیماران مبتلا به اختلال شنوایی، درجـه شدید این عارضه را تجربه میکنند. این رقم در مقایسه با مطالعههای پیشین، نگرانکننده و قابـل تأمل است.
مطالعه آلده و همکاران کـه بر روی بیماران با سابقه طولانی درمان شلاتهکننده انجام شد، اغلب موارد کاهش شنوایی را در محدوده خفیف تا متوسط گزارش کرد و موارد شدید عمدتاً در بیماران با سابقه مصرف طولانی مدت و با دوز بالا دفروکسامین دیده شد (10).
مطالعه تیوانا و همکاران نیز که به بررسی دفرازیروکس پرداخت، شیوع بسیار پائینی از کاهش شنوایی بالینی گزارش کرد و اکثر موارد گزارش شده توسط ادیومتری، در مرز تشخیـص و در محدوده خفیف قرار داشتند (20).
این تقابل نشان میدهد اگر چه ممکن است شیوع کلی اختلال در جمعیت مورد مطالعـه ما پایینتر باشد، ولی بار بیماری (Disease Burden) برای آن دسته از بیمارانی کـه درگیر میشوند، به طور قابل توجهی سنگینتر است. این یافته میتوانـد زنـگ خطری برای سیستم بهداشتی منطقه
باشد که نیاز به پیگیری و مداخله قویتر دارد.
فرضیه میتواند توضیح دهنده شدت بالای آسیب در این
جمعیت باشد:
تأخیر در تشخیص و شروع درمان شلاتهکننده، مدت
زمان مواجهه بافتهای حساس مانند حلزون گوش با سطوح بسیار بالای آهن آزاد طولانیتر شده است. این مواجهه طولانی مدت میتواند منجر به آسیب اکسیداتیو غیر قابل برگشت و در نتیجه شدت بیشتر اختلال شود. الگوی مصرف شلاتورها همان طور که در یافتهها ذکر شد، الگوی ترکیبی مصرف شلاتور (به ویژه دفروکسامین و دفرازیروکس) در این جمعیت شایع بود. اگر چـه از نظر آماری ارتباط معناداری پیدا نشد، اما اثر سینرژیستیک (همافزایی) سمیت این دو دارو بر روی سلولهای مویی گوش نمیتواند به طور کامل رد شود. این پدیده در مطالعههای آزمایشگاهی مورد بحث قرار گرفته است.
عوامل محیطی، تغذیهای یا شیوع بالاتر برخی همابتلاییها (مانند کمبود ویتامینهای آنتیاکسیدان مانند A و E که نقش محافظتی در برابر استرس اکسیداتیو دارند) میتوانـد جمعیت را نسبت به سمیت ناشی از آهن یا شلاتورها آسیبپذیرتر کند و شدت عوارض را افزایش دهد.
یافته مربوط به عدم ارتباط فریتین سرم با اختلال شنوایی، اگر چه ممکن است در نگاه اول غیر منتظره به نظر برسد، اما بـا یافتههای برخی مطالعههای معتبر دیگر همخوانی دارد و از منظر پاتوفیزیولوژیک قابل تفسیر است (4). به طور کلی، فریتین سرم یک شاخص غیر مستقیم و گاهی نـاقص برای ارزیـابی بار آهن در بافتهای خاص مانند حلزون گوش محسوب میشود. ممکن است آسیب به سلولهای حساس شنوایی بیش از آن که تحت تأثیر مستقیم سطح کلی آهن خون باشد، ناشی از سمیت اختصاصی برخی شلاتورهای آهن (به ویژه دفروکسامین)، تجمع موضعی آهن در بافت گوش، یا حساسیت فردی و زمینه ژنتیکی باشد. به عنوان مثال، مرور سیستماتیک تارتاگلیون و همکاران (۲۰۲۰) نیز بر عدم وجود ارتباط ثابت بین فریتین و کاهش شنوایی تأکید کرده و نقش مستقل عوامل دیگری مانند اتوتوکسیسیتی دارویی را برجسته نموده است (4).
این موضوع نشان میدهد که مکانیسم آسیب شنوایی در بیماران تالاسمی چند عاملی و پیچیده است و نمیتوان آن را صرفاً به یک شاخص آزمایشگاهی مانند فریتین سرم تقلیل داد. بنابراین، این یـافته بر اهمیت پایش منظم و مستقیم شنوایی با ادیومتری در تمامی بیماران، صرف نظر از عدد فریتین سرم، به عنوان یک جزء ضروری از برنامه مراقبت جامع این بیماران تاکید میکند. برای روشن شدن دقیقتر این مکـانیسمها، انجام مطالعههای طولی مدت که همزمان مارکرهای دقیقتر بـار آهن بافتی و شاخصهای استرس اکسیداتیو را اندازهگیری کنند، پیشنهاد مــــیشود.
محدودیتهای مطالعه:
طراحی مقطعی مطالعه امکـان استنباط رابطه علّی را فراهم نمیکند. از طرفی، حجم نمونـه محـدود، به ویژه تعداد کم بیماران دارای اختلال شنوایی (10 n=)، ممکن است قدرت آماری را برای شناسایی برخی ارتباطات کاهش داده باشد.
نتیجهگیری
اگر چه این مطالعه ارتباط مستقیمی بین سطح فریتین سرم و اختلالات شنوایی در بیماران بتا تالاسمی ماژور نشان نـداد، اما اهمیت پایش منظم شنوایی و مدیریت بهینه بار آهن را بـه ویژه در بیماران مسنتر برجسته میسازد. همچنین همکاری بین هماتولوژیستها، ادیولوژیستها، متخصصان گوش و حلق و بینی و پزشکان داخلی برای حفظ کیفیت زندگی این بیماران ضروری است. از طرفی ارتباط معنادار بین سن و اختلال شنوایی در مطالعه حاضر، یـک پیام بالینی واضح دارد که بیماران مسنتر مبتلا به تالاسمی ماژور یک گروه پرخطر برای اختلالات شنوایی هستند. این موضوع لزوم اجرای یک دستورالعمل پایش منظم و مادامالعمر شنوایی را که با افزایش سن بیماران تکرار و تشدید میشود، ایجاب میکند.
این رویکرد پیشگیرانـه نه تنها میتواند به تشخیص زود هنگام کمک کند، بلکه امکان تعدیل رژیم درمانی (ماننـد بررسی دوز شلاتورها) را قبل از بروز آسیب غیر قابـل برگشت فراهم میآورد و در نهایت به حفظ کیفیت زندگی این بیماران کـه به لطف پیشرفتهای درمانی، به سنین میانسالی و بالاتر میرسند، کمک شایانی میکند.
حمایت مالی
ایـن پـروژه با حمایت مالی دانشگاه علوم پزشکی یاسوج
انجام شده است.
ملاحظات اخلاقی
ایـن پـژوهش منتـج از پایاننامـه دانشجویـــی با عنوان
بررسی ارتباط سطح فریتین با اختلالات شنوایی در بیماران تـالاسمی ماژور شهر یاسوج بـا کد اخـلاق IR.YUMS.REC.1404.116 به تصویب رسیـده است.
عدم تعارض منافع
نویسندگان اظهار میکنند هیچگونه تعارض منافعی در
این مطالعه وجود نداشته است.
نقش نویسندگان
دکتر غلامعباس سبز: همکاری در طراحی موضوع و مشاوره
بالینی و کمک در تفسیر نتایج، نوشتن مقاله
دکتر فریبا راد: طراحی موضوع، مدیریت پروژه، ادیت مقاله و پاسخ به مجله
عاطفه سرائی: انجام آزمایشها و جمعآوری دادهها
تشکر و قدردانی
بدینوسیله نویسندگان از کارکنان محترم بیمارستان شهید بهشتی یاسوج تشکر و قدردانی مینمایند.
فهرست منابع
1. Ansharullah BA, Sutanto H, Romadhon PZ. Thalassemia and iron overload cardiomyopathy: Pathophysiological insights, clinical implications, and management strategies. Curr Probl Cardiol 2025; 50(1): 102911. [DOI:10.1016/j.cpcardiol.2024.102911] [PMID]
2. Wang LE, Muttar S, Badawy SM. The challenges of iron chelation therapy in thalassemia: how do we overcome them? Expert Rev Hematol 2025; 18(5): 351-7. [DOI:10.1080/17474086.2025.2489562] [PMID] []
3. Herdata HN, Taufani V, Destiani E, Andid R. The association between serum ferritin levels and growth parameters in children with β-thalassemia major. AcTion: Aceh Nutrition Journal 2025; 10(3): 720-5. [DOI:10.30867/action.v10i3.2681]
4. Tartaglione I, Carfora R, Brotto D, Barillari MR, Costa G, Perrotta S, et al. Hearing loss in beta-thalassemia: systematic review. J Clin Med 2021; 11(1): 102. [DOI:10.3390/jcm11010102] [PMID] []
5. Musiek FE, Chermak GD. Handbook of central auditory processing disorder, volume I: Auditory neuroscience and diagnosis. USA: Plural Pub Inc; 2013.
6. Alanazi AA. Understanding auditory processing disorder: A narrative review. Saudi J Med Med Sci 2023; 11(4): 275-82. [DOI:10.4103/sjmms.sjmms_218_23] [PMID] []
7. Khavidaki GA, Gharibi R, Naderi M, Sedaghatkia H. The Investigation of Hearing Loss in Patients with Thalassemia Major Referred to Hazrat Ali Asghar (AS) Hospital in Sistan and Baluchistan Province (Iran). Maedica (Bucur) 2024; 19(4): 731-5. [DOI:10.26574/maedica.2024.19.4.731] [PMID] []
8. Ashrafi M, Mohammadzadeh A. Hearing status of thalassemic patients treated with dessfroxamin. J Kermanshah Univ Med Sci 2012; 15(5): e79024. [Article in Farsi]
9. Mohammed SH, Shab-Bidar S, Abuzerr S, Habtewold TD, Alizadeh S, Djafarian K. Association of anemia with sensorineural hearing loss: a systematic review and meta-analysis. BMC Res Notes 2019; 12(1): 283. [DOI:10.1186/s13104-019-4323-z] [PMID] []
10. Aldè M, Ambrosetti U, Giuditta M, Cassinerio E, Piatti G. Effects on hearing after long-term use of iron chelators in beta-thalassemia: Over twenty years of longitudinal follow-up. Auris Nasus Larynx. 2024; 51(2): 271-5. [DOI:10.1016/j.anl.2023.10.005] [PMID]
11. Horikawa C, Kodama S, Tanaka S, Fujihara K, Hirasawa R, Yachi Y, et al. Diabetes and risk of hearing impairment in adults: a meta-analysis. J Clin Endocrinol Metab 2013; 98(1): 51-8. [DOI:10.1210/jc.2012-2119] [PMID]
12. Hasan AF, Salman HH, Khalaf JM. Evaluation of hearing in patients with Beta Thalassemia Major. Basrah Journal of Surgery 2018; 24: 47-51. [DOI:10.33762/bsurg.2018.160106]
13. Badfar G, Mansouri A, Shohani M, Karimi H, Khalighi Z, Rahmati S, et al. Hearing loss in Iranian thalassemia major patients treated with deferoxamine: A systematic review and meta-analysis. Caspian J Intern Med 2017; 8(4): 239-49.
14. Bhatia PL, Gupta OP, Agrawal MK, Mishr SK. Audiological and vestibular function tests in hypothyroidism. Laryngoscope. 1977; 87(12): 2082-9. [DOI:10.1288/00005537-197712000-00014] [PMID]
15. Reisi N, Kargoshaei AA. Prevalence of hearing loss in patients with Beta thalassemia major, Hajar hospital of Shahrekord, 2002. Journal of Shahrekord University of Medical Sciences 2004; 6(2): 31. [Article in Farsi]
16. Chahkandi T, Moffateh MR, Sharifzadeh Gh.R, Azarkar Z. Hearing impairment in patients with major thalassemia in Southern Khorasan Province, 2007. Journals of Birjand University of Medical Sciences 2011; 18(2): 102-8. [Article in Farsi]
17. Campani F, Rezaei N, Yusefi GH. Evaluation of hearing and otolaryngologic disorders in patients with thalassemia treated with deferoxamine. Sci J Kurdistan Univ Med Sci 2009; 14(3): 47-55. [Article in Farsi]
18. Faranoush M, Faranoush P, Heydari I, Foroughi-Gilvaee MR, Azarkeivan A, Parsai Kia A, et al. Complications in patients with transfusion dependent thalassemia: A descriptive cross-sectional study. Health Sci Rep 2023; 6(10): e1624. [DOI:10.1002/hsr2.1624] [PMID] []
19. Poosheshdoost P, Faraji N, Zeinali T, Baghersalimi A, et al. Visual and auditory complications during deferasirox therapy in beta-thalassemia. Iran J Ped Hematol Oncol 2022; 12(4): 229-39. [Article in Farsi] [DOI:10.18502/ijpho.v12i4.10913]
20. Tiwana BS, Aggarwal A, Bhagat S, Singh H, Sahni D, Yadav V. Assessing the auditory effects of oral chelation therapy drug Deferasirox in individuals with β-thalassemia major. World J Otorhinolaryngol Head Neck Surg 2024; 10(4): 309-14. [DOI:10.1002/wjo2.150] [PMID] []
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |






