جلد 22، شماره 2 - ( تابستان 1404 )
جلد 22 شماره 2 صفحات 149-137 |
برگشت به فهرست نسخه ها
Ethics code: IR.BUMS.REC.1403.233
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Nakhaei Shamahmood M, Nasiri M, Meghdadi M, Mortazi H, Asadifard M, Erfani F, et al . Kell and E Alloantibodies as the Main Causes of Alloimmunization in Transfusion-Dependent Thalassemia Patients: A Cross-Sectional Study. bloodj 2025; 22 (2) :137-149
URL: http://bloodjournal.ir/article-1-1586-fa.html
URL: http://bloodjournal.ir/article-1-1586-fa.html
نخعی شامحمود مبینا، نصیری مازیار، مقدادی محمدرضا، مرتاضی حسن، اسدی فرد معصومه، عرفانی فرزانه، و همکاران.. آلوآنتی بادیهای Kell و E، علل اساسی آلوایمونیزاسیون در بیماران تالاسمی وابسته به تزریق خون: مطالعه مقطعی. فصلنامه پژوهشی خون. 1404; 22 (2) :137-149
مبینا نخعی شامحمود 

 ، مازیار نصیری
، مازیار نصیری 
 ، محمدرضا مقدادی
، محمدرضا مقدادی 

 ، حسن مرتاضی
، حسن مرتاضی 
 ، معصومه اسدی فرد
، معصومه اسدی فرد 
 ، فرزانه عرفانی
، فرزانه عرفانی 
 ، امید حسنی اکبریه
، امید حسنی اکبریه 
 ، فاطمه مزگی نژاد*
، فاطمه مزگی نژاد* 




 ، مازیار نصیری
، مازیار نصیری 
 ، محمدرضا مقدادی
، محمدرضا مقدادی 

 ، حسن مرتاضی
، حسن مرتاضی 
 ، معصومه اسدی فرد
، معصومه اسدی فرد 
 ، فرزانه عرفانی
، فرزانه عرفانی 
 ، امید حسنی اکبریه
، امید حسنی اکبریه 
 ، فاطمه مزگی نژاد*
، فاطمه مزگی نژاد* 


استادیار مرکز تحقیقات سلولی و مولکولی ـ دانشکده پیراپزشکی دانشگاه علوم پزشکی بیرجند
متن کامل [PDF 721 kb]
(582 دریافت)
| چکیده (HTML) (1454 مشاهده)
مقدمه
تالاسمی به عنوان یکی از شایعترین اختلالات ژنتیکی مرتبط با کمخونی ارثی در سطح جهانی شناخته میشود که به علـت نقص در تولید زنجیرههای گلوبین ایجاد شده و منجر بـه کاهش تولید هموگلوبین در گلبولهای قرمز خون (RBCs) میگردد (2، 1)، تـالاسمی بر اساس نوع زنجیره گلوبین درگیر بـه دو گروه اصلی انواع آلفا (α) تالاسمی و بتا (β) تالاسمی طبقهبندی میشود. بتاتالاسمی بر اساس میزان سنتز زنجیرههای β به انواع ماژور، اینترمدیا و مینور طبقهبندی میشود که بتاتالاسمی ماژور به عنوان شدیدترین فرم بیماری شناخته میشود (3). این بیماری به ویژه در مناطقی از حوزه مدیترانه تا خاورمیانه، هند و آسیای جنوب شرقی فراوانی بالایی دارد (4). تالاسمی تقریباً 2/4 نفر از هر 10000 نفر در سراسر جهان را تحت تـأثیر قرار میدهد (5). در ایران نیز بیش از 2 میلیون ناقل تالاسمی (حدود 4% جمعیت) و بیش از بیست هزار بیمار تالاسمی ماژور وجود دارد (7، 6).
بیماران تـالاسمی ماژور قدرت تولید گلبولهای قرمز سالم و فعال را از دست میدهند و در ضمن گلبولهای به ظاهر سالم آنها نیز به سرعت تخریب میشوند در نتیجه، این افراد به درمانهای حمایتی مادامالعمر مانند تزریق منظم خون وابسته هستند (8). اساس درمان بیماران تالاسمی، پیوند سلولهای بنیادی خونساز است، اما تزریق خون مکرر و منظم، درمان انتخابی و در غیاب پیونـد بـه عنوان درمان حمایتی و مهم میباشد (به طور متوسـط هـر ماه یک واحد) (9، 8). در بیماران مبتلا به تالاسمی ماژور، اگر چه تزریـق خون، نقص در تولیـد گلبـولهـای قرمز خـون را اصلاح نمیکند، ولی با افزایش سطح هموگلوبین، عوارض غیـر طبیعـی در تالاسـمی و علائم کـم خونی مزمن را بهبود میبخشد و بقای بیماران را افـزایش میدهـد (10). البته تزریق منظم و مکرر خون با یکسری از مشکلات بالینی با اهمیـت مانند واکنشهای آلرژیک، واکنشهای تـبزای غیرهمولیتیـک تزریق خـون، اضافه بار گردش خون، آسیب ریه مربوط به انتقال خون (TRALI)، عفونتهای باکتریایی و ویروسی، افزایش بار آهن و آلوایمونیزاسیون که از عوارض تزریق خون هستند، همراه است. این موارد سودمندی تزریق خون را در طول زمان کاهش میدهند و ممکن است تهدیدکننده زندگی باشند (11، 10).
تزریق خون موجب ورود آنتیژنهای مختلف گلبولهای
قرمز به بدن بیماران شده و باعث تحریک سیستم ایمنی بیماران فاقد این آنتیژنها و تولید آنتـیبادیها علیه آنها میشود؛ این آنتیبادیها را آلوآنتیبادی مینامند و بیمــاران تولیــد کننــده آلـوآنتــیبــادی را آلوایمــونیزه مـینامنــد. افزایش شیوع آلوایمونیزاسیون علیه گلبولهای قرمز میتوانـد تزریق خون سازگار آزمایشگاهی را دچار مشکلات فراوان نماید که میتوان به واکنشهای همولیتیک ناشی از تزریق خون یا HTR و همچنین کوتاه شدن عمر مفید گلبولهای قرمز تزریق شده اشاره نمود (12). از آنجایی که در انتخاب خون تزریقی فقط سیستمهای گروه خونی ABO و Rh کنترل میشوند و سایر گروهها معمولاً در نظر گرفته نمیشوند، اکثر آلوآنتیبادیها علیه آنها شکل گرفته و عامل ناسازگاری در کراسمچ و یا ناسازگاری بالینی میبـاشد. مطالعههای مختلف نشان دادهاند که در دو سوم ایـن موارد، آنتیبـادی مسئول مربوط به زیرگروههای سیستمRh (E، C، c، e) و گروههای فرعی نظیر Kell، Duffy و Kidd میباشند (15-13).
احتمـال ایجـاد آلوآنتیبادی به دنبـال تزریـق یـک کیسـه خـون 1% تا 6/1% است، در حالی که احتمال ایجاد آنتیبادی در بیمـاران بـا تزریقهای منظم و مکرر مانند بیماران تالاسمی، کـم خـونی داسـی شـکل و بـدخیمیهای هماتولوژیک (لوسمی، سندروم میلودیس پلاستیک) به حدود 60% میرسد (16). همچنین افـرادی که یک آلوآنتیبادی در آنها ایجـاد مـیشـود، دارای خطـر بالاتری برای تولید آلوآنتیبادیها و اتوآنتیبادیهای بیشـتر به دنبال تزریق خونهای بعدی هستند که این امر میتوانـد فرآیند شناسایی خون سازگار را در این بیمـاران بـا مشـکل مواجه ساخته و سبب تأخیر در فرآیند تأمین و تزریق خون سازگار گردد (17).
مطالعههای قبلی میزان فراوانی آلوایمونیزاسـیون را در بیمـاران مبتلا به تالاسمی بین 87/2 % تا 55% گـزارش کـردهانـد (18، 3). علیرغم اهمیت درک فراوانی این آلوآنتیبادیها در بیماران تالاسمی بـرای بهبود شیوههای انتقال خون و بهبود بیماران، مطالعه جـامعی با تمرکز بر این موضوع در شهرستان بیرجند وجود ندارد. این شکاف در دانش، مانع از توسعه استراتژیهای مؤثر برای به حداقل رساندن آلوایمونیزاسیون در بیماران تـالاسمی، به ویژه در مناطقی با فراوانی بالای تالاسمی میشود .بنابراین مطالعه حاضر با هدف بررسی فراوانی آلوآنتی بادیهای شایع در بیماران تالاسمی وابسته به تزریق خون شهرستان بیرجند در سال 1403و ارتبـاط آلوایمونیزاسـیون بـا عـواملی همچون سن، جنس، گروه خونی، برداشتن طحال و تعداد واحدهای تزریق شده خون بود.
مواد و روشها
این مطالعه به صورت توصیفی-مقطعی بـا کـد اخلاق IR.BUMS.REC.1403.233 در سال 1403 در دانشگاه علوم پزشکی بیرجند و با همکاری سازمان انتقال خون بیرجند بر روی بیماران تالاسمی ماژور وابسته به تزریق خون انجام شد. در این مطالعه از تمامی بیماران تالاسمی ماژور که جهت دریافت خون در سال 1403 به بیمارستان ایرانمهر بیرجند مراجعه کردند، نمونهگیری به صورت سرشماری انـجام شد و در نهایت بیمارانی که دارای معیارهای لازم برای ورود به مطالعه بودند، وارد مطالعه شدند. از معیارهای ورود بـه مطالعه میتوان به تایید بیماری تالاسمی ماژور توسط تستهای آزمایشگاهی و پزشک متخصص، کامل بودن پرونده پزشکی بیماران و تزریق مکرر خون (هر هفته حداقل یـک مرتبه) اشاره کرد. همچنین از معیار خروج مطالعه میتوان به ابتلا به بیماری تالاسمی اینترمدیا، کامل نبودن پرونده پزشکی بیماران و ابتلا به بیماریهای عفونی مانند انواع هپاتیت و ایـدز اشاره نمود. در ابتدا، اطلاعات دموگرافیک شامل سن، جنس، اطلاعات بـالینی و آزمایشگاهی شامل CBC (میزان گلبولهای قرمز، گلبولهای سفید، هموگلوبین و پلاکت)، تعداد دفعات تزریق خون در سال و وضعیت طحالبرداری بیماران تـالاسمی وابسته به تزریق خون مکرر بیرجند از پرونده الکترونیک بیماران استخراج گردید.
پس از دریـافت رضایتنامه کتبی از هر بیمار، قبل از تزریق خون، 2 میلیلیتر خون در لوله حاوی ضد انعقاد K2-EDTA برای تعیین فنوتیپ گروههای خونی ABO و 5 میلیلیتر خون بدون ضد انعقاد (لوله لخته) برای آزمایشهای غربـالگری آنتیبادی و تعیین هویت آنتیبادی گرفته شد. فنوتیپ گروههای خونی ABO بیماران با استفاده از روش لولـهای تعیین شد و آنتیژنهای گروه خونی Rh (D، C، E، c، e) و Kell با استفاده از آنتیسرمهای شرکت ایمیون دیاگنوستیکای آلمان مطابق دستورالعمل موجود در کیت تعیین گردید.
آزمایش غربالگری آنتیبادیهای غیـر منتظــره بـر روی
سرم همه بیماران با استفاده از روش پنل سلولی 3 تایی (سلولهای غربالگر R1R1/I، R2R2/II، rr/III) شرکت کیان ژن یـاخته (تهران، ایران) طبق روشهای استاندارد بانک خون که در پایین به آن اشاره شده است، انجام شد. سلولهای غربالگر، 3 ویال حاوی مجموعهای از سلولهای دارای آنتیژنهای مهم بالینی از قبیل P1، Lea، Leb، M، N، Fya، Fyb، S، s، Jka، Jkb، C، c، E، e، D میبـاشند. دو حجم از سرم بیمار با یک حجم سوسپانسیون 2 تا 5 درصد گلبولهای اسکرین مجاور شدند. یک نمونه در دمای اتـاق (RT) و دو نمونـــه در دمای 37 درجه سانتیگراد قـــرار گرفـــت. پـــس از 20 تا 30 دقیقـــه انکوباسیون، لولهها به مـدت 30 ثانیـه بـا دور 3000 در دقیقه سـانتریفوژ شدند و سپس به صـورت میکروسـکوپی و ماکروسکوپی از نظر وجود آگلوتیناسیون مورد بررسی قرار گرفتند. در صورت عدم مشاهده آگلوتیناسـیون، بـه منظـور یافتن آنتیبادیهای ناقص و یا احتمالاً دارای تیتر پـایین، ازAHG استفاده شد. مشاهده آگلوتیناسیون در هـر کـدام از مراحـل ذکر شده به منزلـه مثبت بودن غربالگری آنتـیبـادی تلقـی میگردید.
در صورت منفی بودن واکنش، بـه منظور اطمینان از فعال بودن AHG و صحت نتایج به دست آمـده، نتیجـه حاصله بـا سـلولهـای کنتـرل یـا چک سل (Check Cell) (گلبولهای قرمز حساس شده باIgG ) مورد کنتـرل کیفـی قرار گرفتند و در صورت واکنش مثبت با چک سل، نتیجه آزمایش تـایید شد. سپس تعیین هویت آنتیبادی (Ab Identification) بـر روی نمونههای مثبت از لحاظ غربالگری آنتیبادی با استفاده از روش پنل سلولی 11 تایی (پنلهای سلولی استاندارد تهیه شده در سازمان انتقال خون ایران) مشابه همان مراحل غربالگری آنتیبادی انجام پذیرفت که نتایج حاصله با توجه به جدول آنتـیگرام (Antigram) موجود در کیت تفسیر شد. نتایج به دست آمده در این مطالعه، با استفاده از نرمافزار آماری SPSS نسخه 26 مورد تجزیـه و تحلیل قرار گرفت. دادههای توصیفی با استفاده از فراوانی و درصد و دادههای کمی با استفاده از میانگین ± انحراف معیار گزارش شدند. از آزمونهای آماری کایدو (chi-square) و آزمایش دقیق فیشر (Fisher Exact Test) در تجزیه و تحلیل نتایج استفاده شد و سطح 05/0 p< به عنوان سطح معنـاداری در نظر گرفته شد.
یافتهها
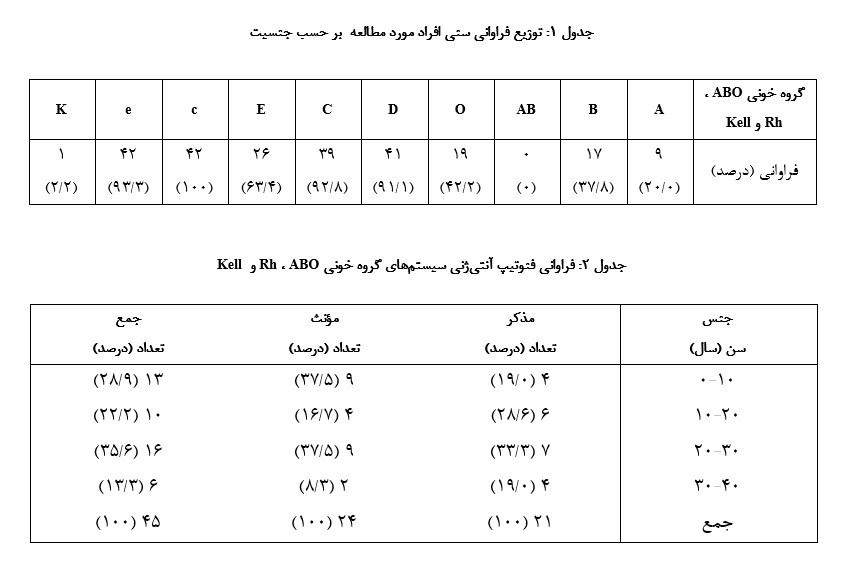
در این مطالعه، تعداد 45 بیمار مبتلا به تالاسمی وابسته به تزریق خون با میانگین سنی 73/10 ±18 سال و دامنه سنی 1 تا 36 سال مورد بررسی قرار گرفتند. اطلاعات مورد نیاز برای تمامی بیماران واجد شرایط به طور کامل از پروندههای الکترونیک استخراج شد و هیچ موردی از داده گمشده (missing data) وجود نـداشت. بنابراین، تمامی ۴۵ بیمار وارد مطالعه شدند و تحلیل دادهها بر اساس اطلاعات کامل انـجام گرفت. از بیـن ایـن بیماران، 21 نفر مرد (6/46 %) با میانگین سنی 29/10 ± 95/19 سال و 24 نفر زن (3/53 %) با میانگین سنی 02/11 ± 29/16 سال بودند (جدول 1).
فنوتیپ آنتیژنی سیستمهای گروه خونی ABO، Rh و Kell تعیین گردیـد (جدول 2). فراوانترین فنوتیپ سیستم ABO، گروه خونی O (2/42 %) و فراوانترین آنتـیژن سیستم Rh، آنتیژن c و e بود کـه به ترتیب در100% و 3/93 % بیماران وجود داشت. فراوانی آنتیژن Kell در جمعیت بیماران استان خراسان جنوبی پـایین بود به طوری که فقط 1 بیمار (2/2%) دارای آنتیژن K بود.
از مجموع 45 بیمار مورد مطالعه، 3 بیمار (بـا فاصله اطمینان 95%: ۲/۲ تـا ۱/18 درصـد) غربالگـری آنتیبـادی
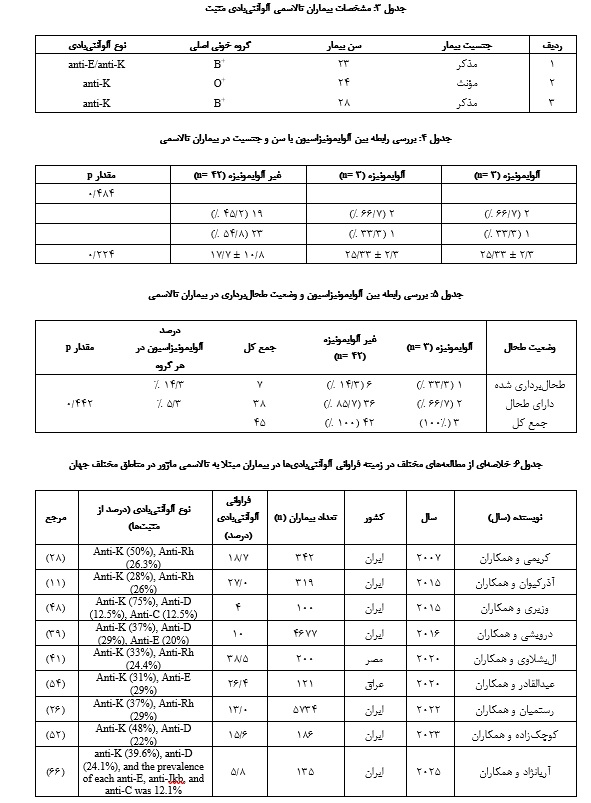
مثبت داشتند و تعداد 4 آلوآنتیبادی شناسایی گردید. با بـررسی نتایج تعیین هویـت آنتیبادی، شایعترین آلوآنتیبادیها شامل anti-K (3 نفر، 100%) و anti-E (1 نفر، 33 %) بود. از 3 بیمــاری کــه تولیـد آلـوآنتیبـادی کردنـد، 2 نفر مرد (6/66%) و 1 نفر زن (3/33%) با میانگین سنی 3/2±33/25 سال بودند (جدول 3). تفاوت معناداری بین آلوایمونیزاسیون و سن و جنس مشاهده نشد (جدول 4). همچنین نتایج آزمون آماری کایدو نشان داد که میان آلوایمونیزاسیون با گروه خونی ABO و Rh(D) ارتباط معناداری وجود ندارد. بیشترین و کمتریـن میزان آلوایمونیزاسیون بـه ترتیب در بیماران تالاسمی با گروه خونی B (2 مورد) و O (1 مورد) بود (جدول 3).
از بین 45 بیمار تالاسمی مورد مطالعه، 7 نفر از بیماران (5/15 %) طحالبـرداری شده بودنـد که شامل 3 مرد (9/42 %) و 4 زن (1/51%) بودند و 38 نفر از بیماران (4/84 %) نیز دارای طحال بودند. بر طبق نتیجه آزمون آماری کـایدو، میان آلوایمونیزاسیون و وضعیت طحال ارتباط معناداری یـافت نشد (جدول 5). همچنین نتایج آزمون آماری نشان داد که ارتباط معناداری میان آلوایمونیزاسیون و تعداد واحدهای تزریق خون در بیماران تالاسمی وابسته به تزریق خون وجود ندارد.

بحث
تزریق خون مکرر در بیماران تـالاسمی میتواند باعث آلوایمونیزاسیون علیه آنتیژنهای مختلف گلبول قرمز اهداکننده شود که در گلبولهای قرمز بیماران وجود ندارد. این آلوایمونیزاسیون میتواند بقای گلبولهای قرمز خون را کاهش داده و همچنین کارآیی انتقال خون را نیز کاهش دهد. عوامل آلوایمونیزاسیون پیچیده هستند و حداقل شامل سه مؤلفه اصلی میشوند: 1) تفاوت آنتیژنی گلبولهای قرمز (RBC) بین اهداکننده و گیرنـده خون 2) وضعیت عملکرد سیستم ایمنی گیرنـده خون 3) اثر ایمونومدولاتوری انتقال خون آلوژنیک بر سیستم ایمنی گیرنده (19). در این مطالعه، ما 4 آلوآنتیبادی بر علیه گلبول قرمز را در 3 بیمار (6/6%) مبتلا به تالاسمی وابسته به تزریق خون شناسایی کردیم. 3 بیمار (75%) دارای anti-K و 1 بیـمار (25%) دارای anti-E بودند. میزان فراوانی آلوآنتیبادی در بیماران تالاسمی وابسته به خون به طور متغیر و با دامنه وسیع از 53/1% تا 55% گزارش شده است (20، 3).
میزان فراوانی آلوآنتیبادی در بیماران تالاسمی وابسته بـه خون به طور متغیر و با دامنه وسیع از 53/1% تا 55% گزارش شده است (20، 3). مشابه و همسو با مطالعه ما، در یک مطالعه گذشتهنگر در کشور عمان، ریامی و سایر همکارانش نشان دادند که میزان فراوانی آلوایمونیزاسیون در بیماران مبتلا به تالاسمی وابسته به تزریق خون مکرر 3/9 % و فراوانترین آلوآنتیبادیهـای ایجاد شده شامل anti-K و anti-E بود (21). علاوه بر این میزان آلوایمونیزاسیون در 64 بیمار چینی مبتلا به تالاسمی ماژور در تـایوان 4/9 % گزارش شد که همه آنتیبادیها علیه آنتیژنهای Rh بودند (22). شیوع آلوآنتیبادی در یـک مطالعه مصری بر روی 501 بیمار مبتلا بـه بتا تالاسمی 3/11 % بود که Anti-K، Anti-E و Anti-C شیوع بیشتری داشتند (23). همچنین عبیدی و همکاران گزارش کردند که شیوع آلوآنتیبـادی در 90 بیمار مبتلا به تالاسمی بوشهری، 9% بود که آلوآنتیبادی علیه سیستم گروه خونی Kell بیشترین فراوانی را داشت (24). احمدی و همکاران نیز بـا مطالعهای که بر روی 142 بیمار مبتلا به تالاسمی وابسته به تزریق خون مکرر انجام دادند، میزان فراوانی آلوآنتیبادیها را 2/9% گزارش کردند (25). تمامی این مطالعهها مشابهت زیادی از لحاظ فراوانی آلوآنتیبـادیها با نتایج مطالعه ما دارند. یک مطالعه سیستماتیک و متاآنالیز با تجزیه و تحلیل 23 مقالـه (شامل 5734 بیمار)، میزان فراوانی آلوآنتیبادیها در بیماران تالاسمی وابسته به تزریق خون در جمعیت ایرانیان را 13% گزارش کرده است که فراوانترین آلوآنتیبادیهای تشکیل شده بر علیه سیستمهای گروه خونی Rh (D، E، C) و Kell بوده است (26). میزان آلوایمونیزاسیون در نقاط مختلف ایران به شرح زیر گزارش شده است: 4/7% (تهران)، 34/5% (استان فارس)، 7/18% (جنوب غربی ایران، اهواز) و 78/2 % (شمال شرق ایران، مشهد) (29-27، 18). به علاوه، فراوانی آلوایمونیزاسیون در کشورهای دیگر شامل 30% (کویت)، 5/19 % (مصر)، 4/7% (هنگکنگ)، 5% (ایتالیا)، 5/9% (هند) و 2/9% (پاکستان) است (35-30). این تفاوت بین میزان آلوایمونیزاسیون بین مطالعههای مختلف، به دلیل تفاوت در موقعیت جغرافیایی مناطق، تفاوت نژادی و هتروزیگوسیتی ژنتیکی بین گروههای مورد مطالعه و میزان همسانی فنوتیپ گروههای خونی اهداکنندگان خون بـا بیماران تالاسمی دریافتکننده این خونها میباشد.
نتایج مطالعه ما نشان داد که فراوانترین آلوآنتیبادیهای ایجاد شده بر علیه گروههای خونی Kell و Rh بودند. مطالعههای مختلف نشان دادهاند که اکثر آلوآنتیبادیهای تشکیل شده در بیماران مبتلا به تالاسمی وابسته به تزریق خون بر علیه سیستمهای گروه خونی Kell و Rh (D، C، E، c، e) بودهانـد. کیخایی و سایر همکاران نشان دادند که الگوی غالب آلوایمونیزاسیون آلوآنتیبادی علیه سیستم زیرگروههای Rh در 55 درصد بیماران و 33 درصد بیماران آلوآنتیبادی علیه سیستم Kell بود (29). در مطالعهای که توسط قاسمی و همکاران انجام شد، نشان دادند که الگوی غالب آلوایمونیزاسیون آلوآنتیبادی علیه سیستم Rh (D، C، E و C) در 3/58% از بیماران و 6/16% از بیماران آلوآنتیبادی علیه سیستم Kell بود (36). آمین و همکاران میزان فراوانی anti-K در 72% و anti-E را در 6/45% از بیماران مبتلا به تـالاسمی دارای آلوآنتیبادی مثبت گزارش کردهاند (30). اغلب آلوآنتیبادیهای تشکیل شده در یک مطالعه که بر روی بیماران مبتلا به تالاسمی شیراز انجام شده است، بر علیه زیر گروه خونی Kell (%50) و Rh (3/%26) بوده است (28). نتایج یـک مطالعه در جنوب شرق ایران (زاهدان) نشان داد که فراوانترین آلوآنتیبـادیهای تشکیل شده بر علیه زیر گروه خونی Rh (%28) و Kell (%8) بوده است (37). محمدی مرام و همکاران در مطالعهای که بر روی بیماران تالاسمی شهر تهران انجام دادند، گزارش کردند که بیشترین میزان آلوآنتیبادی شامل anti-K و anti-E بوده است (38). در مطالعهای سیستماتیک و متاآنالیز که توسط درویشی و همکاران در جمعیت بیماران تـالاسمی ایران انجام شد، میــزان آلوایمونیزاســیون در ایــران 10% گزارش شد و بیشترین آلوآنتیبـادیها مربوط به anti-K (%37)، anti-D (%29) و anti-E (%20) بودند (39). در مطالعه آذرکیوان و همکارانش، شایعترین آلوآنتیبـادیها علیه سیستم Rh (E/e/C/c/Cw) (%26)، anti-K (%28) و anti-D (%16) بود (11). در یک مطالعه که در کشور مصر بر روی بیماران تالاسمی با تزریق خون مکرر انجام شده است، شـایعتـرین آلوآنتیبادیها مرتبط بـا سیستم Rh (به ترتیب anti-E، anti-D، anti-C و anti-c) و گروه خونی Kell بوده است (40). همچنین در مطالعه دیگری در کشور مصر که بر روی 200 بیمار تالاسمی با تزریق خون مکرر انجـام شد، آنتیبـادی علیه گروه خونی Kell (%33) و آنتیبادی علیه گروه خونی Rh (4/%24) شایعترین آلوآنتیبادیهای تشکیل شده بودند (41). یک مطالعه که در کشور عراق انجام شده است، شــایعتــرین ایــن آلوآنتیبادیها به anti-E، anti-D و anti-K نسبت داده شده است (42)(جدول 6).
در مطالعه حاضر ارتباط معناداری بین آلوایمونیزاسیون بـا سن، جنسیت و گروه خونی مشاهده نشد. نتایج مطالعههای قبلی نشاندهنده افزایش فراوانی آلوآنتیبادیها با افزایش سن به دلیل تزریق خون بیشتر بود (45-43). با این حال، مشابـه مطالعه ما، چندین مطالعه، مانند مطالعه افشاری و همکاران، زری طحاننژاد اسدی و همکاران، داوری و همکاران، میرزائیان و همکاران، وزیری و همکاران، ارتباط معناداری بین سن و آلوایمونیزاسیون پیدا نکردند (46-48، 37 ، 3). همچنین مطالعههای صادقیان و همکاران، حسن و همکـاران این نکته را تایید کردند کـه میان آلوایمونیزاسیون و سن ارتباط معناداری وجود ندارد (49، 18).
جنسیت، به عنوان یک عامل خطر، موضوع بحث برانگیز است. به دلیل قرار گرفتن بیشتر در معرض وقایع ایمنسازی، مانند بارداری و تزریق خون، انتظار میرود که زنان میزان بالاتری از آلوایمونیزاسیون RBC را تحمل کنند. اگرچه مطالعهها به طور کلی رابطه معناداری بین جنسیت و فراوانی آنتیبادیها را گزارش کردهاند، به طوری که برخی فراوانی بالاتر آلوآنتیبادی را در بیماران زن و برخی دیگر بیماران مرد گزارش کردهاند (51، 50). چندین مطالعه دیگر همسو و مشابـه با نتایج مطالعه ما نیز هیچ رابطه معناداری بین جنسیت و فراوانی آلوآنتیبادیها پیدا نکردند (52، 48، 45، 44، 11). همچنین نتایج یک مطالعه سیستماتیک و متاآنالیز بر روی بیماران تالاسمی وابسته به تزریق خون جمعیت ایرانیان (5734 بیمار) انجام شد، هیچ تفاوت قابل توجهی در میزان فراوانی آلوایمونیزاسیونRBC بین مردان و زنان تالاسمی (10% و 11% به ترتیب) شناسایی نکرد (26). این نتیجه مشابه نتیجه مطالعه ما بود. این نتایج حاکی از اهمیت در نظر گرفتن عوامل دیگری مانند سابقه بارداری در زنان، سن شروع تزریق خون، تعداد واحدهای خونی تزریق شده و وضعیت اسپلنکتومی است.
بر اساس نتایج مطالعه حاضر، گروه خونی ABO و Rh (D) ارتباط معناداری با فراوانی آلوآنتیبادیها نداشتند که بـا نتایج مطالعه جمعیت ایرانی اقبالی و همکاران همخوانی داشت (53). رئوف عبدالقادر و همکاران مطالعه ای را در یک جمعیت عراقی انجام دادند و به نتایج مشابهی دست یافتند (54). وزیری و همکاران گزارش دادهاند که میان آلوایمونیزاسیون و گروه خونی ABO ارتباط معناداری وجود ندارد (48). علاوه بر این میرزائیان و سایر همکاران نشان دادنـد بین فراوانی آلوایمونیزاسیون و گروه خونی ABO و Rh تفاوت معناداری وجود ندارد (37). این یافتهها در مطالعههای متعددی گزارش شده است و به نظر میرسد گروه خونی نقش مهمی در فراوانی آلوآنتیبادیها نـداشته باشد.
نتایج مطالعه ما نشان داد که 7 نفر (5/15%) از بیماران اسپلنکتومی یا طحالبرداری شده بودند. همچنین در این مطالعه ارتباط معناداری بین آلوایمونیزاسیون با وضعیت طحال و تعداد واحدهای خون تزریق شده در بیماران تالاسمی مشاهده نشد.
بیماران مبتلا بـه تالاسمی اینترمدیا و ماژور، به تزریق خون مکرر برای جبران کمبود گلبولهای قرمز با عملکرد طبیعی نیاز دارنـد (55). با توجه به این که گلبولهای قرمز معیوب یـا آسیب دیده در طحال از بین میروند، بیماران تالاسمی دچار بزرگ شدن عملکردی طحال (هیپراسپلنیسم) میشوند. بنابراین، برداشتن طحال ممکن است بقای گلبولهای قرمز را طولانی کند، که به نوبه خود میتواند نیاز به تزریق خون را کاهش دهد (56). فیلتراسیون یکی از مهمترین نقشهای طحال است که در بیماران طحالبرداری شده حذف میشود. اسپلنکتومی میتواند منجر بـه افزایش خطر آلوایمونیزاسیون شود، به ویژه در بیمارانی که به دلیل اختلالات هماتولوژیک مانند تالاسمی یا کمخونی داسی شکل تحت این عمل قرار میگیرند. این افزایش عمدتاً به دلیل کاهش فیلتراسیون آنتیژنهای گلبولهای قرمز آسیب دیده و بقای طولانیتر آنها در گردش خون است که در نتیجه مواجهه سیستم ایمنی با آنتیژنهای غیرخودی و تشکیل آلوایمونیزاسیون را افزایش میدهد (57). بـا این حال، نتایج مطالعه ما ارتباط معناداری را بین فراوانی آلوایمونیزاسیون و اسپلنکتومی نشان نداد. در مطالعه ما 7 نفر از بیماران (5/15%) اسپلنکتومی شده بودند. رستمیان و همکاران در یک مطالعه سیستماتیک و متاآنـالیز که بر روی بیماران مبتلا به تالاسمی در جمعیت ایرانیان انجام دادند، نشان دادند که میزان اسپلنکتومی در بیماران تالاسمی 10% بود و هیچ ارتباط معناداری بین آلوایمونیزاسیون RBC و اسپلنکتومی یافت نشد (26). علاوه بر این مطالعه سیستماتیک دیگری که به بررسی ایمن بودن و اثربخشی اسپلنکتومی در بیماران بتا تالاسمی پرداخت، نتوانست هیچ مدرک محکمی پیدا کند (56). در مطالعه آذرکیوان و همکاران، ارتباط معناداری بین آلوایمونیزاسیون، اسپلنکتومی و سن اسپلنکتومی وجود نداشت (57). همچنین وزیری و همکاران، میرزائیان و همکاران، زری طحاننژاد اسدی و همکاران، داوری و همکاران نشان دادند که ارتباط معناداری بین آلوایمونیزاسیون و اسپلنکتومی وجود ندارد (48، 47، 37، 3).
با این وجود، به طور متناقضی در مطالعه کیخایی و همکاران و صادقیان و همکاران، میزان آلوایمونیزاسیون با سابقه اسپلنکتومی ارتباط معناداری داشت (29، 18). سینجر و همکاران مشابه تامسون و همکاران، اثر معنادار اسپلنکتومی بر میزان آلوایمونیزاسیون را گزارش کردهاند (58، 19). در تحقیقات آحمد و همکاران، بین اسپلنکتومی و آلوایمونیزاسیون رابطه معناداری وجود داشت، اما با تعداد واحدهای خونی که تزریق شده بود رابطه معناداری وجود نـداشت (23). ال داناسوری و همکاران ارتباط بین میزان آلوایمونیزاسیون و اسپلنکتومی و دفعات بالای انتقال خون را نشان دادند (31). علاوه بر این پازگال و همکـارانش، نشان دادند که بین طحالبرداری با احتمال ایجاد آلوآنتیبـادی ارتبـاط مثبت و معناداری وجود داشت (59). در توجیه وضعیت 2 گانه و متناقض وجود یـا عدم وجود طحال و بروز آلوایمونیزاسیون، به نظر میرسد نقش طحال در پدیده آلوایمونیزاسیون نقشی دوگانه و متناقض باشد. گروهی از محققین طحالبرداری را به دلیل این که مرکز جمعآوری و حذف آنتیژنهای بیگانـه خارج شده، و دیگر پاکسازی کمپلکسهای ایمنی انجام نمیپـذیرد، موجب افزایش شیوع آلوآنتیبادی در سرم بیماران میدانند. بر عکس گروهی دیگر نه تنها چنین ارتباطی را بین وضعیت طحال و شیوع آلوآنتیبـادیها ذکر نکردهاند، بلکه حتی با این استدلال که در طحالبرداری به دلیل این که دیگر گلبولهای قرمز تزریقی از جریان خون حذف نمیشوند را نـه تنهـا مضــر نمیدانند بلکه موجب کاهش نیاز به تزریق
خـون و در نتیجـه کاهـش میـزان فــراوانی آلـوآنتیبادیها
میدانند (3).
ارتباط بین تعداد واحدهای خون تزریق شده و آلوایمونیزاسیون در بیماران تالاسمی ناشناخته است، اما عامل مهمی برای افزایش آلوایمونیزاسیون در بیمارانی است که چندین تزریق خون دریافت میکنند (61، 60، 27). مطالعههای مختلف، نشان دادهانـد که آلوایمونیزاسیون گلبولهای قرمز در بیمارانی که دفعات تزریق خون و در نتیجه واحدهای خون بیشتری دریافت کردهاند، بیشتر است (63، 62). مطالعه ریـامی و بـه طور مشابه مطالعه ال دانا سوری و همکاران، ارتباط معناداری بین تشکیل آلوآنتیبادی و تعداد واحدهای خون دریافتی در بیماران مبتلا به تالاسمی گزارش کردند (31، 21). با این حال نتایج مطالعه ما، ارتباط معناداری را بین آلوایمونیزاسیون و تعداد واحدهای خون تزریق شده نشان نداد. مطابق و همسو با مطالعه ما، آذرکیوان و همکاران گزارش کردهانـد که میان آلوایمونیزاسیون و تعداد واحدهای خون تزریق شده ارتباط معناداری وجود نـدارد (11).
همچنین مطالعه شونویل و همکاران، سعید و همکاران، احمد و همکاران، داوان و همکاران و داوری و همکاران گزارش کردند که میان آلوآنتیبادیهای ایجاد شده و تعداد واحدهای خون تزریق شده ارتبـاط معناداری وجود ندارد (65، 64، 51، 47). در توضیح و توجیه رفتار متناقض و نـاهماهنگ در بحث فوق، برخی از محققین پدیده تحمل یا تولرانس (Tolerance) سیســتم ایمنــی ایــن بیمــاران نســبت بــه آنتیژنهای گلبولهای قرمـز وارد شـده بـه گـردش خـون را به عنوان مکانیسمی که سبب کاهش شیوع آلوآنتیبادیها میشود، یاد میکنند. بدین گونه که اگر آنتیژنهای بیگانه در همان اوایل دوران نوزادی و کودکی و زمانی که هنوز پـاسخهای ایمنی در کودک به شکل تکامل یافته در نیامده است وارد بدن شوند، سیستم ایمنی به جای پاسخ به آنتیژنهای فوق دچار تولرانس شده و حتی در برخوردهای بعدی نیز به شکل کاملاً جدی پاسخ ایمنی برانگیخته نخواهد شد و در نتیجه بـا وجود دفعات تزریق خون بالا، ممکن است بیمار آلوآنتیبادی ایجاد نکند (3).
برای پیشگیری یا کاهش آلوایمونیزاسیون و ایجاد آلوآنتیبادیها در بیماران تالاسمی وابسته به تزریق خون مکرر میتوان پیشنهاداتی ارائه داد که عبارتند از؛ غربالگری آنتیبـادی قبل از هر تزریق خون و فراهم نمودن لوازم آن از قبیل گلبولهای قرمز O معرف و پـانل سلهای مختلف و استاندارد، قرابت نژادی و قومیتی بین دهنده و گیرنـده خون، تطابق گسترده گروههای خونی بین اهداکننده و گیرنده گلبولهای قرمز به ویژه برای سیستم آنتیژنهای Rh و Kell، تزریق خون سازگار از لحاظ سیستمهای گروه خونی Kell و Rh (C، E، c، e) و سایر گروههای خونی مینور، اسـتفاده نمـودن از فیلترهای کاهنده گلبولهای سـفید در حـین تزریـق خـون و برگزاری کارگاههای درمان تالاسمی با هدف اقدامات ممکن برای کنترل و پیشگیری از ایجاد آلوایمونیزاسیون و افزایش نیاز بـه خون، میتواند تا حد زیادی به حل این مشکل کمک کند. از جمله محدودیتهای مطالعه حاضر میتوان به حجم نمونه نسبتاً پـایین و محدود بودن به یک مرکز درمانی اشاره کرد که ممکن است قابلیت تعمیم نتایج را کاهش دهد. با این حال، این مطالعه نخستین بررسی جامع در منطقه بیرجند است که با استفاده از روشهای استاندارد انجام شده و اطلاعات پایه ارزشمندی را فراهم میکند. پیشنهاد میشود در مطالعههای آینده با حجم نمونه بیشتر، در مراکز مختلف و بـا بررسی عوامل ژنتیکی و ایمونولوژیک، و عوامل مؤثر بر آلوایمونیزاسیون در بیماران تالاسمی به طور دقیقتر بررسی شود.
نتیجهگیری
نتایج این مطالعه نشان داد که اکثریت آلوآنتیبادیهای ایجاد شده بر علیه سیستمهای گروه خونی Kell و Rh هستند. از آن جایی که آلوایمونیزاسیون علیه آنتیژنهای گروههای خونی اصلی و فرعی مهم از نظر بالینی، میتوانند بر کیفیت زندگی، بقای کلی بیماران مبتلا به بتا تالاسمی ماژور، اثر بخشی و تعداد دفعات تزریق خون اثر بـگذارند، بنابراین راهبردهای پیشگیرانه مناسب مانند تعیین فنوتیپ RBC برای بیماران قبل از شروع انتقال خون و استفاده از تطابق گسترده اهداکننده و گیرنده RBC، بـه ویژه برای سیستم آنتیژنهای Rh و Kell، میتواند برای جلوگیری از عوارض در این بیماران اجرا شود و از اهمیت بالینی ویژهای برخوردار است. این مطالعه میتواند دید بهتری برای مطالعههای آینده فراهم کند کـه در نهایت ممکن است بـه
مدیریـت بهتـر مشکـل ایجـاد آلـوآنتیبادیهــا در بیماران
تالاسمی وابسته به تزریق خون منجر شود.
حمایت مالی
این مطالعه با حمایت مالی دانشگاه علوم پزشکی بیرجند انجام شد.
ملاحظات اخلاقی
این مطالعـه با کد اخلاق IR.BUMS.REC.1403.233 در کمیته اخلاق پژوهشی دانشگاه علوم پزشکی بیرجند تصویب شد. قبل از ورود بیماران به مطالعه، رضایتنامه کتبی از تمامی بیماران یـا اولیای قانونی آنها اخذ گردید و کلیه اطلاعات بیماران بـه صورت محرمانه و بدون ذکر نام ثبت و تحلیل شد. تمامی مراحل پژوهش مطابق با اصول اخلاقی بیانیه هلسینکی انجام شده است.
عدم تعارض منافع
نویسندگان این مقاله اعلام میدارند که هیچگونه تعارض منافعی در ارتباط با این مطالعه وجود ندارد.
نقش نویسندگان
مبینا نخعی شامحمود: طراحی مطالعه، جمعآوری داده، تحلیل آماری، انجام آزمایشها، ویرایش مقاله
مازیار نصیری: همکاری در جمعآوری دادهها، مشارکت در تحلیل نتایج
محمدرضا مقدادی: تحلیل آماری، نگارش پیشنویس اولیه مقاله
دکتر حسن مرتاضی: راهنمای بالینی، نظارت بر جمعآوری دادههای بیماران و صحت تشخیصها
معصومه اسدی فرد: همکاری در طراحی روش اجرا و انجام آزمایشهای تخصصی
فرزانه عرفانی: مشارکت در جمعآوری اطلاعات
دکتر امید حسنی اکبریه: مشارکت در جمعآوری اطلاعات
دکتر فـاطمه مزگینژاد: راهنمای اصلی پژوهش، طراحی و تائید نهایی طرح تحقیق، نظارت کلی بر مقاله
تشکر و قدردانی
این مطالعه در دانشگاه علوم پزشکی بیرجند و بـا همکاری سازمان انتقال خون شهرستان بیرجند انجام گرفته و تمام هزینههای آن از محل اعتبارات طرحهای تحقیقاتی مصوب دانشگاه ( با شماره طرح 6637) تأمین شده است که بدین وسیله مراتب تقدیر و تشکر خود را از مسئولین این دانشگاه ابراز میداریم. همچنین از پرسنل سازمان انتقال خون شهرستان بیرجند که کمال همکاری را با ما داشتند، صمیمانه تشکر و سپاسگزاری میکنیم.
متن کامل: (308 مشاهده)
آلوآنتی بادیهای Kell و E، علل اساسی آلوایمونیزاسیون در بیماران تالاسمی
وابسته به تزریق خون: مطالعه مقطعی
مبینا نخعی شامحمود1 ، مازیار نصیری1، محمدرضا مقدادی2 ، حسن مرتاضی3، معصومه اسدی فرد4، فرزانه عرفانی5،
امید حسنی اکبریه6، فاطمه مزگینژاد7
1- کارشناس ارشد خون شناسی آزمایشگاهی- کمیته تحقیقات دانشجویی ـ دانشکده پیراپزشکی دانشگاه علوم پزشکی بیرجند ـ بیرجند ـ ایران
2- کارشناس ارشد خون شناسی آزمایشگاهی- دانشکده پزشکی دانشگاه علوم پزشکی مشهد ـ مشهد ـ ایران
3- فوق تخصص خون و سرطان- بیمارستان ایرانمهر ـ بیرجند ـ ایران
4- کارشناس ارشد بیوشیمی عمومی- مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون و اداره کل انتقال خون بیرجند ـ بیرجند ـ ایران
5- کارشناس پرستاری- بیمارستان ایرانمهر ـ بیرجند، ایران
6- پزشک عمومی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون و اداره کل انتقال خون بیرجند ـ بیرجند ـ ایران
7- PhD خون شناسی آزمایشگاهی- استادیار مرکز تحقیقات سلولی و مولکولی ـ دانشکده پیراپزشکی دانشگاه علوم پزشکی بیرجند ـ بیرجند ـ ایران
وابسته به تزریق خون: مطالعه مقطعی
1- کارشناس ارشد خون شناسی آزمایشگاهی- کمیته تحقیقات دانشجویی ـ دانشکده پیراپزشکی دانشگاه علوم پزشکی بیرجند ـ بیرجند ـ ایران
2- کارشناس ارشد خون شناسی آزمایشگاهی- دانشکده پزشکی دانشگاه علوم پزشکی مشهد ـ مشهد ـ ایران
3- فوق تخصص خون و سرطان- بیمارستان ایرانمهر ـ بیرجند ـ ایران
4- کارشناس ارشد بیوشیمی عمومی- مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون و اداره کل انتقال خون بیرجند ـ بیرجند ـ ایران
5- کارشناس پرستاری- بیمارستان ایرانمهر ـ بیرجند، ایران
6- پزشک عمومی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون و اداره کل انتقال خون بیرجند ـ بیرجند ـ ایران
7- PhD خون شناسی آزمایشگاهی- استادیار مرکز تحقیقات سلولی و مولکولی ـ دانشکده پیراپزشکی دانشگاه علوم پزشکی بیرجند ـ بیرجند ـ ایران
https://doi.org/10.18502/avr.v34i2.18052 Citation: Nakhaei M, Nasiri M, Meghdadi M.R, Mortazi H, Asadifard M, Erfani F, Hasani Akbariey O, Mezginejad F. Determining the Prevalence and Types of Alloantibodies in Transfusion-Dependent Thalassemia Patients in Birjand City, 2024. J Iran Blood Transfus. 2025: 22 (2) : 137-149 نویسنده مسئول: فاطمه مزگینژاد. مرکز تحقیقات سلولی و مولکولی ـ دانشکده پیراپزشکی دانشگاه علوم پزشکی بیرجند ـ بیرجند ـ ایران کد پستی: 9717394315 E-mail: mezginejadf@gmail.com
کد اخلاق: IR.BUMS.REC.1403.233 |
چکیده سابقه و هدف بیماران مبتلا به تالاسمی ماژور نیازمند به تزریق خون منظم میباشند و یکی از مهمترین عوارض انتقال مکرر خون در آنها، تولید آلوآنتیبادی است. این مطالعه با هدف بررسی فراوانی و نوع آلوآنتیبادیهای شایع در بیماران مبتلا به تالاسمی انجام شد. مواد و روشها مطالعه توصیفی - مقطعی حاضر بر روی 45 بیمار مبتلا به تالاسمی ماژور وابسته به تزریق خون شهرستان بیرجند در سال 1403 انجام شد. آزمایش غربالگری آنتیبادی انجام و سپس هویت آنتیبادیها تعیین شد. همچنین موارد مربوط به سن، جنس و اطلاعات بالینی و آزمایشگاهی بیماران تالاسمی از پرونده الکترونیک آنها استخراج گردید. دادههای به دست آمده با استفاده از نرمافزار SPSS نسخه 26 مورد تجزیه و تحلیل قرار گرفت و از آزمونهای آماری کایدو و دقیق فیشر برای ارتباط بین متغیرها با یکدیگر استفاده شد. یافتهها در این مطالعه تعداد 45 بیمار شامل 21 مرد (6/46%) و 24 زن (3/53%)، با دامنه سنی 36-1 سال مورد مطالعه قرار گرفتند. شیوع آلوآنتیبادی در بیماران تالاسمی وابسته به تزریق خون در 3 نفر با فاصله اطمینان 95% در محدوده ۲/۲ تا 1/18 درصد بود. 4 آلوآنتیبادی شناسایی شد که شایعترین آلوآنتیبادیها شامل anti-K (3 نفر، 100%) و anti-E (1 نفر، 33%) بود. فراوانترین فنوتیپ سیستم ABO، گروه خونی O (2/%42) و فراوانترین آنتیژن سیستم Rh، آنتیژن c وe بود که بـه ترتیب در100% و 3/93 % بیماران وجود داشت. 7 بیمار (5/15%) تحت عمل طحالبرداری قرار گرفته بودند. ارتباط معناداری بین آلوایمونیزاسیون با گروه سنی، جنس، گروه خونی، تعداد واحدهای خون تزریق شده و وضعیت طحال مشاهده نشد. نتیجه گیری با توجه به شناسایی آلوآنتیبادیها علیه سیستمهای گروه خونی Kell و Rh (E) ، در جامعه تالاسمی مورد مطالعه بایستی از خـونی استفاده شود که حداقل از نظر آنتیژنهای سیستمهای گروههای خونی Kell و Rh با خون بیمار تطابق داشته باشد. کلمات کلیدی: تالاسمی، آلوایمونیزاسیون، آلوآنتیبادی، انتقال خون |
|
1- Acridine Orange
|
|
1- Biological safety cabinet
|
|
1- Platelet Concentrate
2- Food and Drug Administration 3- Normal Skin Flora 4- Platelet Rich Plasma-Platelet Concentrate 5- Eosin-Methylene blue 6- Thioglycolate |
|
1- Acridine Orange
|
|
1- Biological safety cabinet
|
|
1- Platelet Concentrate
2- Food and Drug Administration 3- Normal Skin Flora 4- Platelet Rich Plasma-Platelet Concentrate 5- Eosin-Methylene blue 6- Thioglycolate |
مقدمه
تالاسمی به عنوان یکی از شایعترین اختلالات ژنتیکی مرتبط با کمخونی ارثی در سطح جهانی شناخته میشود که به علـت نقص در تولید زنجیرههای گلوبین ایجاد شده و منجر بـه کاهش تولید هموگلوبین در گلبولهای قرمز خون (RBCs) میگردد (2، 1)، تـالاسمی بر اساس نوع زنجیره گلوبین درگیر بـه دو گروه اصلی انواع آلفا (α) تالاسمی و بتا (β) تالاسمی طبقهبندی میشود. بتاتالاسمی بر اساس میزان سنتز زنجیرههای β به انواع ماژور، اینترمدیا و مینور طبقهبندی میشود که بتاتالاسمی ماژور به عنوان شدیدترین فرم بیماری شناخته میشود (3). این بیماری به ویژه در مناطقی از حوزه مدیترانه تا خاورمیانه، هند و آسیای جنوب شرقی فراوانی بالایی دارد (4). تالاسمی تقریباً 2/4 نفر از هر 10000 نفر در سراسر جهان را تحت تـأثیر قرار میدهد (5). در ایران نیز بیش از 2 میلیون ناقل تالاسمی (حدود 4% جمعیت) و بیش از بیست هزار بیمار تالاسمی ماژور وجود دارد (7، 6).
بیماران تـالاسمی ماژور قدرت تولید گلبولهای قرمز سالم و فعال را از دست میدهند و در ضمن گلبولهای به ظاهر سالم آنها نیز به سرعت تخریب میشوند در نتیجه، این افراد به درمانهای حمایتی مادامالعمر مانند تزریق منظم خون وابسته هستند (8). اساس درمان بیماران تالاسمی، پیوند سلولهای بنیادی خونساز است، اما تزریق خون مکرر و منظم، درمان انتخابی و در غیاب پیونـد بـه عنوان درمان حمایتی و مهم میباشد (به طور متوسـط هـر ماه یک واحد) (9، 8). در بیماران مبتلا به تالاسمی ماژور، اگر چه تزریـق خون، نقص در تولیـد گلبـولهـای قرمز خـون را اصلاح نمیکند، ولی با افزایش سطح هموگلوبین، عوارض غیـر طبیعـی در تالاسـمی و علائم کـم خونی مزمن را بهبود میبخشد و بقای بیماران را افـزایش میدهـد (10). البته تزریق منظم و مکرر خون با یکسری از مشکلات بالینی با اهمیـت مانند واکنشهای آلرژیک، واکنشهای تـبزای غیرهمولیتیـک تزریق خـون، اضافه بار گردش خون، آسیب ریه مربوط به انتقال خون (TRALI)، عفونتهای باکتریایی و ویروسی، افزایش بار آهن و آلوایمونیزاسیون که از عوارض تزریق خون هستند، همراه است. این موارد سودمندی تزریق خون را در طول زمان کاهش میدهند و ممکن است تهدیدکننده زندگی باشند (11، 10).
تزریق خون موجب ورود آنتیژنهای مختلف گلبولهای
قرمز به بدن بیماران شده و باعث تحریک سیستم ایمنی بیماران فاقد این آنتیژنها و تولید آنتـیبادیها علیه آنها میشود؛ این آنتیبادیها را آلوآنتیبادی مینامند و بیمــاران تولیــد کننــده آلـوآنتــیبــادی را آلوایمــونیزه مـینامنــد. افزایش شیوع آلوایمونیزاسیون علیه گلبولهای قرمز میتوانـد تزریق خون سازگار آزمایشگاهی را دچار مشکلات فراوان نماید که میتوان به واکنشهای همولیتیک ناشی از تزریق خون یا HTR و همچنین کوتاه شدن عمر مفید گلبولهای قرمز تزریق شده اشاره نمود (12). از آنجایی که در انتخاب خون تزریقی فقط سیستمهای گروه خونی ABO و Rh کنترل میشوند و سایر گروهها معمولاً در نظر گرفته نمیشوند، اکثر آلوآنتیبادیها علیه آنها شکل گرفته و عامل ناسازگاری در کراسمچ و یا ناسازگاری بالینی میبـاشد. مطالعههای مختلف نشان دادهاند که در دو سوم ایـن موارد، آنتیبـادی مسئول مربوط به زیرگروههای سیستمRh (E، C، c، e) و گروههای فرعی نظیر Kell، Duffy و Kidd میباشند (15-13).
احتمـال ایجـاد آلوآنتیبادی به دنبـال تزریـق یـک کیسـه خـون 1% تا 6/1% است، در حالی که احتمال ایجاد آنتیبادی در بیمـاران بـا تزریقهای منظم و مکرر مانند بیماران تالاسمی، کـم خـونی داسـی شـکل و بـدخیمیهای هماتولوژیک (لوسمی، سندروم میلودیس پلاستیک) به حدود 60% میرسد (16). همچنین افـرادی که یک آلوآنتیبادی در آنها ایجـاد مـیشـود، دارای خطـر بالاتری برای تولید آلوآنتیبادیها و اتوآنتیبادیهای بیشـتر به دنبال تزریق خونهای بعدی هستند که این امر میتوانـد فرآیند شناسایی خون سازگار را در این بیمـاران بـا مشـکل مواجه ساخته و سبب تأخیر در فرآیند تأمین و تزریق خون سازگار گردد (17).
مطالعههای قبلی میزان فراوانی آلوایمونیزاسـیون را در بیمـاران مبتلا به تالاسمی بین 87/2 % تا 55% گـزارش کـردهانـد (18، 3). علیرغم اهمیت درک فراوانی این آلوآنتیبادیها در بیماران تالاسمی بـرای بهبود شیوههای انتقال خون و بهبود بیماران، مطالعه جـامعی با تمرکز بر این موضوع در شهرستان بیرجند وجود ندارد. این شکاف در دانش، مانع از توسعه استراتژیهای مؤثر برای به حداقل رساندن آلوایمونیزاسیون در بیماران تـالاسمی، به ویژه در مناطقی با فراوانی بالای تالاسمی میشود .بنابراین مطالعه حاضر با هدف بررسی فراوانی آلوآنتی بادیهای شایع در بیماران تالاسمی وابسته به تزریق خون شهرستان بیرجند در سال 1403و ارتبـاط آلوایمونیزاسـیون بـا عـواملی همچون سن، جنس، گروه خونی، برداشتن طحال و تعداد واحدهای تزریق شده خون بود.
مواد و روشها
این مطالعه به صورت توصیفی-مقطعی بـا کـد اخلاق IR.BUMS.REC.1403.233 در سال 1403 در دانشگاه علوم پزشکی بیرجند و با همکاری سازمان انتقال خون بیرجند بر روی بیماران تالاسمی ماژور وابسته به تزریق خون انجام شد. در این مطالعه از تمامی بیماران تالاسمی ماژور که جهت دریافت خون در سال 1403 به بیمارستان ایرانمهر بیرجند مراجعه کردند، نمونهگیری به صورت سرشماری انـجام شد و در نهایت بیمارانی که دارای معیارهای لازم برای ورود به مطالعه بودند، وارد مطالعه شدند. از معیارهای ورود بـه مطالعه میتوان به تایید بیماری تالاسمی ماژور توسط تستهای آزمایشگاهی و پزشک متخصص، کامل بودن پرونده پزشکی بیماران و تزریق مکرر خون (هر هفته حداقل یـک مرتبه) اشاره کرد. همچنین از معیار خروج مطالعه میتوان به ابتلا به بیماری تالاسمی اینترمدیا، کامل نبودن پرونده پزشکی بیماران و ابتلا به بیماریهای عفونی مانند انواع هپاتیت و ایـدز اشاره نمود. در ابتدا، اطلاعات دموگرافیک شامل سن، جنس، اطلاعات بـالینی و آزمایشگاهی شامل CBC (میزان گلبولهای قرمز، گلبولهای سفید، هموگلوبین و پلاکت)، تعداد دفعات تزریق خون در سال و وضعیت طحالبرداری بیماران تـالاسمی وابسته به تزریق خون مکرر بیرجند از پرونده الکترونیک بیماران استخراج گردید.
پس از دریـافت رضایتنامه کتبی از هر بیمار، قبل از تزریق خون، 2 میلیلیتر خون در لوله حاوی ضد انعقاد K2-EDTA برای تعیین فنوتیپ گروههای خونی ABO و 5 میلیلیتر خون بدون ضد انعقاد (لوله لخته) برای آزمایشهای غربـالگری آنتیبادی و تعیین هویت آنتیبادی گرفته شد. فنوتیپ گروههای خونی ABO بیماران با استفاده از روش لولـهای تعیین شد و آنتیژنهای گروه خونی Rh (D، C، E، c، e) و Kell با استفاده از آنتیسرمهای شرکت ایمیون دیاگنوستیکای آلمان مطابق دستورالعمل موجود در کیت تعیین گردید.
آزمایش غربالگری آنتیبادیهای غیـر منتظــره بـر روی
سرم همه بیماران با استفاده از روش پنل سلولی 3 تایی (سلولهای غربالگر R1R1/I، R2R2/II، rr/III) شرکت کیان ژن یـاخته (تهران، ایران) طبق روشهای استاندارد بانک خون که در پایین به آن اشاره شده است، انجام شد. سلولهای غربالگر، 3 ویال حاوی مجموعهای از سلولهای دارای آنتیژنهای مهم بالینی از قبیل P1، Lea، Leb، M، N، Fya، Fyb، S، s، Jka، Jkb، C، c، E، e، D میبـاشند. دو حجم از سرم بیمار با یک حجم سوسپانسیون 2 تا 5 درصد گلبولهای اسکرین مجاور شدند. یک نمونه در دمای اتـاق (RT) و دو نمونـــه در دمای 37 درجه سانتیگراد قـــرار گرفـــت. پـــس از 20 تا 30 دقیقـــه انکوباسیون، لولهها به مـدت 30 ثانیـه بـا دور 3000 در دقیقه سـانتریفوژ شدند و سپس به صـورت میکروسـکوپی و ماکروسکوپی از نظر وجود آگلوتیناسیون مورد بررسی قرار گرفتند. در صورت عدم مشاهده آگلوتیناسـیون، بـه منظـور یافتن آنتیبادیهای ناقص و یا احتمالاً دارای تیتر پـایین، ازAHG استفاده شد. مشاهده آگلوتیناسیون در هـر کـدام از مراحـل ذکر شده به منزلـه مثبت بودن غربالگری آنتـیبـادی تلقـی میگردید.
در صورت منفی بودن واکنش، بـه منظور اطمینان از فعال بودن AHG و صحت نتایج به دست آمـده، نتیجـه حاصله بـا سـلولهـای کنتـرل یـا چک سل (Check Cell) (گلبولهای قرمز حساس شده باIgG ) مورد کنتـرل کیفـی قرار گرفتند و در صورت واکنش مثبت با چک سل، نتیجه آزمایش تـایید شد. سپس تعیین هویت آنتیبادی (Ab Identification) بـر روی نمونههای مثبت از لحاظ غربالگری آنتیبادی با استفاده از روش پنل سلولی 11 تایی (پنلهای سلولی استاندارد تهیه شده در سازمان انتقال خون ایران) مشابه همان مراحل غربالگری آنتیبادی انجام پذیرفت که نتایج حاصله با توجه به جدول آنتـیگرام (Antigram) موجود در کیت تفسیر شد. نتایج به دست آمده در این مطالعه، با استفاده از نرمافزار آماری SPSS نسخه 26 مورد تجزیـه و تحلیل قرار گرفت. دادههای توصیفی با استفاده از فراوانی و درصد و دادههای کمی با استفاده از میانگین ± انحراف معیار گزارش شدند. از آزمونهای آماری کایدو (chi-square) و آزمایش دقیق فیشر (Fisher Exact Test) در تجزیه و تحلیل نتایج استفاده شد و سطح 05/0 p< به عنوان سطح معنـاداری در نظر گرفته شد.
یافتهها
در این مطالعه، تعداد 45 بیمار مبتلا به تالاسمی وابسته به تزریق خون با میانگین سنی 73/10 ±18 سال و دامنه سنی 1 تا 36 سال مورد بررسی قرار گرفتند. اطلاعات مورد نیاز برای تمامی بیماران واجد شرایط به طور کامل از پروندههای الکترونیک استخراج شد و هیچ موردی از داده گمشده (missing data) وجود نـداشت. بنابراین، تمامی ۴۵ بیمار وارد مطالعه شدند و تحلیل دادهها بر اساس اطلاعات کامل انـجام گرفت. از بیـن ایـن بیماران، 21 نفر مرد (6/46 %) با میانگین سنی 29/10 ± 95/19 سال و 24 نفر زن (3/53 %) با میانگین سنی 02/11 ± 29/16 سال بودند (جدول 1).
فنوتیپ آنتیژنی سیستمهای گروه خونی ABO، Rh و Kell تعیین گردیـد (جدول 2). فراوانترین فنوتیپ سیستم ABO، گروه خونی O (2/42 %) و فراوانترین آنتـیژن سیستم Rh، آنتیژن c و e بود کـه به ترتیب در100% و 3/93 % بیماران وجود داشت. فراوانی آنتیژن Kell در جمعیت بیماران استان خراسان جنوبی پـایین بود به طوری که فقط 1 بیمار (2/2%) دارای آنتیژن K بود.
از مجموع 45 بیمار مورد مطالعه، 3 بیمار (بـا فاصله اطمینان 95%: ۲/۲ تـا ۱/18 درصـد) غربالگـری آنتیبـادی
مثبت داشتند و تعداد 4 آلوآنتیبادی شناسایی گردید. با بـررسی نتایج تعیین هویـت آنتیبادی، شایعترین آلوآنتیبادیها شامل anti-K (3 نفر، 100%) و anti-E (1 نفر، 33 %) بود. از 3 بیمــاری کــه تولیـد آلـوآنتیبـادی کردنـد، 2 نفر مرد (6/66%) و 1 نفر زن (3/33%) با میانگین سنی 3/2±33/25 سال بودند (جدول 3). تفاوت معناداری بین آلوایمونیزاسیون و سن و جنس مشاهده نشد (جدول 4). همچنین نتایج آزمون آماری کایدو نشان داد که میان آلوایمونیزاسیون با گروه خونی ABO و Rh(D) ارتباط معناداری وجود ندارد. بیشترین و کمتریـن میزان آلوایمونیزاسیون بـه ترتیب در بیماران تالاسمی با گروه خونی B (2 مورد) و O (1 مورد) بود (جدول 3).
از بین 45 بیمار تالاسمی مورد مطالعه، 7 نفر از بیماران (5/15 %) طحالبـرداری شده بودنـد که شامل 3 مرد (9/42 %) و 4 زن (1/51%) بودند و 38 نفر از بیماران (4/84 %) نیز دارای طحال بودند. بر طبق نتیجه آزمون آماری کـایدو، میان آلوایمونیزاسیون و وضعیت طحال ارتباط معناداری یـافت نشد (جدول 5). همچنین نتایج آزمون آماری نشان داد که ارتباط معناداری میان آلوایمونیزاسیون و تعداد واحدهای تزریق خون در بیماران تالاسمی وابسته به تزریق خون وجود ندارد.



بحث
میزان فراوانی آلوآنتیبادی در بیماران تالاسمی وابسته بـه خون به طور متغیر و با دامنه وسیع از 53/1% تا 55% گزارش شده است (20، 3). مشابه و همسو با مطالعه ما، در یک مطالعه گذشتهنگر در کشور عمان، ریامی و سایر همکارانش نشان دادند که میزان فراوانی آلوایمونیزاسیون در بیماران مبتلا به تالاسمی وابسته به تزریق خون مکرر 3/9 % و فراوانترین آلوآنتیبادیهـای ایجاد شده شامل anti-K و anti-E بود (21). علاوه بر این میزان آلوایمونیزاسیون در 64 بیمار چینی مبتلا به تالاسمی ماژور در تـایوان 4/9 % گزارش شد که همه آنتیبادیها علیه آنتیژنهای Rh بودند (22). شیوع آلوآنتیبادی در یـک مطالعه مصری بر روی 501 بیمار مبتلا بـه بتا تالاسمی 3/11 % بود که Anti-K، Anti-E و Anti-C شیوع بیشتری داشتند (23). همچنین عبیدی و همکاران گزارش کردند که شیوع آلوآنتیبـادی در 90 بیمار مبتلا به تالاسمی بوشهری، 9% بود که آلوآنتیبادی علیه سیستم گروه خونی Kell بیشترین فراوانی را داشت (24). احمدی و همکاران نیز بـا مطالعهای که بر روی 142 بیمار مبتلا به تالاسمی وابسته به تزریق خون مکرر انجام دادند، میزان فراوانی آلوآنتیبادیها را 2/9% گزارش کردند (25). تمامی این مطالعهها مشابهت زیادی از لحاظ فراوانی آلوآنتیبـادیها با نتایج مطالعه ما دارند. یک مطالعه سیستماتیک و متاآنالیز با تجزیه و تحلیل 23 مقالـه (شامل 5734 بیمار)، میزان فراوانی آلوآنتیبادیها در بیماران تالاسمی وابسته به تزریق خون در جمعیت ایرانیان را 13% گزارش کرده است که فراوانترین آلوآنتیبادیهای تشکیل شده بر علیه سیستمهای گروه خونی Rh (D، E، C) و Kell بوده است (26). میزان آلوایمونیزاسیون در نقاط مختلف ایران به شرح زیر گزارش شده است: 4/7% (تهران)، 34/5% (استان فارس)، 7/18% (جنوب غربی ایران، اهواز) و 78/2 % (شمال شرق ایران، مشهد) (29-27، 18). به علاوه، فراوانی آلوایمونیزاسیون در کشورهای دیگر شامل 30% (کویت)، 5/19 % (مصر)، 4/7% (هنگکنگ)، 5% (ایتالیا)، 5/9% (هند) و 2/9% (پاکستان) است (35-30). این تفاوت بین میزان آلوایمونیزاسیون بین مطالعههای مختلف، به دلیل تفاوت در موقعیت جغرافیایی مناطق، تفاوت نژادی و هتروزیگوسیتی ژنتیکی بین گروههای مورد مطالعه و میزان همسانی فنوتیپ گروههای خونی اهداکنندگان خون بـا بیماران تالاسمی دریافتکننده این خونها میباشد.
نتایج مطالعه ما نشان داد که فراوانترین آلوآنتیبادیهای ایجاد شده بر علیه گروههای خونی Kell و Rh بودند. مطالعههای مختلف نشان دادهاند که اکثر آلوآنتیبادیهای تشکیل شده در بیماران مبتلا به تالاسمی وابسته به تزریق خون بر علیه سیستمهای گروه خونی Kell و Rh (D، C، E، c، e) بودهانـد. کیخایی و سایر همکاران نشان دادند که الگوی غالب آلوایمونیزاسیون آلوآنتیبادی علیه سیستم زیرگروههای Rh در 55 درصد بیماران و 33 درصد بیماران آلوآنتیبادی علیه سیستم Kell بود (29). در مطالعهای که توسط قاسمی و همکاران انجام شد، نشان دادند که الگوی غالب آلوایمونیزاسیون آلوآنتیبادی علیه سیستم Rh (D، C، E و C) در 3/58% از بیماران و 6/16% از بیماران آلوآنتیبادی علیه سیستم Kell بود (36). آمین و همکاران میزان فراوانی anti-K در 72% و anti-E را در 6/45% از بیماران مبتلا به تـالاسمی دارای آلوآنتیبادی مثبت گزارش کردهاند (30). اغلب آلوآنتیبادیهای تشکیل شده در یک مطالعه که بر روی بیماران مبتلا به تالاسمی شیراز انجام شده است، بر علیه زیر گروه خونی Kell (%50) و Rh (3/%26) بوده است (28). نتایج یـک مطالعه در جنوب شرق ایران (زاهدان) نشان داد که فراوانترین آلوآنتیبـادیهای تشکیل شده بر علیه زیر گروه خونی Rh (%28) و Kell (%8) بوده است (37). محمدی مرام و همکاران در مطالعهای که بر روی بیماران تالاسمی شهر تهران انجام دادند، گزارش کردند که بیشترین میزان آلوآنتیبادی شامل anti-K و anti-E بوده است (38). در مطالعهای سیستماتیک و متاآنالیز که توسط درویشی و همکاران در جمعیت بیماران تـالاسمی ایران انجام شد، میــزان آلوایمونیزاســیون در ایــران 10% گزارش شد و بیشترین آلوآنتیبـادیها مربوط به anti-K (%37)، anti-D (%29) و anti-E (%20) بودند (39). در مطالعه آذرکیوان و همکارانش، شایعترین آلوآنتیبـادیها علیه سیستم Rh (E/e/C/c/Cw) (%26)، anti-K (%28) و anti-D (%16) بود (11). در یک مطالعه که در کشور مصر بر روی بیماران تالاسمی با تزریق خون مکرر انجام شده است، شـایعتـرین آلوآنتیبادیها مرتبط بـا سیستم Rh (به ترتیب anti-E، anti-D، anti-C و anti-c) و گروه خونی Kell بوده است (40). همچنین در مطالعه دیگری در کشور مصر که بر روی 200 بیمار تالاسمی با تزریق خون مکرر انجـام شد، آنتیبـادی علیه گروه خونی Kell (%33) و آنتیبادی علیه گروه خونی Rh (4/%24) شایعترین آلوآنتیبادیهای تشکیل شده بودند (41). یک مطالعه که در کشور عراق انجام شده است، شــایعتــرین ایــن آلوآنتیبادیها به anti-E، anti-D و anti-K نسبت داده شده است (42)(جدول 6).
در مطالعه حاضر ارتباط معناداری بین آلوایمونیزاسیون بـا سن، جنسیت و گروه خونی مشاهده نشد. نتایج مطالعههای قبلی نشاندهنده افزایش فراوانی آلوآنتیبادیها با افزایش سن به دلیل تزریق خون بیشتر بود (45-43). با این حال، مشابـه مطالعه ما، چندین مطالعه، مانند مطالعه افشاری و همکاران، زری طحاننژاد اسدی و همکاران، داوری و همکاران، میرزائیان و همکاران، وزیری و همکاران، ارتباط معناداری بین سن و آلوایمونیزاسیون پیدا نکردند (46-48، 37 ، 3). همچنین مطالعههای صادقیان و همکاران، حسن و همکـاران این نکته را تایید کردند کـه میان آلوایمونیزاسیون و سن ارتباط معناداری وجود ندارد (49، 18).
جنسیت، به عنوان یک عامل خطر، موضوع بحث برانگیز است. به دلیل قرار گرفتن بیشتر در معرض وقایع ایمنسازی، مانند بارداری و تزریق خون، انتظار میرود که زنان میزان بالاتری از آلوایمونیزاسیون RBC را تحمل کنند. اگرچه مطالعهها به طور کلی رابطه معناداری بین جنسیت و فراوانی آنتیبادیها را گزارش کردهاند، به طوری که برخی فراوانی بالاتر آلوآنتیبادی را در بیماران زن و برخی دیگر بیماران مرد گزارش کردهاند (51، 50). چندین مطالعه دیگر همسو و مشابـه با نتایج مطالعه ما نیز هیچ رابطه معناداری بین جنسیت و فراوانی آلوآنتیبادیها پیدا نکردند (52، 48، 45، 44، 11). همچنین نتایج یک مطالعه سیستماتیک و متاآنالیز بر روی بیماران تالاسمی وابسته به تزریق خون جمعیت ایرانیان (5734 بیمار) انجام شد، هیچ تفاوت قابل توجهی در میزان فراوانی آلوایمونیزاسیونRBC بین مردان و زنان تالاسمی (10% و 11% به ترتیب) شناسایی نکرد (26). این نتیجه مشابه نتیجه مطالعه ما بود. این نتایج حاکی از اهمیت در نظر گرفتن عوامل دیگری مانند سابقه بارداری در زنان، سن شروع تزریق خون، تعداد واحدهای خونی تزریق شده و وضعیت اسپلنکتومی است.
بر اساس نتایج مطالعه حاضر، گروه خونی ABO و Rh (D) ارتباط معناداری با فراوانی آلوآنتیبادیها نداشتند که بـا نتایج مطالعه جمعیت ایرانی اقبالی و همکاران همخوانی داشت (53). رئوف عبدالقادر و همکاران مطالعه ای را در یک جمعیت عراقی انجام دادند و به نتایج مشابهی دست یافتند (54). وزیری و همکاران گزارش دادهاند که میان آلوایمونیزاسیون و گروه خونی ABO ارتباط معناداری وجود ندارد (48). علاوه بر این میرزائیان و سایر همکاران نشان دادنـد بین فراوانی آلوایمونیزاسیون و گروه خونی ABO و Rh تفاوت معناداری وجود ندارد (37). این یافتهها در مطالعههای متعددی گزارش شده است و به نظر میرسد گروه خونی نقش مهمی در فراوانی آلوآنتیبادیها نـداشته باشد.
نتایج مطالعه ما نشان داد که 7 نفر (5/15%) از بیماران اسپلنکتومی یا طحالبرداری شده بودند. همچنین در این مطالعه ارتباط معناداری بین آلوایمونیزاسیون با وضعیت طحال و تعداد واحدهای خون تزریق شده در بیماران تالاسمی مشاهده نشد.
بیماران مبتلا بـه تالاسمی اینترمدیا و ماژور، به تزریق خون مکرر برای جبران کمبود گلبولهای قرمز با عملکرد طبیعی نیاز دارنـد (55). با توجه به این که گلبولهای قرمز معیوب یـا آسیب دیده در طحال از بین میروند، بیماران تالاسمی دچار بزرگ شدن عملکردی طحال (هیپراسپلنیسم) میشوند. بنابراین، برداشتن طحال ممکن است بقای گلبولهای قرمز را طولانی کند، که به نوبه خود میتواند نیاز به تزریق خون را کاهش دهد (56). فیلتراسیون یکی از مهمترین نقشهای طحال است که در بیماران طحالبرداری شده حذف میشود. اسپلنکتومی میتواند منجر بـه افزایش خطر آلوایمونیزاسیون شود، به ویژه در بیمارانی که به دلیل اختلالات هماتولوژیک مانند تالاسمی یا کمخونی داسی شکل تحت این عمل قرار میگیرند. این افزایش عمدتاً به دلیل کاهش فیلتراسیون آنتیژنهای گلبولهای قرمز آسیب دیده و بقای طولانیتر آنها در گردش خون است که در نتیجه مواجهه سیستم ایمنی با آنتیژنهای غیرخودی و تشکیل آلوایمونیزاسیون را افزایش میدهد (57). بـا این حال، نتایج مطالعه ما ارتباط معناداری را بین فراوانی آلوایمونیزاسیون و اسپلنکتومی نشان نداد. در مطالعه ما 7 نفر از بیماران (5/15%) اسپلنکتومی شده بودند. رستمیان و همکاران در یک مطالعه سیستماتیک و متاآنـالیز که بر روی بیماران مبتلا به تالاسمی در جمعیت ایرانیان انجام دادند، نشان دادند که میزان اسپلنکتومی در بیماران تالاسمی 10% بود و هیچ ارتباط معناداری بین آلوایمونیزاسیون RBC و اسپلنکتومی یافت نشد (26). علاوه بر این مطالعه سیستماتیک دیگری که به بررسی ایمن بودن و اثربخشی اسپلنکتومی در بیماران بتا تالاسمی پرداخت، نتوانست هیچ مدرک محکمی پیدا کند (56). در مطالعه آذرکیوان و همکاران، ارتباط معناداری بین آلوایمونیزاسیون، اسپلنکتومی و سن اسپلنکتومی وجود نداشت (57). همچنین وزیری و همکاران، میرزائیان و همکاران، زری طحاننژاد اسدی و همکاران، داوری و همکاران نشان دادند که ارتباط معناداری بین آلوایمونیزاسیون و اسپلنکتومی وجود ندارد (48، 47، 37، 3).
با این وجود، به طور متناقضی در مطالعه کیخایی و همکاران و صادقیان و همکاران، میزان آلوایمونیزاسیون با سابقه اسپلنکتومی ارتباط معناداری داشت (29، 18). سینجر و همکاران مشابه تامسون و همکاران، اثر معنادار اسپلنکتومی بر میزان آلوایمونیزاسیون را گزارش کردهاند (58، 19). در تحقیقات آحمد و همکاران، بین اسپلنکتومی و آلوایمونیزاسیون رابطه معناداری وجود داشت، اما با تعداد واحدهای خونی که تزریق شده بود رابطه معناداری وجود نـداشت (23). ال داناسوری و همکاران ارتباط بین میزان آلوایمونیزاسیون و اسپلنکتومی و دفعات بالای انتقال خون را نشان دادند (31). علاوه بر این پازگال و همکـارانش، نشان دادند که بین طحالبرداری با احتمال ایجاد آلوآنتیبـادی ارتبـاط مثبت و معناداری وجود داشت (59). در توجیه وضعیت 2 گانه و متناقض وجود یـا عدم وجود طحال و بروز آلوایمونیزاسیون، به نظر میرسد نقش طحال در پدیده آلوایمونیزاسیون نقشی دوگانه و متناقض باشد. گروهی از محققین طحالبرداری را به دلیل این که مرکز جمعآوری و حذف آنتیژنهای بیگانـه خارج شده، و دیگر پاکسازی کمپلکسهای ایمنی انجام نمیپـذیرد، موجب افزایش شیوع آلوآنتیبادی در سرم بیماران میدانند. بر عکس گروهی دیگر نه تنها چنین ارتباطی را بین وضعیت طحال و شیوع آلوآنتیبـادیها ذکر نکردهاند، بلکه حتی با این استدلال که در طحالبرداری به دلیل این که دیگر گلبولهای قرمز تزریقی از جریان خون حذف نمیشوند را نـه تنهـا مضــر نمیدانند بلکه موجب کاهش نیاز به تزریق
خـون و در نتیجـه کاهـش میـزان فــراوانی آلـوآنتیبادیها
میدانند (3).
ارتباط بین تعداد واحدهای خون تزریق شده و آلوایمونیزاسیون در بیماران تالاسمی ناشناخته است، اما عامل مهمی برای افزایش آلوایمونیزاسیون در بیمارانی است که چندین تزریق خون دریافت میکنند (61، 60، 27). مطالعههای مختلف، نشان دادهانـد که آلوایمونیزاسیون گلبولهای قرمز در بیمارانی که دفعات تزریق خون و در نتیجه واحدهای خون بیشتری دریافت کردهاند، بیشتر است (63، 62). مطالعه ریـامی و بـه طور مشابه مطالعه ال دانا سوری و همکاران، ارتباط معناداری بین تشکیل آلوآنتیبادی و تعداد واحدهای خون دریافتی در بیماران مبتلا به تالاسمی گزارش کردند (31، 21). با این حال نتایج مطالعه ما، ارتباط معناداری را بین آلوایمونیزاسیون و تعداد واحدهای خون تزریق شده نشان نداد. مطابق و همسو با مطالعه ما، آذرکیوان و همکاران گزارش کردهانـد که میان آلوایمونیزاسیون و تعداد واحدهای خون تزریق شده ارتباط معناداری وجود نـدارد (11).
همچنین مطالعه شونویل و همکاران، سعید و همکاران، احمد و همکاران، داوان و همکاران و داوری و همکاران گزارش کردند که میان آلوآنتیبادیهای ایجاد شده و تعداد واحدهای خون تزریق شده ارتبـاط معناداری وجود ندارد (65، 64، 51، 47). در توضیح و توجیه رفتار متناقض و نـاهماهنگ در بحث فوق، برخی از محققین پدیده تحمل یا تولرانس (Tolerance) سیســتم ایمنــی ایــن بیمــاران نســبت بــه آنتیژنهای گلبولهای قرمـز وارد شـده بـه گـردش خـون را به عنوان مکانیسمی که سبب کاهش شیوع آلوآنتیبادیها میشود، یاد میکنند. بدین گونه که اگر آنتیژنهای بیگانه در همان اوایل دوران نوزادی و کودکی و زمانی که هنوز پـاسخهای ایمنی در کودک به شکل تکامل یافته در نیامده است وارد بدن شوند، سیستم ایمنی به جای پاسخ به آنتیژنهای فوق دچار تولرانس شده و حتی در برخوردهای بعدی نیز به شکل کاملاً جدی پاسخ ایمنی برانگیخته نخواهد شد و در نتیجه بـا وجود دفعات تزریق خون بالا، ممکن است بیمار آلوآنتیبادی ایجاد نکند (3).
برای پیشگیری یا کاهش آلوایمونیزاسیون و ایجاد آلوآنتیبادیها در بیماران تالاسمی وابسته به تزریق خون مکرر میتوان پیشنهاداتی ارائه داد که عبارتند از؛ غربالگری آنتیبـادی قبل از هر تزریق خون و فراهم نمودن لوازم آن از قبیل گلبولهای قرمز O معرف و پـانل سلهای مختلف و استاندارد، قرابت نژادی و قومیتی بین دهنده و گیرنـده خون، تطابق گسترده گروههای خونی بین اهداکننده و گیرنده گلبولهای قرمز به ویژه برای سیستم آنتیژنهای Rh و Kell، تزریق خون سازگار از لحاظ سیستمهای گروه خونی Kell و Rh (C، E، c، e) و سایر گروههای خونی مینور، اسـتفاده نمـودن از فیلترهای کاهنده گلبولهای سـفید در حـین تزریـق خـون و برگزاری کارگاههای درمان تالاسمی با هدف اقدامات ممکن برای کنترل و پیشگیری از ایجاد آلوایمونیزاسیون و افزایش نیاز بـه خون، میتواند تا حد زیادی به حل این مشکل کمک کند. از جمله محدودیتهای مطالعه حاضر میتوان به حجم نمونه نسبتاً پـایین و محدود بودن به یک مرکز درمانی اشاره کرد که ممکن است قابلیت تعمیم نتایج را کاهش دهد. با این حال، این مطالعه نخستین بررسی جامع در منطقه بیرجند است که با استفاده از روشهای استاندارد انجام شده و اطلاعات پایه ارزشمندی را فراهم میکند. پیشنهاد میشود در مطالعههای آینده با حجم نمونه بیشتر، در مراکز مختلف و بـا بررسی عوامل ژنتیکی و ایمونولوژیک، و عوامل مؤثر بر آلوایمونیزاسیون در بیماران تالاسمی به طور دقیقتر بررسی شود.
نتیجهگیری
نتایج این مطالعه نشان داد که اکثریت آلوآنتیبادیهای ایجاد شده بر علیه سیستمهای گروه خونی Kell و Rh هستند. از آن جایی که آلوایمونیزاسیون علیه آنتیژنهای گروههای خونی اصلی و فرعی مهم از نظر بالینی، میتوانند بر کیفیت زندگی، بقای کلی بیماران مبتلا به بتا تالاسمی ماژور، اثر بخشی و تعداد دفعات تزریق خون اثر بـگذارند، بنابراین راهبردهای پیشگیرانه مناسب مانند تعیین فنوتیپ RBC برای بیماران قبل از شروع انتقال خون و استفاده از تطابق گسترده اهداکننده و گیرنده RBC، بـه ویژه برای سیستم آنتیژنهای Rh و Kell، میتواند برای جلوگیری از عوارض در این بیماران اجرا شود و از اهمیت بالینی ویژهای برخوردار است. این مطالعه میتواند دید بهتری برای مطالعههای آینده فراهم کند کـه در نهایت ممکن است بـه
مدیریـت بهتـر مشکـل ایجـاد آلـوآنتیبادیهــا در بیماران
تالاسمی وابسته به تزریق خون منجر شود.
حمایت مالی
این مطالعه با حمایت مالی دانشگاه علوم پزشکی بیرجند انجام شد.
ملاحظات اخلاقی
این مطالعـه با کد اخلاق IR.BUMS.REC.1403.233 در کمیته اخلاق پژوهشی دانشگاه علوم پزشکی بیرجند تصویب شد. قبل از ورود بیماران به مطالعه، رضایتنامه کتبی از تمامی بیماران یـا اولیای قانونی آنها اخذ گردید و کلیه اطلاعات بیماران بـه صورت محرمانه و بدون ذکر نام ثبت و تحلیل شد. تمامی مراحل پژوهش مطابق با اصول اخلاقی بیانیه هلسینکی انجام شده است.
عدم تعارض منافع
نویسندگان این مقاله اعلام میدارند که هیچگونه تعارض منافعی در ارتباط با این مطالعه وجود ندارد.
نقش نویسندگان
مبینا نخعی شامحمود: طراحی مطالعه، جمعآوری داده، تحلیل آماری، انجام آزمایشها، ویرایش مقاله
مازیار نصیری: همکاری در جمعآوری دادهها، مشارکت در تحلیل نتایج
محمدرضا مقدادی: تحلیل آماری، نگارش پیشنویس اولیه مقاله
دکتر حسن مرتاضی: راهنمای بالینی، نظارت بر جمعآوری دادههای بیماران و صحت تشخیصها
معصومه اسدی فرد: همکاری در طراحی روش اجرا و انجام آزمایشهای تخصصی
فرزانه عرفانی: مشارکت در جمعآوری اطلاعات
دکتر امید حسنی اکبریه: مشارکت در جمعآوری اطلاعات
دکتر فـاطمه مزگینژاد: راهنمای اصلی پژوهش، طراحی و تائید نهایی طرح تحقیق، نظارت کلی بر مقاله
تشکر و قدردانی
این مطالعه در دانشگاه علوم پزشکی بیرجند و بـا همکاری سازمان انتقال خون شهرستان بیرجند انجام گرفته و تمام هزینههای آن از محل اعتبارات طرحهای تحقیقاتی مصوب دانشگاه ( با شماره طرح 6637) تأمین شده است که بدین وسیله مراتب تقدیر و تشکر خود را از مسئولین این دانشگاه ابراز میداریم. همچنین از پرسنل سازمان انتقال خون شهرستان بیرجند که کمال همکاری را با ما داشتند، صمیمانه تشکر و سپاسگزاری میکنیم.
فهرست منابع
1. Vafaei M, Azad M, Shiargar P, Kazemi Haki B. Quality of life in patients with thalassemia major referred to Ardabil Buali Hospital in 2012-13. Medical Science Journal of Islamic Azad Univesity-Tehran Medical Branch 2015; 25(4): 305-10. [Article in Farsi]
2. Seferi I, Xhetani M, Face M, Burazeri G, Nastas E, Vyshka G. Frequency and specificity of red cell antibodies in thalassemia patients in Albania. Int J Lab Hematol 2015; 37(4): 569-74. [DOI:10.1111/ijlh.12362] [PMID]
3. Tahannejad-Asadi Z, Elahi A, Mohseni A, Talebi M, Khosravi M, Jalalifar MA. Screening and identifying of erythrocyte alloantibodies in patients with Thalassemia major referred to Ahvaz Shafa hospital. Feyz Journals of Kashan University of Medical Sciences 2013; 17(2): 165-72. [Article in Farsi]
4. Davoudi-Kiakalayeh A, Mohammadi R, Pourfathollah AA, Siery Z, Davoudi-Kiakalayeh S. Alloimmunization in thalassemia patients: New insight for healthcare. Int J Prev Med 2017; 8(1): 101. [DOI:10.4103/ijpvm.IJPVM_246_16] [PMID] []
5. De Sanctis V, Kattamis C, Canatan D, Soliman AT, Elsedfy H, Karimi M, et al. β-thalassemia distribution in the old world: an ancient disease seen from a historical standpoint. Mediterr J Hematol Infect Dis 2017; 9(1): e2017018. [DOI:10.4084/mjhid.2017.018] [PMID] []
6. Mahboudi F, Zeinali S, Merat A, Delmaghani S, Mostafavipour K, Moghadam Z, et al. The molecular basis of beta thalassemia mutations in Fars province, Iran. Iran J Med Sci 1996; 21: 99-104.
7. Najmabad H, Teymourian Sh, Jalilnezhad S, Azad M, Khatibi T, Neyshabouri M, et al. Amplification refractory mutation system (arms) and reverse hybridization in the detection of beta - thalassemia mutations. Archives of Iranian Medicine 2001; 4(4): 165-70.
8. Butler E LM, Coller BS. William's Hematology. 6th ed. USA: McgrowHill; 2001. p. 1290-1292.
9. Orkin SH, Nathan DG, Ginsburg D, Look A, Fisher DE, Lux S. Nathan & Oski's hematology of infancy and childhood. Philadelphia: WB Saunders Company; 2003 p. 1173-1174.
10. Cheng C, Lee C, Lin C. Clinically significant red blood cell antibodies in chronically transfused patients: a survey of Chinese thalassemia major patients and literature review. Transfusion 2012; 52(10): 2220-4. [DOI:10.1111/j.1537-2995.2012.03570.x] [PMID]
11. Azarkeivan A, Ahmadi MH, Zolfaghari S, Shaiegan M, Ferdowsi S, Rezaei N, et al. RBC alloimmunization and double alloantibodies in thalassemic patients. Hematology 2015; 20(4): 223-7. [DOI:10.1179/1607845414Y.0000000189] [PMID]
12. Blaney KD, Howard PR. Basic and applied concepts of immunohematology. Philadelphia: Elsevier; 2001. p. 131-132.
13. Michail-Merianou V, Pamphili-Panousopoulou L, Piperi-Lowes L, Pelegrinis E, Karaklis A. Alloimmunization to red cell antigens in thalassemia: comparative study of usual versus better-match transfusion programmes. Vox Sang 1987; 52(1-2): 95-8. [DOI:10.1111/j.1423-0410.1987.tb02999.x] [PMID]
14. Pineda A, Vamvakas E, Gorden L, Winters J, Moore S. Trends in the incidence of delayed hemolytic and delayed serologic transfusion reactions. Transfusion 1999; 39(10): 1097-103. [DOI:10.1046/j.1537-2995.1999.39101097.x] [PMID]
15. Spanos T, Karageorga M, Ladis V, Peristeri J, Hatziliami A, Kattamis C. Red cell alloantibodies in patients with thalassemia. Vox Sang 1990; 58(1): 50-5.
https://doi.org/10.1111/j.1423-0410.1990.tb02055.x [DOI:10.1159/000461077] [PMID]
16. Taher A, Isma'eel H, Cappellini MD. Thalassemia intermedia: revisited. Blood Cells, Molecules, and Diseases 2006; 37(1): 12-20. [DOI:10.1016/j.bcmd.2006.04.005] [PMID]
17. Matteocci A, Pierelli L. Red blood cell alloimmunization in sickle cell disease and in thalassaemia: current status, future perspectives and potential role of molecular typing. Vox Sang 2014; 106(3): 197-208. [DOI:10.1111/vox.12086] [PMID]
18. Sadeghian MH, Keramati MR, Badiei Z, Ravarian M, Ayatollahi H, Rafatpanah H, et al. Alloimmunization among transfusion-dependent thalassemia patients. Asian J Transfus Sci 2009; 3(2): 95-8. [DOI:10.4103/0973-6247.53884] [PMID] []
19. Singer ST, Wu V, Mignacca R, Kuypers FA, Morel P, Vichinsky EP. Alloimmunization and erythrocyte autoimmunization in transfusion-dependent thalassemia patients of predominantly Asian descent. Blood 2000; 96(10): 3369-73.
https://doi.org/10.1182/blood.V96.10.3369 [DOI:10.1182/blood.V96.10.3369.h8003369_3369_3373]
20. Kiani A, Abdi J, Shirkhani Y, Kashi M. Prevalence of alloimmunization against RBC antigens in thalassemia major patients of Lorestan province in 1383. Sci J Iran Blood Transfus Organ 2006; 3(3): 265-71. [Article in Farsi]
21. Al‐Riyami AZ, Al‐Muqbali A, Al‐Sudiri S, Murthi Panchatcharam S, Zacharia M, Al‐Mahrooqi S, et al. Risks of red blood cell alloimmunization in transfusion‐dependent β‐thalassemia in Oman: a 25‐year experience of a university tertiary care reference center and a literature review. Transfusion 2018; 58(4): 871-8. [DOI:10.1111/trf.14508] [PMID]
22. Chao YH, Wu KH, Lu JJ, Shih MC, Peng CT, Chang CW. Red blood cell alloimmunisation among Chinese patients with β-thalassaemia major in Taiwan. Blood Transfus 2013; 11(1): 71-4.
23. Ahmed AM, Hasan NS, Ragab SH, Habib SA, Emara NA, Aly AA. Red cell alloimmunization and autoantibodies in Egyptian transfusion-dependent thalassaemia patients. Arch Med Sci 2010; 6(4): 592-8. [DOI:10.5114/aoms.2010.14473] [PMID] []
24. Obeidi N, Mankhian AR, Hatami G, Emami H. Antibody screening in patients with thalassemia major. Lab Med 2011; 42(10): 618-21. [DOI:10.1309/LMBF1AT2HEVYUS7D]
25. Ahmadi D. Frequency of minor blood group alloantibodies in beta-thalassemia major blood recipients in Kermanashah (1999). 2001. p:23.
26. Rostamian H, Javandoost E, Mohammadian M, Alipour A. Prevalence and specificity of red blood cell alloantibodies and autoantibodies in transfused Iranian β-thalassemia patients: A systematic review and meta-analysis. Asian J Transfus Sci 2022; 16(1): 111-20. [DOI:10.4103/ajts.AJTS_39_20] [PMID] []
27. Shamsian B, Arzanian MT, Shamshiri AR, Alavi S, Khojasteh O. Frequency of red cell alloimmunization in patients with beta-major thalassemia in an Iranian referral hospital. 2008; 2(1): 13-17.
28. Karimi M, Nikrooz P, Kashef S, Jamalian N, Davatolhagh Z. RBC alloimmunization in blood transfusion‐dependent β‐thalassemia patients in southern Iran. Int J Lab Hematol 2007; 29(5): 321-6. [DOI:10.1111/j.1365-2257.2006.00856.x] [PMID]
29. Keikhaei B, Far AH, Abolghasemi H, Mousakhani H, Ghanavat M, Moghadam M. Red blood cell alloimmunization in patients with thalassemia major and intermediate in southwest Iran. Iranian Journal of Blood and Cancer 2013; 6(1): 41-6.
30. Ameen R, Al‐Shemmari S, Al‐Humood S, Chowdhury RI, Al‐Eyaadi O, Al‐Bashir A. RBC alloimmunization and autoimmunization among transfusion‐dependent Arab thalassemia patients. Transfusion 2003; 43(11): 1604-10. [DOI:10.1046/j.1537-2995.2003.00549.x] [PMID]
31. El Danasoury AS, Eissa DG, Abdo RM, Elalfy MS. Red blood cell alloimmunization in transfusion‐dependent Egyptian patients with thalassemia in a limited donor exposure program. Transfusion 2012; 52(1): 43-7. [DOI:10.1111/j.1537-2995.2011.03234.x] [PMID]
32. Ho HK, Ha SY, Lam CK, Chan GC, Lee TL, Chiang AK, et al. Alloimmunization in Hong Kong southern Chinese transfusion-dependent thalassemia patients. Blood 2001; 97(12): 3999-4000. [DOI:10.1182/blood.V97.12.3999] [PMID]
33. Patel AS, Gamit S, Gohil M. Role of RBC's alloimmunization in multiple transfused thalassaemia patients. Int J Res Med Sci 2016; 4(3): 822-8. [DOI:10.18203/2320-6012.ijrms20160526]
34. Gupta R, Singh DK, Singh B, Rusia U. Alloimmunization to red cells in thalassemics: emerging problem and future strategies. Transfus Apher Sci 2011; 45(2): 167-70. [DOI:10.1016/j.transci.2011.07.014] [PMID]
35. Bilwani F, Nabi G, Adil S, Usman M, Hassan F, Khurshid M. Frequency of irregular red cell alloantibodies in patients with thalassemia major: a bicenter study. J Pak Med Assoc 2005; 55(12): 563-5.
36. Ghasemi A, Abbasian S, Ghaffari K, Salmanpour Z. Prevalence of alloantibodies and autoantibodies in transfusion dependent thalassemia patients. Iranian Journal of Blood and Cancer 2016; 8(3): 80-5.
37. Mirzaeian A, Tamaddon G, Naderi M, Hosseinpour M, Sargolzaie N. Prevalence of alloimmunization against RBC antigens in thalassemia major patients. Zahedan Journal of Research in Medical Sciences 2013; 15(7): 55-8.
38. Mohamadimaram M, Gharehbaghian A, Abdollahi A, Khansari M. The prevalence of undesired blood group antibodies in thalassemia patients. Sci J Iran Blood Transfus Organ 2020; 17(2): 91-9. [Article in Farsi]
39. Darvishi P, Azami M, Sayehmiri K, Sayehmiri F, Goodarzi A, Azarkeivan A, et al. Red blood cell alloimmunization in Iranian beta‐thalassemia patients: a systematic review and meta‐analysis. ISBT Science Series 2016; 11(3): 163-73. [DOI:10.1111/voxs.12299]
40. Hussein E, Desooky N, Rihan A, Kamal A. Predictors of red cell alloimmunization in multitransfused Egyptian patients with β-thalassemia. Arch Pathol Lab Med 2014; 138(5): 684-8. [DOI:10.5858/arpa.2013-0016-OA] [PMID]
41. El-Beshlawy A, Salama AA, El-Masry MR, El Husseiny NM, Abdelhameed AM. A study of red blood cell alloimmunization and autoimmunization among 200 multitransfused Egyptian β thalassemia patients. Sci Rep 2020; 10(1): 21079. [DOI:10.1038/s41598-020-78333-y] [PMID] []
42. Al-Mousawi MM, Al-Allawi NA, Alnaqshabandi R. Predictors of red cell alloimmunization in Kurdish multi transfused patients with hemoglobinopathies in Iraq. Hemoglobin 2015; 39(6): 423-6. [DOI:10.3109/03630269.2015.1077460] [PMID]
43. Azarkeivan A, Ansari S, Ahmadi MH, Hajibeigy B, Maghsudlu M, Nasizadeh S, et al. Blood transfusion and alloimmunization in patients with thalassemia: multicenter study. Pediatr Hematol Oncol 2011; 28(6): 479-85. [DOI:10.3109/08880018.2011.568595] [PMID]
44. Ebrahimisadr P, Bakhshandeh Z, Majidiani H. Red cell alloantibodies in beta-thalassaemia major patients' blood referring to the regional blood transfusion center of Tehran, Iran. Bioimpacts 2020; 11(2): 129-33. [DOI:10.34172/bi.2021.20] [PMID] []
45. Keramati MR, Sadeghian MH, Zarmehri AM. Red blood cells alloimmunization and autoimmunization in multi-transfused thalassemia patients in south of Iran. Iran J Pediatr Hematol Oncol 2019; 9(1): 40-7.
46. Afshari M, Amiri F, Seyedi M, Biglari M, Jambozorg H. Evaluation of alloantibodies in thalassemia patients referred to Hamadan Besat hospital in 2019. Sc J Iran Blood Transfus Organ 2021; 18(3): 187-95. [Article in Farsi]
47. Davari K, Soltanpour MS. Study of alloimmunization and autoimmunization in Iranian β-thalassemia major patients. Asian J Transfus Sci 2016; 10(1): 88-92. [DOI:10.4103/0973-6247.172179] [PMID] []
48. Vaziri M, Javadzadeh Shahshahani H, Moghaddam M, Taghvaee N. Prevalence and specificities of red cell alloantibodies in transfusion-dependent beta thalassemia patients in Yazd. Iran J Ped Hematol Oncol 2015; 5(2): 93-9.
49. Hassan K, Younus M, Ikram N, Naseem L, Zaheer HA. Red cell alloimmunization in repeatedly transfused thalassemia major patients. Int J Pathol 2018; 16-9.
50. Reisner E, Kostyu D, Phillips G, Walker C, Dawson D. Alloantibody responses in multiply transfused sickle cell patients. Tissue Antigens 1987; 30(4): 161-6. [DOI:10.1111/j.1399-0039.1987.tb01615.x] [PMID]
51. Saied DA, Kaddah AM, Eldin RMB, Mohaseb SS. Alloimmunization and erythrocyte autoimmunization in transfusion-dependent Egyptian thalassemic patients. J Pediatr Hematol Oncol 2011; 33(6): 409-14. [DOI:10.1097/MPH.0b013e3182208154] [PMID]
52. Koochakzadeh L, Kajiyazdi M, Khoshhal F, Hashemi A, Khabazkhoob M. Prevalence of alloantibodies in thalassemia patients and its relationship with age, gender and blood group. Acta Med Iran 2023; 61(1): 52-6. [DOI:10.18502/acta.v61i1.12126]
53. Eghbali A, Rahimi-Afzal R, Mehrabi S, Sanatkar SA, Mousavi-Hasanzadeh M. Frequency and risk factors of red blood cell alloimmunization in thalassemia major patients in Markazi province. Iran J Pediatr Hematol Oncol 2019; 9(1): 25-31.
54. Abdulqader AMR, Mohammed AI, Mohammed NI. Red cell alloimmunization and autoimmunization in multi-transfused thalassemia patients in Sulaymaniyah Province-Iraq. Korean J Clin Lab Sci 2020; 52(2): 98-104. [DOI:10.15324/kjcls.2020.52.2.98]
55. Paramore C, Vlahiotis A, Moynihan M, Cappell K, Ramirez-Santiago A. Treatment patterns and costs of transfusion and chelation in commercially-insured and medicaid patients with transfusion-dependent β-thalassemia. Blood 2017; 130: 5635. [DOI:10.1016/j.jval.2018.04.1750]
56. Sharma A, Mathew ME, Puri L. Splenectomy for people with thalassaemia major or intermedia. Cochrane Database Syst Rev 2019; 9(9): CD010517. [DOI:10.1002/14651858.CD010517.pub3] [PMID]
57. Azarkeivan A, Ahmadi MH, Gharehbaghian A, Zolfaghari S, Nasizadeh S, Maghsudlu M, et al. Antibody screening and identification by gel method in thalassemic patients. Sci J Iran Blood Transfus Organ 2008; 5(2): 99-108. [Article in Farsi]
58. Thompson AA, Cunningham MJ, Singer ST, Neufeld EJ, Vichinsky E, Yamashita R, et al. Red cell alloimmunization in a diverse population of transfused patients with thalassaemia. Br J Haematol 2011; 153(1): 121-8. [DOI:10.1111/j.1365-2141.2011.08576.x] [PMID] []
59. Pazgal I, Yahalom V, Shalev B, Raanani P, Stark P. Alloimmunization and autoimmunization in adult transfusion-dependent thalassemia patients: a report from a comprehensive center in Israel. Ann Hematol 2020; 99(12): 2731-6. [DOI:10.1007/s00277-020-04104-4] [PMID]
60. Ansari S, Voosogh P, Moshtaghian S. Assessment of frequency of alloimmunization and erythrocyte autoimmunization in transfusion dependent thalassemia patients. Acta Med Iran 2008; 46(2): 137-40.
61. Mincheff M. Changes in donor leukocytes during blood storage. Implications on post‐transfusion immunomodulation and transfusion‐associated GVHD. Vox Sang 1998; 74(S2): 189-200. [DOI:10.1111/j.1423-0410.1998.tb05420.x] [PMID]
62. Fluit C, Kunst V, Drenthe‐Schonk A. Incidence of red cell antibodies after multiple blood transfusion. Transfusion 1990; 30(6): 532-5. [DOI:10.1046/j.1537-2995.1990.30690333485.x] [PMID]
63. Rosse WF, Gallagher D, Kinney TR, Castro O, Dosik H, Moohr J, et al. Transfusion and alloimmunization in sickle cell disease. The Cooperative Study of Sickle Cell Disease. Blood 1990; 76(7): 1431-7.
https://doi.org/10.1182/blood.V76.7.1431.1431 [DOI:10.1182/blood.V76.7.1431.bloodjournal7671431]
64. Schonewille H, Van De Watering LM, Loomans DS, Brand A. Red blood cell alloantibodies after transfusion: factors influencing incidence and specificity. Transfusion 2006; 46(2): 250-6. [DOI:10.1111/j.1537-2995.2006.00708.x] [PMID]
65. Dhawan HK, Kumawat V, Marwaha N, Sharma RR, Sachdev S, Bansal D, et al. Alloimmunization and autoimmunization in transfusion dependent thalassemia major patients: Study on 319 patients. Asian J Transfus Sci 2014; 8(2): 84-8. [DOI:10.4103/0973-6247.137438] [PMID] []
66. Arianezhad A, Eslamizadeh R, Momeni A, Yazdanpanah P, Behzadifard M. Investigation of alloimmunization in beta-thalassemia major patients: a cross-sectional study. Ann Med Surg 2025; 87(4): 1893-6. [DOI:10.1097/MS9.0000000000003092] [PMID] []
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |




