جلد 22، شماره 3 - ( پائیز 1404 )
جلد 22 شماره 3 صفحات 195-183 |
برگشت به فهرست نسخه ها
Ethics code: IR.TMI.REC.1403.023
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Asiyabi S, Amini-Kafiabad S, Teimourpour A, Gholizadeh H R, Alizadeh Haghighi S, Rafiee M H. Evaluation of the Sensitivity and Specificity of a Hemoglobinometer Device Produced by a Knowledge-Enterprise Company in Thalassemia Patients. bloodj 2025; 22 (3) :183-195
URL: http://bloodjournal.ir/article-1-1585-fa.html
URL: http://bloodjournal.ir/article-1-1585-fa.html
آسیابی ساناز، امینی کافیآباد صدیقه، تیمورپور امیر، قلیزاده حمیدرضا، علیزاده حقیقی سمانه، رفیعی محمد حسام. ارزیابی حساسیت و ویژگی یک دستگاه هموگلوبینومتر تولید شده توسط یک شرکت دانش بنیان در بیماران تالاسمی. فصلنامه پژوهشی خون. 1404; 22 (3) :183-195
ساناز آسیابی 

 ، صدیقه امینی کافیآباد
، صدیقه امینی کافیآباد 

 ، امیر تیمورپور
، امیر تیمورپور 

 ، حمیدرضا قلیزاده
، حمیدرضا قلیزاده 
 ، سمانه علیزاده حقیقی
، سمانه علیزاده حقیقی 
 ، محمد حسام رفیعی*
، محمد حسام رفیعی* 




 ، صدیقه امینی کافیآباد
، صدیقه امینی کافیآباد 

 ، امیر تیمورپور
، امیر تیمورپور 

 ، حمیدرضا قلیزاده
، حمیدرضا قلیزاده 
 ، سمانه علیزاده حقیقی
، سمانه علیزاده حقیقی 
 ، محمد حسام رفیعی*
، محمد حسام رفیعی* 


استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون
متن کامل [PDF 791 kb]
(461 دریافت)
| چکیده (HTML) (986 مشاهده)
مقدمه
بیماری تالاسمی که به علت اختلال ژنتیکی غیر طبیعی در زنجیره گلوبولین میباشد، میتواند منجر به ایجاد اختلالات شدید از جمله بتا تالاسمی هموزیگوت، بتا تالاسمی Hb E و هیدروپس جنینی Hb Bart در بیماران گردد (1). علیرغم این که کم خونی میکروسیتیک بیانگر طیف وسیعی از بیماریها میباشد، این نوع کم خونی میتواند به عنوان یکی از علائم اولیه در بیماران تالاسمی مطرح باشد، بنابراین اندازهگیری دقیق هموگلوبین در تمایز بین بیماران تالاسمی و سایر شرایط مانند کم خونی فقر آهن میتواند کمککننده باشد (2، 1).
در بیماران تالاسمی و به ویژه بیماران وابسته به تزریق خون (TDT : Transfusion-Dependent Thalassemia)، که دارای شرایط بالینی سختی هستند، تزریق گلبول قرمز برای حفظ سطح هموگلوبین توصیه میگردد (3). یکی از روشهای اندازهگیری هموگلوبین استفاده از دستگاههای هموگلوبینومتر میباشد که از مزایای عمده آنها میتوان به موارد زیر اشاره نمــود (5، 4):
مواد و روشها
طراحی مطالعه و جمعیت مورد مطالعه:
در این مطالعه مقطعی، یک دستگاه هموگلوبینومتر تولید شده توسط یک شرکت دانش بنیان در مقایسه با یک دستگاه مرجعXP -300 TM Automated Haematology Analyser در اندازهگیری غلظت هموگلوبین در بیماران تالاسمی مورد ارزیابی قرار گرفت. دادههای مورد استفاده در این مطالعه مربوط به بیماران تالاسمی مراجعهکننده به درمانگاه تالاسمی بزرگسالان ظفر در تهران در محدوده زمانی آذر ماه تا اسفند ماه سال 1402 بود. تعداد افراد شرکتکننده در مطالعه 83 نفر (33 نفر آقا و 50 نفر خانم) بودند.
جمعآوری نمونه و انجام آزمایش:
1- نوع نمونه: در این مطالعه، نمونه خون وریدی بیماران تالاسمی برای اندازهگیری غلظت هموگلوبین با دستگاه مرجع و دستگاه هموگلوبینومتر مورد ارزیابی قرار گرفت. به منظور جلوگیری از مداخلـه اضـافه نسـبت بـه شـرایط روتـین اخـذ نمونـه از بیماران تالاسمی، نمونه خون مویرگی جهــت اندازهگیری هموگلــوبین گرفته نشد. بنابراین نمونهگیری از بیماران مطابق با دستورالعمل روش نمونهگیری در درمانگاه تالاسمی انجام شد.
2- شرایط انجام آزمایش: نیاز بـه شـرایط پـره آنـالایتیکی خاصی برای انجام آزمـایش نمـیباشـد. لولـههـا تـا زمـان سنجش در دمای 2 تا 8 درجه سانتیگراد نگهداری و انجام آزمایش بلافاصله بعد از نمونهگیری از بیماران تالاسمی انجـام شد. کارکنان درمانگاه تالاسمی که در این پژوهش همکاری داشتند، برای تمامی مراحل انجام سنجش هموگلوبین با روش مرجـع و فرآیندهای مرتبط بـا آن طبق استانداردهای انتقال خـون و دستورالعملهای مصوب در این زمینه آموزش دیدهانـد و بخشی از کار روتین آنها بوده است. درخصـوص دستگاه هموگلوبینومتر مورد ارزیابی نیز قبل از استفاده و مطابق با بروشور دستگاه، به صـورت محـدود برای کارکنان مدنظر آموزش لازم انجـام شـده بـود.
3- حجم نمونه مورد استفاده در این مطالعه بـرای ارزیـابی
کنترل کیفی: حداقل حجم نمونه مورد نیاز برای برآورد میزان توافق بین نتایج دو دستگاه براساس شاخص ضریب همبستگی درون طبقهای (شاخص ICC) و استفاده از پکیجICC.Sample.Size ؛ از نرمافزار آماری آر یا R نسخه 4.4.1 برای تحلیل دادههای آماری استفاده شد. در نظر گرفتن سطح معناداری 05/0 و توان 95 درصد و مقدار توافق مورد نظر 80 درصد برابر حداقل توافق مورد نظر 60 درصد با حداقل 81 نمونه محاسبه گردید. بدین منظور در این مطالعه، اندازهگیری مقایسهای غلظت هموگلوبین با دو دستگاه بر روی 83 بیمار تالاسمی مراجعهکننده به درمانگاه انجام شد.
دستگاههای تحت مطالعه
1-دستگاه هموگلوبینومتر تولید شده توسط یک شرکت دانش بنیان:
اساس کار: از میکروکووتهای طراحی شده استاندارد جهت جمعآوری 2-3 قطره خون استفاده شد و بلافاصله برای تجزیه و تحلیل در دستگاه قرار داده شد. این میکروکووتها حاوی سدیم دیاکسیکولات هستند که غشای گلبولهای قرمز را متلاشی میکند و Hb را آزاد مینماید. سپس نیترات سدیم، آهن هموگلوبین را از آهن دو ظرفیتی به فرم سه ظرفیتی تبدیل و مت هموگلوبین تشکیل میگردد، مت هموگلوبین با آزید ترکیب میشود و آزیدمت هموگلوبین را تشکیل میدهد. سپس این ترکیب توسط اسپکتروفتومتر در طول موج 540 نانومتر اندازهگیری میشود. کالیبراسیون دستگاه هموگلوبینومتر به صورت خودکار انجام میشود و اگر در بررسیهای دورهای تفاوت معناداری در نتایج مشاهده شود، میتوان از فرآیند کالیبراسیون دستی استفاده کرد، بدین ترتیب که ابتدا با میکروکووت خالی و سپس با میکروکووت پر شده با کالیبراتور، کالیبراسیون تکمیل میگردد. برای ارزیابی دقت و صحت دستگاه، کنترل کیفی روزانه انجام نمیشود و طبق بروشور دستگاه نیازی به استفاده از خون کنترل نمیباشد، ولی طبق پیشنهاد شرکت سازنده، یک محلول کنترلی که توسط شرکت تهیه شده است را میتوان به صورت ماهانه توسط بخش کنترل کیفی به دستگاه داد و عددی که باید قرائت شود در محدوده 5/0 ± 12 است.
ارزیابی مستندات:
بـر اسـاس تاییدیـه ارائـه شـده که مبتنی بر مشخصات
نمونه تحت آزمون و مشخصات پذیرش نمونه میباشد، نتایج دستگاه آنالیزور هموگلوبین با استاندارد I EC 61010-2-101 (International Electrotechnical Commission) مطابقت دارد.
گواهینامـه بینالمللـــی از KASCERT با شماره ISO
12485:2016 (تجهیزات پزشکی- سیستم مدیریت کیفیت)
مطابق با استانداردهای بینالمللی ارائه شده است.
پروانه تولید وسیله پزشکی به شماره 53612149 در مورخ 30/08/1402 از اداره کل تجهیزات پزشکی تحت نظارت سازمان غذا و دارو ایران (IFDA : Iranian Food and Drug Administration)، توسط شرکت ارائه شده است.
گواهینامه به شماره LQF-708-02-01 از شرکت دانش بنیان آزمایشگاههای صنایع انرژی (E.P.I.L : Energy and power Industries Laboratories Co) که مورد تائید سازمان ملی استاندارد، شرکت توانیر، سازمان غذا و دارو و غیره میباشد، ارایه شده است.
از ویژگیهای عملکردی دستگاه هموگلوبینومتر میتوان به آزمون خطی بودن و بررسی دقت دستگاه اشاره نمود.
- آزمون خطی بودن، بیانگر رابطه خطی میان نتایج اندازهگیری شده با خون کنترل شرکت روز آزمون (مقادیر کم، طبیعی و بالای هموگلوبین) میباشد. در مستندات ارائه شده رابطه خطی بر اساس فرمول شیب غلظت 61/0 + x97/0 y= بین نتایج با مقدار 99/0 R2= مشاهده گردید.
- در بررسی دقت دستگاه، از نظر آماری انحراف معیار (SD) و ضریب تغییرات (CV) میانگین سه غلظت مختلف هموگلوبین (2/9، 9/12و 2/16) به ترتیب با مقادیر کم، طبیعی و بالا بر حسب واحد گرم بر دسیلیتر با حجم نمونه 75 عدد برای هر غلظت به طور مجزا بررسی شده بود.
2- دستگاه مرجع (Sysmex XP-300TM Automated Haematology Analyser):
دستگاه مذکور برای بررسی هموگلوبین خون وریدی در این مطالعه مورد استفاده قرار گرفته است. دستگاه فوق ساخت کشور ژاپن میباشد.
اساس کار: از خون وریدی جهت اندازهگیری هموگلوبین استفاده میشود. در این سیستم از سدیم لوریل سولفات برای تبدیل Hb به یک ترکیب رنگی استفاده میکند که توسط اسپکتروفتومتر خودکار اندازهگیری میشود.
کالیبراسیون دستگاه: کنترل کیفی و کالیبراسیـون دستگـاه
طبق کاتالوگ و دستورالعمل مصوب در مرکز تالاسمی انجام شد (9).
جمعآوری دادهها و تجزیه و تحلیلهای آماری:
دادههای خوانش هموگلوبین با هر دو دستگاه (مرجع و هموگلوبینومتر) جمعآوری و در نرمافزار اکسل وارد شدند. برای مقایسه دقت خوانشها، شاخصهای توصیفی آماری (میانگین، انحراف معیار، میانه و ضریب تغییرات) محاسبه گردید. برای مقایسه عملکرد دو دستگاه، شاخصهایی شامل حساسیت، ویژگی، ارزش اخباری مثبت (PPV) و ارزش اخباری منفی (NPV) و ضریب توافق کاپا محاسبه شد. ارزیابی توافق با رگراسیون خطی و تحلیل توافق با ضریب همبستگی درون طبقهای (ICC : Infraclass Correlation Coefficient) و نمودار Bland –Altman انجام شد. کلیه تحلیلها در نرمافزار آماری R نسخه 4.4.1 اجرا گردید.
تعاریف آماری مطالعه:
تعیین حد آستانه یا تصمیم گیری (Cut off):
در افراد مبتلا به سندرم تالاسمی که وابسته به تزریق خون هستند، تزریق گلبول قرمز برای حفظ سطح هموگلوبین با شرط این نکته که میزان هموگلوبین قبل از تزریق بین 5/9 تا 5/10 گرم در دسیلیتر باید باشد، در نظر گرفته میشود (10، 3). با در نظر گرفتن حد آستانه تعریف شده و تجزیه و تحلیل آماری منحنی ROC در این مطالعه، Cut off برابر با 3/10 برای محاسبه حساسیت، ویژگی، ارزش اخباری مثبت و ارزش اخباری منفی تعریف گردید.
مثبت واقعی (TP) :
مواردی که میزان غلظت هموگلوبین در دستگاه مرجع و هموگلوبینومتر پایینتر از 3/10 گرم در دسیلیتر میباشد.
مثبت کاذب (FP) :
مواردی که میزان غلظت هموگلوبین کمتر از 3/10 گرم در دسیلیتر با دستگاه هموگلوبینومتر و غلظت بالاتر از 10 گرم در دسیلیتر با روش مرجع محاسبه شده است.
منفی واقعی (TN) :
مواردی که میزان غلظت هموگلوبین با دستگاه مرجع و هموگلوبینومتر بالاتر از 3/10 گرم در دسیلیتر میباشد.
منفی کاذب (FN) :
مواردی که میزان غلظت هموگلوبین بیشتر از 10 گرم در دسیلیتر با دستگاه هموگلوبینومتر و کمتر از 3/10 گرم در دسیلیتر با روش مرجع محاسبه شده است.
حساسیت:
تعداد موارد مثبت واقعی شناسایی شده توسط دستگاه تقسیم بر مجموع موارد مثبت واقعی و منفی کاذب درصد (11، 9) (جدول 1).
ویژگی:
تعداد موارد منفی واقعی شناسایی شده توسط دستگاه بر مجموع موارد منفی واقعی و مثبت کاذب در صد (11، 9)(جدول 1).
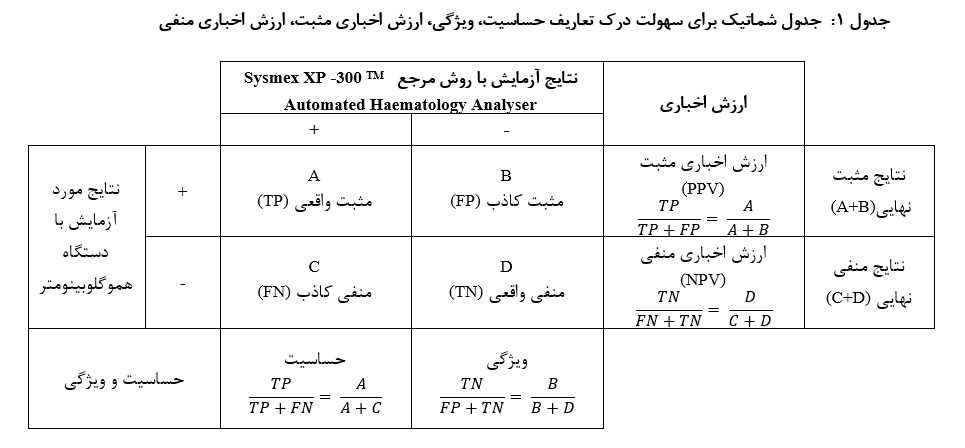 ارزش اخباری مثبت (PPV) :
ارزش اخباری مثبت (PPV) :
تعداد موارد مثبت واقعی شناسایی شده توسط دستگاه تقسیم بر مجموع موارد مثبت واقعی و کاذب در صد (11، 9)(جدول 1).
ارزش اخباری منفی (NPV) :
تعداد موارد منفی واقعی شناسایی شده توسط دستگاه بر مجموع موارد منفی واقعی و کاذب در صد (11، 9)(جدول 1).
یافتهها
در این مطالعه ارزیابی نتایج خوانش غلظت هموگلوبین وریدی بیماران تالاسمی با در نظر گرفتن عدد 3/10 به عنوان حد تصمیمگیری (Cut off)، بین دستگاه هموگلوبینومتر تولید شده توسط شرکت دانش بنیان با دستگاه مرجع Sysmex XP-300TM Automated Haematology Analyser به شرح زیر میباشد:
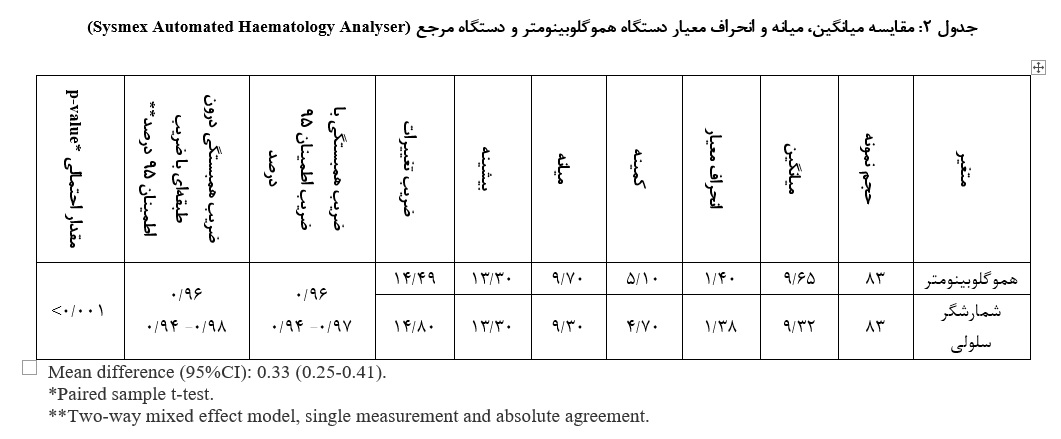
با حجم نمونه 83، میانگین و انحراف معیار خوانش با دستگاه هموگلوبینومتر و دستگاه مرجع، به ترتیب 40/1 ± 65/9 و 38/1 ± 32/9 گرم بر دسیلیتر و مقدار میانه خوانش به ترتیب 70/9 و 30/9 گرم بر دسیلیتر گزارش گردید (جدول 2).
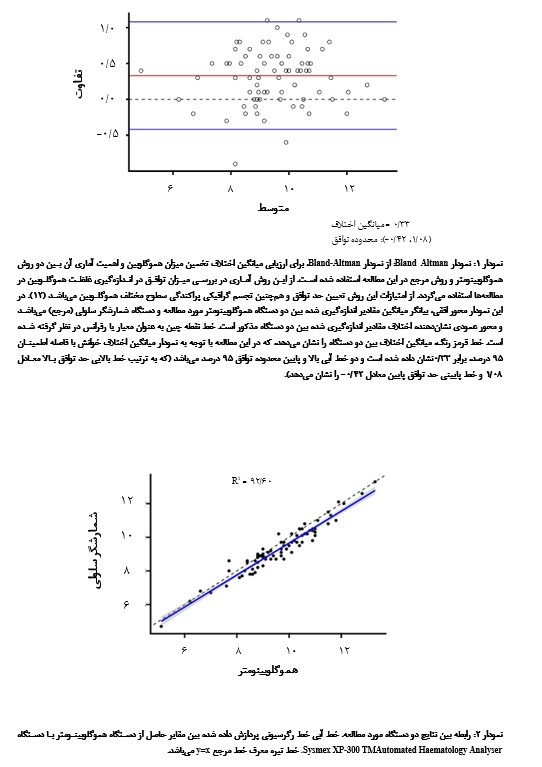
بر اساس نتایج نمودار Bland-Altman، مقایسه توافق بین دو دستگاه در خوانش، در نمودار نشان داده شده است (نمودار 1). میانگین اختلاف خوانش با فاصله اطمینان 95 درصد، برابر 33/0 و حد پایین و بالای توافق به ترتیب 42/0- و 08/1 میباشد. بنابراین با 001/0 p< از نظر
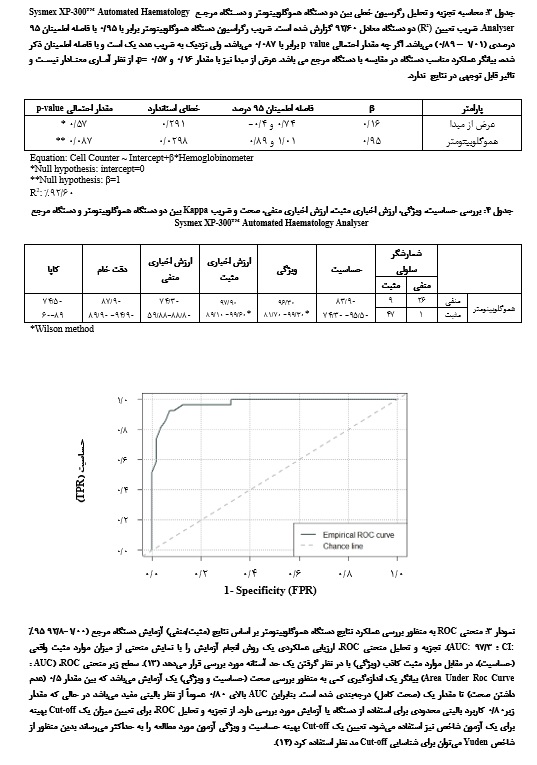
آماری اختلاف معناداری بین خوانش دو دستگاه هموگلوبینومتر و مرجع، وجود دارد، اما این اختلاف در محدوده قابل قبول برای کاربرد مورد نظر قرار دارد و از نظر عملی تاثیر قابل توجهی در روند کاری ندارد و دو دستگاه از نظر خوانش هموگلوبین با یکدیگر توافق و همخوانی داشتهاند. شاخص ICC، بین دستگاه هموگلوبینومتر و دستگاه مرجع عدد 96/0 درصد با فاصله اطمینان 95% محاسبه شد (98/0 – 94/0= CI %95 ، %96 ICC=)(جدول 2). برای بررسی همبستگی بین دو دستگاه، نمودار رگرسیون خطی مورد بررسی قرار گرفت (نمودار 2). بر اساس نمودار 2 ضریب تعیین (R2) دو دستگاه معادل 60/92 % گزارش شد، با توجه به ضریب تعیین محاسبه شده از نظر آماری در سطح 05/0 معنادار نمیباشد (جداول 2 و 3)، اما با ضریب رگرسیون با عدد 0/1 اختلاف معنادار نداشته و از طرفی خط رگرسیون به خط 45 درجه نزدیک است، بنابراین توافق مطلوب مورد نظر را میرساند.
حساسیت دستگاه هموگلوبینومتر در مقایسه با دستگاه مرجع 90/83 درصد با فاصله اطمینان 95% ( 50/93- 30/74)، ویژگی دستگاه 30/96 درصد با فاصله اطمینان %95 (30/99- 70/81) گزارش گردید. همچنین ارزش اخباری مثبت دستگاه 90/97 درصد با فاصله اطمینان 95% (60/99- 10/89) و ارزش اخباری منفی 30/74 درصد با فاصله اطمینان (80/88- 80/59) محاسبه شد. صحت دستگاه هموگلوبینومتر به صورت خام (Crude Accuracy)، 90/87 درصد با فاصله اطمینان 95% (90/94- 90/80) و ضریب کاپا، 50/74 با فاصله اطمینان 95 % (0/89- 0/60) گزارش گردید (جدول 4).
بحث
تالاسمی به عنوان یکی از شایعترین اختلالات ژنی اتوزومال مغلوب در جهان شناخته میشود که ناشی از اختلال در سنتز زنجیرههای هموگلوبین است. بر اساس آمارهای جهانی حدود 1 تا 5 درصد از جمعیت جهان ناقل جهشهای مرتبط با تالاسمی هستند (15). در بیماران با فرمهای متوسط تا شدید تالاسمی، تزریق خون منظم به عنوان درمان استاندارد محسوب میشود. این درمان نه تنها مکانیسمهای پاتولوژیک بیماری را کنترل میکند، بلکه در کاهش عوارض ثانویه بیماری نیز نقش دارد (19-16). نظارت دقیق در بیماران تالاسمی به دلیل ارزیابی شدت بیماری، تصمیمگیری برای نیاز به تزریق خون و در پایش پاسخ به درمان از اهمیت بالایی برخوردار میباشد. در این میان دستگاههای هموگلوبینومتر با توانایی اندازهگیری دقیق غلظت هموگلوبین، نقش کلیدی در مدیریت بیماران تالاسمی ایفا میکنند (20). به کارگیری دستگاههای هموگلوبینومتر در مواردی همانند تشخیص کم خونی فقر آهن، اهداکنندگان خون و موارد دیگری نیز مطرح میباشد. کم خونی فقر آهن به عنوان یک مشکل عمده بهداشت عمومی در سطح جهان مطرح میباشد، این نوع کم خونی به ویژه در کودکان منجر به اختلال در رشد جسمی و شناختی میگردد. بنابراین هر گونه مداخلهای برای درمان کم خونی تا حد زیادی مبتنی بر اندازهگیری سطح هموگلوبین است و میتواند یکی از راههای مؤثر برای تشخیص و طبقهبندی شدت کم خونی باشد، استفاده از دستگاههای هموگلوبینومتر برای تشخیص کم خونی به خصوص در مناطقی که ابزارهای پیشرفته برای اندازهگیری هموگلوبین در دسترس نیست، میتواند قابل اعتماد باشد (21). همچنین اندازهگیری هموگلوبین به عنوان یک آزمایش مهم در فرآیند قبل از اهدای خون است. هدف از اندازهگیری هموگلوبین در انتقال خون، محافظت از سلامت اهداکنندگان در برابر کم خونی و تضمین کیفیت خوب اجزای خون است، که بر سلامت گیرندگان خون تأثیرگذار میباشد، بنابراین استفاده از دستگاههای هموگلوبینومتر در فرآیند انتقال خون به دلیل کاربری راحت، مقرون به صرفه بودن، صحت و دقت بالا میتواند، مؤثر واقع گردد (22، 9).
مطالعه حال حاضر نشان داد دستگاه مورد بررسی با حساسیت 90/83 درصد و ویژگی 30/96 درصد از دقت تشخیصی مطلوبی برای شناسایی کم خونی در بیماران تالاسمی برخوردار است (صحت دستگاه: 90/87 درصد).
در مطالعهای صحت و دقت دستگاههای هموگلوبینومتر در مقایسه با دستگاههای مرجع هماتولوژی برای اندازهگیری هموگلوبین در محیطهای آزمایشگاهی در افراد سالم و بیماران دارای ناهنجاریهای مرتبط با ساختار هموگلوبین به اشکال خفیف تا شدید تأیید شده است، به طوری که کمترین میزان خطا و بیشترین توافق در دادههای آماری مشاهده شده است (23). در یک مطالعه که توسط مایوری و همکارانش در ارتباط با صحت تشخیصی یک دستگاه هموگلوبینومتر در مقایسه با روش مرجع سیانومت هموگلوبین انجام شده است، صحت دستگاه را با بررسی حساسیت و ویژگی بالای 80 درصد با کمترین میزان خطا با روش مرجع نشان دادهاند (24). حساسیت و ویژگی بالای دستگاههای هموگلوبینومتر، تأکیدی بر عملکرد بالینی سریع در شرایطی که تشخیص فوری از الزامات مهم در شناسایی کم خونی در بیماران به ویژه بیماران تالاسمی نیازمند دریافت خون است، میباشد. در مطالعه حال حاضر، میانگین و میانه خوانش هموگلوبین وریدی در بیماران تالاسمی با دستگاه هموگلوبینومتر به ترتیب 65/9 و 70/9 در مقایسه با هموگلوبین اندازهگیری شده از خون وریدی با دستگاه مرجع Sysmex XP-300 TM Automated Haematology Analyser، 32/9 و 30/9 گزارش گردید. میانگین و میانه محاسبه شده با دستگاه هموگلوبینومتر در مقایسه با دستگاه مرجع بالاتر گزارش شده است، اگر چه این میزان خوانش با 001/0 p< از نظر آماری معنادار میباشد، ولی در واقعیت این تفاوت بسیار کم بوده و در محدوده قابل قبولی در کاربردهای بالینی میباشد. در یک مطالعه که مقایسه سه روش اندازهگیری هموگلوبین بر روی نمونههای خون اهداکنندگان مورد بررسی قرار گرفته است، میانگین خوانش با دستگاه هموگلوبینومتر (Compolab TS)، دستگاه Cell counter و روش قدیمی سیانومت هموگلوبین به ترتیب 17/15، 95/14 و 09/15 (میانه به ترتیب 20/15، 0/15 و 0/15) گزارش شده است. در اندازهگیری هموگلوبین با دستگاه Compolab و Cell counter توافق خوبی نشان داده شد، ولی با روش سیانو مت هموگلوبین این توافق کمتر بود (25). با مقایسه نتایج بین دو مطالعه میتوان به این نکته اشاره کرد که در دستگاههایی که برای اندازهگیری هموگلوبین از خون وریدی استفاده میشود، به دلیل تفاوت خون شریانی در وریدها در مقایسه با مویرگها این اختـلاف خوانـش پایینتـر در وریدها توجیـهپذیـر میباشد (26).
در این مطالعه با توجه به نتایج حاصل از تفسیر نمودار Bland-Altman، میانگین اختلاف خوانش با فاصله اطمینان 95 درصد، برابر 33/0 و حد پایین و بالای توافق به ترتیب 42/0- و 08/1 میباشد. بنابراین با 001/0 p< از نظر آماری اختلاف معناداری بین خوانش دو دستگاه هموگلوبینومتر و مرجع وجود دارد، اما این اختلاف در محدوده قابل قبول برای هدف مورد نظر قرار دارد و بین دو دستگاه توافق دیده شد. نتایج حاصل از این میزان اختلاف در خوانش بین دو دستگاه هموگلوبینومتر و مرجع در مطالعههای مشابه نیز نشان داده است (25). از این رو میتوان نتیجه گرفت که دستگاههای هموگلوبینومتر در مقایسه با دستگاههای مرجع در ارزیابی غلظت هموگلوبین از توافق خوبی برخوردار میباشند. همچنین در بررسی ضریب همبستگی (ICC) دستگاه هموگلوبینومتر مورد مطالعه، توافق بسیار خوبی بین دو دستگاه مشاهده گردید (98/0- 94/0= CI 95/0 ، 96/0= ICC). بر اساس نمودار رگرسیون خطی 60/92 = R2 ، توافق مطلوب حاصل شد. همچنین در این پژوهش ارزش اخباری مثبت (PPV) و منفی (NPV) دستگاه هموگلوبینومتر به ترتیب 90/97 و 30/74 محاسبه شد. این نتایج در مقایسه با یک مطالعه در سال 2019، که PPV و NPV را به ترتیب 60/82% و 80/75 % گزارش کرده بود و بیانگر دقت تشخیصی مطلوبی در موارد مثبت می باشد، همسو است (7). در مطالعه حال حاضر، ارزش اخباری مثبت گزارش شده با 90/97 درصد بیانگر این مطلب است که از 47 مورد مثبت گزارش شده، فقط یک مورد مثبت کاذب می باشد و در ارتباط با ارزش اخباری منفی گزارش شده با عدد 30/74% نشاندهنده این است که از 26 مورد منفی گزارش شده، 9 مورد به طور کاذب منفی گزارش شده است (مطابق با جدول 4). علت این موارد منفی کاذب میتواند تحت تاثیر عوامل مختلفی از جمله جهشهای ژنی خاموش و یا خفیف در بعضی افراد مبتلا به تالاسمی، نوع نمونه و روشهای جمعآوری آن، محدودیتهای دستگاههای هموگلوبینومتر و عوامل محیطی، نمونههایی با همولیز خفیف و سایر شرایط مداخلهگر (کمبود آهن، کمبود اسید فولیک و برخی از انواع هموگلوبینها)، باشد (30-27، 22). در تفسیر نتایج گزارش شده در ارتباط با دستگاه هموگلوبینومتر به این نتیجه میرسیم که میتوان به تزریق خون در ارتباط با نتایج مثبت گزارش شده در بیماران تالاسمی اعتماد کرد، ولی در ارتباط با موارد منفی نیاز به بررسی بیشتر با دستگاه مرجع و یا روشهای دیگر تشخیصی در بیماران جهت تزریق خون میباشد. از آن جایی که بررسی آماری PPV و NPV در بالین حائز اهمیت است و در تصمیمگیری پزشکان در تزریق خون به بیماران تالاسمی نیازمند به دریافت خون تاثیرگذار میباشد، بررسی تجزیه و تحلیل آماری موارد مثبت و منفی واقعی با دستگاههایی که مرتبط با اندازهگیری هموگلوبین هستند از اهمیت بالایی برخوردار میباشد.
در ارزیابی هموگلوبین با استفاده از هموگلوبینومتر با استفاده از تجزیه و تحلیل ROC میتوان صحت دستگاه را در اندازهگیری غلظت هموگلوبین تعیین نمود (31). در این مطالعه، در بررسی صحت دستگاه هموگلوبینومتر با دستگاه مرجع با استفاده از منحنی ROC، میتوان به این نتیجه رسید که AUC با عدد 30/97 درصد بیانگر صحت بالای دستگاه مورد مطالعه میباشد. بهترین Cut-off برای دستگاه هموگلوبینومتر 30/10 است. همچنین در یک مطالعه از تجزیه و تحلیل منحنی ROC، برای مقایسه عملکرد دستگاه Hemocue (دستگاه هموگلوبینومتر) با دستگاه مرجع Automated Haematology Analyser استفاده شده است، و بنابر نتایج مشخص شد که هر دو دستگاه با AUC بالای 10 دارای صحت تشخیصی بالایی میباشند (31). از تجزیه و تحلیل منحنی ROC به عنوان یک ابزار قدرتمند در ارزیابی عملکرد تشخیصی آزمایشهای شاخص (آزمایشهایی که برای تشخیص یک بیماری یا شرایطی خاص به کار گرفته میشوند) استفاده میگردد. از طرفی دیگر AUC (سطح زیر منحنی ROC)، توانایی تمایز بین افراد بیمار و غیر بیمار را دارد و در تفسیر AUC حتماً باید فاصله اطمینان 95 درصد در نظر گرفته شود (14).
مزایای استفاده از دستگاههای هموگلوبینومتر علاوه بر امتیازاتی از جمله سادگی در نحوه اندازهگیری هموگلوبین، قابل حمل بودن، کالیبراسیون اتوماتیک و قابلیت استفاده در شرایط محدود آزمایشگاهی که دارند، با بررسی مطالعههای مقایسهای صورت گرفته از نظر ایندکسهای آماری، نزدیکترین نتایج را با روشهای مرجع دارا میباشند. بنابراین با رعایت دستورالعملهای استاندارد مرتبط با دستگاههای هموگلوبینومتر، ارائه آموزش کافی به کاربران و حصول اطمینان از کنترل کیفی دقیق، میتوان خطاهای احتمالی اندازهگیری هموگلوبین را با دستگاههـای هموگلوبینومتر به حداقل رساند (23).
نتیجهگیری
با توجه به نتایج این مطالعه، هموگلوبینومتر، در تشخیص موارد مثبت (90/97% = PPV) از دقت بالایی برخوردار است، زیرا از 47 مورد مثبت تنها یک مثبت کاذب داشت. بنابراین برای شناسایی بیماران تالاسمی نیازمند خون قابل اعتماد میباشد. ولی در موارد منفی (30/74 %= NPV) از 26 مورد، 9 مورد منفی کاذب گزارش شده است؛ توصیه میگردد نتایج با یک دستگاه مرجع یا سایر روشهای تشخیصی بررسی گردند.
محدودیتهای مطالعه:
علیرغم مزایای دستگاههای هموگلوبینومتر توجه به این نکته حائز اهمیت است که استفاده از دستگاههای هموگلوبینومتر در مواردی همانند تالاسمی بینابینی یا ماژور، ممکن است نیاز به تایید نتایج با روشهای دقیقتر مانند الکتروفورز هموگلوبین باشد. از طرفی دیگر در مواردی که میزان حجم متوسط گلبول قرمز (MCV) و غلظت متوسط هموگلوبین در گلبول قرمز (MCHC) هم در کم خونی فقر آهن و هم در تالاسمی مینور مشاهده میشود، باعث میشود که گاهی اوقات افتراق این دو بیماری از هم، به ویژه با روشهای ساده اندازهگیری هموگلوبین مانند دستگاههای هموگلوبینومتر دشوار باشد. زیرا این روش فقط عدد هموگلوبین کل را نشان میدهد و در مورد سایر شاخصهای خونی مانند MCV، MCHC و.... اطلاعات کافی را نشان نمیدهد.
حمایت مالی
مطالعه حاضر بدون حمایت مالی مرکز یا ارگان خاصی
انجام شده است.
ملاحظات اخلاقی
مطالعه فوق دارای کد اخلاق IR.TMI.REC.1403.023 از کمیته اخلاق مؤسسه عالی آموزشی و پژوهشی طب انتقال خون تهران، ایران است.
عدم تعارض منافع
نویسندگان مطالعه اظهار میکنند، هیچگونه تعارض منافعی در این پژوهش وجود نداشته است.
نقش نویسندگان
دکتر محمدحسام رفیعی: طراحی مطالعه، نگارش و ویرایش مقاله، جمعآوری و راستی آزمایی اطلاعات، تجزیه و تحلیل آماری و آمادهسازی جداول آماری
دکتر صدیقه امینی کافیآباد: طراحی مطالعه، ویرایش مقاله، راستی آزمایی اطلاعات
دکتر ساناز آسیابی: نگارش و ویرایش مقاله، جمعآوری و راستیآزمایی اطلاعات، تجزیه و تحلیل آماری و آمادهسازی جداول آماری
دکتر امیر تیمورپور: مشاور آماری در تجزیه و تحلیل آمار و نتایج
حمیدرضا قلیزاده: جمعآوری و راستیآزمایی اطلاعات
سمانه علیزاده حقیقی: کارشناس انجام آزمایشها در درمانگاه تالاسمی بزرگسالان ظفر
تشکر و قدردانی
بدین وسیله از همکاری صمیمانه کارکنان درمانگاه تالاسمی بزرگسالان ظفر و بیماران تالاسمی مراجعهکننده به درمانگاه نهایت تشکر و قدردانی را داریم. از دکتر مهدیزاده مسئول محترم درمانگاه بابت هماهنگی انجام شده، پرستاران دلسوز و متعهد درمانگاه تالاسمی خانم آزاده بیگلرپور و خانم حدیث ثابت جهت همکاری در نمونهگیری و بررسی هموگلوبین بیماران با دستگاه هموگلوبینومتر مورد مطالعه نهایت سپاسگزاری را داریم. همچنین از داوری و ارائه نقطه نظرات ارزشمند اساتید مؤسسه عالی آموزشی و پژوهشی طب انتقال خون کمال سپاس و قدردانی را داریم.
متن کامل: (221 مشاهده)
ارزیابی حساسیت و ویژگی یک دستگاه هموگلوبینومتر تولید شده توسط یک
شرکت دانش بنیان در بیماران تالاسمی
ساناز آسیابی1 ، صدیقه امینی کافیآباد2 ، امیر تیمورپور3 ،حمیدرضا قلیزاده4، سمانه علیزاده حقیقی5، محمد حسام رفیعی6
1- PhD ویروسشناسی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- متخصص آسیبشناسی ـ استاد مرکز تحقیقات فرآوردههای بیولوژیک و سلامت خون ـ موسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
3- PhD آمار زیستی ـ استادیار مرکز تحقیقات فرآوردههای بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
4- کارشناس ارشد بیوشیمی بالینی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
5- کارشناس علوم آزمایشگاهی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
6- PhD بیوشیمی بالینی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
شرکت دانش بنیان در بیماران تالاسمی
1- PhD ویروسشناسی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- متخصص آسیبشناسی ـ استاد مرکز تحقیقات فرآوردههای بیولوژیک و سلامت خون ـ موسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
3- PhD آمار زیستی ـ استادیار مرکز تحقیقات فرآوردههای بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
4- کارشناس ارشد بیوشیمی بالینی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
5- کارشناس علوم آزمایشگاهی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
6- PhD بیوشیمی بالینی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران

 http://dx.doi.org/10.61186/bloodj.22.1.54 Citation: Asiyabi S, Amini-Kafiabad S, Teimourpour A, Gholizadeh H.R, Alizadeh Haghighi S, Rafiee M.H. Evaluation of the Sensitivity and Specificity of a Hemoglobinometer Device Produced by a Knowledge-Enterprise Company in Thalassemia Patients. J Iran Blood Transfus. 2025: 22 (3) : 183-195 نویسنده مسئول: دکتر محمد حسام رفیعی. استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران صندوق پستی: 1157-14665 E-mail:
کد اخلاق: IR.TMI.REC.1403.023 |
چکیده سابقه و هدف اندازهگیری دقیق هموگلوبین در بیماران تالاسمی نقش حیاتی در مدیریت درمان و پیشگیری از بروز عوارض دارد. دستگاههای هموگلوبینومتر به دلیل دقت بالا، سرعت و سهولت عملکرد، ابزارهای مناسبی برای پایش سطح هموگلوبین هستند. این مطالعه با هدف ارزیابی عملکرد یک دستگاه هموگلوبینومتر ساخت یک شرکت دانش بنیان به بررسی کارآیی آن در اندازهگیری هموگلوبین در مقایسه با دستگاه مرجع میپردازد. مواد و روشها در این مطالعه مقطعی، هموگلوبین 83 بیمار تالاسمی مراجعهکننده به درمانگاه تالاسمی با هموگلوبینومتر و دستگاه مرجع (Sysmex XP-300) اندازهگیری شد. تحلیلهای آماری شامل ارزیابی حساسیت، ویژگی، ارزش اخباری مثبت/منفی، نمودار Bland-Altman ، شاخص همبستگی درون طبقهای (ICC) و منحنی ROC انجام شد. یافتهها میانگین هموگلوبین اندازهگیری شده توسط هموگلوبینومتر g/dL 40/1 ± 65/9 با میانه g/dL 70/9 بود. تحلیلها نشان داد همبستگی قوی بین دو دستگاه (] 98/0- 94/0[ CI %95 ، 96/0 % ICC=) و عدم اختلاف معنادار در تحلیل Bland- Altman وجود دارد و ضریب تعیین60/92% میباشد. حساسیت (90/83 %)، ویژگی (30/96 %)، ارزش اخباری مثبت (90/97 %)، ارزش اخباری منفی (30/74 %)، دقت کلی (90/87 %)، ضریب کاپا (50/74 %) و بر اساس منحنی ROC ، Cut-off معادل 30/10 محاسبه شد. نتیجه گیری نتایج هموگلوبینومتر در تشخیص موارد مثبت از دقت بالایی برخوردار بود (90/97 % =PPV). به طوری که در 48 مورد مثبت شناسایی شده تنها یک مورد مثبت کاذب گزارش شد. این ویژگی میتواند نشاندهنده قابلیت اعتماد بالای دستگاه در شناسایی بیماران تالاسمی نیازمند خون باشد. از طرفی از 35 مورد منفی شناسایی شده توسط این دستگاه، 9 مورد منفی کاذب گزارش شد (30/74 % = NPV) که بیانگر ضرورت بررسی مجدد نتایج منفی با یک دستگاه مرجع یا سایر روشهای تشخیصی بررسی میباشد. کلمات کلیدی: هموگلوبینها، تالاسمی، واکنشهای مثبت کاذب، واکنشهای منفی کاذب |
مقدمه
بیماری تالاسمی که به علت اختلال ژنتیکی غیر طبیعی در زنجیره گلوبولین میباشد، میتواند منجر به ایجاد اختلالات شدید از جمله بتا تالاسمی هموزیگوت، بتا تالاسمی Hb E و هیدروپس جنینی Hb Bart در بیماران گردد (1). علیرغم این که کم خونی میکروسیتیک بیانگر طیف وسیعی از بیماریها میباشد، این نوع کم خونی میتواند به عنوان یکی از علائم اولیه در بیماران تالاسمی مطرح باشد، بنابراین اندازهگیری دقیق هموگلوبین در تمایز بین بیماران تالاسمی و سایر شرایط مانند کم خونی فقر آهن میتواند کمککننده باشد (2، 1).
در بیماران تالاسمی و به ویژه بیماران وابسته به تزریق خون (TDT : Transfusion-Dependent Thalassemia)، که دارای شرایط بالینی سختی هستند، تزریق گلبول قرمز برای حفظ سطح هموگلوبین توصیه میگردد (3). یکی از روشهای اندازهگیری هموگلوبین استفاده از دستگاههای هموگلوبینومتر میباشد که از مزایای عمده آنها میتوان به موارد زیر اشاره نمــود (5، 4):
- علیرغم این که جزو روشهای تهاجمی برای آزمایش هموگلوبین محسوب شده اما به دلیل عدم نیاز به خونگیری معمول وریدی و کاهش خطرات زیستی، امکان استفاده از نمونه خون مویرگی با حداقل درد را فراهم میکند (7، 6).
- هموگلوبینومترها مقرون به صرفه هستند و نتایج را در کمتر از یک دقیقه ارائه میدهندکه این امر در نظارت مستمر بیماران تالاسمی جهت تصمیمات بالینی فوری جهت تزریق خون و یا سایر مداخلات پزشکی تأثیرگذار است (8، 6).
- در مدیریت بیماران تالاسمی هدف از به کارگیری هموگلوبینومترها، نظارت مستمر در بیماران نیازمند به تزریق خون و پایش پاسخ به درمان در جهت رسیدن سطح هموگلوبین به حد مطلوب میباشد. این دستگاهها میتوانند با ارائه نتایج دقیق و سریع در بهبود کیفیت زندگی بیماران تالاسمی تاثیرگذار باشند.
مواد و روشها
طراحی مطالعه و جمعیت مورد مطالعه:
در این مطالعه مقطعی، یک دستگاه هموگلوبینومتر تولید شده توسط یک شرکت دانش بنیان در مقایسه با یک دستگاه مرجعXP -300 TM Automated Haematology Analyser در اندازهگیری غلظت هموگلوبین در بیماران تالاسمی مورد ارزیابی قرار گرفت. دادههای مورد استفاده در این مطالعه مربوط به بیماران تالاسمی مراجعهکننده به درمانگاه تالاسمی بزرگسالان ظفر در تهران در محدوده زمانی آذر ماه تا اسفند ماه سال 1402 بود. تعداد افراد شرکتکننده در مطالعه 83 نفر (33 نفر آقا و 50 نفر خانم) بودند.
جمعآوری نمونه و انجام آزمایش:
1- نوع نمونه: در این مطالعه، نمونه خون وریدی بیماران تالاسمی برای اندازهگیری غلظت هموگلوبین با دستگاه مرجع و دستگاه هموگلوبینومتر مورد ارزیابی قرار گرفت. به منظور جلوگیری از مداخلـه اضـافه نسـبت بـه شـرایط روتـین اخـذ نمونـه از بیماران تالاسمی، نمونه خون مویرگی جهــت اندازهگیری هموگلــوبین گرفته نشد. بنابراین نمونهگیری از بیماران مطابق با دستورالعمل روش نمونهگیری در درمانگاه تالاسمی انجام شد.
2- شرایط انجام آزمایش: نیاز بـه شـرایط پـره آنـالایتیکی خاصی برای انجام آزمـایش نمـیباشـد. لولـههـا تـا زمـان سنجش در دمای 2 تا 8 درجه سانتیگراد نگهداری و انجام آزمایش بلافاصله بعد از نمونهگیری از بیماران تالاسمی انجـام شد. کارکنان درمانگاه تالاسمی که در این پژوهش همکاری داشتند، برای تمامی مراحل انجام سنجش هموگلوبین با روش مرجـع و فرآیندهای مرتبط بـا آن طبق استانداردهای انتقال خـون و دستورالعملهای مصوب در این زمینه آموزش دیدهانـد و بخشی از کار روتین آنها بوده است. درخصـوص دستگاه هموگلوبینومتر مورد ارزیابی نیز قبل از استفاده و مطابق با بروشور دستگاه، به صـورت محـدود برای کارکنان مدنظر آموزش لازم انجـام شـده بـود.
3- حجم نمونه مورد استفاده در این مطالعه بـرای ارزیـابی
کنترل کیفی: حداقل حجم نمونه مورد نیاز برای برآورد میزان توافق بین نتایج دو دستگاه براساس شاخص ضریب همبستگی درون طبقهای (شاخص ICC) و استفاده از پکیجICC.Sample.Size ؛ از نرمافزار آماری آر یا R نسخه 4.4.1 برای تحلیل دادههای آماری استفاده شد. در نظر گرفتن سطح معناداری 05/0 و توان 95 درصد و مقدار توافق مورد نظر 80 درصد برابر حداقل توافق مورد نظر 60 درصد با حداقل 81 نمونه محاسبه گردید. بدین منظور در این مطالعه، اندازهگیری مقایسهای غلظت هموگلوبین با دو دستگاه بر روی 83 بیمار تالاسمی مراجعهکننده به درمانگاه انجام شد.
دستگاههای تحت مطالعه
1-دستگاه هموگلوبینومتر تولید شده توسط یک شرکت دانش بنیان:
اساس کار: از میکروکووتهای طراحی شده استاندارد جهت جمعآوری 2-3 قطره خون استفاده شد و بلافاصله برای تجزیه و تحلیل در دستگاه قرار داده شد. این میکروکووتها حاوی سدیم دیاکسیکولات هستند که غشای گلبولهای قرمز را متلاشی میکند و Hb را آزاد مینماید. سپس نیترات سدیم، آهن هموگلوبین را از آهن دو ظرفیتی به فرم سه ظرفیتی تبدیل و مت هموگلوبین تشکیل میگردد، مت هموگلوبین با آزید ترکیب میشود و آزیدمت هموگلوبین را تشکیل میدهد. سپس این ترکیب توسط اسپکتروفتومتر در طول موج 540 نانومتر اندازهگیری میشود. کالیبراسیون دستگاه هموگلوبینومتر به صورت خودکار انجام میشود و اگر در بررسیهای دورهای تفاوت معناداری در نتایج مشاهده شود، میتوان از فرآیند کالیبراسیون دستی استفاده کرد، بدین ترتیب که ابتدا با میکروکووت خالی و سپس با میکروکووت پر شده با کالیبراتور، کالیبراسیون تکمیل میگردد. برای ارزیابی دقت و صحت دستگاه، کنترل کیفی روزانه انجام نمیشود و طبق بروشور دستگاه نیازی به استفاده از خون کنترل نمیباشد، ولی طبق پیشنهاد شرکت سازنده، یک محلول کنترلی که توسط شرکت تهیه شده است را میتوان به صورت ماهانه توسط بخش کنترل کیفی به دستگاه داد و عددی که باید قرائت شود در محدوده 5/0 ± 12 است.
ارزیابی مستندات:
بـر اسـاس تاییدیـه ارائـه شـده که مبتنی بر مشخصات
نمونه تحت آزمون و مشخصات پذیرش نمونه میباشد، نتایج دستگاه آنالیزور هموگلوبین با استاندارد I EC 61010-2-101 (International Electrotechnical Commission) مطابقت دارد.
گواهینامـه بینالمللـــی از KASCERT با شماره ISO
12485:2016 (تجهیزات پزشکی- سیستم مدیریت کیفیت)
مطابق با استانداردهای بینالمللی ارائه شده است.
پروانه تولید وسیله پزشکی به شماره 53612149 در مورخ 30/08/1402 از اداره کل تجهیزات پزشکی تحت نظارت سازمان غذا و دارو ایران (IFDA : Iranian Food and Drug Administration)، توسط شرکت ارائه شده است.
گواهینامه به شماره LQF-708-02-01 از شرکت دانش بنیان آزمایشگاههای صنایع انرژی (E.P.I.L : Energy and power Industries Laboratories Co) که مورد تائید سازمان ملی استاندارد، شرکت توانیر، سازمان غذا و دارو و غیره میباشد، ارایه شده است.
از ویژگیهای عملکردی دستگاه هموگلوبینومتر میتوان به آزمون خطی بودن و بررسی دقت دستگاه اشاره نمود.
- آزمون خطی بودن، بیانگر رابطه خطی میان نتایج اندازهگیری شده با خون کنترل شرکت روز آزمون (مقادیر کم، طبیعی و بالای هموگلوبین) میباشد. در مستندات ارائه شده رابطه خطی بر اساس فرمول شیب غلظت 61/0 + x97/0 y= بین نتایج با مقدار 99/0 R2= مشاهده گردید.
- در بررسی دقت دستگاه، از نظر آماری انحراف معیار (SD) و ضریب تغییرات (CV) میانگین سه غلظت مختلف هموگلوبین (2/9، 9/12و 2/16) به ترتیب با مقادیر کم، طبیعی و بالا بر حسب واحد گرم بر دسیلیتر با حجم نمونه 75 عدد برای هر غلظت به طور مجزا بررسی شده بود.
2- دستگاه مرجع (Sysmex XP-300TM Automated Haematology Analyser):
دستگاه مذکور برای بررسی هموگلوبین خون وریدی در این مطالعه مورد استفاده قرار گرفته است. دستگاه فوق ساخت کشور ژاپن میباشد.
اساس کار: از خون وریدی جهت اندازهگیری هموگلوبین استفاده میشود. در این سیستم از سدیم لوریل سولفات برای تبدیل Hb به یک ترکیب رنگی استفاده میکند که توسط اسپکتروفتومتر خودکار اندازهگیری میشود.
کالیبراسیون دستگاه: کنترل کیفی و کالیبراسیـون دستگـاه
طبق کاتالوگ و دستورالعمل مصوب در مرکز تالاسمی انجام شد (9).
جمعآوری دادهها و تجزیه و تحلیلهای آماری:
دادههای خوانش هموگلوبین با هر دو دستگاه (مرجع و هموگلوبینومتر) جمعآوری و در نرمافزار اکسل وارد شدند. برای مقایسه دقت خوانشها، شاخصهای توصیفی آماری (میانگین، انحراف معیار، میانه و ضریب تغییرات) محاسبه گردید. برای مقایسه عملکرد دو دستگاه، شاخصهایی شامل حساسیت، ویژگی، ارزش اخباری مثبت (PPV) و ارزش اخباری منفی (NPV) و ضریب توافق کاپا محاسبه شد. ارزیابی توافق با رگراسیون خطی و تحلیل توافق با ضریب همبستگی درون طبقهای (ICC : Infraclass Correlation Coefficient) و نمودار Bland –Altman انجام شد. کلیه تحلیلها در نرمافزار آماری R نسخه 4.4.1 اجرا گردید.
تعاریف آماری مطالعه:
تعیین حد آستانه یا تصمیم گیری (Cut off):
در افراد مبتلا به سندرم تالاسمی که وابسته به تزریق خون هستند، تزریق گلبول قرمز برای حفظ سطح هموگلوبین با شرط این نکته که میزان هموگلوبین قبل از تزریق بین 5/9 تا 5/10 گرم در دسیلیتر باید باشد، در نظر گرفته میشود (10، 3). با در نظر گرفتن حد آستانه تعریف شده و تجزیه و تحلیل آماری منحنی ROC در این مطالعه، Cut off برابر با 3/10 برای محاسبه حساسیت، ویژگی، ارزش اخباری مثبت و ارزش اخباری منفی تعریف گردید.
مثبت واقعی (TP) :
مواردی که میزان غلظت هموگلوبین در دستگاه مرجع و هموگلوبینومتر پایینتر از 3/10 گرم در دسیلیتر میباشد.
مثبت کاذب (FP) :
مواردی که میزان غلظت هموگلوبین کمتر از 3/10 گرم در دسیلیتر با دستگاه هموگلوبینومتر و غلظت بالاتر از 10 گرم در دسیلیتر با روش مرجع محاسبه شده است.
منفی واقعی (TN) :
مواردی که میزان غلظت هموگلوبین با دستگاه مرجع و هموگلوبینومتر بالاتر از 3/10 گرم در دسیلیتر میباشد.
منفی کاذب (FN) :
مواردی که میزان غلظت هموگلوبین بیشتر از 10 گرم در دسیلیتر با دستگاه هموگلوبینومتر و کمتر از 3/10 گرم در دسیلیتر با روش مرجع محاسبه شده است.
حساسیت:
تعداد موارد مثبت واقعی شناسایی شده توسط دستگاه تقسیم بر مجموع موارد مثبت واقعی و منفی کاذب درصد (11، 9) (جدول 1).
ویژگی:
تعداد موارد منفی واقعی شناسایی شده توسط دستگاه بر مجموع موارد منفی واقعی و مثبت کاذب در صد (11، 9)(جدول 1).
 ارزش اخباری مثبت (PPV) :
ارزش اخباری مثبت (PPV) :تعداد موارد مثبت واقعی شناسایی شده توسط دستگاه تقسیم بر مجموع موارد مثبت واقعی و کاذب در صد (11، 9)(جدول 1).
ارزش اخباری منفی (NPV) :
تعداد موارد منفی واقعی شناسایی شده توسط دستگاه بر مجموع موارد منفی واقعی و کاذب در صد (11، 9)(جدول 1).
یافتهها
در این مطالعه ارزیابی نتایج خوانش غلظت هموگلوبین وریدی بیماران تالاسمی با در نظر گرفتن عدد 3/10 به عنوان حد تصمیمگیری (Cut off)، بین دستگاه هموگلوبینومتر تولید شده توسط شرکت دانش بنیان با دستگاه مرجع Sysmex XP-300TM Automated Haematology Analyser به شرح زیر میباشد:
با حجم نمونه 83، میانگین و انحراف معیار خوانش با دستگاه هموگلوبینومتر و دستگاه مرجع، به ترتیب 40/1 ± 65/9 و 38/1 ± 32/9 گرم بر دسیلیتر و مقدار میانه خوانش به ترتیب 70/9 و 30/9 گرم بر دسیلیتر گزارش گردید (جدول 2).
بر اساس نتایج نمودار Bland-Altman، مقایسه توافق بین دو دستگاه در خوانش، در نمودار نشان داده شده است (نمودار 1). میانگین اختلاف خوانش با فاصله اطمینان 95 درصد، برابر 33/0 و حد پایین و بالای توافق به ترتیب 42/0- و 08/1 میباشد. بنابراین با 001/0 p< از نظر
آماری اختلاف معناداری بین خوانش دو دستگاه هموگلوبینومتر و مرجع، وجود دارد، اما این اختلاف در محدوده قابل قبول برای کاربرد مورد نظر قرار دارد و از نظر عملی تاثیر قابل توجهی در روند کاری ندارد و دو دستگاه از نظر خوانش هموگلوبین با یکدیگر توافق و همخوانی داشتهاند. شاخص ICC، بین دستگاه هموگلوبینومتر و دستگاه مرجع عدد 96/0 درصد با فاصله اطمینان 95% محاسبه شد (98/0 – 94/0= CI %95 ، %96 ICC=)(جدول 2). برای بررسی همبستگی بین دو دستگاه، نمودار رگرسیون خطی مورد بررسی قرار گرفت (نمودار 2). بر اساس نمودار 2 ضریب تعیین (R2) دو دستگاه معادل 60/92 % گزارش شد، با توجه به ضریب تعیین محاسبه شده از نظر آماری در سطح 05/0 معنادار نمیباشد (جداول 2 و 3)، اما با ضریب رگرسیون با عدد 0/1 اختلاف معنادار نداشته و از طرفی خط رگرسیون به خط 45 درجه نزدیک است، بنابراین توافق مطلوب مورد نظر را میرساند.
حساسیت دستگاه هموگلوبینومتر در مقایسه با دستگاه مرجع 90/83 درصد با فاصله اطمینان 95% ( 50/93- 30/74)، ویژگی دستگاه 30/96 درصد با فاصله اطمینان %95 (30/99- 70/81) گزارش گردید. همچنین ارزش اخباری مثبت دستگاه 90/97 درصد با فاصله اطمینان 95% (60/99- 10/89) و ارزش اخباری منفی 30/74 درصد با فاصله اطمینان (80/88- 80/59) محاسبه شد. صحت دستگاه هموگلوبینومتر به صورت خام (Crude Accuracy)، 90/87 درصد با فاصله اطمینان 95% (90/94- 90/80) و ضریب کاپا، 50/74 با فاصله اطمینان 95 % (0/89- 0/60) گزارش گردید (جدول 4).



بحث
مطالعه حال حاضر نشان داد دستگاه مورد بررسی با حساسیت 90/83 درصد و ویژگی 30/96 درصد از دقت تشخیصی مطلوبی برای شناسایی کم خونی در بیماران تالاسمی برخوردار است (صحت دستگاه: 90/87 درصد).
در مطالعهای صحت و دقت دستگاههای هموگلوبینومتر در مقایسه با دستگاههای مرجع هماتولوژی برای اندازهگیری هموگلوبین در محیطهای آزمایشگاهی در افراد سالم و بیماران دارای ناهنجاریهای مرتبط با ساختار هموگلوبین به اشکال خفیف تا شدید تأیید شده است، به طوری که کمترین میزان خطا و بیشترین توافق در دادههای آماری مشاهده شده است (23). در یک مطالعه که توسط مایوری و همکارانش در ارتباط با صحت تشخیصی یک دستگاه هموگلوبینومتر در مقایسه با روش مرجع سیانومت هموگلوبین انجام شده است، صحت دستگاه را با بررسی حساسیت و ویژگی بالای 80 درصد با کمترین میزان خطا با روش مرجع نشان دادهاند (24). حساسیت و ویژگی بالای دستگاههای هموگلوبینومتر، تأکیدی بر عملکرد بالینی سریع در شرایطی که تشخیص فوری از الزامات مهم در شناسایی کم خونی در بیماران به ویژه بیماران تالاسمی نیازمند دریافت خون است، میباشد. در مطالعه حال حاضر، میانگین و میانه خوانش هموگلوبین وریدی در بیماران تالاسمی با دستگاه هموگلوبینومتر به ترتیب 65/9 و 70/9 در مقایسه با هموگلوبین اندازهگیری شده از خون وریدی با دستگاه مرجع Sysmex XP-300 TM Automated Haematology Analyser، 32/9 و 30/9 گزارش گردید. میانگین و میانه محاسبه شده با دستگاه هموگلوبینومتر در مقایسه با دستگاه مرجع بالاتر گزارش شده است، اگر چه این میزان خوانش با 001/0 p< از نظر آماری معنادار میباشد، ولی در واقعیت این تفاوت بسیار کم بوده و در محدوده قابل قبولی در کاربردهای بالینی میباشد. در یک مطالعه که مقایسه سه روش اندازهگیری هموگلوبین بر روی نمونههای خون اهداکنندگان مورد بررسی قرار گرفته است، میانگین خوانش با دستگاه هموگلوبینومتر (Compolab TS)، دستگاه Cell counter و روش قدیمی سیانومت هموگلوبین به ترتیب 17/15، 95/14 و 09/15 (میانه به ترتیب 20/15، 0/15 و 0/15) گزارش شده است. در اندازهگیری هموگلوبین با دستگاه Compolab و Cell counter توافق خوبی نشان داده شد، ولی با روش سیانو مت هموگلوبین این توافق کمتر بود (25). با مقایسه نتایج بین دو مطالعه میتوان به این نکته اشاره کرد که در دستگاههایی که برای اندازهگیری هموگلوبین از خون وریدی استفاده میشود، به دلیل تفاوت خون شریانی در وریدها در مقایسه با مویرگها این اختـلاف خوانـش پایینتـر در وریدها توجیـهپذیـر میباشد (26).
در این مطالعه با توجه به نتایج حاصل از تفسیر نمودار Bland-Altman، میانگین اختلاف خوانش با فاصله اطمینان 95 درصد، برابر 33/0 و حد پایین و بالای توافق به ترتیب 42/0- و 08/1 میباشد. بنابراین با 001/0 p< از نظر آماری اختلاف معناداری بین خوانش دو دستگاه هموگلوبینومتر و مرجع وجود دارد، اما این اختلاف در محدوده قابل قبول برای هدف مورد نظر قرار دارد و بین دو دستگاه توافق دیده شد. نتایج حاصل از این میزان اختلاف در خوانش بین دو دستگاه هموگلوبینومتر و مرجع در مطالعههای مشابه نیز نشان داده است (25). از این رو میتوان نتیجه گرفت که دستگاههای هموگلوبینومتر در مقایسه با دستگاههای مرجع در ارزیابی غلظت هموگلوبین از توافق خوبی برخوردار میباشند. همچنین در بررسی ضریب همبستگی (ICC) دستگاه هموگلوبینومتر مورد مطالعه، توافق بسیار خوبی بین دو دستگاه مشاهده گردید (98/0- 94/0= CI 95/0 ، 96/0= ICC). بر اساس نمودار رگرسیون خطی 60/92 = R2 ، توافق مطلوب حاصل شد. همچنین در این پژوهش ارزش اخباری مثبت (PPV) و منفی (NPV) دستگاه هموگلوبینومتر به ترتیب 90/97 و 30/74 محاسبه شد. این نتایج در مقایسه با یک مطالعه در سال 2019، که PPV و NPV را به ترتیب 60/82% و 80/75 % گزارش کرده بود و بیانگر دقت تشخیصی مطلوبی در موارد مثبت می باشد، همسو است (7). در مطالعه حال حاضر، ارزش اخباری مثبت گزارش شده با 90/97 درصد بیانگر این مطلب است که از 47 مورد مثبت گزارش شده، فقط یک مورد مثبت کاذب می باشد و در ارتباط با ارزش اخباری منفی گزارش شده با عدد 30/74% نشاندهنده این است که از 26 مورد منفی گزارش شده، 9 مورد به طور کاذب منفی گزارش شده است (مطابق با جدول 4). علت این موارد منفی کاذب میتواند تحت تاثیر عوامل مختلفی از جمله جهشهای ژنی خاموش و یا خفیف در بعضی افراد مبتلا به تالاسمی، نوع نمونه و روشهای جمعآوری آن، محدودیتهای دستگاههای هموگلوبینومتر و عوامل محیطی، نمونههایی با همولیز خفیف و سایر شرایط مداخلهگر (کمبود آهن، کمبود اسید فولیک و برخی از انواع هموگلوبینها)، باشد (30-27، 22). در تفسیر نتایج گزارش شده در ارتباط با دستگاه هموگلوبینومتر به این نتیجه میرسیم که میتوان به تزریق خون در ارتباط با نتایج مثبت گزارش شده در بیماران تالاسمی اعتماد کرد، ولی در ارتباط با موارد منفی نیاز به بررسی بیشتر با دستگاه مرجع و یا روشهای دیگر تشخیصی در بیماران جهت تزریق خون میباشد. از آن جایی که بررسی آماری PPV و NPV در بالین حائز اهمیت است و در تصمیمگیری پزشکان در تزریق خون به بیماران تالاسمی نیازمند به دریافت خون تاثیرگذار میباشد، بررسی تجزیه و تحلیل آماری موارد مثبت و منفی واقعی با دستگاههایی که مرتبط با اندازهگیری هموگلوبین هستند از اهمیت بالایی برخوردار میباشد.
در ارزیابی هموگلوبین با استفاده از هموگلوبینومتر با استفاده از تجزیه و تحلیل ROC میتوان صحت دستگاه را در اندازهگیری غلظت هموگلوبین تعیین نمود (31). در این مطالعه، در بررسی صحت دستگاه هموگلوبینومتر با دستگاه مرجع با استفاده از منحنی ROC، میتوان به این نتیجه رسید که AUC با عدد 30/97 درصد بیانگر صحت بالای دستگاه مورد مطالعه میباشد. بهترین Cut-off برای دستگاه هموگلوبینومتر 30/10 است. همچنین در یک مطالعه از تجزیه و تحلیل منحنی ROC، برای مقایسه عملکرد دستگاه Hemocue (دستگاه هموگلوبینومتر) با دستگاه مرجع Automated Haematology Analyser استفاده شده است، و بنابر نتایج مشخص شد که هر دو دستگاه با AUC بالای 10 دارای صحت تشخیصی بالایی میباشند (31). از تجزیه و تحلیل منحنی ROC به عنوان یک ابزار قدرتمند در ارزیابی عملکرد تشخیصی آزمایشهای شاخص (آزمایشهایی که برای تشخیص یک بیماری یا شرایطی خاص به کار گرفته میشوند) استفاده میگردد. از طرفی دیگر AUC (سطح زیر منحنی ROC)، توانایی تمایز بین افراد بیمار و غیر بیمار را دارد و در تفسیر AUC حتماً باید فاصله اطمینان 95 درصد در نظر گرفته شود (14).
مزایای استفاده از دستگاههای هموگلوبینومتر علاوه بر امتیازاتی از جمله سادگی در نحوه اندازهگیری هموگلوبین، قابل حمل بودن، کالیبراسیون اتوماتیک و قابلیت استفاده در شرایط محدود آزمایشگاهی که دارند، با بررسی مطالعههای مقایسهای صورت گرفته از نظر ایندکسهای آماری، نزدیکترین نتایج را با روشهای مرجع دارا میباشند. بنابراین با رعایت دستورالعملهای استاندارد مرتبط با دستگاههای هموگلوبینومتر، ارائه آموزش کافی به کاربران و حصول اطمینان از کنترل کیفی دقیق، میتوان خطاهای احتمالی اندازهگیری هموگلوبین را با دستگاههـای هموگلوبینومتر به حداقل رساند (23).
نتیجهگیری
با توجه به نتایج این مطالعه، هموگلوبینومتر، در تشخیص موارد مثبت (90/97% = PPV) از دقت بالایی برخوردار است، زیرا از 47 مورد مثبت تنها یک مثبت کاذب داشت. بنابراین برای شناسایی بیماران تالاسمی نیازمند خون قابل اعتماد میباشد. ولی در موارد منفی (30/74 %= NPV) از 26 مورد، 9 مورد منفی کاذب گزارش شده است؛ توصیه میگردد نتایج با یک دستگاه مرجع یا سایر روشهای تشخیصی بررسی گردند.
محدودیتهای مطالعه:
علیرغم مزایای دستگاههای هموگلوبینومتر توجه به این نکته حائز اهمیت است که استفاده از دستگاههای هموگلوبینومتر در مواردی همانند تالاسمی بینابینی یا ماژور، ممکن است نیاز به تایید نتایج با روشهای دقیقتر مانند الکتروفورز هموگلوبین باشد. از طرفی دیگر در مواردی که میزان حجم متوسط گلبول قرمز (MCV) و غلظت متوسط هموگلوبین در گلبول قرمز (MCHC) هم در کم خونی فقر آهن و هم در تالاسمی مینور مشاهده میشود، باعث میشود که گاهی اوقات افتراق این دو بیماری از هم، به ویژه با روشهای ساده اندازهگیری هموگلوبین مانند دستگاههای هموگلوبینومتر دشوار باشد. زیرا این روش فقط عدد هموگلوبین کل را نشان میدهد و در مورد سایر شاخصهای خونی مانند MCV، MCHC و.... اطلاعات کافی را نشان نمیدهد.
حمایت مالی
مطالعه حاضر بدون حمایت مالی مرکز یا ارگان خاصی
انجام شده است.
ملاحظات اخلاقی
مطالعه فوق دارای کد اخلاق IR.TMI.REC.1403.023 از کمیته اخلاق مؤسسه عالی آموزشی و پژوهشی طب انتقال خون تهران، ایران است.
عدم تعارض منافع
نویسندگان مطالعه اظهار میکنند، هیچگونه تعارض منافعی در این پژوهش وجود نداشته است.
نقش نویسندگان
دکتر محمدحسام رفیعی: طراحی مطالعه، نگارش و ویرایش مقاله، جمعآوری و راستی آزمایی اطلاعات، تجزیه و تحلیل آماری و آمادهسازی جداول آماری
دکتر صدیقه امینی کافیآباد: طراحی مطالعه، ویرایش مقاله، راستی آزمایی اطلاعات
دکتر ساناز آسیابی: نگارش و ویرایش مقاله، جمعآوری و راستیآزمایی اطلاعات، تجزیه و تحلیل آماری و آمادهسازی جداول آماری
دکتر امیر تیمورپور: مشاور آماری در تجزیه و تحلیل آمار و نتایج
حمیدرضا قلیزاده: جمعآوری و راستیآزمایی اطلاعات
سمانه علیزاده حقیقی: کارشناس انجام آزمایشها در درمانگاه تالاسمی بزرگسالان ظفر
تشکر و قدردانی
بدین وسیله از همکاری صمیمانه کارکنان درمانگاه تالاسمی بزرگسالان ظفر و بیماران تالاسمی مراجعهکننده به درمانگاه نهایت تشکر و قدردانی را داریم. از دکتر مهدیزاده مسئول محترم درمانگاه بابت هماهنگی انجام شده، پرستاران دلسوز و متعهد درمانگاه تالاسمی خانم آزاده بیگلرپور و خانم حدیث ثابت جهت همکاری در نمونهگیری و بررسی هموگلوبین بیماران با دستگاه هموگلوبینومتر مورد مطالعه نهایت سپاسگزاری را داریم. همچنین از داوری و ارائه نقطه نظرات ارزشمند اساتید مؤسسه عالی آموزشی و پژوهشی طب انتقال خون کمال سپاس و قدردانی را داریم.
فهرست منابع
1. Munkongdee T, Chen P, Winichagoon P, Fucharoen S, Paiboonsukwong K. Update in laboratory diagnosis of thalassemia. Front Mol Biosci 2020; 7: 74. [DOI:10.3389/fmolb.2020.00074] [PMID] []
2. Lee YK, Kim HJ, Lee K, Park SH, Song SH, Seong M-W, et al. Recent progress in laboratory diagnosis of thalassemia and hemoglobinopathy: a study by the Korean Red Blood Cell Disorder Working Party of the Korean Society of Hematology. Blood Res 2019; 54(1): 17-22. [DOI:10.5045/br.2019.54.1.17] [PMID] []
3. Farmakis D, Porter J, Taher A, Cappellini MD, Angastiniotis M, Eleftheriou A. 2021 Thalassaemia International Federation guidelines for the management of transfusion-dependent thalassemia. Hemasphere 2022; 6(8): e732. [DOI:10.1097/HS9.0000000000000732] [PMID] []
4. Karakochuk CD, Hess SY, Moorthy D, Namaste S, Parker ME, Rappaport AI, et al. Measurement and interpretation of hemoglobin concentration in clinical and field settings: a narrative review. Ann N Y Acad Sci 2019; 1450(1): 126-46. [DOI:10.1111/nyas.14003] [PMID]
5. Whitehead Jr RD, Mei Z, Mapango C, Jefferds MED. Methods and analyzers for hemoglobin measurement in clinical laboratories and field settings. Ann N Y Acad Sci 2019; 1450(1): 147-71. [DOI:10.1111/nyas.14124] [PMID] []
6. Amrutha A, Sidenur B, PS B, SV S, MR NG, Rajagopal H. Estimation of hemoglobin using non-invasive portable device with spectroscopic signal application. Sci Rep 2024; 14(1): 8697. [DOI:10.1038/s41598-024-58990-z] [PMID] []
7. Toppo M, Pal DK, Gour D, Melwani V, Dubey M, Mishra A. Comparison of performance of digital Hemoglobinometer over automated hematology analyzer for hemoglobin estimation and its user-friendliness among the pregnant women in selected district hospitals of Madhya Pradesh. Indian J Community Med 2019; 44(1): 31-4. [DOI:10.4103/ijcm.IJCM_216_18] [PMID] []
8. Ranjith R, Priya S, Kaviya Dharshinti AS, Jeeva J. Non-invasive hemoglobin measurement using optical method. Heliyon 2024; 10(15): e35777. [DOI:10.1016/j.heliyon.2024.e35777] [PMID] []
9. Asiyabi S, Amini-Kafiabad S, Gholizadeh HR, Salek Moghaddam E, Abbasian A, Rafiee MH. Evaluation and diagnostic value of the Knowledge enterprise hemoglobinometer compared to the Reference method (Sysmex XT 2000i Automated Haematology Analyser) and the ComPoLab TM hemoglobinometer. J Iran Blood Transfus 2024; 21(4): 281-94. [Article in Farsi] [DOI:10.61186/bloodj.21.4.281]
10. Association Bulletin #23-02. Pretransfusion hemoglobin thresholds for choronic, non- emergent RBC transfusion in patients with beta thalassemia. AABB; 2022. Available from: https://www. aabb.org/ docs/default -source/default-document-library/ resources/ association -bulletins/ ab23-02.pdf? sfvrsn=1 f310ce5_6.
11. Rout D, Sachdev S, Marwaha N. Evaluation of new non-invasive & conventional invasive methods of hemoglobin estimation in blood donors. Indian J Med Res 2019; 149(6): 755-62. [DOI:10.4103/ijmr.IJMR_301_17] [PMID] []
12. Bland JM, Altman D. Statistical methods for assessing agreement between two methods of clinical measurement. Lancet 1986; 7(8476): 307-10. [DOI:10.1016/S0140-6736(86)90837-8]
13. Hajian- Tilaki K. Receiver operating characteristic (ROC) curve analysis for medical diagnostic test evaluation. Caspian J Intern Med 2013; 4(2): 627-35.
14. Çorbacıoğlu ŞK, Aksel G. Receiver operating characteristic curve analysis in diagnostic accuracy studies: A guide to interpreting the area under the curve value. Turk J Emerg Med 2023; 23(4): 195-8. [DOI:10.4103/tjem.tjem_182_23] [PMID] []
15. Brancaleoni V, Di Pierro E, Motta I, Cappellini M. Laboratory diagnosis of thalassemia. Int J Lab Hematol 2016; 38: 32-40. [DOI:10.1111/ijlh.12527] [PMID]
16. Cazzola M, Pootrakul P, Huebers HA, Eng M, Eschbach J, Finch CA. Erythroid marrow function in anemic patients. Blood 1987; 69(1): 296-301. [DOI:10.1182/blood.V69.1.296.bloodjournal691296] [PMID]
17. Galanello R, Origa R. Beta-thalassemia. Orphanet J Rare Dis 2012; 14(1): 33-4.
18. Danjou F, Anni F, Galanello R. Beta-thalassemia: from genotype to phenotype. Haematologica 2011; 96(11): 1573. [DOI:10.3324/haematol.2011.055962] [PMID] []
19. Weatherall DJ. The definition and epidemiology of non-transfusion-dependent thalassemia. Blood Rev 2012; 26: S3-S6. [DOI:10.1016/S0268-960X(12)70003-6] [PMID]
20. Sari DP, Wahidiyat PA, Setianingsih I, Timan IS, Gatot D, Kekalih A. Hematological parameters in individuals with beta thalassemia trait in South Sumatra, Indonesia. Anemia 2022; 2022(1): 3572986. [DOI:10.1155/2022/3572986] [PMID] []
21. Aravindan T, Dhakshayani R, Veda Senthil Velan G, Dinesh S, Sridevi S, Sembiah S, et al. Diagnostic Role of Digital Hemoglobinometer versus Automated Cell Count Analyzer as Point of Care Device for Screening Anemia in Children Aged 6 to 59 Months in a Rural Tertiary Care Hospital: A Cross-Sectional Study. Int J Current Pharm Rev Res 2025; 17(4): 364-70.
22. Chaudhary R, Dubey A, Sonker A. Techniques used for the screening of hemoglobin levels in blood donors: current insights and future directions. J Blood Med 2017; 8: 75-88. [DOI:10.2147/JBM.S103788] [PMID] []
23. Karakochuk CD, Janmohamed A, Whitfield KC, Barr SI, Vercauteren SM, Kroeun H, et al. Evaluation of two methods to measure hemoglobin concentration among women with genetic hemoglobin disorders in Cambodia: a method-comparison study. Clin Chim Acta 2015; 441: 148-55. [DOI:10.1016/j.cca.2014.12.021] [PMID]
24. Neogi SB, Sharma J, Pandey S, Zaidi N, Bhattacharya M, Kar R, et al. Diagnostic accuracy of point-of-care devices for detection of anemia in community settings in India. BMC Health Serv Res 2020; 20(1): 468. [DOI:10.1186/s12913-020-05329-9] [PMID] []
25. Meter: A Comparative Study with the Cyanmethemoglobin Method. International Journal of Pharmaceutical and Clinical Research. 2024;; 16(9); 600-604.
26. Gaddam Harikrishna JP, Araveti Y, Boddapati A. Evaluation of three hemoglobin estimation methods for screening blood donors: An experience in a south Indian Hospital. Journal of Research in Applied and Basic Medical Sciences 2022; 8(1): 1-7. [Article in Farsi] [DOI:10.52547/rabms.8.1.1]
27. Ranjan V, Rana R, Kant R, Khillan K. Comparison of Two Techniques Used for the Evaluation of Point-of-Care Methodology for Testing Hemoglobin in Blood Donors. Global Journal of Transfusion Medicine 2021; 6(2): 193-7. [DOI:10.4103/gjtm.gjtm_47_21]
28. Thilakarathne S, Jayaweera UP, Premawardhena A. Unresolved laboratory issues of the heterozygous state of β-thalassemia: a literature review. Haematologica 2023; 109(1): 23. [DOI:10.3324/haematol.2022.282667] []
29. de Jonge G, Dos Santos TL, Cruz BR, Simionatto M, Bittencourt JI, Krum EA, et al. Interference of in vitro hemolysis complete blood count. J Clin Lab Anal 2018; 32(5): e22396. [DOI:10.1002/jcla.22396] [PMID] []
30. Singha K, Sanchaisuriya K, Fucharoen G, Fucharoen S. Genetic and non-genetic factors affecting hemoglobin A2 expression in a large cohort of Thai individuals: implication for population screening for thalassemia. Am J Transl Res 2021; 13(10): 11632.
31. Kassam NA, Mwanga GA, Yusuph EL, Maundi EM, Josephat M, Kulaya NB, et al. Performance of Hb HemoCue machine compared to automated hematology analyzer for hemoglobin measurements among adult patients at Kilimanjaro Christian Medical Centre. medRxiv 2024:2024.12. 07.24318466. [DOI:10.1101/2024.12.07.24318646]
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |




