جلد 22، شماره 2 - ( تابستان 1404 )
جلد 22 شماره 2 صفحات 99-91 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Teimoori R, Sharifi Z, Pourkarim M R, Ajorloo M. Development of a TaqMan Real Time PCR Assay for Quantifying the HTLV-1 Proviral Load Using the HBZ Gene. bloodj 2025; 22 (2) :91-99
URL: http://bloodjournal.ir/article-1-1573-fa.html
URL: http://bloodjournal.ir/article-1-1573-fa.html
تیموری ریحانه، شریفی زهره، پورکریم محمودرضا، آجورلو مهدی. راه اندازی روش TaqMan Real Time PCR جهت تعیین میزان بار پرووایرال ویروس HTLV-1 با استفاده از ژن HBZ. فصلنامه پژوهشی خون. 1404; 22 (2) :91-99
استادیار مرکز تحقیقات فرآوردههای بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون
متن کامل [PDF 798 kb]
(541 دریافت)
| چکیده (HTML) (1302 مشاهده)
مقدمه
ویروس HTLV-1 (Human T-Cell Leukemia Virus-1) در سال 1980 به وسیله پوئز و همکاران از طریق بررسی لنفوسیتهای خون محیطی از یک بیمار مبتلا به لنفوم سلول T پوستی یافت شد (1). ویروسHTLV نوع ۱ و ۲ با دو بیماری، لوسمی/ لنفوم سلول T بالغین (ATL) و پاراپارسیس اسپاستیک گرمسیری (HAM/TSP) در انسان مرتبط بوده، که تقریباً ۱۰ تـا ۲۰ میلیون نفر را در سراسر جهان درگیر کرده است (3، 2). برخی از مطالعهها نشان دادهاند که این ویروس در مناطقی همچون جنوب غربی ژاپن، بخشهایی از آفریقا، آمریکای لاتین، جزایرکارائیب و در شمال شرق ایران از جمله شهرهای مشهد، سبزوار و نیشابور شیوع بالایی دارد (4). راههای انتقال ویروس شامل دریافت خون و یا فرآوردههای خونی آلوده، تماس جنسی، انتقال از مادر به کودک از طریق شیر دادن، تزریق داروهای وریدی و پیوند عضو میباشد (5). ژنوم HTLV دارای kbp 9 است که شامل ژنهای ساختاری gag ، pol و env بوده و در دو انتها به وسیله توالیهای تکراری طویل 3′ LTR (Long terminal repeat) و LTR′۵ احاطه شده و ناحیهای موسوم به px دارد که بین ژن env و3′ LTR قرار دارد (6) .ناحیه px که نقش تنظیمکنندگی را دارد شامل p30 ، p13 ، p12 ، rex ، tax و HBZ (HTLV-1 basic leucine zipper factor) میباشد (6). ژنtax در رشته مثبت (sense) ژنوم قرار دارد و از LTR ′۵ رونویسی میشود که نقش مرکزی در رونویسی از ژن، همانندسازی ویروس و تکثیر سلولهای آلوده به ویروس را دارد (7). از آن جایی که tax بسیار ایمنزا بوده و هدف اصلی لنفوسیتهای سیتوتوکسیک است، بنابراین ویروس استراتژیهای متعددی را برای تنظیم دقیق و کاهش بیان این پروتئین به کار میبرد. یکی از این استراتژیها استفاده از پروتئین HBZ است که با مهار رشته مثبت ژنوم ویروسی، موجب کاهش تولید پروتئین tax میگردد (8). ژن HBZ از رشته منفی (antisense) کد شده و از 3′ LTR رونویسی میشود که نقش کلیدی در تداوم و پاتوژنز این ویروس دارد (8). بیان ژن HBZ سبب مهار رشته مثبت ژنوم ویروسی و کاهش تولید پروتئین tax میگردد (9). با توجه به انتقال ویروس HTLV از طریق فرآوردههای خونی آلوده، غربالگری بر روی خونهای اهدایی، در مناطقی که شیوع ویروس بالاست انجام میشود. که به طور معمول روش EIA (Enzyme Immunoassays) در ابتدا برای شناسایی آنتیبادیهای HTLV در خون استفاده شده و اگر آزمایش اولیه مثبت باشد، از تست وسترن بلات برای تایید استفاده میشود (10). وسترن بلات روشی است که پروتئینهای gag، p19، p24، p53 و rgp46 را تشخیص میدهد. در آزمایش وسترن بلات حداقل یک باند gag و یک باند envgp۴۶ باید شناسایی شود تا نتیجه HTLV مثبت تلقی گردد. در سایر الگوها، نتیجه وسترن بلات نامعلوم در نظر گرفته میشود و تشخیص صحیح عفونت را مشکل میکند، بـه همین دلیل برای کاهش پاسخهای نامعلوم، نیاز به روشهای تشخیصی با حساسیت و اختصاصیت بالا میباشد (10).
در برخی مطالعهها، زمانی که الگوهای وسترن بلات نامشخص (IND ، Indeterminate) بررسی شد، مشاهده گردید که ژنtax قابل شناسایی نبوده و دلیل حذف این ژن مشخص نبود به همین دلیل در مطالعهها تأکید شده که برای تشخیص ویروس باید بیش از یک بخش ژنوم را جستجو کرد (11). همچنین مشخص شده تعیین لود ویروس HTLV-1 در پیش آگهی ایجاد بیماریها، نتایج عفونت و پیشرفت بیماری دارای اهمیت میباشد. برای پیشبینی نتایج عفونت و پیشرفت بیماری در مطالعه حاضر آزمـایش TaqMan Real Time PCRبا هدف طراحی یک روش حساس به منظور تعیین لود ویروس HTLV-1 راهاندازی شد.
مواد و روشها
طراحی آغازگر و پروب اختصاصی:
در این پژوهش از آغازگرها و پروب مورد نظر برای ژن HBZ، که به وسیله نرمافزارهای Gene Runner و AlleleID طراحی شده بود، استفاده گردید. سپس توالی آنها در بانک اطلاعات NCBI بلاست (BLAST) گردید تا از ویژگی آغازگرها و پروب برای نواحی مکمل با ژن HBZ اطمینان حاصل شود (جدول1).
استخراج DNA از سلولهای تک هستهای خون محیطی (PBMC) و انجام آزمایش PCR :
در این مطالعه تجربی، افرادی که مورد بررسی قرار گرفتند شامل اهداکنندگان با نتیجه Reactive آزمایش غربالگری CLEIA برای ویروس HTLV-1/2 و نتیجه آزمایش تائیدی وسترن بلات مثبت بودند. این اهداکنندگان از نظر سایر ویروسهای منتقله از راه خون مانند HIV، HBV، HSV

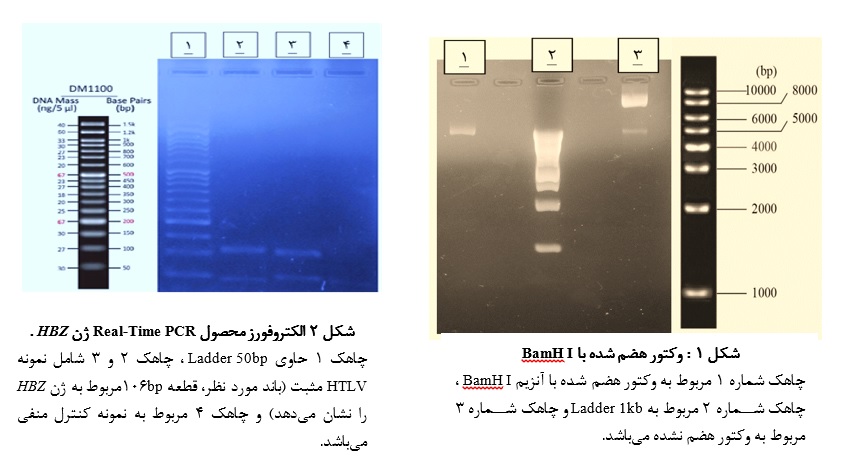
پس از بهینهسازی آزمایش TaqMan Real Time PCR، نتایج آن بر روی ژل آگارز 5/1% الکتروفورز شد (شکل 2).
راهاندازی آزمایشReal Time PCR :TaqMan probe
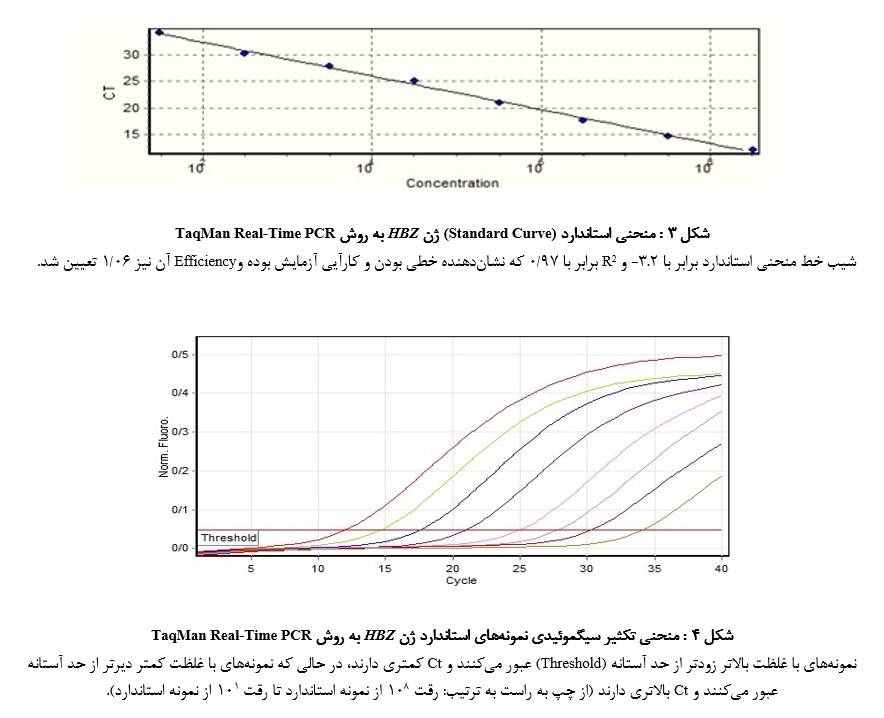
پس از تهیه رقتهای مختلف از پلاسمید خطی شده و انجام آزمایش Real Time PCR (به وسیله دستگاه Rotor Gene RG-3000)، منحنی استاندارد رسم شد. شیب خط منحنی استاندارد برابر بـا 3.2- وR2 برابر با 97/0 بود که نشاندهنده خطی بودن و کارآیی آزمایش بوده وEfficiency آن نیز 06/1 تعیین شد (اشکال 3 و 4). نتایج تکرارپذیری واکنش در سطح درون سنجی و بین سنجی بررسی و میانگین ضریب تغییرات CV نمونههای استاندارد، کمتر از 3/5 % برای اینتراسی و 9/5% برای اینترااسی بود. مشاهدات حاکی از آن بود که LOD (Limit of detection) این آزمایش برابر باCopies/µL 101× 2/1 بوده که نشاندهنده حساسیت بالای این روش میباشد. LOD این آزمایش بر اسـاس معیـارهای موجـود در راهنمـای FDA جهت اعتبار
سنجی روشهای بیوآنالیتیکی تعیین گردید (14).
بحث
ویروس HTLV عمدتاً از طریق انتقال عمودی مــادر بـه
نوزاد در دوران شیردهی، انتقال افقی، تماس جنسی و تزریق فرآوردههای سلولی حاوی این ویروس منتقل میشود (15). روشهای تشخیصی ویروس HTLV-1 عمدتاً شامل آزمایشهای سرولوژیکی هستند که به دنبال آنتیبادیهای خاص علیه آنتیژنهای مختلف HTLV-1 میگردند. آزمایشهای غربالگری معمولاً شامل الایزا (ELISA) یا آگلوتیناسیون ذرات (PA) هستند. آزمایشهای تأییدی شامل ایمونوفلورسانس (IFA) و وسترن بلات (WB) می باشد، اما عمدتاً از وسترن بلات استفاده میشود (16). با وجود برخی بهبودها در دقت آزمایش وسترن بلات طی دو دهه گذشته، همچنان الگوهای سرولوژیکی نامشخص پس از تحلیل وسترن بلات رایج هستند (17). در مقالههای متعددی از سنجش لود ویروس به عنوان یک فاکتور پیشآگهی و پایش بیماران تحت درمان نام برده شده است. بـه همین دلیل بررسی میزان لود ویروس با استفاده از ژنهایHBZ, tax, pol…. ویروس میتواند مزایای زیادی از جمله تشخیص و بررسی پیشرفت بیماریهای مرتبط با ویروس HTLV-1، ارزیابی اثربخشی درمانهای ضد ویروسی، درک بهتر از مکانیسمهای بیماریزایی ویروس و در نهایت توسعه درمانهای جدید داشته باشد (18).
در مطالعه حاضر روش Real Time PCR TaqMan برای ژن HBZ با هدف طراحی یک روش حساس به منظور تعیین پرووایرال لود ویروس HTLV-1 طراحی و راهاندازی شد. بـدین منظور در ابتدا جهت رسم منحنی استاندارد، از پلاسمید نوترکیب حاوی ژن HBZ ویروس، رقتهای لگاریتمی تهیه گردید. پس از بهینه شدن شرایط آزمایش، نتایج حاکی از آن بود کهLOD این آزمایش برابر باCopies/µL 101× 2/1 بوده که نشاندهنده حساسیت بالای این روش میباشد.
واترز و همکاران در مطالعه خود بیان کردنـد کـه آزمایش qPCR (Quantitative PCR) معتبر شده، بـه عنـوان یـک آزمایش کارآمد که قادر به اندازهگیری پرووایرال لود باشـد و همچنین قابلیت تکرارپـذیری داشـته باشـد، مـورد نیـاز است. از آن جایی که هنوز یک بیومارکر اختصاصـی بـرای پیشبینی پیشرفت بیماری در افـراد بـدون علامـت وجـود ندارد و از طرفی میزان آنتیبادی اختصاصی علیه HTLV-1 بـا پرووایـرال لـود ویـروس همبسـتگی دارد، مـیتـوان از پرووایرال لود به عنوان روشی برای پیشبینی نتایج عفونت و پیشرفت بیماری استفاده نمود (19).
مطالعهای توسط مانیکی سایتمو و همکاران، جهت بررسی میزان بیان ژن HBZ و ارتباط آن با لود ویروس HTLV انجام شد. به منظور رسم منحنیهای استاندارد برای تعیین میزان بیان ژنهای Tax و HBZ ویروس HTLV-1 ، همچنین ژن مرجع hypoxanthine guanine phosphoribosyltransferase (HPRT)، cDNA تهیهشده از سلولهای MT-2 آلوده به HTLV-1 که بهصورت سریالی رقیقسازی شده بود، استفاده شد. در این مطالعه ضریب همبستگی یا 99/0 =R2 گزارش شد (18).
مطالعهای توسط کلودیا کازولی و همکاران در سال 2014 جهت بررسی لود ویروس HTLV-1/2 انجام شد. در این مطالعه آزمونهای single-plex جداگانهای برای ژنهای 1tax- از HTLV-1 و tax-2 و pol-2 از HTLV-2 طراحی شدند تا بار پروویروسی HTLV-1 و HTLV-2 به طور کمی اندازهگیری شود. اختصاصیت آزمونهای tax-2 و pol-2 با آزمایش DNA استخراج شده از سلول 10C، که یک رده سلولی آلوده به 1HTLV- است و به عنوان کنترل منفی استفاده شد، تأیید گردید. در مورد آزمون HTLV-2 ، اختصاصیت با آزمایش سلولهای 344C که به طور پایدار به HTLV-2 آلوده هستند، بررسی شد. تعیین کمی بار پروویروسی HTLV با انجام منحنیهای استاندارد مرجع از طریق رقتسازی سریالی DNA استخراج شده از سلولهای 10C و 344 Cانجام شد، با این فرض که هر سلول 10C دارای یک ژنوم پروویروسی و هر سلول 344C دارای دو ژنوم پروویروسی است نموداری با 4/3- =Slop و 99/0 =R2 رسم شد. ژن آلبومین انسانی که دارای دو نسخه در هر سلول است، برای طبیعیسازی نتایج در همان واکنشها اندازهگیری شد (20). در اکثر مطالعههایی که مورد بررسی قرار گرفته است، جهت رسم منحنی استاندارد از رده سلولی استفاده شده بود، اما در مطالعه حاضر به دلیل عدم دسترسی به این رده سلولی، از پلاسمید نوترکیب حاوی ژن HBZ ویروس HTLV-1 جهت رسم نمودار استاندارد استفاده شد. رسم منحنی استاندارد از طریق وکتور حاوی ژن HBZ نشان داد که این روش با شیب خط برابر با 3.2- و 97/0 =R2 و حد تشخیص 101×2/1 روشی با حساسیت و اختصاصیت بالاست که نتایج آن قابل مقایسه با نتایجی است که در آن برای رسم نمودار استاندارد از رده سلولی استفاده شده است.
در سال 2019 مطالعهای به وسیله حمیده قاسمزادگان و همکاران در ایران انجام شد. این مطالعه با هدف طراحی آزمایشReal Time PCR به روش سایبرگرین جهت تعیین لود ویروس HTLV-1 با استفاده از ژن Tax راهاندازی شد. به همین منظور DNA ژنومی از سلولهای تک هستهای خون محیطی استخراج سپس محصولPCR ژن Tax درون پلاسمید pTZ57 R/T قرار گرفت و با رقتسازی، منحنی استاندارد با شیب خط 3/3= Slop و 99/0=R2 رسم شد. در این مطالعه جهت طبیعیسازی نتایج از ژن GAPDH استفاده شد (12).
مطالعه دیگری به وسیله هومین جی و همکاران در سال 2023 با هدف و توسعه و اعتبارسنجی یک آزمون TaqMan qPCR برای اندازهگیری بار پروویروسی HTLV-1 انجام شد. در این مطالعه جهت رسم منحنی استاندارد از PcDNA3.1(-)HTLV-1RPPH1 plasmid استفاده شد. ژن انسانی RPPH-1 و بخشهای pol و tax از ویروس HTLV-1 با استفاده از gDNA، سلولهای 102Hut تکثیر و استخراج شده، سپس درون وکتور pcDNA3.1(-)-Rluc- Fluc vector قرار گرفتند. رقتهای سریالی از وکتور مورد نظر جهت رسم منحنی استانـدارد تهیه و نموداری با 2/3 =slope ، 99/0=R2 و 003/103 =efficiency به دست آمد. حد تشخیص (LOD) در این مطالعه برای غلظت سلولهای 102Hut ، معادل 0218/0 % (با فاصله اطمینان 95% بین 0179/0 % تا 0298/0 %) بـه دست آمد. در این مطالعه جهت بررسی اختصاصیت این واکنش، gDNA استخراجشده از نمونههای منفی برای HTLV-1 (که شامل ۳ نمونه مبتلا به HBV ، ۳ نمونه مبتلا به HCV، ۳ نمونه مبتلا به Treponema pallidum، ۳ نمونـه مبتلا به HIV و ۱۲ نمونه افراد سالم بودند) و همچنین رده سلولهای MOT (آلوده به HTLV-2) بـا استفاده از این آزمایش مورد بررسی قرار گرفتند (102 Hut که حاوی ژنوم HTLV-1 بود بـه عنوان کنترل مثبت استفاده شد).
تمامی نمونـههای منفی برای HTLV-1 و همچنین رده سلولی MOT (آلوده به HTLV-2) ، تنها ژن 1RPPH را با این روش تکثیر دادند که نشاندهنده اختصاصیت 100% این واکنش می باشد (13).
در هر دو مطالعه مورد بررسی، همانند مطالعه حاضر از وکتور جهت رسم منحنی استاندارد استفاده شده با این تفاوت که ژن کنترل داخلی مورد استفاده در این مطالعه ERV-3 بوده، در حالی که در سایر مطالعهها از ژنهای GAPDH، RPPH1 و آلبومین به عنوان ژن مرجع استفاده شده است. همچنین اکثر مطالعهها، ژنهای Tax و pol ویروسHTLV را مورد بررسی قرار دادند اما در مطالعه حاضر ژن HBZ جهت تعیین لود ویروس مورد بررسی قرار گرفت که این وجه تمایز مطالعه حاضر با مطالعههای قبلی به شمار میرود.
مطالعههای بیشتر میتواند به درک عمیقتری از عفونتهای ویروسی و پاسخهای ایمنی مرتبط منجر شود. در همین راستا، پیشنهاد میشود ژنهایی از جمله LTR ، Env و سایر ژنهای کلیدی ویروس HTLV ، به منظور تعیین بار ویروسی و بررسی ارتباط آن با بیماریزایی، مورد
مطالعه قرار گیرند.
نتیجهگیری
این آزمایش با دارا بودن کمترین حد تشخیص (LOD) که Copies/µL 101× 2/1 در هر واکنش بود و همچنین استفاده از ژن HBZ که نقش اساسی در تنظیم فعالیتها و انـکوژنز ویروس HTLV دارد، میتوانـد به عنوان گزینه مناسبی جهت تعیین میزان لود ویروس و ارتباط آن با بیماریزایی ویروس مورد استفاده قرار گیرد.
حمایت مالی
این پروژه توسط مرکز تحقیقات انتقال خون، مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ایران تأمین مالی شده است.
ملاحظات اخلاقی
مطالعه حاضر دارای کد اخلاق IR.TMI.REC.1402.016 از کمیته اخلاق مؤسسه عالی آموزشی و پژوهشی طب انتقال خون تهران ، ایران است.
عدم تعارض منافع
نویسندگان اظهار میکنند هیچگونه تعارض منافعی در این مطالعه وجود نداشته است.
نقش نویسندگان
ریحانه تیموری: نگارش اولیه مقاله و تحلیل اطلاعات
دکتر زهره شریفی: نظارت بر اجرای طرح پژوهشی و نگارش مقاله
دکتر مهدی آجورلو: طراحی مطالعه، نظارت بر اجرای طرح و نگارش نهایی مقاله
تشکر و قدردانی
این تحقیق حاصل پایاننامه کارشناسی ارشد زیست فناوری پزشکی مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ایران میباشد. بدینوسیله نویسندگان مقاله از این مؤسسه به دلیل حمایتهای مالی، تشکر و قدردانی مینمایند.
متن کامل: (256 مشاهده)
راه اندازی روشReal Time PCR TaqManجهت تعیین میزان بار پرووایرال
ویروس HTLV-1 با استفاده از ژن HBZ
ریحانه تیموری1، زهره شریفی2 ، دکتر محمودرضا پورکریم3 ، مهدی آجورلو4
1- دانشجوی کارشناسی ارشد زیست فناوری پزشکی ـ مرکز تحقیقات فرآوردههای بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- PhD ویروسشناسی ـ استاد مرکز تحقیقات فرآورده های بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
3- PhD ویروسشناسی ـ انستیتو تحقیقاتی بالینی و آزمایشگاهی اپیدمیولوژی ویروسشناسی رگا ـ لوون ـ بلژیک
4- PhD ویروسشناسی ـ استادیار مرکز تحقیقات فرآوردههای بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
ویروس HTLV-1 با استفاده از ژن HBZ
1- دانشجوی کارشناسی ارشد زیست فناوری پزشکی ـ مرکز تحقیقات فرآوردههای بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- PhD ویروسشناسی ـ استاد مرکز تحقیقات فرآورده های بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
3- PhD ویروسشناسی ـ انستیتو تحقیقاتی بالینی و آزمایشگاهی اپیدمیولوژی ویروسشناسی رگا ـ لوون ـ بلژیک
4- PhD ویروسشناسی ـ استادیار مرکز تحقیقات فرآوردههای بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
https://doi.org/10.18502/avr.v34i2.18052 Citation: Teimoori R, Sharifi Z, Pourkarim M.R, Ajorloo M. Development of a TaqMan Real Time PCR Assay for Quantifying the HTLV-1 Proviral Load Using the HBZ Gene. J Iran Blood Transfus. 2025: 22 (2) : 91-99 نویسنده مسئول: دکتر مهدی آجورلو. استادیار مرکز تحقیقات فرآورده های بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون، تهران، ایران صندوق پستی: 1157-14665 E-mail: m.ajorloo@ibto.ir
کد اخلاق: IR.TMI.REC.1402.016 |
چکیده سابقه و هدف ویروس HTLV-1 اولین رتروویروس انکوژن انسانی است که با بیماریهای ATL و HAM/TSP مرتبط میباشد. ژن HBZ بهعنوان یکی از ژنهای کلیدی این ویروس، به دلیل ایمنیزایی پایین و پایداری ژنتیکی، نقش مهمی در پیشرفت بیماری ایفا میکند. با وجود پیشرفت روشهای تشخیصی مانند الایزا و وسترن بلات، در برخی موارد نتایج نامشخص گزارش میشود. از سوی دیگر، اندازهگیری بار ویروسی در پیشآگهی بیماری اهمیت دارد. در این مطالعه، با استفاده از روش TaqMan Real Time PCR، سیستمی حساس برای تعیین پرووایرال لود HTLV-1 بر اساس ژن HBZ طراحی و راهاندازی شد. مواد و روشها در این مطالعه تجربی، آغازگرها و پروب برای ناحیهای از ژن HBZ به طولbp 106 طراحی گردید. سپس DNA ژنومی از سلولهای تک هستهای خون محیطی یا PBMCs استخراج شد. پس از تکثیر ژن HBZ ، محصول PCR در پلاسمیدTOPO TA vector کلون گردید و از آن به عنوان استاندارد جهت راهاندازی روش TaqMan Real Time PCR استفاده شد. یافتهها برای رسم منحنی استاندارد، از پلاسمید نوترکیب رقتهای لگاریتمی 108-101× 2/1 تهیه گردید. در این آزمایش، شیب خط منحنی استاندارد برابر با 2/3- وR2 برابر با 97/0 بود که نشاندهنده خطی بودن و کارآیی آزمایش میباشد. نتایج تکرارپذیری واکنش در سطح درونسنجی و بین سنجی (در قالب سه تکرار در هر مرحله کاری) و میانگین ضریب تغییرات CV برای نمونههای استاندارد، به ترتیب کمتر از 3/5 % و 9/5 % بود. همچنین کمترین حد تشخیص این آزمایش برابر باCopies/µL 101× 2/1 بوده که نشاندهنده حساسیت بالای این روش میباشد. نتیجه گیری استفاده از روش Real Time PCR TaqMan با توجه به حساسیت بالا، آنالیز و کاربرد آسان میتواند روش مناسبی برای تعیین بار پرووایرال ویروس HTLV-1 باشد و امکان پیشآگهی دقیقتری از بروز بیماریها به واسطه این ویروس را فراهم کند. کلمات کلیدی: بار ویروسی، Real Time PCR ، HTLV-1 |
|
1- Acridine Orange
|
|
1- Biological safety cabinet
|
|
1- Platelet Concentrate
2- Food and Drug Administration 3- Normal Skin Flora 4- Platelet Rich Plasma-Platelet Concentrate 5- Eosin-Methylene blue 6- Thioglycolate |
|
1- Acridine Orange
|
|
1- Biological safety cabinet
|
|
1- Platelet Concentrate
2- Food and Drug Administration 3- Normal Skin Flora 4- Platelet Rich Plasma-Platelet Concentrate 5- Eosin-Methylene blue 6- Thioglycolate |
مقدمه
ویروس HTLV-1 (Human T-Cell Leukemia Virus-1) در سال 1980 به وسیله پوئز و همکاران از طریق بررسی لنفوسیتهای خون محیطی از یک بیمار مبتلا به لنفوم سلول T پوستی یافت شد (1). ویروسHTLV نوع ۱ و ۲ با دو بیماری، لوسمی/ لنفوم سلول T بالغین (ATL) و پاراپارسیس اسپاستیک گرمسیری (HAM/TSP) در انسان مرتبط بوده، که تقریباً ۱۰ تـا ۲۰ میلیون نفر را در سراسر جهان درگیر کرده است (3، 2). برخی از مطالعهها نشان دادهاند که این ویروس در مناطقی همچون جنوب غربی ژاپن، بخشهایی از آفریقا، آمریکای لاتین، جزایرکارائیب و در شمال شرق ایران از جمله شهرهای مشهد، سبزوار و نیشابور شیوع بالایی دارد (4). راههای انتقال ویروس شامل دریافت خون و یا فرآوردههای خونی آلوده، تماس جنسی، انتقال از مادر به کودک از طریق شیر دادن، تزریق داروهای وریدی و پیوند عضو میباشد (5). ژنوم HTLV دارای kbp 9 است که شامل ژنهای ساختاری gag ، pol و env بوده و در دو انتها به وسیله توالیهای تکراری طویل 3′ LTR (Long terminal repeat) و LTR′۵ احاطه شده و ناحیهای موسوم به px دارد که بین ژن env و3′ LTR قرار دارد (6) .ناحیه px که نقش تنظیمکنندگی را دارد شامل p30 ، p13 ، p12 ، rex ، tax و HBZ (HTLV-1 basic leucine zipper factor) میباشد (6). ژنtax در رشته مثبت (sense) ژنوم قرار دارد و از LTR ′۵ رونویسی میشود که نقش مرکزی در رونویسی از ژن، همانندسازی ویروس و تکثیر سلولهای آلوده به ویروس را دارد (7). از آن جایی که tax بسیار ایمنزا بوده و هدف اصلی لنفوسیتهای سیتوتوکسیک است، بنابراین ویروس استراتژیهای متعددی را برای تنظیم دقیق و کاهش بیان این پروتئین به کار میبرد. یکی از این استراتژیها استفاده از پروتئین HBZ است که با مهار رشته مثبت ژنوم ویروسی، موجب کاهش تولید پروتئین tax میگردد (8). ژن HBZ از رشته منفی (antisense) کد شده و از 3′ LTR رونویسی میشود که نقش کلیدی در تداوم و پاتوژنز این ویروس دارد (8). بیان ژن HBZ سبب مهار رشته مثبت ژنوم ویروسی و کاهش تولید پروتئین tax میگردد (9). با توجه به انتقال ویروس HTLV از طریق فرآوردههای خونی آلوده، غربالگری بر روی خونهای اهدایی، در مناطقی که شیوع ویروس بالاست انجام میشود. که به طور معمول روش EIA (Enzyme Immunoassays) در ابتدا برای شناسایی آنتیبادیهای HTLV در خون استفاده شده و اگر آزمایش اولیه مثبت باشد، از تست وسترن بلات برای تایید استفاده میشود (10). وسترن بلات روشی است که پروتئینهای gag، p19، p24، p53 و rgp46 را تشخیص میدهد. در آزمایش وسترن بلات حداقل یک باند gag و یک باند envgp۴۶ باید شناسایی شود تا نتیجه HTLV مثبت تلقی گردد. در سایر الگوها، نتیجه وسترن بلات نامعلوم در نظر گرفته میشود و تشخیص صحیح عفونت را مشکل میکند، بـه همین دلیل برای کاهش پاسخهای نامعلوم، نیاز به روشهای تشخیصی با حساسیت و اختصاصیت بالا میباشد (10).
در برخی مطالعهها، زمانی که الگوهای وسترن بلات نامشخص (IND ، Indeterminate) بررسی شد، مشاهده گردید که ژنtax قابل شناسایی نبوده و دلیل حذف این ژن مشخص نبود به همین دلیل در مطالعهها تأکید شده که برای تشخیص ویروس باید بیش از یک بخش ژنوم را جستجو کرد (11). همچنین مشخص شده تعیین لود ویروس HTLV-1 در پیش آگهی ایجاد بیماریها، نتایج عفونت و پیشرفت بیماری دارای اهمیت میباشد. برای پیشبینی نتایج عفونت و پیشرفت بیماری در مطالعه حاضر آزمـایش TaqMan Real Time PCRبا هدف طراحی یک روش حساس به منظور تعیین لود ویروس HTLV-1 راهاندازی شد.
مواد و روشها
طراحی آغازگر و پروب اختصاصی:
در این پژوهش از آغازگرها و پروب مورد نظر برای ژن HBZ، که به وسیله نرمافزارهای Gene Runner و AlleleID طراحی شده بود، استفاده گردید. سپس توالی آنها در بانک اطلاعات NCBI بلاست (BLAST) گردید تا از ویژگی آغازگرها و پروب برای نواحی مکمل با ژن HBZ اطمینان حاصل شود (جدول1).
استخراج DNA از سلولهای تک هستهای خون محیطی (PBMC) و انجام آزمایش PCR :
در این مطالعه تجربی، افرادی که مورد بررسی قرار گرفتند شامل اهداکنندگان با نتیجه Reactive آزمایش غربالگری CLEIA برای ویروس HTLV-1/2 و نتیجه آزمایش تائیدی وسترن بلات مثبت بودند. این اهداکنندگان از نظر سایر ویروسهای منتقله از راه خون مانند HIV، HBV، HSV

وHCV منفی بـودند. نمونـهها از فراخوان اهداکنندگان استانهای خراسان رضوی، خراسان جنوبی، خراسان شمالی، آذربایجان غربی، اردبیل، البرز و گیلان بر روی ماده ضد انعقاد EDTA تهیه گردید. سپس سلولهای تک هستهای خون محیطی به روش فایکول جدا شدند. اســتخراج DNA از سلولهای تک هستهای خون محیطی اهداکنندگان آلوده به HTLV-1 با استفاده از کیت اســتخراج DNA (شرکت یکتا تجهیز آزما - ایران) انجام شـد. سپس آزمایش PCR بر روی نمونههای مثبت جهت اطمینان از حضور ژن HBZبا استفاده از Master mix 2X (آمپلیکون، آلمان)(10 میکرولیتر)، آغازگرها (5/0 میکرولیتر از هر کدام) و DNA استخراج شده (2 میکرولیتر) در حجم نهایی 20 میکرولیتر، در چرخه دمایی مشخص انجام شد (جدول 2). سپس محصول PCR جهت تعیین توالی همراه بـا آغازگر جلوبرنده ژن HBZ به شرکت زیست فناوری پیشگام فرستاده شد.
کلونینگ محصول PCR :
محصول PCR ژن HBZ به وسیله کیت TOPO TA Cloning Kit (آمریکا، اینویتروژن) درون وکتور TOPO TA (PCR 2.1 TOPO) قرار گرفت و صحت کلونینگ با colony PCR سنجیده شد. پلاسمید نوترکیب به وسیله کیت رُوش (آلمان) استخراج و در ژل آگارز 1% الکتروفورز شد. سپس پلاسمید نوترکیب به وسیله آنزیمBamH I ، خطی شده و تعداد کپی آن بر اساس فرمول زیر محاسبه شد:
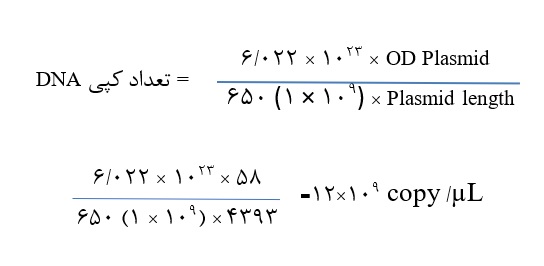
بهینهسازی و راهاندازی آزمایش TaqMan Real Time PCR:
بـا توجـه بـه دستـورالعمــل مسترمیکس (Ampliqon:
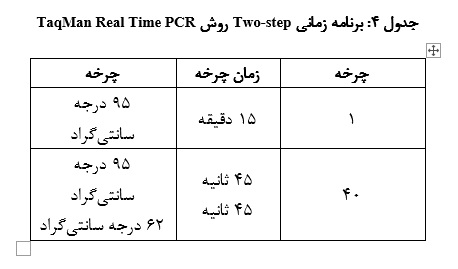
Cat.No: A314402)، دما، حجم و غلظت اجزاء واکنش، جهت راهاندازی آزمایش مورد نظر، بهینهسازی و تعیین شد (جداول 3 و 4).
در مرحله بعد جهت رسم منحنی استاندارد، از پلاسمید خطی نوترکیب رقتهای سریالی 108-101 تهیه، سپس واکنش Real Time PCR TaqMan با استفاده از آغازگرها و پروب اختصاصی ژن HBZ و ERV-3 (به عنوان کنترل داخلی)، بر اساس چرخه دمایی و زمانی بهینه شده انجام گردید.
معتبرسازی (Validation) آزمایش Real Time PCR :
به منظور ارزیابی صحت (Accuracy) آزمایش، از استاندارد (Copy/µL 108- Copy/µL 101) به صورت تکرارهای 3 تایی در 3 روز متفاوت استفاده شد (12). جهت ارزیابی حساسیت (Analytical Sensitivity) آزمایش از استاندارد (Copy/µL 103- Copy/µL 101) به صورت تکرارهای 3 تایی در 3 روز متفاوت استفاده شد (12). برای تعیین محدوده خطی بودن نمودار تست (Linearity)، استانداردهای (Copy/µL 108- Copy/µL 101) به صورت تکرارهای 3 تـایی در یک روز انجام شد (12). جهت تعیین دقت (Precision) آزمایش، از استاندارد (Copy/µL 108- Copy/µL 101) بـه صـورت تکرارهـای 3
تایی در 3 نوبت کاری متفاوت در یک روز به منظور درونسنجی Intra assay و تکرارهای 3 تایی در یک نوبت کاری در 3 روز متفاوت به منظور بین سنجی Inter assay استفاده گردید (13).
به منظور ارزیابی ویژگی (Analytical Specificity) آزمایش، آغازگرها با سکانسهای موجود در بانک ژنی با استفاده از سرور BLAST در سایت NCBI چک و مقایسه شدند. آغازگرها از مناطق محافظت شده ژنوم HTLV-1 که با بقیه سکانسها شباهت نداشته باشد، انتخاب شدند. این آغازگرها بـه گونهای انتخاب شده بودند که با ژنوم سایر ویروسها واکنش متقاطع نداشته باشند. به همین منظور از DNAهای استخراج شده ویروسهایHBV ، HCV ، HIV،HSV و 12نمونه منفی (افراد سالم) از لحاظ حضور ویروس بـه صـورت تکرارهـای 5 تـایی استفـاده شــد (13). ارزیابی کارآیی تکثیر (Efficiency)، از طریق فرمول /slope10-1 E= محاسبه میشود. در این فرمول Slope شیب خط نمودار و E کارآیی تکثیر میباشد. R2 خطی بودن نمودار را نشان میدهد (12).
یافتهها
آزمایش PCR و کلونینگ ژن HBZ :
پس از PCR و تعیین توالی ژن مورد نظر، نتیجه تعیین توالی در پایگاه NCBI ، BLAST و تایید شد. سپس ژن HBZ در وکتور (PCR 2.1 TOPO) TOPO TA کلون گردید و جهت تـایید کلونینگ، پلاسمید نوترکیب با روش کلونی PCR و با استفاده از آنزیم BamH I خطی شد (شکل 1).
کلونینگ محصول PCR :
محصول PCR ژن HBZ به وسیله کیت TOPO TA Cloning Kit (آمریکا، اینویتروژن) درون وکتور TOPO TA (PCR 2.1 TOPO) قرار گرفت و صحت کلونینگ با colony PCR سنجیده شد. پلاسمید نوترکیب به وسیله کیت رُوش (آلمان) استخراج و در ژل آگارز 1% الکتروفورز شد. سپس پلاسمید نوترکیب به وسیله آنزیمBamH I ، خطی شده و تعداد کپی آن بر اساس فرمول زیر محاسبه شد:
|
OD Plasmid × 1023 × 022/6
Plasmid length × (109 × 1) 650 |
|
= تعداد کپی DNA
|
|
58 × 1023 × 022/6
4393 × (109 × 1) 650 |
|
µL/copy 109×12=
|
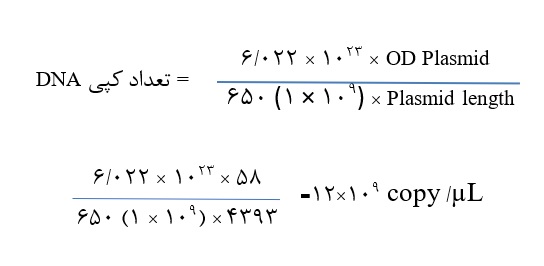
بهینهسازی و راهاندازی آزمایش TaqMan Real Time PCR:
بـا توجـه بـه دستـورالعمــل مسترمیکس (Ampliqon:
Cat.No: A314402)، دما، حجم و غلظت اجزاء واکنش، جهت راهاندازی آزمایش مورد نظر، بهینهسازی و تعیین شد (جداول 3 و 4).


در مرحله بعد جهت رسم منحنی استاندارد، از پلاسمید خطی نوترکیب رقتهای سریالی 108-101 تهیه، سپس واکنش Real Time PCR TaqMan با استفاده از آغازگرها و پروب اختصاصی ژن HBZ و ERV-3 (به عنوان کنترل داخلی)، بر اساس چرخه دمایی و زمانی بهینه شده انجام گردید.
معتبرسازی (Validation) آزمایش Real Time PCR :
به منظور ارزیابی صحت (Accuracy) آزمایش، از استاندارد (Copy/µL 108- Copy/µL 101) به صورت تکرارهای 3 تایی در 3 روز متفاوت استفاده شد (12). جهت ارزیابی حساسیت (Analytical Sensitivity) آزمایش از استاندارد (Copy/µL 103- Copy/µL 101) به صورت تکرارهای 3 تایی در 3 روز متفاوت استفاده شد (12). برای تعیین محدوده خطی بودن نمودار تست (Linearity)، استانداردهای (Copy/µL 108- Copy/µL 101) به صورت تکرارهای 3 تـایی در یک روز انجام شد (12). جهت تعیین دقت (Precision) آزمایش، از استاندارد (Copy/µL 108- Copy/µL 101) بـه صـورت تکرارهـای 3
تایی در 3 نوبت کاری متفاوت در یک روز به منظور درونسنجی Intra assay و تکرارهای 3 تایی در یک نوبت کاری در 3 روز متفاوت به منظور بین سنجی Inter assay استفاده گردید (13).
به منظور ارزیابی ویژگی (Analytical Specificity) آزمایش، آغازگرها با سکانسهای موجود در بانک ژنی با استفاده از سرور BLAST در سایت NCBI چک و مقایسه شدند. آغازگرها از مناطق محافظت شده ژنوم HTLV-1 که با بقیه سکانسها شباهت نداشته باشد، انتخاب شدند. این آغازگرها بـه گونهای انتخاب شده بودند که با ژنوم سایر ویروسها واکنش متقاطع نداشته باشند. به همین منظور از DNAهای استخراج شده ویروسهایHBV ، HCV ، HIV،HSV و 12نمونه منفی (افراد سالم) از لحاظ حضور ویروس بـه صـورت تکرارهـای 5 تـایی استفـاده شــد (13). ارزیابی کارآیی تکثیر (Efficiency)، از طریق فرمول /slope10-1 E= محاسبه میشود. در این فرمول Slope شیب خط نمودار و E کارآیی تکثیر میباشد. R2 خطی بودن نمودار را نشان میدهد (12).
یافتهها
آزمایش PCR و کلونینگ ژن HBZ :
پس از PCR و تعیین توالی ژن مورد نظر، نتیجه تعیین توالی در پایگاه NCBI ، BLAST و تایید شد. سپس ژن HBZ در وکتور (PCR 2.1 TOPO) TOPO TA کلون گردید و جهت تـایید کلونینگ، پلاسمید نوترکیب با روش کلونی PCR و با استفاده از آنزیم BamH I خطی شد (شکل 1).


بهینهسازی آزمایش TaqMan Real Time PCR :
پس از بهینهسازی آزمایش TaqMan Real Time PCR، نتایج آن بر روی ژل آگارز 5/1% الکتروفورز شد (شکل 2).
راهاندازی آزمایشReal Time PCR :TaqMan probe
پس از تهیه رقتهای مختلف از پلاسمید خطی شده و انجام آزمایش Real Time PCR (به وسیله دستگاه Rotor Gene RG-3000)، منحنی استاندارد رسم شد. شیب خط منحنی استاندارد برابر بـا 3.2- وR2 برابر با 97/0 بود که نشاندهنده خطی بودن و کارآیی آزمایش بوده وEfficiency آن نیز 06/1 تعیین شد (اشکال 3 و 4). نتایج تکرارپذیری واکنش در سطح درون سنجی و بین سنجی بررسی و میانگین ضریب تغییرات CV نمونههای استاندارد، کمتر از 3/5 % برای اینتراسی و 9/5% برای اینترااسی بود. مشاهدات حاکی از آن بود که LOD (Limit of detection) این آزمایش برابر باCopies/µL 101× 2/1 بوده که نشاندهنده حساسیت بالای این روش میباشد. LOD این آزمایش بر اسـاس معیـارهای موجـود در راهنمـای FDA جهت اعتبار
سنجی روشهای بیوآنالیتیکی تعیین گردید (14).
بحث
ویروس HTLV عمدتاً از طریق انتقال عمودی مــادر بـه
نوزاد در دوران شیردهی، انتقال افقی، تماس جنسی و تزریق فرآوردههای سلولی حاوی این ویروس منتقل میشود (15). روشهای تشخیصی ویروس HTLV-1 عمدتاً شامل آزمایشهای سرولوژیکی هستند که به دنبال آنتیبادیهای خاص علیه آنتیژنهای مختلف HTLV-1 میگردند. آزمایشهای غربالگری معمولاً شامل الایزا (ELISA) یا آگلوتیناسیون ذرات (PA) هستند. آزمایشهای تأییدی شامل ایمونوفلورسانس (IFA) و وسترن بلات (WB) می باشد، اما عمدتاً از وسترن بلات استفاده میشود (16). با وجود برخی بهبودها در دقت آزمایش وسترن بلات طی دو دهه گذشته، همچنان الگوهای سرولوژیکی نامشخص پس از تحلیل وسترن بلات رایج هستند (17). در مقالههای متعددی از سنجش لود ویروس به عنوان یک فاکتور پیشآگهی و پایش بیماران تحت درمان نام برده شده است. بـه همین دلیل بررسی میزان لود ویروس با استفاده از ژنهایHBZ, tax, pol…. ویروس میتواند مزایای زیادی از جمله تشخیص و بررسی پیشرفت بیماریهای مرتبط با ویروس HTLV-1، ارزیابی اثربخشی درمانهای ضد ویروسی، درک بهتر از مکانیسمهای بیماریزایی ویروس و در نهایت توسعه درمانهای جدید داشته باشد (18).
در مطالعه حاضر روش Real Time PCR TaqMan برای ژن HBZ با هدف طراحی یک روش حساس به منظور تعیین پرووایرال لود ویروس HTLV-1 طراحی و راهاندازی شد. بـدین منظور در ابتدا جهت رسم منحنی استاندارد، از پلاسمید نوترکیب حاوی ژن HBZ ویروس، رقتهای لگاریتمی تهیه گردید. پس از بهینه شدن شرایط آزمایش، نتایج حاکی از آن بود کهLOD این آزمایش برابر باCopies/µL 101× 2/1 بوده که نشاندهنده حساسیت بالای این روش میباشد.
واترز و همکاران در مطالعه خود بیان کردنـد کـه آزمایش qPCR (Quantitative PCR) معتبر شده، بـه عنـوان یـک آزمایش کارآمد که قادر به اندازهگیری پرووایرال لود باشـد و همچنین قابلیت تکرارپـذیری داشـته باشـد، مـورد نیـاز است. از آن جایی که هنوز یک بیومارکر اختصاصـی بـرای پیشبینی پیشرفت بیماری در افـراد بـدون علامـت وجـود ندارد و از طرفی میزان آنتیبادی اختصاصی علیه HTLV-1 بـا پرووایـرال لـود ویـروس همبسـتگی دارد، مـیتـوان از پرووایرال لود به عنوان روشی برای پیشبینی نتایج عفونت و پیشرفت بیماری استفاده نمود (19).
مطالعهای توسط مانیکی سایتمو و همکاران، جهت بررسی میزان بیان ژن HBZ و ارتباط آن با لود ویروس HTLV انجام شد. به منظور رسم منحنیهای استاندارد برای تعیین میزان بیان ژنهای Tax و HBZ ویروس HTLV-1 ، همچنین ژن مرجع hypoxanthine guanine phosphoribosyltransferase (HPRT)، cDNA تهیهشده از سلولهای MT-2 آلوده به HTLV-1 که بهصورت سریالی رقیقسازی شده بود، استفاده شد. در این مطالعه ضریب همبستگی یا 99/0 =R2 گزارش شد (18).
مطالعهای توسط کلودیا کازولی و همکاران در سال 2014 جهت بررسی لود ویروس HTLV-1/2 انجام شد. در این مطالعه آزمونهای single-plex جداگانهای برای ژنهای 1tax- از HTLV-1 و tax-2 و pol-2 از HTLV-2 طراحی شدند تا بار پروویروسی HTLV-1 و HTLV-2 به طور کمی اندازهگیری شود. اختصاصیت آزمونهای tax-2 و pol-2 با آزمایش DNA استخراج شده از سلول 10C، که یک رده سلولی آلوده به 1HTLV- است و به عنوان کنترل منفی استفاده شد، تأیید گردید. در مورد آزمون HTLV-2 ، اختصاصیت با آزمایش سلولهای 344C که به طور پایدار به HTLV-2 آلوده هستند، بررسی شد. تعیین کمی بار پروویروسی HTLV با انجام منحنیهای استاندارد مرجع از طریق رقتسازی سریالی DNA استخراج شده از سلولهای 10C و 344 Cانجام شد، با این فرض که هر سلول 10C دارای یک ژنوم پروویروسی و هر سلول 344C دارای دو ژنوم پروویروسی است نموداری با 4/3- =Slop و 99/0 =R2 رسم شد. ژن آلبومین انسانی که دارای دو نسخه در هر سلول است، برای طبیعیسازی نتایج در همان واکنشها اندازهگیری شد (20). در اکثر مطالعههایی که مورد بررسی قرار گرفته است، جهت رسم منحنی استاندارد از رده سلولی استفاده شده بود، اما در مطالعه حاضر به دلیل عدم دسترسی به این رده سلولی، از پلاسمید نوترکیب حاوی ژن HBZ ویروس HTLV-1 جهت رسم نمودار استاندارد استفاده شد. رسم منحنی استاندارد از طریق وکتور حاوی ژن HBZ نشان داد که این روش با شیب خط برابر با 3.2- و 97/0 =R2 و حد تشخیص 101×2/1 روشی با حساسیت و اختصاصیت بالاست که نتایج آن قابل مقایسه با نتایجی است که در آن برای رسم نمودار استاندارد از رده سلولی استفاده شده است.
در سال 2019 مطالعهای به وسیله حمیده قاسمزادگان و همکاران در ایران انجام شد. این مطالعه با هدف طراحی آزمایشReal Time PCR به روش سایبرگرین جهت تعیین لود ویروس HTLV-1 با استفاده از ژن Tax راهاندازی شد. به همین منظور DNA ژنومی از سلولهای تک هستهای خون محیطی استخراج سپس محصولPCR ژن Tax درون پلاسمید pTZ57 R/T قرار گرفت و با رقتسازی، منحنی استاندارد با شیب خط 3/3= Slop و 99/0=R2 رسم شد. در این مطالعه جهت طبیعیسازی نتایج از ژن GAPDH استفاده شد (12).
مطالعه دیگری به وسیله هومین جی و همکاران در سال 2023 با هدف و توسعه و اعتبارسنجی یک آزمون TaqMan qPCR برای اندازهگیری بار پروویروسی HTLV-1 انجام شد. در این مطالعه جهت رسم منحنی استاندارد از PcDNA3.1(-)HTLV-1RPPH1 plasmid استفاده شد. ژن انسانی RPPH-1 و بخشهای pol و tax از ویروس HTLV-1 با استفاده از gDNA، سلولهای 102Hut تکثیر و استخراج شده، سپس درون وکتور pcDNA3.1(-)-Rluc- Fluc vector قرار گرفتند. رقتهای سریالی از وکتور مورد نظر جهت رسم منحنی استانـدارد تهیه و نموداری با 2/3 =slope ، 99/0=R2 و 003/103 =efficiency به دست آمد. حد تشخیص (LOD) در این مطالعه برای غلظت سلولهای 102Hut ، معادل 0218/0 % (با فاصله اطمینان 95% بین 0179/0 % تا 0298/0 %) بـه دست آمد. در این مطالعه جهت بررسی اختصاصیت این واکنش، gDNA استخراجشده از نمونههای منفی برای HTLV-1 (که شامل ۳ نمونه مبتلا به HBV ، ۳ نمونه مبتلا به HCV، ۳ نمونه مبتلا به Treponema pallidum، ۳ نمونـه مبتلا به HIV و ۱۲ نمونه افراد سالم بودند) و همچنین رده سلولهای MOT (آلوده به HTLV-2) بـا استفاده از این آزمایش مورد بررسی قرار گرفتند (102 Hut که حاوی ژنوم HTLV-1 بود بـه عنوان کنترل مثبت استفاده شد).
تمامی نمونـههای منفی برای HTLV-1 و همچنین رده سلولی MOT (آلوده به HTLV-2) ، تنها ژن 1RPPH را با این روش تکثیر دادند که نشاندهنده اختصاصیت 100% این واکنش می باشد (13).
در هر دو مطالعه مورد بررسی، همانند مطالعه حاضر از وکتور جهت رسم منحنی استاندارد استفاده شده با این تفاوت که ژن کنترل داخلی مورد استفاده در این مطالعه ERV-3 بوده، در حالی که در سایر مطالعهها از ژنهای GAPDH، RPPH1 و آلبومین به عنوان ژن مرجع استفاده شده است. همچنین اکثر مطالعهها، ژنهای Tax و pol ویروسHTLV را مورد بررسی قرار دادند اما در مطالعه حاضر ژن HBZ جهت تعیین لود ویروس مورد بررسی قرار گرفت که این وجه تمایز مطالعه حاضر با مطالعههای قبلی به شمار میرود.
مطالعههای بیشتر میتواند به درک عمیقتری از عفونتهای ویروسی و پاسخهای ایمنی مرتبط منجر شود. در همین راستا، پیشنهاد میشود ژنهایی از جمله LTR ، Env و سایر ژنهای کلیدی ویروس HTLV ، به منظور تعیین بار ویروسی و بررسی ارتباط آن با بیماریزایی، مورد
مطالعه قرار گیرند.
نتیجهگیری
این آزمایش با دارا بودن کمترین حد تشخیص (LOD) که Copies/µL 101× 2/1 در هر واکنش بود و همچنین استفاده از ژن HBZ که نقش اساسی در تنظیم فعالیتها و انـکوژنز ویروس HTLV دارد، میتوانـد به عنوان گزینه مناسبی جهت تعیین میزان لود ویروس و ارتباط آن با بیماریزایی ویروس مورد استفاده قرار گیرد.
حمایت مالی
این پروژه توسط مرکز تحقیقات انتقال خون، مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ایران تأمین مالی شده است.
ملاحظات اخلاقی
مطالعه حاضر دارای کد اخلاق IR.TMI.REC.1402.016 از کمیته اخلاق مؤسسه عالی آموزشی و پژوهشی طب انتقال خون تهران ، ایران است.
عدم تعارض منافع
نویسندگان اظهار میکنند هیچگونه تعارض منافعی در این مطالعه وجود نداشته است.
نقش نویسندگان
ریحانه تیموری: نگارش اولیه مقاله و تحلیل اطلاعات
دکتر زهره شریفی: نظارت بر اجرای طرح پژوهشی و نگارش مقاله
دکتر مهدی آجورلو: طراحی مطالعه، نظارت بر اجرای طرح و نگارش نهایی مقاله
تشکر و قدردانی
این تحقیق حاصل پایاننامه کارشناسی ارشد زیست فناوری پزشکی مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ایران میباشد. بدینوسیله نویسندگان مقاله از این مؤسسه به دلیل حمایتهای مالی، تشکر و قدردانی مینمایند.
نوع مطالعه: پژوهشي |
موضوع مقاله:
ويروس شناسي
فهرست منابع
1. Poiesz BJ, Ruscetti FW, Gazdar AF, Bunn PA, Minna JD, Gallo RC. Detection and isolation of type C retrovirus particles from fresh and cultured lymphocytes of a patient with cutaneous T-cell lymphoma. Proc Natl Acad Sci U S A. 1980 Dec;77(12):7415-9. [DOI:10.1073/pnas.77.12.7415] [PMID] []
2. Naderi M, Talebi S, Buyzan A, Yousefi Nojookambari N, Yazdansetad S. The Interaction of Cell-Human T-cell Leukemia Virus Type 1 (HTLV-1) in the Development of Adult T-cell Leukemia/Lymphoma: The Molecular Aspects of Leukemogenesis. Razi Journal of Medical Sciences. 2022;29(6):25-37.https://rjms.iums.ac.ir/article-1-7259-en.html
3. Keikha M, Karbalaei Zadeh Babaki M, Marcondes Fonseca LA, Casseb J. The Relevance of HTLV-1-associated Myelopathy/Tropical Spastic Paraparesis in Iran: A Review Study. Reviews in Clinical Medicine. 2019;6(2):60-5. [DOI:10.22038/rcm.2019.38759.1266]
4. Mohanty S, Harhaj EW. Mechanisms of Innate Immune Sensing of HTLV-1 and Viral Immune Evasion. Pathogens. 2023 May 19;12(5):735. [DOI:10.3390/pathogens12050735] [PMID] []
5. Letafati A, Bahari M, Salahi Ardekani O, Nayerain Jazi N, Nikzad A, Norouzi F, Mahdavi B, Aboofazeli A, Mozhgani SH. HTLV-1 vaccination Landscape: Current developments and challenges. Vaccine X. 2024 Jul16;19:100525. [DOI:10.1016/j.jvacx.2024.100525] [PMID] []
6. Herrmann D, Meng S, Yang H, Mansky LM, Saad JS. The Assembly of HTLV-1-How Does It Differ from HIV-1? Viruses. 2024 Sep 27;16(10):1528. [DOI:10.3390/v16101528] [PMID] []
7. Enose-Akahata Y, Vellucci A, Jacobson S. Role of HTLV-1 Tax and HBZ in the Pathogenesis of HAM/TSP. Front Microbiol. 2017 Dec 21;8:2563. [DOI:10.3389/fmicb.2017.02563] [PMID] []
8. Giam CZ, Semmes OJ. HTLV-1 Infection and Adult T-Cell Leukemia/Lymphoma-A Tale of Two Proteins: Tax and HBZ. Viruses. 2016 Jun 16;8(6):161. [DOI:10.3390/v8060161] [PMID] []
9. El Hajj H, Bazarbachi A. Interplay between innate immunity and the viral oncoproteins Tax and HBZ in the pathogenesis and therapeutic response of HTLV-1 associated adult T cell leukemia. Front Immunol. 2022 Jul 22;13:957535. [DOI:10.3389/fimmu.2022.957535] [PMID] []
10. Cassar O, Gessain A. Serological and Molecular Methods to Study Epidemiological Aspects of Human T-Cell Lymphotropic Virus Type 1 Infection. Methods Mol Biol. 2017;1582:3-24. [DOI:10.1007/978-1-4939-6872-5_1] [PMID]
11. Caterino-de-Araujo A, Campos KR. Defective particles of human T-lymphotropic virus and negative results in molecular assays. Infect Genet Evol. 2021 Dec;96:105141. [DOI:10.1016/j.meegid.2021.105141] [PMID]
12. Ghasemzadegan H, Shahabi M, Rezaei N, Sharifi Z. Design a Real Time PCR with SYBR Green for quantification of HTLV-1 proviral load for blood donors. The Scientific Journal of Iranian Blood Transfusion Organization. 2019;16(3):194-200. https://bloodjournal.ir/browse.php?a_id=1248&sid=1&slc_lang=en
13. Ji H, Chang L, Yan Y, Wang L. Development and validation of a duplex real-time PCR for the rapid detection and quantitation of HTLV-1. Virol J. 2023 Jan 17;20(1):9. [DOI:10.1186/s12985-023-01970-y] [PMID] []
14. Eusebio-Ponce E, Anguita E, Paulino-Ramirez R, Candel FJ. HTLV-1 infection: An emerging risk. Pathogenesis, epidemiology, diagnosis and associated diseases. Rev Esp Quimioter. 2019 Dec;32(6):485-496. https://seq.es/abstract/rev-esp-quimioter-2019-october-25-2/
15. Zhao J, Zhao F, Han W, Xu X, Wang L, Li R, et al. HTLV screening of blood donors using chemiluminescence immunoassay in three major provincial blood centers of China. BMC Infect Dis. 2020 Aug 6;20(1):581. [DOI:10.1186/s12879-020-05282-2] [PMID] []
16. A Strategy for Screening and Confirmation of HTLV-1/2 Infections in Low-Endemic Areas. Front Microbiol. 2020 Jun 3;11:1151. [DOI:10.3389/fmicb.2020.01151] [PMID] []
17. Saito M, Matsuzaki T, Satou Y, Yasunaga J, Saito K, Arimura K, et al. In vivo expression of the HBZ gene of HTLV-1 correlates with proviral load, inflammatory markers and disease severity in HTLV-1 associated myelopathy/tropical spastic paraparesis (HAM/TSP). Retrovirology. 2009 Feb 19;6:19. [DOI:10.1186/1742-4690-6-19] [PMID] []
18. Waters A, Oliveira AL, Coughlan S, de Venecia C, Schor D, Leite AC, et al. Multiplex real-time PCR for the detection and quantitation of HTLV-1 and HTLV-2 proviral load: addressing the issue of indeterminate HTLV results. J Clin Virol. 2011 Sep;52(1):38-44. [DOI:10.1016/j.jcv.2011.05.022] [PMID]
19. Casoli C, Pilotti E, Bertazzoni U. Proviral load determination of HTLV-1 and HTLV-2 in patients' peripheral blood mononuclear cells by real-time PCR. Methods Mol Biol. 2014;1087:315-23. [DOI:10.1007/978-1-62703-670-2_25] [PMID]
20. U.S. Department of Health and Human Services Food and Drug Administration. Bioanalytical Method Validation Guidance for Industry. Silver Spring, MD: U.S. Department of Health and Human Services, Center for Drug Evaluation and Research (CDER); May 2018. https://www.fda.gov/files/drugs/published/Bioanalytical-Method-Validation-Guidance-for-Industry.pdf
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







