جلد 22، شماره 2 - ( تابستان 1404 )
جلد 22 شماره 2 صفحات 110-100 |
برگشت به فهرست نسخه ها
Ethics code: IR.TMI.REC.1402.011.
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Sharif Zandieh Z, Samiee S, MousaviHosseini K, Sharifi Z. In Silico Synthesis of HSV-2 Positive Control Using Polymerase Cycling Assembly. bloodj 2025; 22 (2) :100-110
URL: http://bloodjournal.ir/article-1-1572-fa.html
URL: http://bloodjournal.ir/article-1-1572-fa.html
شریف زندیه زهرا، سمیعی شهرام، موسوی حسینی کامران، شریفی زهره. سنتز اینسیلیکو کنترل مثبت HSV-2 با استفاده از روش Polymerase Cycling Assembly. فصلنامه پژوهشی خون. 1404; 22 (2) :100-110
مربی مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون
متن کامل [PDF 731 kb]
(460 دریافت)
| چکیده (HTML) (1236 مشاهده)
مقدمه
ساخت DNA سنتتیک که به طور عام به آن"سنتز ژن" اطلاق میشود، به فرآیند سنتز توالیهایی از DNA به طول 250 تا 2000 جفت باز از اولیگونوکلئوتیدهای تک رشتهای DNA سنتتیک اشاره دارد. این اولیگونوکلئوتیدها عمدتاً با استفاده از روشهای شیمیایی فسفرآمیدیت تولید میشوند و سپس با استفاده از روشهای مختلفی به ساختارهای بزرگ تر مونتاژ میگردند (1).
در میان روشهای موجود برای سنتز ژن، روش “Polymerase Cycle Assembly” به عنوان یک نوآوری برجسته شاخته میشود که میتواند جایگزین مناسبی برای روشهای سنتی باشد. روشهای قدیمیتر نظیر سنتز شیمیایی با محدودیتهایی در زمینه تولید کنترل مثبت مواجه هستند؛ به ویژه زمانی که طول قطعه مورد نظر بیشتر از 300 نوکلئوتید باشد، کارآیی این روشها کاهش مییابد. علاوه بر این، وابستگی به حلالهای آلی در این روشها میتواند تأثیرات منفی بر محیط زیست داشته باشد.
برای غلبه بر این محدودیتها و ساخت DNA با همان کارآیی که در خوانش DNA وجود دارد، تکنولوژیهای جایگزین توسعه یافتهاند و شامل مونتاژ مولکولی و روشهای کلونینگ، روش سنتز آنزیمی مستقل از الگو، میکروآرایه و تکثیر حلقه چرخان توسعه یافته میباشند (2). به طور کلی، پیشرفتهای اخیر در زمینه سنتز DNA سنتتیک، به ویژه با ظهور روشهای نوین مانند Polymerase Cycle Assembly، نه تنها کارآیی فرآیندها را افزایش داده بلکه به حفظ محیط زیست نیز کمک میکند.
به علت پتانسیل بالای کاربردهای سنتز اولیگونوکلئوتیدها در مقیاس وسیع، پیشرفتهای قابل توجهی در علوم تجربی، به ویژه در زمینههای زیستشناسی سنتتیک، مهندسی پروتئین، مهندسی ژنوم و مهندسی متابولیک حاصل شده است (3). با توجه به اندازه کوچک ویروسها و نقش حیاتی آنها در پیشرفت سلامت و بیوتکنولوژی، پیشرفتهای چشمگیری در سنتز ژنومهای ویروسی مشاهده شده است (4).
ویـروس هرپـس سیمپلکـس نـــوع ۲ (HSV-2) یکی از
عفونتهای منتقله از راه رابطه جنسی است که حدود ۴۹۱ میلیون نفر (13%) از افراد بین 15 تا 49 سال در سراسر جهان به آن مبتلا هستند (5). گزارشهای متعددی نشان میدهند که حضور DNA مرتبط با HSV در خون ممکن است رخ دهد؛ بنابراین، احتمال انتقال HSV از طریق محصولات خونی وجود دارد. با این حال، این پدیده محدود به عفونتهای اولیه است و در عفونتهای راجعه مشاهده نمیشود. از این رو، افرادی که دچار عفونت اولیه هستند باید اهدای خون را به تعویق بیندازد (6).
Real Time PCR یکی از روشهای اصلی برای تشخیص این عفونت و از پرکاربردترین روشها برای اندازهگیری بیان ژن است، زیرا دامنهای پویا و حساسیت مناسبی دارد و میتواند به طور اختصاصی برای هر توالی عمل کند (9-7). کنترلهای مثبت در PCR به عنوان یک اقدام تأییدی کیفی به کار میروند تا اطمینان حاصل شود که شرایط واکنش ( مواد و وضعیت چرخهها) به درستی عمل میکنند و نتایج منفی تنها به دلیل فقدان DNA هدف در نمونههای آزمایش است (10). تولید کنترلهای سنتتیک با استفاده از روش سنتز آنزیمی نیاز به کلونینگ یا تجهیزات خاص فراتر از وسایل آزمایشگاههای تشخیص مولکولی ندارد. این روش احتمال آلودگی یا گزارش اشتباه واکنشهای مثبت کاذب را به علت آلودگی با مواد کنترل مثبت کاهش میدهد (11). کنترلهای سنتتیک تولید شده با این روش در همه آزمایشهای تشخیص مولکولی و صرف نظر از این که ما ارگانیسم را داریم یا خیر به کار گرفته میشوند. از مزایای این روش میتوان سهولت، اختصاصیت و کارآیی بالای 11را متذکر شد اما در زمینه ساخت کنترل مثبت HSV-2 به طور کامل مورد بررسی قرار نگرفته است. با ذکر محدودیت در روشهای موجود، این پژوهش منجر به دقت تشخیصی بهتر و اعتبار در شناسایی HSV-2 شد. هدف ما از این پژوهش، اطمینان از دقت و قابل اعتماد بودن نتایج کنترلهای مثبت سنتز شده به روش آنزیمی در شناسایی HSV-2 نسبت به کنترلهای بالینی بود که در حال حاضر برای این ویروس موجود است. روش آنزیمی شامل ساخت قطعات DNA HSV-2دارای همپوشانی و مشابه با توالی DNA ویروسی است. برای سنتز آنزیمی قطعه DNA نیاز به مطالعههای in silico است بدین صورت که با مقایسه ژنوم ویروس HSV-1 و HSV-2 ، نقاط ثابت ژنوم ویروس HSV-2 جهت تعیین مکان سنتز ژن تعیین شود.
مواد و روشها
این پژوهش یک مطالعه تجربی بود.
در این پروژه استفاده از اطلاعات فردی انسانی یا استفاده از حیوان آزمایشگاهی وجود نداشت.
طراحی آغازگر با نرمافزار AlleleID :
فرآیند انتخاب ناحیه مناسب برای تفکیک سویههای هرپس عمدتاً به دلیل درجه شباهت توالیها در خانواده هرپس ویریده دشوار بود. استراتژی ما شامل شناسایی توالیهای حفاظت شدهای بود که نه تنها تفاوتها را میان تایپهای هرپس ویروس نشان دهند بلکه این ویروس را از دیگر ویروسهای هم خانواده و سایر DNA ویروسها تمیز دهد. در این ارتباط نخست با یک مطالعه گذشتهنگر به انتخاب ناحیهUS6 رسیدیم.
اولین مرحله در این پژوهش، طراحی آغازگر برای ناحیهای منحصر به فرد در ژن US6 در ژنوم HSV-2 بود. این تصمیم با استفاده از نرمافزار MEGA نسخه 11 صورت گرفت و با آن حداقل دو توالی مجزا از HSV-2 و HSV-1 که از NCBI گرفته شده بودند، مورد هم ردیفی قرار گرفتند. پس از وارد کردن توالیهای DNA در نرمافزار AlleleID نسخه 7 با توجه به الگوریتمهای پایه نرمافزار، آغازگرهای متعدد و پروب مناسب پیشنهاد شد. با این حال، تصمیم ما به کارگیری آغازگرها و پروب طراحی شده به صورت دستی به جای استفاده از پیشنهادهای نرمافزار مربوطه بود. از این نرمافزار برای بررسی ساختارهای ثانویه از جمله ساختارهای سنجاق سر، self-dimer و cross dimer با توجه به پارامترهای ترمودینامیکی مربوطه استفاده میشود. با توجه به انرژی آزاد گیبس (ΔG)، میزان انجامپذیری و پایداری ساختارهای ثانویه تعیین میشود.
بررسی ژنوم HSV-2 با نرمافزار SnapGene :
با انتخاب آغازگر جلوبرنده و معکوس در نرمافزار SnapGene ، اندازه قطعه تکثیر یافته در این مطالعه PCR in silico تخمین زده شد. با توجه به آغازگرها و با انتخاب simulate agarose gel در قسمت tools ، اندازه قطعه تکثیر یافته و موقعیت آن در ژل 2% تخمین زده شد.
نهایتاً محصول in silico PCR مورد جست و جوی بلاست برای اطمینان از اختصاصیت برای HSV-2 قرار گرفت. این عمل مکمل بلاست آغازگر است که در محیط SnapGene انجام گرفت؛ بدین صورت که با وارد کردن توالی آغازگر و انتخاب گزینه tools و اجرای بلاست برای آغازگرهای انتخاب شده، از اتصال اختصاصی آغازگر به ارگانیسم هدف اطمینان حاصل شد.
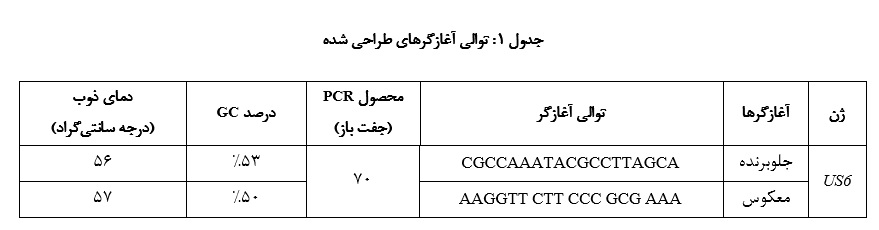
برای محصول in silico PCR نیز تمام نتایج گزارش شده مربوط به HSV-2 بودند. حتی زمانی که ارگانیسم HSV-1 در هم ردیفیNCBI انتخاب شد، هیچ نتیجهای برایin silico PCR گزارش نشد. توالی آغازگرها در جدول قابل مشاهده هستند (جدول 1). ترادف آغازگرهای HSV-2 نیز با استفاده از نرمافزار MEGA نسخه 11 و الگوریتمهای پایه نسبت به ژنوم ویروس HSV-1 و HSV-2 مورد بررسی multiple sequence alignment قرار گرفت.
بررسی تکمیلی ساختارهای ثانویه با نرمافزار MFold :
خود آغازگرها و محصول آنها از نظر ساختار ثانویه با MFold چک شدند.MFold یک ابزار تحت وب است که ساختار ثانویه توالیهای اسید نوکلئیک مانند DNA یا RNA را بر اساس ویژگیهای ترمودینامیکی پیشبینی میکند. در حقیقت، نرمافزار MFold توالی سکانسی را که قرار است برای آن آغازگر طراحی شود از نظر وجود ساختارهای ثانویه چک میکند.
بدین صورت که انواع پیچ و تابهای توالی را در فایلهای مختلف ارائه میدهد (یک توالی با حالتهای مختلف پیچ خوردگی). زمانی که پیچ خوردگی به ویژه در نواحی GC هدف زیاد باشد پیشنهاد میشود که برای PCR از بتائین استفاده شود. بتائین میزان تکثیر را در چنین نواحی بالا میبرد.
طراحی قطعات همپوشان برای کنترل مثبت HSV-2 :
در طراحـی قطعـات همپوشان ابتـدا باید به محل جفت آغازگرهای جلوبرنده و معکوس توجه کرد. محل قطعات دارای همپوشانی باید در مجاورت این دو باشد. طول این قطعات حدود 50 نوکلئوتید و دمای ذوب این قطعات در محل همپوشانی بهتر است حدود 66 درجه سانتیگراد باشد. در حدود 5-4 نوکلئوتید سر 3′ هر یک از قطعات از نظر درصد بازهای پورینی و پیریمیدینی میبایستی متناسب باشند.
یافتهها
طراحی آغازگر با نرمافزار AlleleID :
همان طور که در جدول 2 مشاهده میشود، امتیاز آغازگرهای پیشنهادی در نرمافزار AlleleID خوب تلقی شد. تنها در رشته antisense ساختار ثانویه self-dimer
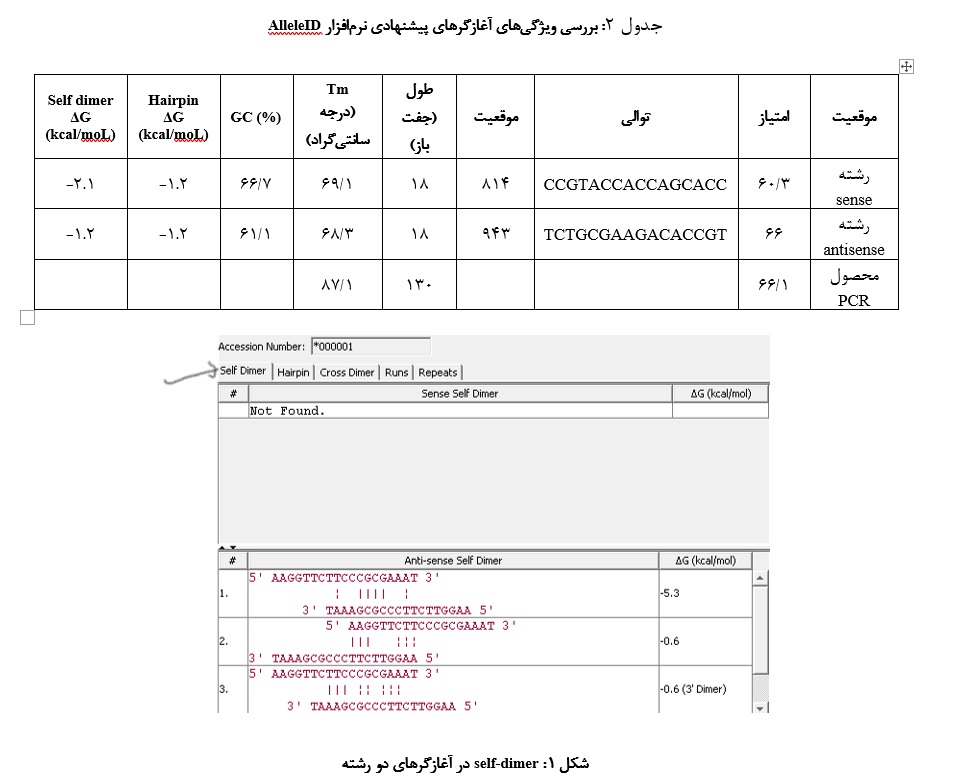
مشاهده شد و این ساختار در رشته sense وجود نداشت (شکل 1). از آن جایی که مقدار انرژی لازم برای شکستن این ساختارها بیش از Kcal/moL 5- است (ΔG)، از منظر پایدارای، تشکیل این ساختار ثانویه قابل قبول است.
انرژی آزاد گیبس (ΔG)، انرژی لازم برای شکستن ساختار ثانویه میباشد و مقادیر بسیار منفی آن نشاندهنده تمایل بیشتر آغازگرها برای اتصال به یکدیگر است و چون این انرژی برای ساختار cross dimer در شکل 2، از kcal/moL6- بیشتر است، نشاندهنده قابل قبول بودن این پارامتر میباشد (شکل 2).
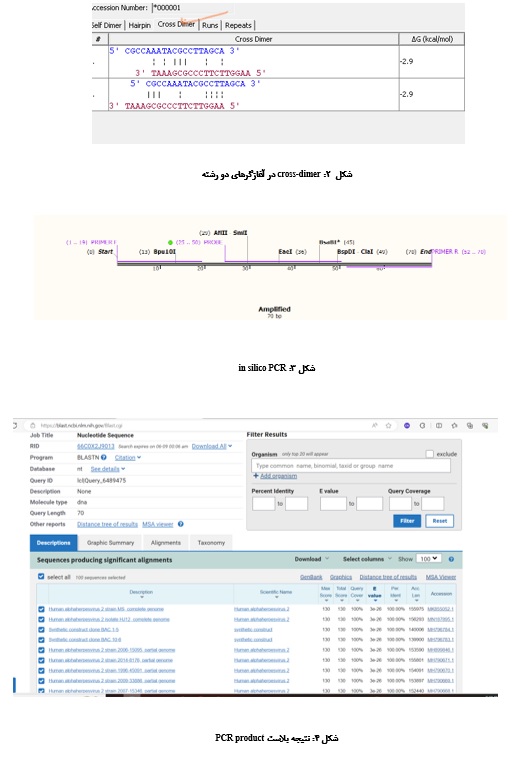
با انتخاب آغازگر جلوبرنده و معکوس در نرمافزار SnapGene ، اندازه قطعه تکثیر یافته در این مطالعه in silico PCR تخمین زده شد که میزان 70 جفت باز بود (شکل 3). توالی قطعات همپوشان با توجه به قطعه جلوبرنده و قطعه معکوس در جدول 3 آمده است.

با توجه به بررسیهای in silico ، روش PCA در تولید کنترل مثبت HSV-2 نتایج قابل قبولی به ارمغان آورد. این امر میتواند پایه پیشرفت در بیولوژی سنتتیک با انقلاب در تشخیصهای مولکولی از طریق فراهمسازی سنتز دقیق و قابل اعتماد کنترلهای مثبت شود. در مقاله هیوز و همکاران نقش حیاتی مونتاژ DNA سنتتیک در این پیشرفتها برجسته شده است. در این مطالعه روشهای متعددی برای سنتز DNA سنتتیک از جمله ترکیب روشهای شیمیایی مانند روش microarray و روش آنزیمی برای اصلاح خطا بیان شده است (1). به علاوه به روشهای مونتاژ از جمله انواع PCA (Polymerase Chain Assembly) به عنوان پرکاربردترین روش برای ساخت قطعات بزرگ اولیگونوکلئوتیدی اشاره شده است. بر این اساس مطالعه ما کاربردPolymerase Cycle Assembly را برای سنتز کنترلهای مثبت HSV-2 در تجزیه و تحلیلهای مولکولی بررسی میکند. یافتههای ما نشان داد که در مطالعههای in silico روش PCA جایگزینی قدرتمند برای سنتز کنترلهای مثبت HSV-2 است؛ به ویژه در شرایط محدود از نظر منابع که دسترسی و هزینه معقول به صرفه حیاتی هستند.
در مقاله ترمات و همکاران از روش PCA Integrated برای ساخت کنترل مثبت استفاده شد که این مطالعه دارای شرایط بهینه نظیر زمان آنیلینگ کوتاه، Thermal cycler های سریع و غلظتهای اندک اولیگو (حدود 10-5 نانومولار) بود (12). این پارامترها مونتاژ همزمان و تکثیر ژن را تسهیل مینمایند. نقطه تلاقی این پژوهش با پژوهش ما موفقیت در طراحی اولیگو و شرایط بهینه واکنش است که برای هریک منحصر به فرد میباشد. تأکید مقاله ترمات بر اهمیت تنظیم غلظت اولیگو برای توالیهای طویلتر ژنی یا زمان به کارگیری تعداد بیشتری از قطعات اولیگـو اســت.
لذا از این روش به دلیل رقابت آغـازگرهـا و misannealing برای ساخت قطعات ژن طویلتر کمتر استفاده میشود. با توجه به اندازه کوچک کنترل مثبت طراحی شده در پژوهش ما، چنین چالشی که در سنتز توالیهای طویل ژنی وجود دارد، در بخش آزمایشگاهی پژوهش ما دیده نخواهد شد.
در مقاله هوز و همکاران شکاف تکنولوژی برای ساخت توالیهای طویلDNA بحث میشود که منعکسکننده چالشهای مونتاژ برای ساخت کنترلهای دقیق است که این با کاربرد PCA به عنوان روشی نوین همراستا میباشد (2). به علاوه قابلیت دسترسی نیز به طور غیر مستقیم توان روش PCA را در بیولوژی سنتتیک به منظور کاهش پیچیدگی ذکر شده تایید میکند. کاربرد مطالعه ما به طور خاص محدود به حوزه تشخیص ذکر شده است در حالی که در مقاله هوز این کاربردها گستردهتر بوده و روند روشهای سنتز DNA و رقابت تجاری آنها بیان شده است. در حقیقت مطالعه ما مثالی از یک راه حل هدفمند برای مشکلی در زمینهای گستردهتر است.
در مقاله چن و همکاران برای شناسایی HSV-2 از جفت آغازگرهایی استفاده شد که UL52 را شناسایی میکردند اما در مقاله ما جفت آغازگرها برای شناسایی US6 طراحی شده بود (13). ناحیه UL52 در همانندسازی این ویروس دخالت دارد و در چرخه ویروس ضروری است. آغازگرهای طراحی شده برای این ناحیه فعالیت ویروس و نشانههای همانندسازی را شناسایی میکند. در حالی که US6 گلیکوپروتئین D را کد میکند که نقشی حیاتی در ورود ویروس به سلولهای میزبان دارد و هدف واکسنها و مداخلات درمانی است. هر جفت آغازگر با موفقیت HSV-2 را شناسایی میکنند اما انتخاب ناحیه هدف، حساسیت و اختصاصیت روش تشخیصی را تحت تاثیر قرار میدهد. ناحیه US6 در مکانیسمهای گریز سیستم ایمنی به درک پاتوژنیسیتی ویروس و تعاملات آن با سیستم ایمنی میزبان کمک میکند. به نظر میرسد که تفاوتهای دو ویروس HSV-1 و HSV-2 در US6 هنگام بررسی Alignment بیشتر بوده و لذا توان افتراقی این ناحیه برای طراحی آغازگر و پروب احتمالاً بهتر است.
از محدودیتهای این پژوهش عدم دسترسی به نرمافزارهای گران قیمت بیوانفورماتیکی نظیرDNASTAR Lasergene Suite میباشد که یک پکیج کامل بـرای مونتـاژ
توالیها، هم ردیفی و تجزیه و تحلیل آنهاست.
پیشنهاد میشود این پژوهش با تمرکز بر طراحی کنترل
مثبت دیگر پاتوژنها از جمله non-tuberclosis mycobacteria و حتی کنترل مثبت سرطانها ادامه یابد.
نتیجهگیری
طبق بررسیهای in silico کنترلهای مثبتی که با روش PCA طراحی شدند، از منظر طول قطعه و محتوای توالی قابل مقایسه با کنترلهای طبیعی بودند. در ساخت کنترل مثبت طویلتر با این روش، تنظیم غلظت قطعات همپوشان حائز اهمیت بود اما با توجه به اندازه کوچک کنترل مثبت در پژوهش ما، این چالش برای این اندازه از قطعات پررنگ نیست. لذا به نظر میرسد که در شرایطی که دسترسی به نمونه بالینی فراهم نباشد میتوان از نمونه سنتتیک استفاده کرد.
حمایت مالی
این پروژه توسط مرکز تحقیقات انتقال خون مؤسسه عالی آموزشی و پژوهشی طب انتقال خون تأمین مالی شده است.
ملاحظات اخلاقی
مطالعه حاضر دارای کد اخلاق IR.TMI.REC.1402.011 از کمیته اخلاق مؤسسه عالی آموزشی و پژوهشی طب انتقال خون تهران ، ایران است.
عدم تعارض منافع
نویسندگان اظهار میکنند هیچگونه تعارض منافعی در این مطالعه وجود نداشته است.
نقش نویسندگان
زهرا شریف زندیه: نگارش مقاله و انجام آزمایشها
شهرام سمیعی: ایده مقاله و نظارت بر انجام مطالعه و نگارش مقاله
دکتر کامران موسوی حسینی: ایده مقاله و نظارت بر نگارش مقاله
زهره شریفی: ایده مقاله و نظارت بر نگارش مقاله
تشکر و قدردانی
بدینوسیله نویسندگان مقاله از مؤسسه عالی آموزشی و پژوهشی طب انتقال خون به جهت تأمین هزینهها تشکر و قدردانی مینمایند.
متن کامل: (266 مشاهده)
سنتز اینسیلیکو کنترل مثبت HSV-2 با استفاده از روش Polymerase Cycling Assembly
زهرا شریف زندیه1، شهرام سمیعی2 ، کامران موسوی حسینی3 ، زهره شریفی4
1- دانشجوی کارشناسی ارشد بیوتکنولوژی پزشکی ـ مرکز تحقیقات انتقال خون ـ موسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- کارشناس ارشد بیوشیمی ـ مربی مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
3- PhD شیمی دارویی ـ استاد مرکز تحقیقات فرآوردههای بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
4- PhD ویروسشناسی ـ استاد مرکز تحقیقات فرآوردههای بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
1- دانشجوی کارشناسی ارشد بیوتکنولوژی پزشکی ـ مرکز تحقیقات انتقال خون ـ موسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- کارشناس ارشد بیوشیمی ـ مربی مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
3- PhD شیمی دارویی ـ استاد مرکز تحقیقات فرآوردههای بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
4- PhD ویروسشناسی ـ استاد مرکز تحقیقات فرآوردههای بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
https://doi.org/10.18502/avr.v34i2.18052 Citation: Sharif Zandieh Z, Samiee Sh, Mousavi Hosseini K, Sharifi Z. In Silico Synthesis of HSV-2 Positive Control Using Polymerase Cycling Assembly. J Iran Blood Transfuse. 2025: 22 (2) : 100-110 نویسنده مسئول: شهرام سمیعی. مربی مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران صندوق پستی: 1157-14665 E-mail: s.samiee@tmi.ac.ir
نویسنده مسئول: کامران موسوی حسینی. استاد مرکز تحقیقات فرآوردههای بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران صندوق پستی: 1157-14665 E-mail: ka.mousavi@tmi.ac.ir
کد اخلاق: IR.TMI.REC.1402.011 |
چکیده سابقه و هدف استفاده از کنترل مثبت در آزمایشهای Real-Time PCR برای اطمینان از صحت آزمایش ضروری است که این کنترلها در حال حاضر عمدتاً از منابع بالینی تهیه میشوند. زمانی که دسترسی به نمونههای مثبت بیولوژیک فراهم نباشد استفاده از روش PCA یا Polymerase Cycle Assembly برای ساخت کنترل مثبت، راهگشا خواهد بود. هدف از این پژوهش تعیین کارآیی روش سنتز آنزیمی برای تولید قطعات DNA ژنومیک جهت کاربردهای بیولوژی مولکولی بود. تاکنون مطالعهای پیرامون بررسی کارآیی روش PCA به منظور تولید کنترل مثبت HSV-2 انجام نگرفته است و این روش عمدتاً برای مونتاژ توالی استفاده شده است. مواد و روشها اولین قدم در این مطالعه تجربی، طراحی قطعات همپوشان بود. ناحیهای در ژنوم HSV-2 که برای آن این قطعات طراحی شدند، ناحیهای منحصر به فرد به نام US6 بود. این ناحیه از طریق یک مطالعه گذشتهنگر انتخاب شد. سپس ساختارهای ثانویه و پارامترهای ترمودینامیکی قطعات همپوشان با نرمافزار AllelelD بررسی شد. با استفاده از نرم افزار MEGA نسخه 11، طراحی آغازگرها برای ناحیه ای منحصر به فرد در ژن US6 در ژنوم HSV-2 صورت گرفت. ژنوم HSV-2 با نرم افزار SnapGene مورد بررسی قرار گرفت. بررسی تکمیلی خود آغازگرها و محصول آنها از ساحتار ثانویه با MFold صورت گرفت. این نرمافزار، توالی که قرار است برای آغازگر طراحی شود از نظر ساختار ثانویه بررسی میکند. یافتهها با توجه به درجه بالای شباهت توالیهای HSV-1 و HSV-2 در بررسیهای هم ردیفی، با سختگیری شدید برای نواحی با بیشترین تفاوت طبیعی در محل ژن US6، آغازگر و قطعات همپوشان طراحی شد. نتایج بلاست برای محصول PCR در محیط in silico و حصول بالاترین امتیاز برای HSV-2 اختصاصیت آغازگرهای طراحی شده را تایید کرد. توسط نرمافزار SnapGene، اندازه قطعه تکثیر یافته در این مطالعه تخمین زده شد که برای مطالعههای بعدی 70 جفت باز باشد. نتیجه گیری نتایج حاصله نشان داد روش سنتتیک میتواند کیفیت مناسبی برای ساخت کنترل مثبت داشته باشد و در حقیقت در محیط in silico توالیهای طراحی شده به عنوان کنترل مثبت HSV-2 از منظر محتوای توالی مشابه با توالیهای طبیعی این ویروس بودند که این مهم نشان میدهد نتایج روش PCA معادل کاربرد کنترل بالینی مثبت است. کلمات کلیدی: الیگونوکلئوتیدها، Real-Time PCR ، هرپس ویروس 2 |
مقدمه
ساخت DNA سنتتیک که به طور عام به آن"سنتز ژن" اطلاق میشود، به فرآیند سنتز توالیهایی از DNA به طول 250 تا 2000 جفت باز از اولیگونوکلئوتیدهای تک رشتهای DNA سنتتیک اشاره دارد. این اولیگونوکلئوتیدها عمدتاً با استفاده از روشهای شیمیایی فسفرآمیدیت تولید میشوند و سپس با استفاده از روشهای مختلفی به ساختارهای بزرگ تر مونتاژ میگردند (1).
در میان روشهای موجود برای سنتز ژن، روش “Polymerase Cycle Assembly” به عنوان یک نوآوری برجسته شاخته میشود که میتواند جایگزین مناسبی برای روشهای سنتی باشد. روشهای قدیمیتر نظیر سنتز شیمیایی با محدودیتهایی در زمینه تولید کنترل مثبت مواجه هستند؛ به ویژه زمانی که طول قطعه مورد نظر بیشتر از 300 نوکلئوتید باشد، کارآیی این روشها کاهش مییابد. علاوه بر این، وابستگی به حلالهای آلی در این روشها میتواند تأثیرات منفی بر محیط زیست داشته باشد.
برای غلبه بر این محدودیتها و ساخت DNA با همان کارآیی که در خوانش DNA وجود دارد، تکنولوژیهای جایگزین توسعه یافتهاند و شامل مونتاژ مولکولی و روشهای کلونینگ، روش سنتز آنزیمی مستقل از الگو، میکروآرایه و تکثیر حلقه چرخان توسعه یافته میباشند (2). به طور کلی، پیشرفتهای اخیر در زمینه سنتز DNA سنتتیک، به ویژه با ظهور روشهای نوین مانند Polymerase Cycle Assembly، نه تنها کارآیی فرآیندها را افزایش داده بلکه به حفظ محیط زیست نیز کمک میکند.
به علت پتانسیل بالای کاربردهای سنتز اولیگونوکلئوتیدها در مقیاس وسیع، پیشرفتهای قابل توجهی در علوم تجربی، به ویژه در زمینههای زیستشناسی سنتتیک، مهندسی پروتئین، مهندسی ژنوم و مهندسی متابولیک حاصل شده است (3). با توجه به اندازه کوچک ویروسها و نقش حیاتی آنها در پیشرفت سلامت و بیوتکنولوژی، پیشرفتهای چشمگیری در سنتز ژنومهای ویروسی مشاهده شده است (4).
ویـروس هرپـس سیمپلکـس نـــوع ۲ (HSV-2) یکی از
عفونتهای منتقله از راه رابطه جنسی است که حدود ۴۹۱ میلیون نفر (13%) از افراد بین 15 تا 49 سال در سراسر جهان به آن مبتلا هستند (5). گزارشهای متعددی نشان میدهند که حضور DNA مرتبط با HSV در خون ممکن است رخ دهد؛ بنابراین، احتمال انتقال HSV از طریق محصولات خونی وجود دارد. با این حال، این پدیده محدود به عفونتهای اولیه است و در عفونتهای راجعه مشاهده نمیشود. از این رو، افرادی که دچار عفونت اولیه هستند باید اهدای خون را به تعویق بیندازد (6).
Real Time PCR یکی از روشهای اصلی برای تشخیص این عفونت و از پرکاربردترین روشها برای اندازهگیری بیان ژن است، زیرا دامنهای پویا و حساسیت مناسبی دارد و میتواند به طور اختصاصی برای هر توالی عمل کند (9-7). کنترلهای مثبت در PCR به عنوان یک اقدام تأییدی کیفی به کار میروند تا اطمینان حاصل شود که شرایط واکنش ( مواد و وضعیت چرخهها) به درستی عمل میکنند و نتایج منفی تنها به دلیل فقدان DNA هدف در نمونههای آزمایش است (10). تولید کنترلهای سنتتیک با استفاده از روش سنتز آنزیمی نیاز به کلونینگ یا تجهیزات خاص فراتر از وسایل آزمایشگاههای تشخیص مولکولی ندارد. این روش احتمال آلودگی یا گزارش اشتباه واکنشهای مثبت کاذب را به علت آلودگی با مواد کنترل مثبت کاهش میدهد (11). کنترلهای سنتتیک تولید شده با این روش در همه آزمایشهای تشخیص مولکولی و صرف نظر از این که ما ارگانیسم را داریم یا خیر به کار گرفته میشوند. از مزایای این روش میتوان سهولت، اختصاصیت و کارآیی بالای 11را متذکر شد اما در زمینه ساخت کنترل مثبت HSV-2 به طور کامل مورد بررسی قرار نگرفته است. با ذکر محدودیت در روشهای موجود، این پژوهش منجر به دقت تشخیصی بهتر و اعتبار در شناسایی HSV-2 شد. هدف ما از این پژوهش، اطمینان از دقت و قابل اعتماد بودن نتایج کنترلهای مثبت سنتز شده به روش آنزیمی در شناسایی HSV-2 نسبت به کنترلهای بالینی بود که در حال حاضر برای این ویروس موجود است. روش آنزیمی شامل ساخت قطعات DNA HSV-2دارای همپوشانی و مشابه با توالی DNA ویروسی است. برای سنتز آنزیمی قطعه DNA نیاز به مطالعههای in silico است بدین صورت که با مقایسه ژنوم ویروس HSV-1 و HSV-2 ، نقاط ثابت ژنوم ویروس HSV-2 جهت تعیین مکان سنتز ژن تعیین شود.
مواد و روشها
این پژوهش یک مطالعه تجربی بود.
در این پروژه استفاده از اطلاعات فردی انسانی یا استفاده از حیوان آزمایشگاهی وجود نداشت.
طراحی آغازگر با نرمافزار AlleleID :
فرآیند انتخاب ناحیه مناسب برای تفکیک سویههای هرپس عمدتاً به دلیل درجه شباهت توالیها در خانواده هرپس ویریده دشوار بود. استراتژی ما شامل شناسایی توالیهای حفاظت شدهای بود که نه تنها تفاوتها را میان تایپهای هرپس ویروس نشان دهند بلکه این ویروس را از دیگر ویروسهای هم خانواده و سایر DNA ویروسها تمیز دهد. در این ارتباط نخست با یک مطالعه گذشتهنگر به انتخاب ناحیهUS6 رسیدیم.
اولین مرحله در این پژوهش، طراحی آغازگر برای ناحیهای منحصر به فرد در ژن US6 در ژنوم HSV-2 بود. این تصمیم با استفاده از نرمافزار MEGA نسخه 11 صورت گرفت و با آن حداقل دو توالی مجزا از HSV-2 و HSV-1 که از NCBI گرفته شده بودند، مورد هم ردیفی قرار گرفتند. پس از وارد کردن توالیهای DNA در نرمافزار AlleleID نسخه 7 با توجه به الگوریتمهای پایه نرمافزار، آغازگرهای متعدد و پروب مناسب پیشنهاد شد. با این حال، تصمیم ما به کارگیری آغازگرها و پروب طراحی شده به صورت دستی به جای استفاده از پیشنهادهای نرمافزار مربوطه بود. از این نرمافزار برای بررسی ساختارهای ثانویه از جمله ساختارهای سنجاق سر، self-dimer و cross dimer با توجه به پارامترهای ترمودینامیکی مربوطه استفاده میشود. با توجه به انرژی آزاد گیبس (ΔG)، میزان انجامپذیری و پایداری ساختارهای ثانویه تعیین میشود.
بررسی ژنوم HSV-2 با نرمافزار SnapGene :
با انتخاب آغازگر جلوبرنده و معکوس در نرمافزار SnapGene ، اندازه قطعه تکثیر یافته در این مطالعه PCR in silico تخمین زده شد. با توجه به آغازگرها و با انتخاب simulate agarose gel در قسمت tools ، اندازه قطعه تکثیر یافته و موقعیت آن در ژل 2% تخمین زده شد.
نهایتاً محصول in silico PCR مورد جست و جوی بلاست برای اطمینان از اختصاصیت برای HSV-2 قرار گرفت. این عمل مکمل بلاست آغازگر است که در محیط SnapGene انجام گرفت؛ بدین صورت که با وارد کردن توالی آغازگر و انتخاب گزینه tools و اجرای بلاست برای آغازگرهای انتخاب شده، از اتصال اختصاصی آغازگر به ارگانیسم هدف اطمینان حاصل شد.
برای محصول in silico PCR نیز تمام نتایج گزارش شده مربوط به HSV-2 بودند. حتی زمانی که ارگانیسم HSV-1 در هم ردیفیNCBI انتخاب شد، هیچ نتیجهای برایin silico PCR گزارش نشد. توالی آغازگرها در جدول قابل مشاهده هستند (جدول 1). ترادف آغازگرهای HSV-2 نیز با استفاده از نرمافزار MEGA نسخه 11 و الگوریتمهای پایه نسبت به ژنوم ویروس HSV-1 و HSV-2 مورد بررسی multiple sequence alignment قرار گرفت.
بررسی تکمیلی ساختارهای ثانویه با نرمافزار MFold :
خود آغازگرها و محصول آنها از نظر ساختار ثانویه با MFold چک شدند.MFold یک ابزار تحت وب است که ساختار ثانویه توالیهای اسید نوکلئیک مانند DNA یا RNA را بر اساس ویژگیهای ترمودینامیکی پیشبینی میکند. در حقیقت، نرمافزار MFold توالی سکانسی را که قرار است برای آن آغازگر طراحی شود از نظر وجود ساختارهای ثانویه چک میکند.
بدین صورت که انواع پیچ و تابهای توالی را در فایلهای مختلف ارائه میدهد (یک توالی با حالتهای مختلف پیچ خوردگی). زمانی که پیچ خوردگی به ویژه در نواحی GC هدف زیاد باشد پیشنهاد میشود که برای PCR از بتائین استفاده شود. بتائین میزان تکثیر را در چنین نواحی بالا میبرد.

طراحی قطعات همپوشان برای کنترل مثبت HSV-2 :
در طراحـی قطعـات همپوشان ابتـدا باید به محل جفت آغازگرهای جلوبرنده و معکوس توجه کرد. محل قطعات دارای همپوشانی باید در مجاورت این دو باشد. طول این قطعات حدود 50 نوکلئوتید و دمای ذوب این قطعات در محل همپوشانی بهتر است حدود 66 درجه سانتیگراد باشد. در حدود 5-4 نوکلئوتید سر 3′ هر یک از قطعات از نظر درصد بازهای پورینی و پیریمیدینی میبایستی متناسب باشند.
یافتهها
طراحی آغازگر با نرمافزار AlleleID :
همان طور که در جدول 2 مشاهده میشود، امتیاز آغازگرهای پیشنهادی در نرمافزار AlleleID خوب تلقی شد. تنها در رشته antisense ساختار ثانویه self-dimer
مشاهده شد و این ساختار در رشته sense وجود نداشت (شکل 1). از آن جایی که مقدار انرژی لازم برای شکستن این ساختارها بیش از Kcal/moL 5- است (ΔG)، از منظر پایدارای، تشکیل این ساختار ثانویه قابل قبول است.
انرژی آزاد گیبس (ΔG)، انرژی لازم برای شکستن ساختار ثانویه میباشد و مقادیر بسیار منفی آن نشاندهنده تمایل بیشتر آغازگرها برای اتصال به یکدیگر است و چون این انرژی برای ساختار cross dimer در شکل 2، از kcal/moL6- بیشتر است، نشاندهنده قابل قبول بودن این پارامتر میباشد (شکل 2).
با انتخاب آغازگر جلوبرنده و معکوس در نرمافزار SnapGene ، اندازه قطعه تکثیر یافته در این مطالعه in silico PCR تخمین زده شد که میزان 70 جفت باز بود (شکل 3). توالی قطعات همپوشان با توجه به قطعه جلوبرنده و قطعه معکوس در جدول 3 آمده است.


قدم بعدی در این ارتباط ، تجزیه و تحلیل in silico آغازگرها و پروب در رابطه با ترادف متناظر میباشد. در این رابطه از نرمافزارSnap gene استفاده شد. علاوه بر تعیین موقعیت، تجزیه و تحلیلPCR حاصله در محیط in silico متناظر با واقعیت تعیین گردید. طول قطعات، محاسبه شده و تجزیه و تحلیل الکتروفورز حاصل از PCR مشخص شد. علاوه بر آن با استفاده از قابلیت این نرمافزار به انجام بلاست قطعه مورد نظر پرداخته شد.
نتیجه بلاست برای محصول PCR در شکل مشاهده میشود (شکل 4). همان طور که قابل رؤیت است، این نتایج همگی مربوط به HSV-2 بوده و محصول غیر اختصاصی با این آغازگرها شناسایی نمیشود.
بر مبنای اطلاعات موجود در Gene Bank ، نواحی ثبت شده از سویههای مختلف HSV-1 و HSV-2 انتخاب و مورد تجزیه و تحلیل multiple sequence alignment توسط نرمافزار Mega نسخه 11 و سرور ClustalW قرار داده شد. در شکل 5 نتیجه هم ردیفی در MEGA میان آغازگرهای جلوبرنده و معکوس با توجه به ژنوم HSV-1 و HSV-2 قابل رؤیت است. همان طور که قابل بررسی است، در جایگاه طراحی آغازگر، ژنوم این دو ویروس تفاوتهای اندکی دارند که از این مهم در طراحی آغازگر بهره گرفته شد.
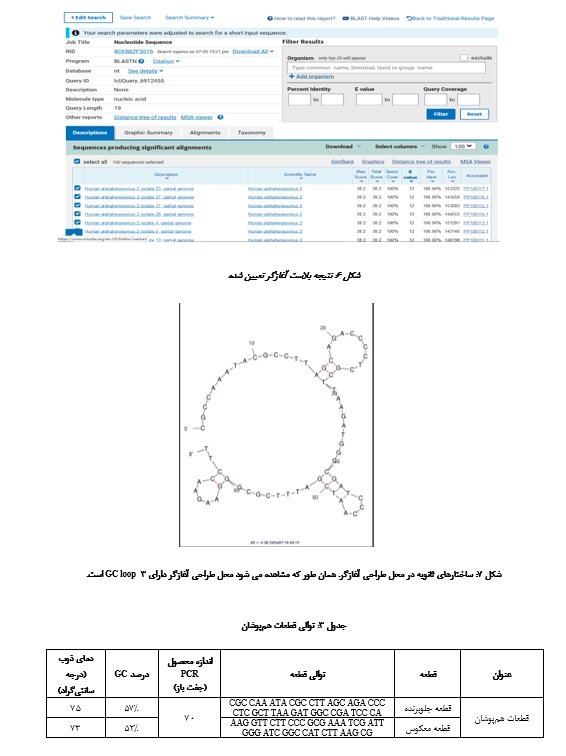
بررسیهای مدل ارائه شده تغییرات بسیار کمی را از خود نشان میداد و این مورد انتخاب را مشکل مینمود؛ به طوری که در نتایج قابل مشاهده است، میزان تغییرات از درصد کمی بین دو گونه ویروس برخوردار بود. بر این اساس هنگام طراحی آغازگر و پروبهای موجود، بیشتر توجه به تغییرات در سمت 3’ آغازگرها و پروب معطوف گردید. این مورد اختصاصیت و تمایز بین دو گونه را به بالاترین حد خود رسانید به طوری که هنگامی که ترادفها مورد تجزیه و تحلیل BLAST قرار میگرفتند نتیجه نوع alignment در مورد HSV-2 با بالاترین امتیاز کاملاً مشخص بود (شکل 6).
همانطور که در نتیجه بلاست قابل مشاهده است، آغازگر طراحی شده صرفاً HSV-2 را شناسایی کرد و طبق این نتیجه، آغازگر جایگاه اتصال غیر اختصاصی در ارگانیسمهای دیگر نداشت.
بررسی تکمیلی ساختارهای ثانویه با MFold :
همان طور که در شکل 7 مشاهده میشود، تعداد 3GC loop در محصول PCR پیشبینی میشود که برای جلوگیری از تشکیل آنها در شرایط آزمایشگاه پیشنهاد شد که از بتائین استفاده شود.
نتیجه بلاست برای محصول PCR در شکل مشاهده میشود (شکل 4). همان طور که قابل رؤیت است، این نتایج همگی مربوط به HSV-2 بوده و محصول غیر اختصاصی با این آغازگرها شناسایی نمیشود.
بر مبنای اطلاعات موجود در Gene Bank ، نواحی ثبت شده از سویههای مختلف HSV-1 و HSV-2 انتخاب و مورد تجزیه و تحلیل multiple sequence alignment توسط نرمافزار Mega نسخه 11 و سرور ClustalW قرار داده شد. در شکل 5 نتیجه هم ردیفی در MEGA میان آغازگرهای جلوبرنده و معکوس با توجه به ژنوم HSV-1 و HSV-2 قابل رؤیت است. همان طور که قابل بررسی است، در جایگاه طراحی آغازگر، ژنوم این دو ویروس تفاوتهای اندکی دارند که از این مهم در طراحی آغازگر بهره گرفته شد.
بررسیهای مدل ارائه شده تغییرات بسیار کمی را از خود نشان میداد و این مورد انتخاب را مشکل مینمود؛ به طوری که در نتایج قابل مشاهده است، میزان تغییرات از درصد کمی بین دو گونه ویروس برخوردار بود. بر این اساس هنگام طراحی آغازگر و پروبهای موجود، بیشتر توجه به تغییرات در سمت 3’ آغازگرها و پروب معطوف گردید. این مورد اختصاصیت و تمایز بین دو گونه را به بالاترین حد خود رسانید به طوری که هنگامی که ترادفها مورد تجزیه و تحلیل BLAST قرار میگرفتند نتیجه نوع alignment در مورد HSV-2 با بالاترین امتیاز کاملاً مشخص بود (شکل 6).
همانطور که در نتیجه بلاست قابل مشاهده است، آغازگر طراحی شده صرفاً HSV-2 را شناسایی کرد و طبق این نتیجه، آغازگر جایگاه اتصال غیر اختصاصی در ارگانیسمهای دیگر نداشت.
بررسی تکمیلی ساختارهای ثانویه با MFold :
همان طور که در شکل 7 مشاهده میشود، تعداد 3GC loop در محصول PCR پیشبینی میشود که برای جلوگیری از تشکیل آنها در شرایط آزمایشگاه پیشنهاد شد که از بتائین استفاده شود.


بحث
هدف این مطالعه ساخت قطعات اولیگونوکلئوتیدی بود که به عنوان اجزای کلیدی سنتز ژن استفاده میشود. از کاربردهای سنتز قطعات اولیگونوکلئوتیدی، تولید کالیبراتورها برای واکنشهای کمی PCR (qPCR)، ساخت عناصر ژنتیکی پایه برای مهندسی ژنتیک و بهبود ویژگیهای مورد نظر یک آنزیم یا پروتئین و تولید RNA antisense به منظوردرمان ناهنجاریهای اسکلتی و .. میباشد. با توجه به بررسیهای in silico ، روش PCA در تولید کنترل مثبت HSV-2 نتایج قابل قبولی به ارمغان آورد. این امر میتواند پایه پیشرفت در بیولوژی سنتتیک با انقلاب در تشخیصهای مولکولی از طریق فراهمسازی سنتز دقیق و قابل اعتماد کنترلهای مثبت شود. در مقاله هیوز و همکاران نقش حیاتی مونتاژ DNA سنتتیک در این پیشرفتها برجسته شده است. در این مطالعه روشهای متعددی برای سنتز DNA سنتتیک از جمله ترکیب روشهای شیمیایی مانند روش microarray و روش آنزیمی برای اصلاح خطا بیان شده است (1). به علاوه به روشهای مونتاژ از جمله انواع PCA (Polymerase Chain Assembly) به عنوان پرکاربردترین روش برای ساخت قطعات بزرگ اولیگونوکلئوتیدی اشاره شده است. بر این اساس مطالعه ما کاربردPolymerase Cycle Assembly را برای سنتز کنترلهای مثبت HSV-2 در تجزیه و تحلیلهای مولکولی بررسی میکند. یافتههای ما نشان داد که در مطالعههای in silico روش PCA جایگزینی قدرتمند برای سنتز کنترلهای مثبت HSV-2 است؛ به ویژه در شرایط محدود از نظر منابع که دسترسی و هزینه معقول به صرفه حیاتی هستند.
در مقاله ترمات و همکاران از روش PCA Integrated برای ساخت کنترل مثبت استفاده شد که این مطالعه دارای شرایط بهینه نظیر زمان آنیلینگ کوتاه، Thermal cycler های سریع و غلظتهای اندک اولیگو (حدود 10-5 نانومولار) بود (12). این پارامترها مونتاژ همزمان و تکثیر ژن را تسهیل مینمایند. نقطه تلاقی این پژوهش با پژوهش ما موفقیت در طراحی اولیگو و شرایط بهینه واکنش است که برای هریک منحصر به فرد میباشد. تأکید مقاله ترمات بر اهمیت تنظیم غلظت اولیگو برای توالیهای طویلتر ژنی یا زمان به کارگیری تعداد بیشتری از قطعات اولیگـو اســت.
لذا از این روش به دلیل رقابت آغـازگرهـا و misannealing برای ساخت قطعات ژن طویلتر کمتر استفاده میشود. با توجه به اندازه کوچک کنترل مثبت طراحی شده در پژوهش ما، چنین چالشی که در سنتز توالیهای طویل ژنی وجود دارد، در بخش آزمایشگاهی پژوهش ما دیده نخواهد شد.
در مقاله هوز و همکاران شکاف تکنولوژی برای ساخت توالیهای طویلDNA بحث میشود که منعکسکننده چالشهای مونتاژ برای ساخت کنترلهای دقیق است که این با کاربرد PCA به عنوان روشی نوین همراستا میباشد (2). به علاوه قابلیت دسترسی نیز به طور غیر مستقیم توان روش PCA را در بیولوژی سنتتیک به منظور کاهش پیچیدگی ذکر شده تایید میکند. کاربرد مطالعه ما به طور خاص محدود به حوزه تشخیص ذکر شده است در حالی که در مقاله هوز این کاربردها گستردهتر بوده و روند روشهای سنتز DNA و رقابت تجاری آنها بیان شده است. در حقیقت مطالعه ما مثالی از یک راه حل هدفمند برای مشکلی در زمینهای گستردهتر است.
در مقاله چن و همکاران برای شناسایی HSV-2 از جفت آغازگرهایی استفاده شد که UL52 را شناسایی میکردند اما در مقاله ما جفت آغازگرها برای شناسایی US6 طراحی شده بود (13). ناحیه UL52 در همانندسازی این ویروس دخالت دارد و در چرخه ویروس ضروری است. آغازگرهای طراحی شده برای این ناحیه فعالیت ویروس و نشانههای همانندسازی را شناسایی میکند. در حالی که US6 گلیکوپروتئین D را کد میکند که نقشی حیاتی در ورود ویروس به سلولهای میزبان دارد و هدف واکسنها و مداخلات درمانی است. هر جفت آغازگر با موفقیت HSV-2 را شناسایی میکنند اما انتخاب ناحیه هدف، حساسیت و اختصاصیت روش تشخیصی را تحت تاثیر قرار میدهد. ناحیه US6 در مکانیسمهای گریز سیستم ایمنی به درک پاتوژنیسیتی ویروس و تعاملات آن با سیستم ایمنی میزبان کمک میکند. به نظر میرسد که تفاوتهای دو ویروس HSV-1 و HSV-2 در US6 هنگام بررسی Alignment بیشتر بوده و لذا توان افتراقی این ناحیه برای طراحی آغازگر و پروب احتمالاً بهتر است.
از محدودیتهای این پژوهش عدم دسترسی به نرمافزارهای گران قیمت بیوانفورماتیکی نظیرDNASTAR Lasergene Suite میباشد که یک پکیج کامل بـرای مونتـاژ
توالیها، هم ردیفی و تجزیه و تحلیل آنهاست.
پیشنهاد میشود این پژوهش با تمرکز بر طراحی کنترل
مثبت دیگر پاتوژنها از جمله non-tuberclosis mycobacteria و حتی کنترل مثبت سرطانها ادامه یابد.
نتیجهگیری
طبق بررسیهای in silico کنترلهای مثبتی که با روش PCA طراحی شدند، از منظر طول قطعه و محتوای توالی قابل مقایسه با کنترلهای طبیعی بودند. در ساخت کنترل مثبت طویلتر با این روش، تنظیم غلظت قطعات همپوشان حائز اهمیت بود اما با توجه به اندازه کوچک کنترل مثبت در پژوهش ما، این چالش برای این اندازه از قطعات پررنگ نیست. لذا به نظر میرسد که در شرایطی که دسترسی به نمونه بالینی فراهم نباشد میتوان از نمونه سنتتیک استفاده کرد.
حمایت مالی
این پروژه توسط مرکز تحقیقات انتقال خون مؤسسه عالی آموزشی و پژوهشی طب انتقال خون تأمین مالی شده است.
ملاحظات اخلاقی
مطالعه حاضر دارای کد اخلاق IR.TMI.REC.1402.011 از کمیته اخلاق مؤسسه عالی آموزشی و پژوهشی طب انتقال خون تهران ، ایران است.
عدم تعارض منافع
نویسندگان اظهار میکنند هیچگونه تعارض منافعی در این مطالعه وجود نداشته است.
نقش نویسندگان
زهرا شریف زندیه: نگارش مقاله و انجام آزمایشها
شهرام سمیعی: ایده مقاله و نظارت بر انجام مطالعه و نگارش مقاله
دکتر کامران موسوی حسینی: ایده مقاله و نظارت بر نگارش مقاله
زهره شریفی: ایده مقاله و نظارت بر نگارش مقاله
تشکر و قدردانی
بدینوسیله نویسندگان مقاله از مؤسسه عالی آموزشی و پژوهشی طب انتقال خون به جهت تأمین هزینهها تشکر و قدردانی مینمایند.
نوع مطالعه: پژوهشي |
موضوع مقاله:
بيوتكنولوژي
فهرست منابع
1. Hughes RA, Ellington AD. Synthetic DNA Synthesis and Assembly: Putting the Synthetic in Synthetic Biology. Cold Spring Harb Perspect Biol. 2017 Jan 3;9(1):a023812. [DOI:10.1101/cshperspect.a023812] [PMID] []
2. Hoose A, Vellacott R, Storch M, Freemont PS, Ryadnov MG. Publisher Correction: DNA synthesis technologies to close the gene writing gap. Nat Rev Chem. 2023 Aug;7(8):590. [DOI:10.1038/s41570-022-00456-9] [PMID] []
3. Song LF, Deng ZH, Gong ZY, Li LL, Li BZ. Large-Scale de novo Oligonucleotide Synthesis for Whole-Genome Synthesis and Data Storage: Challenges and Opportunities. Front Bioeng Biotechnol. 2021 Jun 22;9:689797. [DOI:10.3389/fbioe.2021.689797] [PMID] []
4. Cello J, Paul AV, Wimmer E. Chemical synthesis of poliovirus cDNA: generation of infectious virus in the absence of natural template. Science. 2002 Aug 9;297(5583):1016-8. https://doi.org/ 10.1126/science.1072266 [DOI:10.1126/science.1072266] [PMID]
5. Herpes: HSV1 and HSV2. https://www.hopkinsmedicine.org/health/conditions-and-diseases/herpes-hsv1-and-hsv2#:~:text=In%20the%20case%20of%20HSV,is%20active%20at%20that%20time.
6. Juhl D, Mosel C, Nawroth F, Funke AM, Dadgar SM, Hagenström H, et al. Detection of herpes simplex virus DNA in plasma of patients with primary but not with recurrent infection: implications for transfusion medicine? Transfus Med. 2010 Feb;20(1):38-47. [DOI:10.1111/j.1365-3148.2009.00951.x] [PMID]
7. Wong ML, Medrano JF. Real-time PCR for mRNA quantitation. Biotechniques. 2005 Jul;39(1):75-85. [DOI:10.2144/05391RV01] [PMID]
8. Han X, Beck K, Bürgmann H, Frey B, Stierli B, Frossard A. Synthetic oligonucleotides as quantitative PCR standards for quantifying microbial genes. Front Microbiol. 2023 Oct 24;14:1279041. [DOI:10.3389/fmicb.2023.1279041] [PMID] []
9. Kadkhodaei S, Rajabi Memari H, Abbasiliasi S, Akhavan Rezaei M, Movahedi A, Joo Shun T, et al. Multiple overlap extension PCR (MOE-PCR): an effective technical shortcut to high throughput synthetic biology. RSC Advances 2016;6(71):66682-66694. [DOI:10.1039/C6RA13172G]
10. Wilson CC, Wozney KM, Smith CM. Recognizing false positives: synthetic oligonucleotide controls for environmental DNA surveillance. Methods in Ecology and Evolution 2016;7(1):23-29. [DOI:10.1111/2041-210X.12452]
11. Borst A, Box AT, Fluit AC. False-positive results and contamination in nucleic acid amplification assays: suggestions for a prevent and destroy strategy. Eur J Clin Microbiol Infect Dis. 2004 Apr;23(4):289-99. [DOI:10.1007/s10096-004-1100-1] [PMID]
12. TerMaat JR, Pienaar E, Whitney SE, Mamedov TG, Subramanian A. Gene synthesis by integrated polymerase chain assembly and PCR amplification using a high-speed thermocycler. J Microbiol Methods. 2009 Dec;79(3):295-300. [DOI:10.1016/j.mimet.2009.09.015] [PMID] []
13. Chen Z, Zhao K, Tan B, Tong Z, He Z, Luo X, et al. Development of a high specificity typing method for the detection of herpes simplex virus. Front Bioeng Biotechnol. 2022 Aug 17;10:955713. [DOI:10.3389/fbioe.2022.955713] [PMID] []
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







