جلد 10، شماره 4 - ( زمستان 1392 )
جلد 10 شماره 4 صفحات 418-411 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Khatami S, Rouhi Dehnabeh S, Najmabadi H. Hemoglobin Q-Iran and the importance of using suitable laboratory screening methods-Case report. bloodj 2014; 10 (4) :411-418
URL: http://bloodjournal.ir/article-1-833-fa.html
URL: http://bloodjournal.ir/article-1-833-fa.html
خاتمی شهره، روحی دهنبه صغری، نجمآبادی حسین. هموگلوبین Q – ایران و اهمیت استفاده از روشهای آزمایشگاهی غربالگری مناسب جهت شناسایی آن . فصلنامه پژوهشی خون. 1392; 10 (4) :411-418
انستیتو پاستور ایران ـ تهران
متن کامل [PDF 410 kb]
(2491 دریافت)
| چکیده (HTML) (10788 مشاهده)
مقدمه
هموگلوبینوپاتیها یک دسته شایع از اختلالات هماتولوژیک در انسان میباشند که تاکنون بیشتر از یک صد نوع آن شناخته شده است. هموگلوبین S ، E ،DPunjab ، OArab و لپور از جمله شایعترین انواع این عارضه هستند که توارث آنها در فرمهای هموزیگوت و یا در الحاق با اشکال خاصی از تالاسمی، میتواند بیماریزا باشد. به دلیل ایجاد مشکلات جدی در سلامت مردم، غربالگری و تشخیص صحیح هموگلوبینوپاتیها از اهمیت ویژهای برخوردار است.
در بین هموگلوبینوپاتیها، نوع خاصی از هموگلوبین به نام هموگلوبین Q با آزمایش حلالیت منفی وجود دارد که در آن تغییر اسید آسپارتیک به هیستیدین در یکی از جایگاههای اسید آمینهای در زنجیره آلفا دیده میشود(3-1). انواع شناخته شده از این اختلال، هموگلوبینQ - هند (α64Asp→His)، هموگلوبین Q- تایلند (α74Asp→His)و هموگلوبین Q- ایران(α75Asp→His) میباشند که خانواده هموگلوبین Q را تشکیل میدهند(1)(شکل 1).

شکل 1: توالی اسیدهای آمینه انواع هموگلوبین Q
هموگلوبینوپاتی Qبیشتر به شکل هتروزیگوت به ارث میرسد و در آن تغییر بار الکتریکی ایجاد شده ناشی از تغییر اسید آمینه، تاثیری بر ویژگیهای مولکول هموگلوبین ندارد لذا تظاهرات بالینی خاص نیز دیده نمیشود(4). با این حال، گزارشهایی در زمینه تداخل آن در اندازهگیری هموگلوبین A1C در بیماران دیابتیک و همراهی آن با تالاسمی و هم چنین توارث نادر آن با بیماری هموگلوبین H ارایه شده است(7-4). به طور کلی در توارث همزمان α تالاسمی با هموگلوبین Q ، تولید زنجیره αQ بیشتر شده اما در توارث همزمان β تالاسمی با هموگلوبین Q ، تولید زنجیره αQ کاهش مییابد(9، 8).
روشهای تشخیص هموگلوبینوپاتیها در آزمایشگاههای ایران طبق روشهای غربالگری شامل الکتروفورز هموگلوبین بر روی استات سلولز در pH قلیایی، الکتروفورز روی سیترات آگار در pH اسیدی، آزمایش حلالیت و آزمایش ایزوپروپانول میباشند که باید با روشهای تاییدی مانند HPLC و کاپیلری زون الکتروفورزیس و بررسیهای مولکولی در سطح ژن، صحهگذاری شود. این روند در مورد تشخیص هموگلوبین Q- ایران نیز مصداق دارد یعنی با توجه به این که حرکت الکتروفورتیک هموگلوبین Q- ایران با هموگلوبین S روی استات سلولز مشابه میباشد، لذا جهت تشخیص صحیح آن باید الکتروفورز روی سیترات آگار و آزمایش حلالیت نیز انجام شود. اما در این میان باید نکاتی را هنگام تفسیر نتایج الکتروفورز روی سیترات آگار مد نظر داشت تا نتیجه مطلوب در امر تشخیص آزمایشگاهی حاصل شود. نویسندگان با گزارش مسایل به وجود آمده جهت تشخیص یک مورد هموگلوبینوپاتی که به آزمایشگاه تخصصی بیوسنتز زنجیرههای گلوبین ارجاع شده است، سعی خواهند نمود تا توجه دستاندرکاران آزمایشگاههای تشخیص طبی را به زوایای خاصی از نکات در تفسیر و تشخیص هموگلوبینوپاتی Q- ایران معطوف سازند.
مورد
در روند برنامه کشوری بررسی تالاسمی و هموگلوبینوپاتیها، خانمی 33 ساله از آزمایشگاه ژنتیک با در دست داشتن دو سری جواب آزمایش متفاوت از CBC و الکتروفورز هموگلوبین از دو آزمایشگاه مختلف، جهت ادامه روند تشخیص به آزمایشگاه بیوسنتز زنجیرههای گلوبین در انستیتو پاستور ایران معرفی گردید. در این آزمایشگاه، به عنوان آزمایشهای تکمیلی، آزمایش بیوسنتز زنجیرههای گلوبین با استفاده از ماده لوسین نشاندار و آنالیز زنجیرههای گلوبین با استفاده از دستگاه HPLC (ستون تعویض یونی) انجام شد(10). هم چنین آزمایشهای تکمیلی دیگر شامل تعیین درصد رتیکولوسیتها، بررسی مورفولوژی سلولهای قرمز، بررسی انکلوزیونهای هموگلوبین H و تعیین توالی نوکلئوتیدهای ژن آلفاگلوبین با استفاده از دستگاه ABI377 نیز برای بیمار انجام شد.
آزمایش بیوسنتز زنجیرههای گلوبین که با استفاده از خون محیطی جهت تشخیص انواع تالاسمی انجام میگیرد، از آن لحاظ ارزشمند است که میتواند بازده نهایی ژنهای گلوبین را نشان دهد(10). سلولهای قرمز افراد سالم و بالغ به نسبت مساوی از زنجیرههای α و like β (زنجیرههای شرکتکننده در ساختمان تترامر پروتئینی هموگلوبین) تولید میکنند. این روش برای تشخیص تالاسمی که یک نوع کم خونی همولیتیک میباشد، بسیار ارزشمند است زیرا در این اختلال، تولید یکی از دو نوع زنجیره شرکتکننده در ساختمان مولکول هموگلوبین کاهش مییابد(10). با توجه به این که این بیماری به صورت اتوزومال مغلوب به ارث میرسد، بسته به نوع و تعداد موتاسیون یا حذف روی ژن α یا β ، انواع مختلف α تالاسمی و یا β تالاسمی مشاهده میشود. برای آشکار کردن عدم تعادل در تولید زنجیرههای α و β ، رتیکولوسیتهای خون محیطی در شرایط مناسب محیط کشت و دما در مجاورت لوسین نشاندار با H3 قرار داده میشوند تا زنجیرههای جدید نشاندار شده تولید شوند. بدین ترتیب است که ردیابی زنجیرههای تازه ساخته شده امکانپذیر میگردد. برای تعیین نسبت α به β ، آنالیز زنجیرههای گلوبینی با استفاده از روش کروماتوگرافی انجام میشود. در مرحله آنالیز با استفاده از ستون تعویض یون، فراکشنهای مربوط به پیکهای α و β به صورت جداگانه جمعآوری میشود. با اضافه کردن مایع سنتیلاسیون، رادیواکتیویتی موجود در فراکشنهای ذکر شده به وسیله دستگاه β کانتر(1409 Wallac) اندازهگیری میشود. در پایان از تقسیم مجموع رادیواکتیویتی موجود در ناحیه باند α به مجموع رادیواکتیویتی موجود در ناحیه باند β ، نسبت α به β محاسبه میگردد. لازم به ذکر است جهت تشخیص هموگلوبینوپاتیها نیازی به انجام مرحله بیوسنتز نمیباشد و آنالیز همولیزیت با دستگاه HPLC میتواند در تشخیص نوع هموگلوبینوپاتی کمککننده باشد. انجام آزمایش بیوسنتز زنجیرههای گلوبین برای فرد مطرح شده در ایـن مقالـه به درخواست پزشک متخصص ژنتیک و به دلیل سرگردان بودن بیش از اندازه بیمار جهت تشخیص نهایی انجام شده است.
نتایج آزمایش CBC و الکتروفورز هموگلوبین بیمار و تشخیص نهایی اعلام شده از دو آزمایشگاه مختلف معتبر در جدول 1 نشان داده شده است. در این جدول عدم انجام الکتروفورز روی سیترات آگار در pH اسیدی توسط آزمایشگاه اول و عدم انجام آزمایش حلالیت توسط آزمایشگاه دوم گزارش شده است. به همین علت برای بیمار وجود دو نوع هموگلوبینوپاتی مختلف، هموگلوبینوپاتی S و هموگلوبینوپاتی D/G مطرح گردیده است. در آزمایشگاه ژنتیک با انجام آزمایش تعیین توالی نوکلئوتیدها، وجود هموگلوبین Dبه اثبات نرسیده بود.
جدول 1: اطلاعات هماتولوژیک بیمار از دو آزمایشگاه مختلف
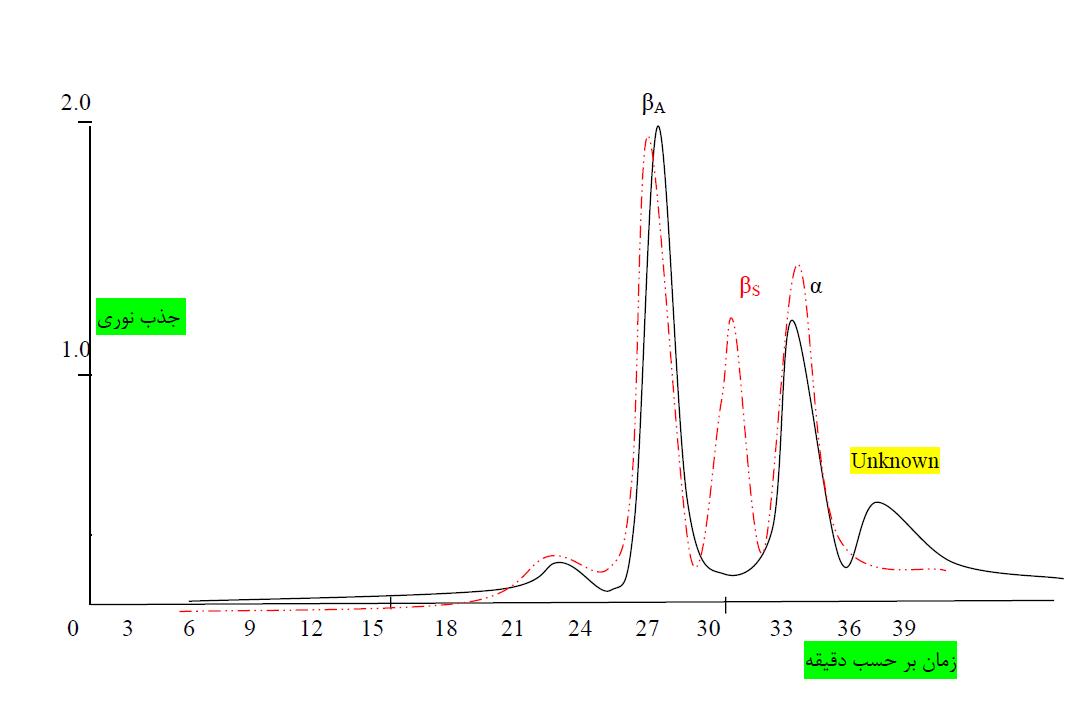
شکل 2: مقایسه کروماتوگرام زنجیرههای گلوبین بیمار(خط ممتد) با کروماتوگرام نمونه کنترل با هموگلوبینوپاتی S (خط نقطه چین) βA : زنجیره β ـ گلوبین مربوط به هموگلوبین A ، βS : زنجیره β - گلوبین مربوط به هموگلوبین S، α : زنجیره α - گلوبین مربوط به هموگلوبین A و S ، Unknown: زنجیره ناشناخته گلوبین مربوط به هموگلوبینوپاتی فرد مورد مطالعه
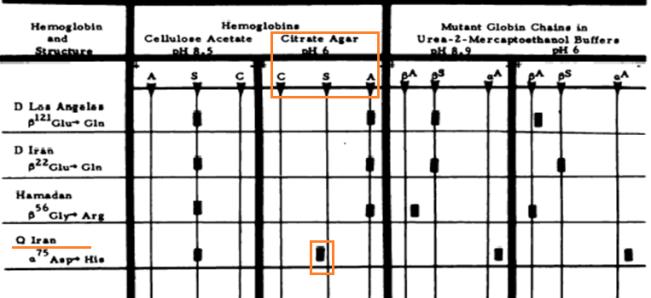
شکل 3: هموگلوبین Q – ایران از نظر حرکت الکتروفورتیک روی سیترات آگار(11)
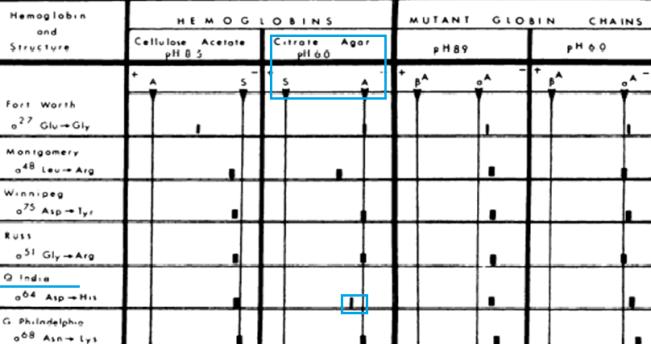
شکل 4: هموگلوبین Q – هند از نظر حرکت الکتروفورتیک روی سیترات آگار(11)
متن کامل: (3388 مشاهده)
هموگلوبین Q – ایران و اهمیت استفاده از روشهای آزمایشگاهی غربالگری
مناسب جهت شناسایی آن
شهره خاتمی1، صغری روحی دهنبه2، حسین نجمآبادی3
چکیده
سابقه و هدف
استفاده از روشهای مناسب آزمایشگاهی جهت تشخیص هموگلوبینوپاتیها، در آزمایشگاههایی که مجهز به سیستمهای اتوماتیک نیستند، بسیار ضروری است. در میان هموگلوبینوپاتیها، تشخیص صحیح هموگلوبین Q- ایران ((α75Asp→His اهمیت خاصی دارد.
مورد
خانمی 33 ساله از آزمایشگاه ژنتیک جهت تشخیص نهایی به آزمایشگاه مرجع کشوری بیوسنتز زنجیرههای گلوبین معرفی گردید. در بررسی کروماتوگرام زنجیرههای گلوبین، باند زنجیرهای ناشناخته با باند زنجیره βD و βS مطابقت نداشت. در بررسی تعیین توالی نوکلئوتیدها، هموگلوبینوپاتی بیمار از نوع هموگلوبین Q- ایران تعیین گردید.
نتیجه گیری
آزمایشگاههای تشخیص پزشکی که به سیستمهای اتوماتیک مدرن مجهز نیستند، بعد از الکتروفورز هموگلوبین روی استات سلولز در pH قلیایی و مشاهده باند در محدوده هموگلوبین Sو D/G ، باید هر دو آزمایش حلالیت و الکتروفورز روی سیترات آگار را به عنوان آزمون تکمیلی اجرا نمایند.
کلمات کلیدی: هموگلوبین Q، هموگلوبینوپاتی ها، غربالگری، ایران
تاریخ دریافت : 27/10/91
تاریخ پذیرش : 24/4 /92
1- PhD بیوشیمی ـ دانشیار انستیتو پاستور ایران ـ بخش بیوشیمی ـ تهران ـ ایران
2- مؤلف مسؤول: دکترای علوم آزمایشگاهی ـ انستیتو پاستور ایران ـ تهران ـ خیابان پاستور ـ خیابان 12 فروردین ـ پلاک 358 ـ ایران ـ کدپستی: 1316943551
3- PhD ژنتیک انسانی ـ استاد مرکز تحقیقات ژنتیک دانشگاه علوم بهزیستی و توانبخشی ـ تهران ـ ایران
مناسب جهت شناسایی آن
شهره خاتمی1، صغری روحی دهنبه2، حسین نجمآبادی3
چکیده
سابقه و هدف
استفاده از روشهای مناسب آزمایشگاهی جهت تشخیص هموگلوبینوپاتیها، در آزمایشگاههایی که مجهز به سیستمهای اتوماتیک نیستند، بسیار ضروری است. در میان هموگلوبینوپاتیها، تشخیص صحیح هموگلوبین Q- ایران ((α75Asp→His اهمیت خاصی دارد.
مورد
خانمی 33 ساله از آزمایشگاه ژنتیک جهت تشخیص نهایی به آزمایشگاه مرجع کشوری بیوسنتز زنجیرههای گلوبین معرفی گردید. در بررسی کروماتوگرام زنجیرههای گلوبین، باند زنجیرهای ناشناخته با باند زنجیره βD و βS مطابقت نداشت. در بررسی تعیین توالی نوکلئوتیدها، هموگلوبینوپاتی بیمار از نوع هموگلوبین Q- ایران تعیین گردید.
نتیجه گیری
آزمایشگاههای تشخیص پزشکی که به سیستمهای اتوماتیک مدرن مجهز نیستند، بعد از الکتروفورز هموگلوبین روی استات سلولز در pH قلیایی و مشاهده باند در محدوده هموگلوبین Sو D/G ، باید هر دو آزمایش حلالیت و الکتروفورز روی سیترات آگار را به عنوان آزمون تکمیلی اجرا نمایند.
کلمات کلیدی: هموگلوبین Q، هموگلوبینوپاتی ها، غربالگری، ایران
تاریخ دریافت : 27/10/91
تاریخ پذیرش : 24/4 /92
1- PhD بیوشیمی ـ دانشیار انستیتو پاستور ایران ـ بخش بیوشیمی ـ تهران ـ ایران
2- مؤلف مسؤول: دکترای علوم آزمایشگاهی ـ انستیتو پاستور ایران ـ تهران ـ خیابان پاستور ـ خیابان 12 فروردین ـ پلاک 358 ـ ایران ـ کدپستی: 1316943551
3- PhD ژنتیک انسانی ـ استاد مرکز تحقیقات ژنتیک دانشگاه علوم بهزیستی و توانبخشی ـ تهران ـ ایران
مقدمه
هموگلوبینوپاتیها یک دسته شایع از اختلالات هماتولوژیک در انسان میباشند که تاکنون بیشتر از یک صد نوع آن شناخته شده است. هموگلوبین S ، E ،DPunjab ، OArab و لپور از جمله شایعترین انواع این عارضه هستند که توارث آنها در فرمهای هموزیگوت و یا در الحاق با اشکال خاصی از تالاسمی، میتواند بیماریزا باشد. به دلیل ایجاد مشکلات جدی در سلامت مردم، غربالگری و تشخیص صحیح هموگلوبینوپاتیها از اهمیت ویژهای برخوردار است.
در بین هموگلوبینوپاتیها، نوع خاصی از هموگلوبین به نام هموگلوبین Q با آزمایش حلالیت منفی وجود دارد که در آن تغییر اسید آسپارتیک به هیستیدین در یکی از جایگاههای اسید آمینهای در زنجیره آلفا دیده میشود(3-1). انواع شناخته شده از این اختلال، هموگلوبینQ - هند (α64Asp→His)، هموگلوبین Q- تایلند (α74Asp→His)و هموگلوبین Q- ایران(α75Asp→His) میباشند که خانواده هموگلوبین Q را تشکیل میدهند(1)(شکل 1).

شکل 1: توالی اسیدهای آمینه انواع هموگلوبین Q
هموگلوبینوپاتی Qبیشتر به شکل هتروزیگوت به ارث میرسد و در آن تغییر بار الکتریکی ایجاد شده ناشی از تغییر اسید آمینه، تاثیری بر ویژگیهای مولکول هموگلوبین ندارد لذا تظاهرات بالینی خاص نیز دیده نمیشود(4). با این حال، گزارشهایی در زمینه تداخل آن در اندازهگیری هموگلوبین A1C در بیماران دیابتیک و همراهی آن با تالاسمی و هم چنین توارث نادر آن با بیماری هموگلوبین H ارایه شده است(7-4). به طور کلی در توارث همزمان α تالاسمی با هموگلوبین Q ، تولید زنجیره αQ بیشتر شده اما در توارث همزمان β تالاسمی با هموگلوبین Q ، تولید زنجیره αQ کاهش مییابد(9، 8).
روشهای تشخیص هموگلوبینوپاتیها در آزمایشگاههای ایران طبق روشهای غربالگری شامل الکتروفورز هموگلوبین بر روی استات سلولز در pH قلیایی، الکتروفورز روی سیترات آگار در pH اسیدی، آزمایش حلالیت و آزمایش ایزوپروپانول میباشند که باید با روشهای تاییدی مانند HPLC و کاپیلری زون الکتروفورزیس و بررسیهای مولکولی در سطح ژن، صحهگذاری شود. این روند در مورد تشخیص هموگلوبین Q- ایران نیز مصداق دارد یعنی با توجه به این که حرکت الکتروفورتیک هموگلوبین Q- ایران با هموگلوبین S روی استات سلولز مشابه میباشد، لذا جهت تشخیص صحیح آن باید الکتروفورز روی سیترات آگار و آزمایش حلالیت نیز انجام شود. اما در این میان باید نکاتی را هنگام تفسیر نتایج الکتروفورز روی سیترات آگار مد نظر داشت تا نتیجه مطلوب در امر تشخیص آزمایشگاهی حاصل شود. نویسندگان با گزارش مسایل به وجود آمده جهت تشخیص یک مورد هموگلوبینوپاتی که به آزمایشگاه تخصصی بیوسنتز زنجیرههای گلوبین ارجاع شده است، سعی خواهند نمود تا توجه دستاندرکاران آزمایشگاههای تشخیص طبی را به زوایای خاصی از نکات در تفسیر و تشخیص هموگلوبینوپاتی Q- ایران معطوف سازند.
مورد
در روند برنامه کشوری بررسی تالاسمی و هموگلوبینوپاتیها، خانمی 33 ساله از آزمایشگاه ژنتیک با در دست داشتن دو سری جواب آزمایش متفاوت از CBC و الکتروفورز هموگلوبین از دو آزمایشگاه مختلف، جهت ادامه روند تشخیص به آزمایشگاه بیوسنتز زنجیرههای گلوبین در انستیتو پاستور ایران معرفی گردید. در این آزمایشگاه، به عنوان آزمایشهای تکمیلی، آزمایش بیوسنتز زنجیرههای گلوبین با استفاده از ماده لوسین نشاندار و آنالیز زنجیرههای گلوبین با استفاده از دستگاه HPLC (ستون تعویض یونی) انجام شد(10). هم چنین آزمایشهای تکمیلی دیگر شامل تعیین درصد رتیکولوسیتها، بررسی مورفولوژی سلولهای قرمز، بررسی انکلوزیونهای هموگلوبین H و تعیین توالی نوکلئوتیدهای ژن آلفاگلوبین با استفاده از دستگاه ABI377 نیز برای بیمار انجام شد.
آزمایش بیوسنتز زنجیرههای گلوبین که با استفاده از خون محیطی جهت تشخیص انواع تالاسمی انجام میگیرد، از آن لحاظ ارزشمند است که میتواند بازده نهایی ژنهای گلوبین را نشان دهد(10). سلولهای قرمز افراد سالم و بالغ به نسبت مساوی از زنجیرههای α و like β (زنجیرههای شرکتکننده در ساختمان تترامر پروتئینی هموگلوبین) تولید میکنند. این روش برای تشخیص تالاسمی که یک نوع کم خونی همولیتیک میباشد، بسیار ارزشمند است زیرا در این اختلال، تولید یکی از دو نوع زنجیره شرکتکننده در ساختمان مولکول هموگلوبین کاهش مییابد(10). با توجه به این که این بیماری به صورت اتوزومال مغلوب به ارث میرسد، بسته به نوع و تعداد موتاسیون یا حذف روی ژن α یا β ، انواع مختلف α تالاسمی و یا β تالاسمی مشاهده میشود. برای آشکار کردن عدم تعادل در تولید زنجیرههای α و β ، رتیکولوسیتهای خون محیطی در شرایط مناسب محیط کشت و دما در مجاورت لوسین نشاندار با H3 قرار داده میشوند تا زنجیرههای جدید نشاندار شده تولید شوند. بدین ترتیب است که ردیابی زنجیرههای تازه ساخته شده امکانپذیر میگردد. برای تعیین نسبت α به β ، آنالیز زنجیرههای گلوبینی با استفاده از روش کروماتوگرافی انجام میشود. در مرحله آنالیز با استفاده از ستون تعویض یون، فراکشنهای مربوط به پیکهای α و β به صورت جداگانه جمعآوری میشود. با اضافه کردن مایع سنتیلاسیون، رادیواکتیویتی موجود در فراکشنهای ذکر شده به وسیله دستگاه β کانتر(1409 Wallac) اندازهگیری میشود. در پایان از تقسیم مجموع رادیواکتیویتی موجود در ناحیه باند α به مجموع رادیواکتیویتی موجود در ناحیه باند β ، نسبت α به β محاسبه میگردد. لازم به ذکر است جهت تشخیص هموگلوبینوپاتیها نیازی به انجام مرحله بیوسنتز نمیباشد و آنالیز همولیزیت با دستگاه HPLC میتواند در تشخیص نوع هموگلوبینوپاتی کمککننده باشد. انجام آزمایش بیوسنتز زنجیرههای گلوبین برای فرد مطرح شده در ایـن مقالـه به درخواست پزشک متخصص ژنتیک و به دلیل سرگردان بودن بیش از اندازه بیمار جهت تشخیص نهایی انجام شده است.
نتایج آزمایش CBC و الکتروفورز هموگلوبین بیمار و تشخیص نهایی اعلام شده از دو آزمایشگاه مختلف معتبر در جدول 1 نشان داده شده است. در این جدول عدم انجام الکتروفورز روی سیترات آگار در pH اسیدی توسط آزمایشگاه اول و عدم انجام آزمایش حلالیت توسط آزمایشگاه دوم گزارش شده است. به همین علت برای بیمار وجود دو نوع هموگلوبینوپاتی مختلف، هموگلوبینوپاتی S و هموگلوبینوپاتی D/G مطرح گردیده است. در آزمایشگاه ژنتیک با انجام آزمایش تعیین توالی نوکلئوتیدها، وجود هموگلوبین Dبه اثبات نرسیده بود.
جدول 1: اطلاعات هماتولوژیک بیمار از دو آزمایشگاه مختلف
| شماره آزمایشگاه متغیر |
1 | 2 |
| گلبول قرمز(mili/mm3) | 61/4 | 86/4 |
| هموگلوبین (g/dL) | 40/12 | 40/13 |
| هماتوکریت(%) | 50/35 | 40/40 |
| MCV(fL) | 00/77 | 10/83 |
| MCH(pg) | 90/26 | 10/28 |
| MCHC(g/dL) | 90/34 | 80/33 |
| هموگلوبین A (%) | 20/78 | 00/81 |
| هموگلوبین A2 (%) | 40/2 | 80/2 |
| هموگلوبین F (%) | 00/1 | 20/0 |
| هموگلوبین D/G (%) | 40/18 | - |
| هموگلوبین S (%) | - | 00/16 |
| آهن تام (ug/dL) | - | 00/53 |
| TIBC(ug/dL) | - | 00/362 |
| نتیجه آزمایش حلالیت | منفی | انجام نشده است |
| نتایج الکتروفورز سیترات آگار | انجام نشده است | گزارش HbS |
| گزارش نهایی آزمایشگاه | هموگلوبینوپاتی D/G | هموگلوبینوپاتی S |

شکل 2: مقایسه کروماتوگرام زنجیرههای گلوبین بیمار(خط ممتد) با کروماتوگرام نمونه کنترل با هموگلوبینوپاتی S (خط نقطه چین) βA : زنجیره β ـ گلوبین مربوط به هموگلوبین A ، βS : زنجیره β - گلوبین مربوط به هموگلوبین S، α : زنجیره α - گلوبین مربوط به هموگلوبین A و S ، Unknown: زنجیره ناشناخته گلوبین مربوط به هموگلوبینوپاتی فرد مورد مطالعه
نتایج آزمایشهای تکمیلی در آزمایشگاه بیوسنتز زنجیرههای گلوبین نشان داد که شمارش رتیکولوسیـت بیمـار 8/0% است و سلولهای قرمز مورفولوژی میکروسیتوز- آنیزوسیتـوز خفیف داشتـه و در رنگآمیـزی اختصاصی نمونه خون بیمار با برلیانت کرزول بلو، انکلوزیونهای هموگلوبین H مشاهده نگردید. با توجه به وجود تناقض در زمینه تشخیص وضعیت نهایی بیمار، جداسازی زنجیرههای گلوبین توسط روش کروماتوگرافی تعویض یون انجام گرفت، در بررسی کروماتوگرام حاصله مشخص گردید که بیمار دو باند زنجیرهای β و α و یک باند زنجیرهای ناشناخته دارد به طوری که باند زنجیره ناشناخته بعد از باند زنجیره α قرار گرفته بود( شکل 2). با مقایسه کروماتوگرام به دست آمده از آنالیز نمونه بیمار با نمونه کنترل(هموگلوبینوپاتی S و هموگلوبینوپاتی D)، مشاهده گردید که باند زنجیره ناشناخته با باند زنجیرههای βS وβD مطابقت نداشته و به این ترتیب مشخص گردید که هموگلوبینوپاتی بیمار از نوع هموگلوبین S و هموگلوبین D نمیباشد. با توجه به این که آزمایشگاه ژنتیـک وجـود هموگلوبین D را نیز با استفاده از روشهای
مولکولی تایید نکرده بود، لذا جهت تعیین وضعیت نهایی بیمار، ضرورت انجام آزمایش تعیین توالی نوکلئوتیدها در ژن α گلوبین اعلام گردید.
در آزمایشگاه ژنتیک با انجام آزمایش تعیین توالی نوکلئوتیدها به صورت اتوماتیک با استفاده از دستگاه 377ABI ، مشخص گردید که موتاسیونی به صورت تغییر GAC>CAC ؛ c.226G>C در کدون 75 در ژن α به صورت هتروزیگوت وجود داشته که در قسمت EF4 به صورت تغییر اسید آمینه اسید آسپارتیک به هیستیدین، سبب تولید یک نوع نادر از هموگلوبین یعنی هموگلوبین Q- ایران شده است.
بحث
هموگلوبین –Q ایران برای اولین بار توسط دکتر رهبر در سال 1978 معرفی گردید و اگر چـه بـه تنهایـی تظاهـر بالینی و کلینیکی خاصی ندارد اما تشخیص صحیح آن در ایران از اهمیت خاصی برخوردار میباشد(11، 6). با وجود عدم اطلاع از آمار دقیق شیوع، گزارشهایی از مشاهده این نوع هموگلوبینوپاتی در نقاط مختلف کشور ایران وجود دارد، به طوری که شیوع هموگلوبین Q- ایران در یک مطالعه در بین جمعیت مبتلا به هموگلوبینوپاتی با نژاد کرد از منطقه غرب ایران 8/31 درصد گزارش شده است(15-12). بنابراین در مناطق پر شیوع لازم است که به برقراری آزمایشهای تکمیلی تاییدی، توجه ویژه مبذول گردد. از طرفی با توجه به روند مهاجرت در دنیا، مواردی از وجود هموگلوبین Q- ایران در نقاط دیگر دنیا نیز گزارش شده است(16).
با وجود تشابه سه نوع هموگلوبین Q از نظر فیلوژنی، ظاهراً اختلاف در ساختمان دوم و سوم آنها باعث تفاوت حرکت الکتروفورتیک این سه نوع هموگلوبین است(1). بدین ترتیب که مشخص گردیده است، بین ساختمان دوم زنجیره آلفا هموگلوبین A و زنجیره آلفا هموگلوبین Q- هند(آلفا 64 اسید آسپارتیک به هیستیدین) هیچ تفاوتی وجود ندارد در حالی که ساختمـان دوم زنجیره آلفا هموگلوبین Q- ایران(آلفا 75 اسید آسپارتیک به هیستیدین)، یک هلیکس اضافی و هموگلوبین Q- تایلند(آلفا 74 اسید آسپارتیک به هیستیدین)، دو
هلیکس اضافی دارد.
نتایج حاصل از بررسی ساختمان سوم این مولکولها، نیز این یافتهها را تایید نموده است(17). ظاهراً وجود این حقایق سبب شده است حرکت الکتروفورتیک هموگلوبین Q- ایران نسبت به هموگلوبین Q- هند در الکتروفورز روی سیترات آگار در pH اسیدی متفاوت باشد بدین ترتیب که هموگلوبین Q- ایران در الکتروفورز روی سیترات آگار نزدیک به باند هموگلوبین S باقی میماند در حالی که هموگلوبین Q- هند از راستای هموگلوبین S فاصله معنادار میگیرد(شکلهای 3 و 4)(11).
نزدیک بودن حرکت الکتروفورتیک هموگلوبین Q- ایران با هموگلوبین S در الکتروفورز روی سیترات آگار میتواند اهمیت خاص انجام آزمایش حلالیت را جهت تشخیص این نوع هموگلوبینوپاتی بیان نماید، زیرا در غیر این صورت با کمترین بیدقتی در تفسیر آزمایش الکتروفورز روی سیترات آگار، احتمال تشخیص نادرست هموگلوبینوپاتی S به جای هموگلوبینوپاتی Q- ایران برای بیمار وجود دارد.
مولکولی تایید نکرده بود، لذا جهت تعیین وضعیت نهایی بیمار، ضرورت انجام آزمایش تعیین توالی نوکلئوتیدها در ژن α گلوبین اعلام گردید.
در آزمایشگاه ژنتیک با انجام آزمایش تعیین توالی نوکلئوتیدها به صورت اتوماتیک با استفاده از دستگاه 377ABI ، مشخص گردید که موتاسیونی به صورت تغییر GAC>CAC ؛ c.226G>C در کدون 75 در ژن α به صورت هتروزیگوت وجود داشته که در قسمت EF4 به صورت تغییر اسید آمینه اسید آسپارتیک به هیستیدین، سبب تولید یک نوع نادر از هموگلوبین یعنی هموگلوبین Q- ایران شده است.
بحث
هموگلوبین –Q ایران برای اولین بار توسط دکتر رهبر در سال 1978 معرفی گردید و اگر چـه بـه تنهایـی تظاهـر بالینی و کلینیکی خاصی ندارد اما تشخیص صحیح آن در ایران از اهمیت خاصی برخوردار میباشد(11، 6). با وجود عدم اطلاع از آمار دقیق شیوع، گزارشهایی از مشاهده این نوع هموگلوبینوپاتی در نقاط مختلف کشور ایران وجود دارد، به طوری که شیوع هموگلوبین Q- ایران در یک مطالعه در بین جمعیت مبتلا به هموگلوبینوپاتی با نژاد کرد از منطقه غرب ایران 8/31 درصد گزارش شده است(15-12). بنابراین در مناطق پر شیوع لازم است که به برقراری آزمایشهای تکمیلی تاییدی، توجه ویژه مبذول گردد. از طرفی با توجه به روند مهاجرت در دنیا، مواردی از وجود هموگلوبین Q- ایران در نقاط دیگر دنیا نیز گزارش شده است(16).
با وجود تشابه سه نوع هموگلوبین Q از نظر فیلوژنی، ظاهراً اختلاف در ساختمان دوم و سوم آنها باعث تفاوت حرکت الکتروفورتیک این سه نوع هموگلوبین است(1). بدین ترتیب که مشخص گردیده است، بین ساختمان دوم زنجیره آلفا هموگلوبین A و زنجیره آلفا هموگلوبین Q- هند(آلفا 64 اسید آسپارتیک به هیستیدین) هیچ تفاوتی وجود ندارد در حالی که ساختمـان دوم زنجیره آلفا هموگلوبین Q- ایران(آلفا 75 اسید آسپارتیک به هیستیدین)، یک هلیکس اضافی و هموگلوبین Q- تایلند(آلفا 74 اسید آسپارتیک به هیستیدین)، دو
هلیکس اضافی دارد.
نتایج حاصل از بررسی ساختمان سوم این مولکولها، نیز این یافتهها را تایید نموده است(17). ظاهراً وجود این حقایق سبب شده است حرکت الکتروفورتیک هموگلوبین Q- ایران نسبت به هموگلوبین Q- هند در الکتروفورز روی سیترات آگار در pH اسیدی متفاوت باشد بدین ترتیب که هموگلوبین Q- ایران در الکتروفورز روی سیترات آگار نزدیک به باند هموگلوبین S باقی میماند در حالی که هموگلوبین Q- هند از راستای هموگلوبین S فاصله معنادار میگیرد(شکلهای 3 و 4)(11).
نزدیک بودن حرکت الکتروفورتیک هموگلوبین Q- ایران با هموگلوبین S در الکتروفورز روی سیترات آگار میتواند اهمیت خاص انجام آزمایش حلالیت را جهت تشخیص این نوع هموگلوبینوپاتی بیان نماید، زیرا در غیر این صورت با کمترین بیدقتی در تفسیر آزمایش الکتروفورز روی سیترات آگار، احتمال تشخیص نادرست هموگلوبینوپاتی S به جای هموگلوبینوپاتی Q- ایران برای بیمار وجود دارد.

شکل 3: هموگلوبین Q – ایران از نظر حرکت الکتروفورتیک روی سیترات آگار(11)

شکل 4: هموگلوبین Q – هند از نظر حرکت الکتروفورتیک روی سیترات آگار(11)
نتیجهگیری
آزمایشگاههای تشخیص پزشکی که به سیستمهای اتوماتیک مدرن مثل کاپیلری زون الکتروفورزیس و سیستم کروماتوگرافی مایع با فشار بالا مجهز نیستند، بعد از انجام الکتروفورز هموگلوبین بر روی استات سلولز در pH قلیایی و مشاهده باند در محدوده هموگلوبین S و D/G ، باید هر دو آزمایش حلالیت و الکتروفورز روی سیترات آگار در pH اسیدی را به عنوان آزمون تکمیلی اجرا نمایند تا تشخیص نهایی حاصل گردد و در صورت امکان، تایید جواب را با ارسال نمونه به آزمایشگاههای مجهز به سیستمهای اتوماتیک مدرن و یا آزمایشگاههای ژنتیـک نیـز
دریافت نمایند.
در مورد بیمار مطرح شده، اگر اولین آزمایشگاه با نتیجه منفی برای آزمایش حلالیت، الکتروفورز روی سیترات آگار را انجام داده بود، گزارش هموگلوبین D/Gمطرح نمیشد. از طرف دیگر اگر در دومین آزمایشگاه آزمایش حلالیت انجام میگرفت، با مشاهده نتیجه منفی با وجود حضور باند هموگلوبینوپاتی بیمار در راستای نزدیک به باند هموگلوبین S در الکتروفورز روی سیترات آگار، تشخیص هموگلوبین S داده نمیشد. عدم توجه به تفاوت مختصر حرکت الکتروفورتیک این دو نوع هموگلوبین، توسط کارشناس مربوطه، موجبات تشخیص نادرست را در آزمایشگاه دوم فراهم آورده است.
تاکید این مقاله بر این مطلب است که جهت تشخیص هموگلوبینوپاتی Q- ایران خصوصاً در مناطق پرشیوع، باید از روشهای آزمایشگاهی مناسب که با روشهای تکمیلی تشخیصی مانند HPLC یا کاپیلری زون الکتروفورزیس و بررسیهای مولکولی در سطح ژن دنبال میشود، جهت غربالگری استفاده نمود زیرا انجام ندادن یک آزمایش به صرف انجام دادن آزمایش دیگر، میتواند سبب ایجاد اشتباه در تشخیص آزمایشگاهی و نهایتاً اشتباه در تشخیص بالینی و تاثیر بر تصمیمات آتی پزشک برای بیمار و خانواده وی شود. بدیهی است تشخیص صحیح در سطح آزمایشگاههای تشخیص طبی از ارزش خاصی برخوردار بوده زیرا به این ترتیب ضمن جلوگیری از اتلاف وقت پزشک، از صرف هزینه توسط بیمار، جهت انجام آزمایشهای غیر ضروری نیز کاسته میشود.
آزمایشگاههای تشخیص پزشکی که به سیستمهای اتوماتیک مدرن مثل کاپیلری زون الکتروفورزیس و سیستم کروماتوگرافی مایع با فشار بالا مجهز نیستند، بعد از انجام الکتروفورز هموگلوبین بر روی استات سلولز در pH قلیایی و مشاهده باند در محدوده هموگلوبین S و D/G ، باید هر دو آزمایش حلالیت و الکتروفورز روی سیترات آگار در pH اسیدی را به عنوان آزمون تکمیلی اجرا نمایند تا تشخیص نهایی حاصل گردد و در صورت امکان، تایید جواب را با ارسال نمونه به آزمایشگاههای مجهز به سیستمهای اتوماتیک مدرن و یا آزمایشگاههای ژنتیـک نیـز
دریافت نمایند.
در مورد بیمار مطرح شده، اگر اولین آزمایشگاه با نتیجه منفی برای آزمایش حلالیت، الکتروفورز روی سیترات آگار را انجام داده بود، گزارش هموگلوبین D/Gمطرح نمیشد. از طرف دیگر اگر در دومین آزمایشگاه آزمایش حلالیت انجام میگرفت، با مشاهده نتیجه منفی با وجود حضور باند هموگلوبینوپاتی بیمار در راستای نزدیک به باند هموگلوبین S در الکتروفورز روی سیترات آگار، تشخیص هموگلوبین S داده نمیشد. عدم توجه به تفاوت مختصر حرکت الکتروفورتیک این دو نوع هموگلوبین، توسط کارشناس مربوطه، موجبات تشخیص نادرست را در آزمایشگاه دوم فراهم آورده است.
تاکید این مقاله بر این مطلب است که جهت تشخیص هموگلوبینوپاتی Q- ایران خصوصاً در مناطق پرشیوع، باید از روشهای آزمایشگاهی مناسب که با روشهای تکمیلی تشخیصی مانند HPLC یا کاپیلری زون الکتروفورزیس و بررسیهای مولکولی در سطح ژن دنبال میشود، جهت غربالگری استفاده نمود زیرا انجام ندادن یک آزمایش به صرف انجام دادن آزمایش دیگر، میتواند سبب ایجاد اشتباه در تشخیص آزمایشگاهی و نهایتاً اشتباه در تشخیص بالینی و تاثیر بر تصمیمات آتی پزشک برای بیمار و خانواده وی شود. بدیهی است تشخیص صحیح در سطح آزمایشگاههای تشخیص طبی از ارزش خاصی برخوردار بوده زیرا به این ترتیب ضمن جلوگیری از اتلاف وقت پزشک، از صرف هزینه توسط بیمار، جهت انجام آزمایشهای غیر ضروری نیز کاسته میشود.
نوع مطالعه: گزارش مورد |
موضوع مقاله:
هماتولوژي
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |





