جلد 11، شماره 3 - ( پاييز 1393 )
جلد 11 شماره 3 صفحات 196-190 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Poopak B, Taghdisi S, Heidari M, Fallah P, Khosravipour G, Bolouri S et al . Evaluation of common polymorphisms of CYP2C19 in Clopidogrel-treated patients. bloodj 2014; 11 (3) :190-196
URL: http://bloodjournal.ir/article-1-782-fa.html
URL: http://bloodjournal.ir/article-1-782-fa.html
پوپک بهزاد، تقدیسی شهرام، حیدری معید، فلاح پرویز، خسروی پور گلاره، بلوری شیرین و همکاران.. ارزیابی پلیمورفیسمهای رایج ژن CYP2C19 در بیماران تحت درمان با داروی کلوپیدوگرل. فصلنامه پژوهشی خون. 1393; 11 (3) :190-196
تهران ـ ایران ـ صندوق پستی: 1495/19395
متن کامل [PDF 307 kb]
(2179 دریافت)
| چکیده (HTML) (8608 مشاهده)
مقدمه
بیماریهای قلبی ـ عروقی، از مهمترین عوامل مرگ و میر در ایران و جهان میباشند که شیوع آنها نیز به صورت گسترده در حال افزایش است. لذا برای مقابله با این چالش، داروهای متعددی جهت پیشگیری و یا درمان بیماریهای قلبی و عروقی پیشنهاد شده است که کلوپیدوگرل به دلیل طیف وسیع مصرف و اثرات بالای درمانی، از پرمصرفترین داروهای این گروه میباشد.
کلوپیدوگرل(پلاویکس) یکی از رایجترین داروهای ضد پلاکتی است که در موارد متعددی از جمله جلوگیری از ایسکمی عروقی در بیماران آترواسکلروتیک، سندروم کرونری حاد و نیز پیشگیری از ترومبوز پس از کارگذاری stent مورد استفاده قرار میگیرد(2، 1). به هر حال 3% تا 40% بیمارانی که پلاویکس مصرف میکنند، پاسخ مناسبی به آن نمیدهند(3). با توجه به میزان دوز مصرف پلاویکس و نوع روش مورد بررسی، مقاومت به پلاویکس در بیمارانی که قادر به مهار تجمع پلاکتی نیستند، تشخیص داده شده است(4، 3). اما این دارو به صورت پیش دارو(Pro-drug) است و تبدیل شدن به فرم فعال آن تحت تاثیر سیتوکروم (CYP2C19) P-450 میباشد. ژنوتیپ طبیعی CYP2C19 (1*1*) است، از جمله ژنوتیپهای جهش یافته هموزیگوت CYP2C19 (2*2*) ، CYP2C19 (3*3*) و از جمله ژنوتیپهای جهش یافته هتروزیگوت، CYP2C19 (2*3*) میباشد. CYP2C19 در متابولیسم بسیاری از داروها نقش اساسی ایفا میکند و ظرفیت این سیستم از فرد به فرد متفاوت است که موجب سطوح مختلف سرمی یک دارو با دوز مشابه میشود به همین دلیل اثر بخشی و عوارض دارو بین افراد مختلف متفاوت است(6، 5). CYP2C19 نقش قابل توجهی در فعال کردن پلاویکس ایفا میکند(7). CYP2C19 توسط ژن CYP2C19 که روی کروموزوم شماره 10 قرار دارد کد میشود. تغییر در این ژن، باعث فقدان عملکرد آللهای CYP2C19*2 و CYP2C19*3 و در نتیجه کاهش این آنزیم میشود(8). تغییرات ژنتیکی چه به صورت هموزیگوت و چه هتروزیگوت در ژن CYP2C19 ، از تبدیل شدن پلاویکس به متابولیت فعالش جلوگیری میکند که میتواند شاخص خوبی برای نشان دادن عملکرد پلاویکس باشد(10، 9). میزان شیوع این دو آلل در جمعیتهای مختلفی بررسی شده است اما چنین مطالعهای برای جمعیت ایرانی گزارش نشده است. مطالعههایی که انجام شده نشان میدهند که میزان شیوع آلل CYP2C19*2 بین 11/0% تا 15/0% متغیر میباشد(11). در مطالعهای که در جمعیت هند انجام شده، میزان شیوع آللهای CYP2C19*1/*1 ، CYP2C19*1/*2 ، CYP2C19*2/*2 ، CYP2C19*1/*17، CYP2C19*17/*17 و CYP2C19*2/*17به ترتیب 1/16% ، 31%، 4/18%، 7/20%، 2/1% و 6/12% گزارش شده است. در این مطالعه هم چنین میزان شیوع آلل ناقص CYP2C19*2 و فقدان آلل CYP2C19*17 به ترتیب 2/40% و 9/17% گزارش شده است(12).
با توجه به این که مناطق جغرافیایی مختلف، درصدهای متنوعی از شیوع پلیمورفیسم را دارند و در افراد مختلف اثرات دارو با دوز یکسان متفاوت است، FDA خواستار تعیین ژنوتیپ CYP2C19 قبل از تجویز دارو شد. در کشور ما علیرغم مصرف بالای این دارو، هیچ آماری از شیوع پلیمورفیسم این ژن وجود ندارد، لذا هدف از این مطالعه بررسی فراوانی پلیمورفیسمهای رایج ژن CYP2C19 به منظور تعیین دوز داروی کلوپیدوگرل (پلاویکس) در جمعیت ایرانی و مقایسه آن با مطالعههای صورت گرفته در کشورهای دیگر بود.
مواد و روشها
این مطالعه با طراحی cross-sectional بر روی 154 بیمار که به کلینیک قلب بیمارستان بوعلی یا مطب مراجعه کردند انجام شد. معیار ورود به این مطالعه مصرف پلاویکس بود. معیار خروج بیماریهایی بودند که در متابولیسم پلاویکس اختلال ایجاد میکنند. در ابتدای ورود، از بیماران فرم رضایتنامه کتبی گرفته شد. سپس پرسشنامه مطالعه توسط پژوهشگر با مصاحبه از بیمار و استفاده از اطلاعات پرونده تکمیل گردید. از 154 بیمار، 5 میلیلیتر خون در لولههای حاوی ضد انعقادEDTA جمعآوری شد. لولهها به آزمایشگاه منتقل شده و در آن جا لایه بافی کوت جدا شده و DNA با کیت شرکت فرمنتاز طبق دستورالعمل موجود در کیت استخراج گردید. DNA استخراج شده، کنترل کیفی شده و به روش واکنش زنجیرهای پلیمراز(PCR) برای ژن بتاگلوبین از نظر سلامت DNA (Integrity) چک شد. روی نمونههای با DNA مطلوب، واکنش زنجیرهای پلیمراز به این صورت انجام شد: واکنش در حجم 25 میکرولیتری شامل 100 نانوگرم DNA ، 1 میکرولیتر از هر آغازگر، 5/2 میکرولیتر از بافر X 10، 5/2 میکرولیتر MgCl2 ، 5/0میکرولیتر dNTPs و 1 واحد از آنزیم پلیمراز Taq انجام شد. شرایط دمایی واکنش PCR در جدول 1 آورده شده است.
جدول 1: شرایط انجام واکنش زنجیرهای پلیمراز
سپس 10 میکرولیتر از محصول PCR ، با 10 واحد از آنزیم اندونوکلئاز BamHI برای CYP2C19*3 در یک
واکنش 20 میکرولیتری در 37 درجه سانتیگراد و همچنین با 10 واحد آنزیم اندونوکلئاز SmaI برایCYP2C19*2 در 30 درجه سانتیگراد به مدت یک شبانه روز هضم شد. محصولات PCR هضم آنزیمی شده روی ژل پلیآکریل آمید 6% از هم جدا شدند(جدول 2).
جدول 2 : محصولات PCR هضم آنزیمی شده
پس از تکمیل اطلاعات بیماران، یافتههای آزمایشگاهی و پرسشنامـه وارد نـرمافـزار 13 SPSS شـد و با آزمون کایدو آنالیز آماری صورت گرفت.
یافتهها
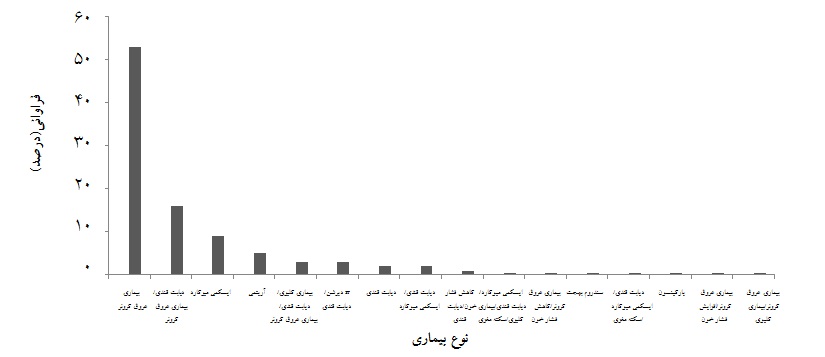
این مطالعه روی 154 بیمار مصرفکننده پلاویکس که شرایط ورود به مطالعه را داشتند انجام شد. تعداد 85 نفر (2/55%) مرد و 69 نفر (2/44%) زن بودند. میانگین سنی بیماران، 59 سال با انحراف معیار 9/12± و حداقل و حداکثـر سنـی بیماران 18 و 81 سال بود(نمودار 1).
نمودار 2: درصد فراوانی نسبی تغییرات ژنی در بیماران تحت مطالعه
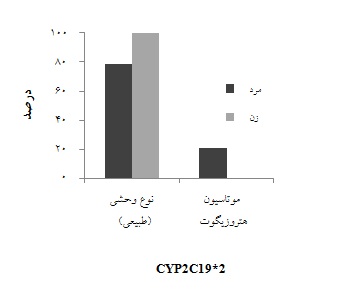
نمودار 3: درصد فراوانی میزان مقاومت به پلاویکس و جنسیت بیماران: از کل بیماران در این مطالعه 100 درصد خانمها و 9/78 درصد مردان ژنوتیپ نرمال داشته و به پلاویکس مقاوم نبودند اما 1/21 درصد مردان که جهش به صورت هتروزیگوت داشتند، به آن مقاوم بودند.
در بیمـاران تحـت مطالعه 24 بیمار مصرفکننده داروی پلاویکس بودند، در این بیماران 3/83% افراد از لحاظ تغییرات ژنی نرمال و 7/16% افراد برای آلل 2 ژن CYP2C19 هتروزیگوت بودند(نمودار 3). طبق آزمون کایدو، ارتباط آماری معناداری بین جنسیت با مقاومت دارویی پلاویکس وجود نداشت. در بیمارانی که پلاویکس مصرف میکردند، از لحاظ تغییرات ژنی و مقاومت دارویی، بیمارانی که نرمال بودند 9/78% مرد و 1/21% زن بودند و 100% بیماران هتروزیگوت، زن بودند.
بحث
بیماریهای قلبی عروقی از مهمترین عوامل مرگ و میر در ایران و جهان میباشد که شیوع آن نیز به صورت گسترده در حال افزایش است. لذا برای مقابله با این چالش، داروهای متعددی جهت پیشگیری و یا درمان بیماریهای قلبی و عروقی پیشنهاد شده است که کلوپیدوگرل به دلیل طیف وسیع مصرف و اثرات بالای درمانی، از پرمصرفترین داروهای این گروه میباشد. تاثیر تغییرات ژنتیکی CYP2C19 بر پاسخ ضد پلاکتی پلاویکس در تعدادی از مطالعهها مشخص شده است. اهمیت ژنوتیپ CYP2C19*2/*3 در پلاویکس درمانی توسط اداره غذا و داروی آمریکا (FDA) تاکید شده است، آللهای با خطر زیاد برای داروی پلاویکس، CYP2C19*2 و CYP2C19*3 میباشند که افراد دارای این آللها مستعد مقاومت به این دارو هستند، مبنی بر این که پلاویکس در جمعیتهایی که شیوع بالای آللهای با خطر زیاد را دارند باید به دقت تجویز شود(14، 13). کاهش متابولیسم داروی پلاویکس توسط آنزیم موتاسیون یافته CYP2C19 ، منجر به کمبود غلظت 30 تا 50 درصدی متابولیت فعال و در نتیجه کاهش مهار پلاکت میشود(15). در مارس 2010، FDA اعلام کرد که تجزیه کنندههای ضعیف پلاویکس ممکن است به طور کامل، از حمله قلبی، سکته و مرگ قلبی - عروقی حفاظت نکنند. هم چنین، آزمایشهایی برای تعیین مشخصات ژنتیکی CYP2C19 در دسترس میباشد که میتواند ناکارآمدی بیمار برای تبدیل پلاویکس به فرم فعال آن را پیشبینی کند. در یک مطالعه متا- آنالیز که اخیراً توسط اسنوپ و همکارانش انجام شد، آنها به این نتیجه رسیدند که در بیماران تحت مطالعه، از هر پنج نفر یک نفر به احتمال زیاد به درمان با پلاویکس پاسخی نمیدهد، که این افراد هشت برابر بیشتر دچار عوارض بالینی نامطلوب از جمله سکته قلبی- عروقی و سندرم کرونری حاد میشوند(4). به منظور این که بتوان به پزشکان در ایران تخمینی از این که داروی پلاویکس چقدر در بیماران تحت درمان با این دارو میتواند کارآمد باشد داد، در این مطالعه بر آن شدیم تا میزان شیوع آللهای پرخطر CYP2C19*2/*3 را در جمعیت ایرانی بررسی کنیم. در این مطالعه، 5/73% بیماران دو داروی ضد پلاکتی پلاویکس و آسپرین را مصرف میکردند. در نتایجی که از این مطالعه به دست آمد شیوع CYP2C19 *2 به صورت هتروزیگوت 4/23% و به صورت هموزیگوت 9/3% بود که اینها خیلی بالاتر از میزانی است که در جمعیتهای قفقازی گزارش شده است (میزان شیوع CYP2C19 *2 16/0% و CYP2C19*3 7/0%)(16). در گزارش دیگری که در جمعیت مصر برای این دو آلل شده است CYP2C19*2 11/0% و برای CYP2C19*3 002/0% بود(11). در جمعیت لبنان شیوع دو آلل CYP2C19 *2 و CYP2C19 *3 به ترتیب 13/0% و 03/0% گزارش شده است(15).
نتیجهگیری
نتایج مطالعه حاضر نشان میدهد که کاربرد توصیههای
سازمان غذا و دارو (FDA) در کشور ما بیش از کشورهای دیگر میتواند مفید باشد. پزشکان باید با شناسایی بیمارانی که خطر بالای پدیدههای ترومبوز را با درمان داروی ضد پلاکتی پلاویکس دارند، به استفاده از داروهای ضد پلاکت دیگر و یا استفاده از دوزهای متغیر که دارای متابولیتهای ضعیفی هستند، مشاوره دهند.
در این مطالعه محدودیتهایی وجود داشت از جمله این که ما نتوانستیم سطح متابولیت فعال پلاویکس پلاسما را اندازهگیری کنیم و هم چنین ارتباط ژنتیکی با جنبههای فارماکوکینتیک این دارو مشخص نشد. هم چنین در این مطالعه ما به رابطه بین علایم کلینیکی و پلیمورفیسم ژنتیکی CYP2C19 نپرداختیم که در آینده به مطالعههای دیگری با این هدف نیاز میباشد.
تشکر و قدردانی
بدین وسیله از همکاری مستمر معاون محترم پژوهش و فناوری و همکاران آن حوزه در دانشگاه آزاد اسلامی واحد پزشکی تهران, کارکنان بخش قلب بیمارستان بوعلی و آزمایشگاه تشخیص طبی و تخصصی پیوند که ما را در انجام امور یاری نمودند، تشکر مینماییم.
متن کامل: (3084 مشاهده)
ارزیابی پلیمورفیسمهای رایج ژن CYP2C19 در بیماران تحت درمان
با داروی کلوپیدوگرل
بهزاد پوپک1، شهرام تقدیسی2، معید حیدری3، پرویز فلاح4، گلاره خسرویپور5، شیرین بلوری6، طلوع گلکار7
چکیده
سابقه و هدف
کلوپیدوگرل، یکی از رایجترین داروهای ضد پلاکتی میباشد که در موارد متعددی از جمله جلوگیری از ایسکمی عروقی در بیماران آترواسکلروتیک، سندروم کرونری حاد و نیز پیشگیری از ترومبوز، مورد استفاده قرار میگیرد. اما کلوپیدوگرل باید توسط آنزیم CYP2C19 به متابولیت فعال خود تبدیل شود تا اثرات خود را داشته باشد که با توجه به پلیمورفیسم آن، اثرات دارو در افراد مختلف متفاوت است. لذا هدف از این مطالعه، بررسی فراوانی پلیمورفیسمهای رایج ژن CYP2C19 در جمعیت ایرانی به منظور تعیین دوز داروی کلوپیدوگرل بود.
مواد و روشها
مطالعه به روش مقطعی بر روی بیماران مبتلا به بیماری قلبی عروقی تحت درمان با کلوپیدوگرل در تابستان 1392 در آزمایشگاه پیوند انجام شد. پلیمورفیسمهای ژن CYP2C19 به روشPCR-RFLP مورد بررسی قرار گرفتند. یافتهها توسط آزمون کایدو و 13 SPSS ، تجزیه و تحلیل شدند.
یافتهها
مطالعه روی 154 بیمار انجام شد. محدوده سنی بیماران 9/12 ± 59 سال بود که 2/55% آنها مذکر بودند. 7/72% از بیماران ژنوتیپ نرمال، 4/23% موتاسیون به صورت هتروزیگوت و 9/3% موتاسیون به صورت هموزیگوت آلل 2 را داشتند.
نتیجه گیری
نتایج تحقیق نشان میدهد که کاربرد توصیههای سازمان غذا و دارو در کشور ایران، بیش از کشورهای دیگر میتواند مفید باشد. پزشکان باید با شناسایی بیمارانی که خطر بالای پدیدههای ترومبوز را با درمان داروی ضد پلاکتی پلاویکس دارند، به سمت استفاده از داروهای ضد پلاکتی دیگر و یا استفاده از دوزهای متغیر که دارای متابولیتهای ضعیفی هستند، مشاوره دهند.
کلمات کلیدی: کلوپیدوگرل، ژنتیک پلیمورفیسم، CYP2C19 انسانی، بیماری ایسکمیک قلبی
تاریخ دریافت : 12/6 /92
تاریخ پذیرش : 12/12/92
1- مؤلف مسؤول: PhD هماتولوژی و بانک خون ـ استادیار دانشگاه آزاد اسلامی- واحد پزشکی تهران ـ تهران ـ ایران ـ صندوق پستی: 1495/19395
2- متخصص قلب و عروق ـ استادیار بخش قلب بیمارستان بوعلی دانشگاه آزاد اسلامی ـ واحد پزشکی تهران ـ تهران ـ ایران
3- پزشک عمومی ـ دانشگاه آزاد اسلامی ـ واحد پزشکی تهران ـ تهران ـ ایران
4- دانشجوی PhD هماتولوژی - دانشکده پیراپزشکی- دانشگاه علوم پزشکی البرز ـ کرج ـ ایران
5- پزشک عمومی- مشاور بالینی - آزمایشگاه تشخیص طبی و تخصصی پیوند ـ تهران ـ ایران
6- کارشناس ارشد بیوشیمی - آزمایشگاه تشخیص طبی و تخصصی پیوند ـ تهران ـ ایران
7- کارشناس ارشد زیستشناسی سلولی مولکولی ـ آزمایشگاه تشخیص طبی و تخصصی پیوند ـ تهران ـ ایران
با داروی کلوپیدوگرل
بهزاد پوپک1، شهرام تقدیسی2، معید حیدری3، پرویز فلاح4، گلاره خسرویپور5، شیرین بلوری6، طلوع گلکار7
چکیده
سابقه و هدف
کلوپیدوگرل، یکی از رایجترین داروهای ضد پلاکتی میباشد که در موارد متعددی از جمله جلوگیری از ایسکمی عروقی در بیماران آترواسکلروتیک، سندروم کرونری حاد و نیز پیشگیری از ترومبوز، مورد استفاده قرار میگیرد. اما کلوپیدوگرل باید توسط آنزیم CYP2C19 به متابولیت فعال خود تبدیل شود تا اثرات خود را داشته باشد که با توجه به پلیمورفیسم آن، اثرات دارو در افراد مختلف متفاوت است. لذا هدف از این مطالعه، بررسی فراوانی پلیمورفیسمهای رایج ژن CYP2C19 در جمعیت ایرانی به منظور تعیین دوز داروی کلوپیدوگرل بود.
مواد و روشها
مطالعه به روش مقطعی بر روی بیماران مبتلا به بیماری قلبی عروقی تحت درمان با کلوپیدوگرل در تابستان 1392 در آزمایشگاه پیوند انجام شد. پلیمورفیسمهای ژن CYP2C19 به روشPCR-RFLP مورد بررسی قرار گرفتند. یافتهها توسط آزمون کایدو و 13 SPSS ، تجزیه و تحلیل شدند.
یافتهها
مطالعه روی 154 بیمار انجام شد. محدوده سنی بیماران 9/12 ± 59 سال بود که 2/55% آنها مذکر بودند. 7/72% از بیماران ژنوتیپ نرمال، 4/23% موتاسیون به صورت هتروزیگوت و 9/3% موتاسیون به صورت هموزیگوت آلل 2 را داشتند.
نتیجه گیری
نتایج تحقیق نشان میدهد که کاربرد توصیههای سازمان غذا و دارو در کشور ایران، بیش از کشورهای دیگر میتواند مفید باشد. پزشکان باید با شناسایی بیمارانی که خطر بالای پدیدههای ترومبوز را با درمان داروی ضد پلاکتی پلاویکس دارند، به سمت استفاده از داروهای ضد پلاکتی دیگر و یا استفاده از دوزهای متغیر که دارای متابولیتهای ضعیفی هستند، مشاوره دهند.
کلمات کلیدی: کلوپیدوگرل، ژنتیک پلیمورفیسم، CYP2C19 انسانی، بیماری ایسکمیک قلبی
تاریخ دریافت : 12/6 /92
تاریخ پذیرش : 12/12/92
1- مؤلف مسؤول: PhD هماتولوژی و بانک خون ـ استادیار دانشگاه آزاد اسلامی- واحد پزشکی تهران ـ تهران ـ ایران ـ صندوق پستی: 1495/19395
2- متخصص قلب و عروق ـ استادیار بخش قلب بیمارستان بوعلی دانشگاه آزاد اسلامی ـ واحد پزشکی تهران ـ تهران ـ ایران
3- پزشک عمومی ـ دانشگاه آزاد اسلامی ـ واحد پزشکی تهران ـ تهران ـ ایران
4- دانشجوی PhD هماتولوژی - دانشکده پیراپزشکی- دانشگاه علوم پزشکی البرز ـ کرج ـ ایران
5- پزشک عمومی- مشاور بالینی - آزمایشگاه تشخیص طبی و تخصصی پیوند ـ تهران ـ ایران
6- کارشناس ارشد بیوشیمی - آزمایشگاه تشخیص طبی و تخصصی پیوند ـ تهران ـ ایران
7- کارشناس ارشد زیستشناسی سلولی مولکولی ـ آزمایشگاه تشخیص طبی و تخصصی پیوند ـ تهران ـ ایران
مقدمه
بیماریهای قلبی ـ عروقی، از مهمترین عوامل مرگ و میر در ایران و جهان میباشند که شیوع آنها نیز به صورت گسترده در حال افزایش است. لذا برای مقابله با این چالش، داروهای متعددی جهت پیشگیری و یا درمان بیماریهای قلبی و عروقی پیشنهاد شده است که کلوپیدوگرل به دلیل طیف وسیع مصرف و اثرات بالای درمانی، از پرمصرفترین داروهای این گروه میباشد.
کلوپیدوگرل(پلاویکس) یکی از رایجترین داروهای ضد پلاکتی است که در موارد متعددی از جمله جلوگیری از ایسکمی عروقی در بیماران آترواسکلروتیک، سندروم کرونری حاد و نیز پیشگیری از ترومبوز پس از کارگذاری stent مورد استفاده قرار میگیرد(2، 1). به هر حال 3% تا 40% بیمارانی که پلاویکس مصرف میکنند، پاسخ مناسبی به آن نمیدهند(3). با توجه به میزان دوز مصرف پلاویکس و نوع روش مورد بررسی، مقاومت به پلاویکس در بیمارانی که قادر به مهار تجمع پلاکتی نیستند، تشخیص داده شده است(4، 3). اما این دارو به صورت پیش دارو(Pro-drug) است و تبدیل شدن به فرم فعال آن تحت تاثیر سیتوکروم (CYP2C19) P-450 میباشد. ژنوتیپ طبیعی CYP2C19 (1*1*) است، از جمله ژنوتیپهای جهش یافته هموزیگوت CYP2C19 (2*2*) ، CYP2C19 (3*3*) و از جمله ژنوتیپهای جهش یافته هتروزیگوت، CYP2C19 (2*3*) میباشد. CYP2C19 در متابولیسم بسیاری از داروها نقش اساسی ایفا میکند و ظرفیت این سیستم از فرد به فرد متفاوت است که موجب سطوح مختلف سرمی یک دارو با دوز مشابه میشود به همین دلیل اثر بخشی و عوارض دارو بین افراد مختلف متفاوت است(6، 5). CYP2C19 نقش قابل توجهی در فعال کردن پلاویکس ایفا میکند(7). CYP2C19 توسط ژن CYP2C19 که روی کروموزوم شماره 10 قرار دارد کد میشود. تغییر در این ژن، باعث فقدان عملکرد آللهای CYP2C19*2 و CYP2C19*3 و در نتیجه کاهش این آنزیم میشود(8). تغییرات ژنتیکی چه به صورت هموزیگوت و چه هتروزیگوت در ژن CYP2C19 ، از تبدیل شدن پلاویکس به متابولیت فعالش جلوگیری میکند که میتواند شاخص خوبی برای نشان دادن عملکرد پلاویکس باشد(10، 9). میزان شیوع این دو آلل در جمعیتهای مختلفی بررسی شده است اما چنین مطالعهای برای جمعیت ایرانی گزارش نشده است. مطالعههایی که انجام شده نشان میدهند که میزان شیوع آلل CYP2C19*2 بین 11/0% تا 15/0% متغیر میباشد(11). در مطالعهای که در جمعیت هند انجام شده، میزان شیوع آللهای CYP2C19*1/*1 ، CYP2C19*1/*2 ، CYP2C19*2/*2 ، CYP2C19*1/*17، CYP2C19*17/*17 و CYP2C19*2/*17به ترتیب 1/16% ، 31%، 4/18%، 7/20%، 2/1% و 6/12% گزارش شده است. در این مطالعه هم چنین میزان شیوع آلل ناقص CYP2C19*2 و فقدان آلل CYP2C19*17 به ترتیب 2/40% و 9/17% گزارش شده است(12).
با توجه به این که مناطق جغرافیایی مختلف، درصدهای متنوعی از شیوع پلیمورفیسم را دارند و در افراد مختلف اثرات دارو با دوز یکسان متفاوت است، FDA خواستار تعیین ژنوتیپ CYP2C19 قبل از تجویز دارو شد. در کشور ما علیرغم مصرف بالای این دارو، هیچ آماری از شیوع پلیمورفیسم این ژن وجود ندارد، لذا هدف از این مطالعه بررسی فراوانی پلیمورفیسمهای رایج ژن CYP2C19 به منظور تعیین دوز داروی کلوپیدوگرل (پلاویکس) در جمعیت ایرانی و مقایسه آن با مطالعههای صورت گرفته در کشورهای دیگر بود.
مواد و روشها
این مطالعه با طراحی cross-sectional بر روی 154 بیمار که به کلینیک قلب بیمارستان بوعلی یا مطب مراجعه کردند انجام شد. معیار ورود به این مطالعه مصرف پلاویکس بود. معیار خروج بیماریهایی بودند که در متابولیسم پلاویکس اختلال ایجاد میکنند. در ابتدای ورود، از بیماران فرم رضایتنامه کتبی گرفته شد. سپس پرسشنامه مطالعه توسط پژوهشگر با مصاحبه از بیمار و استفاده از اطلاعات پرونده تکمیل گردید. از 154 بیمار، 5 میلیلیتر خون در لولههای حاوی ضد انعقادEDTA جمعآوری شد. لولهها به آزمایشگاه منتقل شده و در آن جا لایه بافی کوت جدا شده و DNA با کیت شرکت فرمنتاز طبق دستورالعمل موجود در کیت استخراج گردید. DNA استخراج شده، کنترل کیفی شده و به روش واکنش زنجیرهای پلیمراز(PCR) برای ژن بتاگلوبین از نظر سلامت DNA (Integrity) چک شد. روی نمونههای با DNA مطلوب، واکنش زنجیرهای پلیمراز به این صورت انجام شد: واکنش در حجم 25 میکرولیتری شامل 100 نانوگرم DNA ، 1 میکرولیتر از هر آغازگر، 5/2 میکرولیتر از بافر X 10، 5/2 میکرولیتر MgCl2 ، 5/0میکرولیتر dNTPs و 1 واحد از آنزیم پلیمراز Taq انجام شد. شرایط دمایی واکنش PCR در جدول 1 آورده شده است.
جدول 1: شرایط انجام واکنش زنجیرهای پلیمراز
| تکرار | زمان | دما (درجه سانتیگراد) |
| 1 سیکل | 7 دقیقه | 94 |
| 24 سیکل | 30 ثانیه | 94 |
| 30 ثانیه | 56 | |
| 20 ثانیه | 72 | |
| 1 سیکل | 5 دقیقه | 72 |
سپس 10 میکرولیتر از محصول PCR ، با 10 واحد از آنزیم اندونوکلئاز BamHI برای CYP2C19*3 در یک
واکنش 20 میکرولیتری در 37 درجه سانتیگراد و همچنین با 10 واحد آنزیم اندونوکلئاز SmaI برایCYP2C19*2 در 30 درجه سانتیگراد به مدت یک شبانه روز هضم شد. محصولات PCR هضم آنزیمی شده روی ژل پلیآکریل آمید 6% از هم جدا شدند(جدول 2).
جدول 2 : محصولات PCR هضم آنزیمی شده
| آلل | قطعه PCR | قطعه نرمال | قطعه جهش نرمال |
| CYP2C19*2 | 322 | 212+110 | 322 |
| CYP2C19*3 | 266 | 96+170 | 266 |
پس از تکمیل اطلاعات بیماران، یافتههای آزمایشگاهی و پرسشنامـه وارد نـرمافـزار 13 SPSS شـد و با آزمون کایدو آنالیز آماری صورت گرفت.
یافتهها
این مطالعه روی 154 بیمار مصرفکننده پلاویکس که شرایط ورود به مطالعه را داشتند انجام شد. تعداد 85 نفر (2/55%) مرد و 69 نفر (2/44%) زن بودند. میانگین سنی بیماران، 59 سال با انحراف معیار 9/12± و حداقل و حداکثـر سنـی بیماران 18 و 81 سال بود(نمودار 1).

نمودار 1: درصد فراوانی تشخیص بیماری در بیماران تحت مطالعه
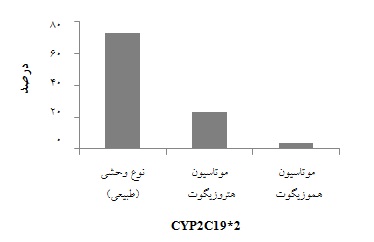
در این تحقیق از 154 بیمار، 116 نفر آسپرین مصرف میکردهاند که در 4/97% دوز مصرفی کمتر از 100 میلیگرم و در 6/2% دوز مصرفی بیش از 100 میلیگرم بوده است. در بیماران تحت مطالعه، 7/72% نرمال، 4/23% موتاسیون به صورت هتروزیگوت و 9/3% موتاسیون به صورت هموزیگوت آلل 2 را داشتند(نمودار 2). 
نمودار 2: درصد فراوانی نسبی تغییرات ژنی در بیماران تحت مطالعه

نمودار 3: درصد فراوانی میزان مقاومت به پلاویکس و جنسیت بیماران: از کل بیماران در این مطالعه 100 درصد خانمها و 9/78 درصد مردان ژنوتیپ نرمال داشته و به پلاویکس مقاوم نبودند اما 1/21 درصد مردان که جهش به صورت هتروزیگوت داشتند، به آن مقاوم بودند.
در بیمـاران تحـت مطالعه 24 بیمار مصرفکننده داروی پلاویکس بودند، در این بیماران 3/83% افراد از لحاظ تغییرات ژنی نرمال و 7/16% افراد برای آلل 2 ژن CYP2C19 هتروزیگوت بودند(نمودار 3). طبق آزمون کایدو، ارتباط آماری معناداری بین جنسیت با مقاومت دارویی پلاویکس وجود نداشت. در بیمارانی که پلاویکس مصرف میکردند، از لحاظ تغییرات ژنی و مقاومت دارویی، بیمارانی که نرمال بودند 9/78% مرد و 1/21% زن بودند و 100% بیماران هتروزیگوت، زن بودند.
بحث
بیماریهای قلبی عروقی از مهمترین عوامل مرگ و میر در ایران و جهان میباشد که شیوع آن نیز به صورت گسترده در حال افزایش است. لذا برای مقابله با این چالش، داروهای متعددی جهت پیشگیری و یا درمان بیماریهای قلبی و عروقی پیشنهاد شده است که کلوپیدوگرل به دلیل طیف وسیع مصرف و اثرات بالای درمانی، از پرمصرفترین داروهای این گروه میباشد. تاثیر تغییرات ژنتیکی CYP2C19 بر پاسخ ضد پلاکتی پلاویکس در تعدادی از مطالعهها مشخص شده است. اهمیت ژنوتیپ CYP2C19*2/*3 در پلاویکس درمانی توسط اداره غذا و داروی آمریکا (FDA) تاکید شده است، آللهای با خطر زیاد برای داروی پلاویکس، CYP2C19*2 و CYP2C19*3 میباشند که افراد دارای این آللها مستعد مقاومت به این دارو هستند، مبنی بر این که پلاویکس در جمعیتهایی که شیوع بالای آللهای با خطر زیاد را دارند باید به دقت تجویز شود(14، 13). کاهش متابولیسم داروی پلاویکس توسط آنزیم موتاسیون یافته CYP2C19 ، منجر به کمبود غلظت 30 تا 50 درصدی متابولیت فعال و در نتیجه کاهش مهار پلاکت میشود(15). در مارس 2010، FDA اعلام کرد که تجزیه کنندههای ضعیف پلاویکس ممکن است به طور کامل، از حمله قلبی، سکته و مرگ قلبی - عروقی حفاظت نکنند. هم چنین، آزمایشهایی برای تعیین مشخصات ژنتیکی CYP2C19 در دسترس میباشد که میتواند ناکارآمدی بیمار برای تبدیل پلاویکس به فرم فعال آن را پیشبینی کند. در یک مطالعه متا- آنالیز که اخیراً توسط اسنوپ و همکارانش انجام شد، آنها به این نتیجه رسیدند که در بیماران تحت مطالعه، از هر پنج نفر یک نفر به احتمال زیاد به درمان با پلاویکس پاسخی نمیدهد، که این افراد هشت برابر بیشتر دچار عوارض بالینی نامطلوب از جمله سکته قلبی- عروقی و سندرم کرونری حاد میشوند(4). به منظور این که بتوان به پزشکان در ایران تخمینی از این که داروی پلاویکس چقدر در بیماران تحت درمان با این دارو میتواند کارآمد باشد داد، در این مطالعه بر آن شدیم تا میزان شیوع آللهای پرخطر CYP2C19*2/*3 را در جمعیت ایرانی بررسی کنیم. در این مطالعه، 5/73% بیماران دو داروی ضد پلاکتی پلاویکس و آسپرین را مصرف میکردند. در نتایجی که از این مطالعه به دست آمد شیوع CYP2C19 *2 به صورت هتروزیگوت 4/23% و به صورت هموزیگوت 9/3% بود که اینها خیلی بالاتر از میزانی است که در جمعیتهای قفقازی گزارش شده است (میزان شیوع CYP2C19 *2 16/0% و CYP2C19*3 7/0%)(16). در گزارش دیگری که در جمعیت مصر برای این دو آلل شده است CYP2C19*2 11/0% و برای CYP2C19*3 002/0% بود(11). در جمعیت لبنان شیوع دو آلل CYP2C19 *2 و CYP2C19 *3 به ترتیب 13/0% و 03/0% گزارش شده است(15).
نتیجهگیری
نتایج مطالعه حاضر نشان میدهد که کاربرد توصیههای
سازمان غذا و دارو (FDA) در کشور ما بیش از کشورهای دیگر میتواند مفید باشد. پزشکان باید با شناسایی بیمارانی که خطر بالای پدیدههای ترومبوز را با درمان داروی ضد پلاکتی پلاویکس دارند، به استفاده از داروهای ضد پلاکت دیگر و یا استفاده از دوزهای متغیر که دارای متابولیتهای ضعیفی هستند، مشاوره دهند.
در این مطالعه محدودیتهایی وجود داشت از جمله این که ما نتوانستیم سطح متابولیت فعال پلاویکس پلاسما را اندازهگیری کنیم و هم چنین ارتباط ژنتیکی با جنبههای فارماکوکینتیک این دارو مشخص نشد. هم چنین در این مطالعه ما به رابطه بین علایم کلینیکی و پلیمورفیسم ژنتیکی CYP2C19 نپرداختیم که در آینده به مطالعههای دیگری با این هدف نیاز میباشد.
تشکر و قدردانی
بدین وسیله از همکاری مستمر معاون محترم پژوهش و فناوری و همکاران آن حوزه در دانشگاه آزاد اسلامی واحد پزشکی تهران, کارکنان بخش قلب بیمارستان بوعلی و آزمایشگاه تشخیص طبی و تخصصی پیوند که ما را در انجام امور یاری نمودند، تشکر مینماییم.
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |





