جلد 22، شماره 1 - ( بهار 1404 )
جلد 22 شماره 1 صفحات 85-76 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Pourmokhtar M, Teimourpour A, Banazadeh S. Determination of Blood Concentrations of Lead, Mercury and Cadmium in Blood Donors: A Systematic Review and Meta-Analysis. bloodj 2025; 22 (1) :76-85
URL: http://bloodjournal.ir/article-1-1566-fa.html
URL: http://bloodjournal.ir/article-1-1566-fa.html
پورمختار مژگان، تیمورپور امیر، بنازاده سودابه. تعیین غلظت خونی سرب، جیوه و کادمیوم در اهداکنندگان خون: یک مرور نظام مند و متاآنالیز. فصلنامه پژوهشی خون. 1404; 22 (1) :76-85
استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون
متن کامل [PDF 828 kb]
(648 دریافت)
| چکیده (HTML) (1824 مشاهده)
مقدمه
آلایندههای محیطی سرب، جیوه و کادمیوم، تهدیدی جدی برای افراد به ویژه گروههای آسیبپذیر همچون نوزادان نارس، کودکان و زنان باردار و چالشی بزرگ در حوزه بهداشت عمومی میباشند. زیرا مواجهههای طولانی مدت با این فلزات سنگین در نتیجه عوامل شغلی یا محیطی، سبب بروز مواردی چون اختلال در فرآیندهای عصبی، شناختی و متابولیکی، بینظمی در سیستم ایمنی و یا سرطانزایی میشوند. همچنین سقط خود به خودی، زایمان زودرس، آسیبهای برگشتناپذیر مغزی و ناهنجاریهای مادرزادی از دیگر پیامدهای مواجهه با این آلایندههای محیطی در دوران بارداری، جنینی و یا کودکی میباشند. لذا محدود کردن این مواجهه از اهمیت ویژهای برخوردار است (27-1).
بر اساس پارهای از مطالعههای انجام شده، علاوه بر مشاغل پر خطر، عادات غذایی خاص، استعمال دخانیات و سکونت در مناطق آلوده که از جمله مهمترین منابع شناخته شده مواجهه با سرب، جیوه و کادمیوم میباشند، غلظت خونی این فلزات سنگین در درصد قابل توجهی از اهداکنندگان خون نیز بالا و نگرانکننده بوده است (30-28). بنابراین مواجهههای طولانی مدت (ناشی از آلودگی محل سکونت دائمی اهداکنندگان) یا کوتاه مدت (ناشی از آلودگی محل قرارگیری مراکز خونگیری و تأثیر آن بر واحدهای اهدایی در مدت نگهداری)، سبب میشوند که انتقال خون و فرآوردههای خونی نیز، به عنوان منبعی پنهان و بالقوه برای مواجهه با این فلزات محسوب شوند. به عنوان مثال مشخص شده است که بین غلظت سرب در فرآورده گلبول قرمز (pRBCs) و سطوح خونی سرب (BLL) در نوزادان نارس، متعاقب تزریق فرآورده، رابطه میزان مصرف ـ پاسخ (Dose-Response) وجود دارد. به علاوه شدت مسمومیت با سرب با سطح خونی آن ارتباط دارد (34-31). بنابراین با توجه به تبعات و عواقب نامطلوب مواجهه با فلزات سنگین به ویژه در گروههای آسیبپذیر، به نظر میرسد سنجش غلظت خونی آنها در اهداکنندگان خون، به خصوص ساکنین مناطق مشکوک به آلودگی و یا در معرض مواجهه محیطی حائز اهمیت باشد (45-35).
به گونهای که بر اساس دستورالعمل WHO ، غلظت خونی مجاز سرب در اهداکنندگان mg/dL 80/1 میباشد. این در حالی است که سازمان ایمنی غذایی اروپا (EFSA : European Food Safety Authority) حد مجاز جیوه را در خون اهداکنندگانmg/dL 475/0 و آژانس حفاظت محیط زیست ایالات متحده آمریکا (EPA : US Environmental Protection Agency) میزان مجاز کادمیوم در خون اهداکنندگان را معادل mg/dL 18/0 اعلام کردهاند (28).
در حال حاضر با وجود تأکید بسیاری از مطالعههای انجام شده به اهمیت انجام غربالگری خون اهداکنندگان از نظر وجود فلزات سنگین، هنوز این غربالگری در مراکز انتقال خون به صورت معمول و روتین انجام نمیگردد (49-46). لذا این پژوهش با هدف مرور نظاممند مطالعههای بررسیکننده غلظت خونی سرب، جیوه و کادمیوم در اهداکنندگان خون و استفاده از نتایج حاصله، برای کمک به تصمیمگیری درخصوص ضرورت انجام غربالگری خون اهداکنندگان از نظر وجود این فلزات سنگین، استفاده از پرسشنامههای مرتبط و در صورت لزوم معاف نمودن اهداکنندگان متعلق به جوامع مستعد از نظر مواجهه با این آلایندههای محیطی، با هدف دستیابی به فرآوردههای ایمنتر و با کیفیتتر به ویژه برای تزریق به گروههای آسیبپذیر انجام شد.
از مزایای این پژوهش نسبت به مطالعههای مرور نظاممند قبلی در این زمینه، میتوان به مواردی همچون جستجو در پایگاههای اطلاعاتی بیشتر و معتبرتر شامل PubMed ، Web of Science ، Scopus و ProQuest ، پوشش زمانی بیشتر مطالعهها (تا پایان ژوئیه 2023) و عدم محدودیت در نوع مطالعههای مورد بررسی اشاره کرد.
مواد و روشها
برای انجام پژوهش حاضر، از یک مرور نظاممند جهت بررسی غلظت خونی فلزات سنگین سرب، جیوه و کادمیوم در اهداکنندگان خون در سطح جهان استفاده شد. به این منظور پس از طرح سؤال و تعیین عنوان پژوهش، پروتکلی مشتمل بر معیارهای ورود و خروج، راهبرد جستجو، نحوه جمعآوری، استخراج و تجزیه و تحلیل دادهها و ارزیابی کیفیت و سوگیری مطالعهها تدوین شد. پروتکل مذکور براساس مدل POLIS (با در نظر گرفتن شرکتکنندگان، پیامد، محل، شاخص و طراحی مطالعه)، مطابق با بیانیه هلسینکی و با پیروی از رهنمودهای دستورالعمل PRISMA-P یاPreferred Reporting Items for Systematic Reviews and Meta-analysis Protocols تدوین شد (50).
سپس پایگاههای اطلاعاتیPubMed ، Scopus ، Web of Science و ProQuest براساس راهبرد جستجوی تعریف شـده، بـه طور جامع و با توجه به کلید واژه های انگلیسی Cd ، Hg ، Pb ، Cadmium ، Mercury ، Lead و "blood donor" به صورت آنلاین، بدون محدودیت زبانی و تا پایان ژوئیه 2023 جستجو شدند. همه مقالاتی که طی جستجوی اولیه دارای کلید واژههای مورد نظر در قسمت عنوان، خلاصه و کلمات کلیدی بودند، وارد مطالعه شدند. سپس به دنبال غربالگری منابع به دست آمده براساس معیارهای ورود و خروج در نظر گرفته شده و با استخراج متن کامل آنها، مقالات مرتبط انتخاب شدند. معیارهای ورود شامل گزارش غلظت خونی فلزات سنگین سرب، جیوه و کادمیوم (پیامد) در نمونه خون کامل وریدی اهداکنندگان خون (شرکتکنندگان) بودند. از طرفی مطالعههای تکراری، نمونههایی غیر از خون کامل وریدی و نمونههای خونی متعلق به افرادی غیر از اهداکنندگان خون از جمله معیارهای خروج در نظر گرفته شدند.
هنگام استخراج دادهها، ابتدا دو داور به صورت مستقل مطالعههای انتخاب شده را مورد ارزیابی کامل قرار دادند و به منظور دستیابی به یک نتیجه واحد، هرگونه اختلاف نظر بین داوران از طریق توافق و یا متعاقب مشورت با داور سوم مستقل رفع گردید. سپس با توجه به نظرات دو داور و با استفاده از یک فرم استاندارد و هدفمند، اطلاعات لازم پس از استخراج مورد بحث قرار گرفتند. در نهایت دادهها با توجه به چک لیست نهایی مورد توافق دو داور، استخراج و ثبت شدند. به منظور ادغام نتایج مطالعههای اولیه و محاسبه میانگین نهایی و فاصله اطمینان 95% از مدل اثر تصادفی (Random effect model) یا روش برآورد REML استفاده شد. میانگین و انحراف معیار به عنوان اندازه اثر در این مطالعه در نظر گرفته شدند. به منظور ارزیابی میزان ناهمگنی نتایج مطالعههای اولیه، از شاخصهای I2 و Q و برای بررسی روند تغییرات در طی زمان از تحلیل متارگرسیون استفاده شد. گزارش و خلاصهسازی نتایج به صورت جدول و توسط نمودار Funnel plot و محاسبات آماری توسط نرمافزار R و پکیج meta انجام شدند.
یافتهها
نتایج مرور نظاممند:
از مجموع 17 مطالعه مورد بررسی در این مرور نظاممند، 14 مورد حاوی اطلاعات مورد نظر برای سرب، 3 مورد حاوی اطلاعات مورد نظر برای جیوه و 9 مورد حاوی اطلاعات مورد نظر برای کادمیوم بودند (شکل 1).
نتایج فراتحلیل:
غلظت سرب در خون اهداکنندگان:
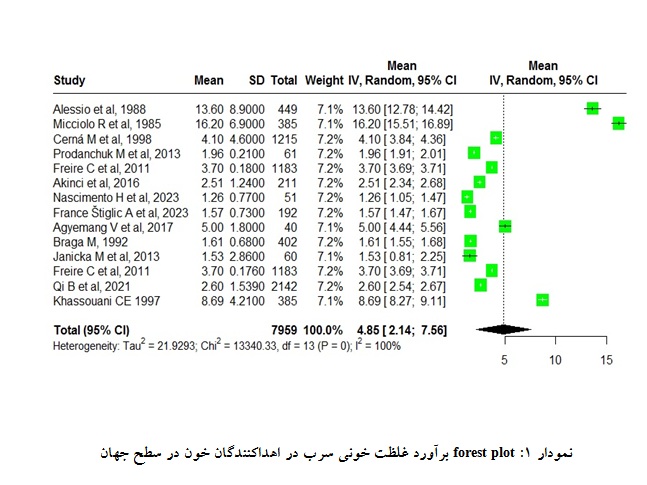
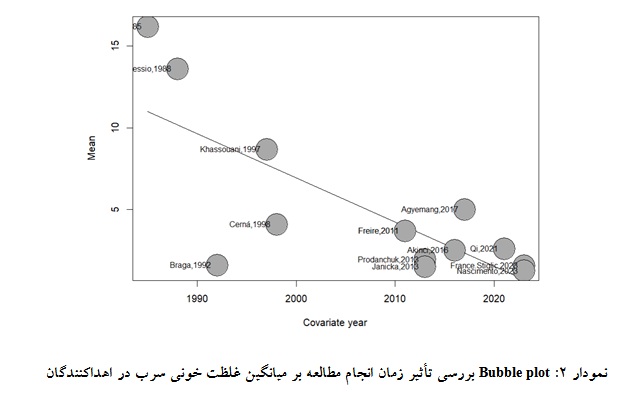
بر اساس مرور نظاممند انجام شده و مطابق با معیارهای ورود و خروج، در نهایت تعداد 14 مطالعه وارد مرحله فراتحلیل گردید. تعداد کل نمونهها برابر 7959 نمونه بود. مقدار شاخص 9/99% = 2I نشاندهنده وجود هتروژنیته میان مطالعهها بود. با استفاده از مدل اثر تصادفی (Random effect) برای ادغام نتایج 14 مطالعه، در نهایت میانگین و فاصله اطمینان 95% غلظت خونی فلز سرب در اهداکنندگان خون در سطح جهان برابر mg/dL 85/4 (56/7؛ 14/2 CI: 95%) محاسبه گردید. اطلاعات مربوط به هر مطالعه و مقدار شاخص میانگین ادغام شده به وسیله مدل اثر تصادفی و نتایج فرا تحلیل برآورد غلظت خونی سرب در اهداکنندگان خون در نمودار گزارش شدهاند (نمودار 1). بر اساس نتایج متارگرسیون، زمان انجام مطالعه یک عامل مهم و تاثیرگذار در تبیین میانگین غلظت خونی سرب در اهداکنندگان خون در سطح جهان بود (0018/0 p=). بـه گونـهای کـه از سال 1985 تا سال 2023 میانگین غلظت خونی سرب در اهداکنندگان خون در سطح جهان، بهطور متوسط سالانه به میزان µg/dL 27/2 (12/0- ؛42/0- : CI 95%) کاهـش یافته است (نمـودار 2) (0018/0 p=).
.jpg)
غلظت جیوه در خون اهداکنندگان:
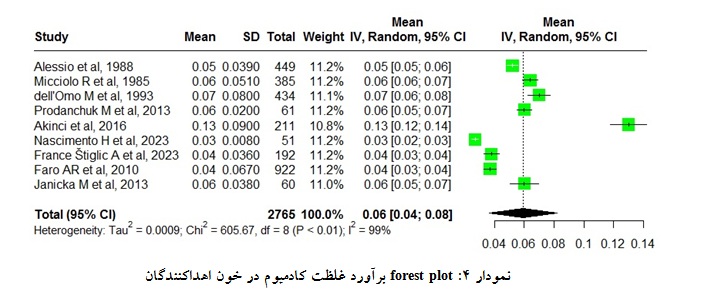
وسیله مدل اثر تصادفی و نتایج فراتحلیل برآورد غلظت خونی کادمیوم در نمودار گزارش شدهاند (نمودار 4). در بررسی تأثیر زمان انجام مطالعه در میانگین غلظت خونی فلز کادمیوم در اهداکنندگان خون در سطح جهان، روند معناداری مشاهده نشد.
بحث
با توجه به این که هدف اصلی مراکز انتقال خون، تأمین به موقع و کافی خون و فرآوردههای خونی سالم و بیخطر میباشد، انتخاب بهینه اهداکنندگان به منظور اطمینان از سلامت واحدهای اهدایی آنها جهت تزریق بیخطر به گیرندگان و تضمین ایمنی فرآوردههای خونی از اهمیت بالایی برخوردار است (52، 51).
مواجهه با فلزات سنگین سـرب، جیوه و کادمیوم، سبب
سمیت سیستمیک و ایجاد آسیبهای متعدد در اندامها میشود (53). به علاوه آژانس حفاظت از محیط زیست ایالات متحده آمریکا (USEPA) و آژانس بینالمللی تحقیقات سرطان (IARC) فلزات مذکور را به عنوان مواد سرطانزای بالقوه طبقهبندی کرده و آنها را تهدیدی جدی برای انسان در نظر میگیرند (56-54). لذا محدود کردن مواجهه با این فلزات به ویژه در نوزادان نارس، کودکان و زنان باردار به عنوان گروههای آسیبپذیر ضروری میباشد.
از طرفی بر اساس برخی از مطالعههای منتشر شده، انتقال خون و فرآوردههای خونی منبعی پنهان و بالقوه برای مواجهه با فلزات سنگین سرب، جیوه و کادمیوم میباشند (49-28). بنابراین مرور نظاممند مطالعههای اندازهگیری کننده غلظت خونی فلزات مورد اشاره در اهداکنندگان خون و استخراج دادههای مربوطه میتواند به تصمیمگیری درخصوص ضرورت غربالگری اهداکنندگان خون از نظر وجود این فلزات سنگین، به منظور انتخاب فرآوردههای خونی ایمنتر برای تزریق به گروههای آسیبپذیر و جلوگیری از تبعات و عواقب نامطلوب مواجهه با آنها کمک کند.
بر اساس نتایج این مرور نظاممند، میانگین غلظت خونی فلز سرب در اهداکنندگان mg/dL 85/4 و بالاتر از mg/dL 80/1 (میزان مجاز اعلام شده توسط WHO ) بود (28). با این توضیح که زمان انجام مطالعه، عاملی مهم و تأثیرگذار در میانگین غلظت خونی فلز سرب در اهداکنندگان بود (0018/0 p=). به گونهای که این میانگین در بازه زمانی 2023-1985 میلادی، به طور متوسط سالانه mg/dL 27/2 کاهش نشان داد. این کاهش قابل توجه غلظتهای خونی سرب اهداکنندگان در طول زمان را میتوان با کاهش تدریجی استفاده از سرب در بنزین، رنگ، لحیم کاری، لولهکشی و ... در سطح جهانی مرتبط دانست (58، 57). اگر چه این میانگین همچنان بالاتر از غلظت خونی مجاز سرب در اهداکنندگان خون است و تلاشهای بیشتری جهت کاهش استفاده از سرب و انتشار آن و همچنین کاهش مواجهههای محیطی و شغلی با آن لازم میباشد. به عنوان مثال آورینا و همکاران و دلاژ و همکاران، غلظت خونی سرب را به ترتیب در 18% از اهداکنندگان نروژی و 5/15% از اهداکنندگان کانادایی بالاتر از حد مجاز برآورد کردند (30، 28).
از طرفی بر اساس نتایج این مرور نظاممند، میانگین غلظت خونی کادمیوم در اهداکنندگان mg/dL 0595/0 و کمتر از سقف مجاز اعلام شده توسط EPA یعنی mg/dL 18/0 بود (28). به علاوه در بررسی تأثیر زمان انجام مطالعه بر میانگین غلظت خونی کادمیوم در اهداکنندگان، روند معناداری مشاهده نشد. میانگین غلظت خونی جیوه نیز در این مرور نظاممند mg/dL 154/0 و کمتر از mg/dL 475/0 که سقف مجاز اعلام شده توسط EFSA بود، برآورد شد (28).
به این ترتیب بر اساس نتایج این مرور نظاممند و با توجه به محدودیت تعداد مطالعههای اولیه در این خصوص، و هم چنین تأثیر احتمالی عواملی همچون سن، جنسیت، محل سکونت و محل اشتغال اهداکنندگان با مشاغل خاص و در مناطق پرخطر بر غلظت خونی فلزات سنگین پیشنهاد میشود برای تصمیمگیری جهت ضرورت غربالگری سرب در اهداکنندگان خون، مطالعههای اولیه جدید و بیشتر به ویژه در اهداکنندگان مناطق پرخطر یا مشاغل خاص انجام شوند. ضمن آن که این غربالگری فعلاً برای کادمیوم و جیوه ضرورت ندارد.
از مزایای این مطالعه میتوان به متدولوژی دقیق و داوری پروتکل آن در PROSPERO اشاره کرد که خطر سوگیری را کاهش داده و منجر به شفافسازی فرآیند شد. ضمن آن که شواهد مفید حاصل از این مرور نظاممند، امکان سیاستگذاری و تصمیمگیری بهتر در زمینه غربالگری اهداکنندگان خون از نظر فلزات سنگین سرب، جیوه و کادمیوم را به منظور انتخاب بهینه اهداکنندگان، دستیابی به فرآوردههای ایمنتر و جلوگیری از تبعات و عواقب نامطلوب انتقال خون فراهم مینماید.
البته با توجه به هتروژنیته بالای نتایج مطالعه به علت تفاوت در زمان انجام مطالعههای مورد بررسی، پیشنهاد میشود در آینده برای چنین مرور نظاممندی از مطالعههایی که در بازههای زمانی مشابه و نزدیک به هم انجام شدهاند، جهت مقایسه نتایج استفاده شود.
نتیجهگیری
بـا تـوجـه بـه نتایـج ایــن مرور نظاممند، تصمیمگیری
درخصوص ضرورت غربالگری اهداکنندگان خون از نظر سرب، همچنان نیازمند انجام مطالعههای اولیه بیشتر به ویژه در اهداکنندگان مناطق پرخطر یا مشاغل خاص میباشد. در حالی که به نظر میرسد در شرایط فعلی این امر برای کادمیوم و جیوه ضرورت نداشته باشد.
حمایت مالی
این مرور نظاممند با حمایت مالی مؤسسه عالی آموزشی و پژوهشی طب انتقال خون انجام شد.
ملاحظات اخلاقی
این مرور نظاممند بر اساس پروتکل شماره PROSPERO 2023 CRD42023352397 ثبت شده در سامانه PROSPERO و مطابق با بیانیه هلسینکی انجام شد و کلیه موازین اخلاقی توسط نویسندگان رعایت شدند.
عدم تعارض منافع
نویسندگان در انجام این مرور نظاممند هیچگونه منافع تجاری نداشتند.
نقش نویسندگان
دکتر مژگان پورمختار: پیشنهاد و طراحی مرور نظاممند، تدوین و ثبت پروتکل در سامانه PROSPERO ، جستجو در پایگاههای اطلاعاتی، غربالگری منابع و انتخاب مقالات مرتبط، استخراج دادهها، نگارش مقاله
دکتر امیر تیمورپور: تجزیه و تحلیل دادهها، متاآنالیز و تفسیر نتایج
سودابه بنازاده: جستجو در پایگاههای اطلاعاتی، غربالگری منابع و انتخاب مقالات مرتبط، استخراج دادهها
تشکر و قدردانی
نویسندگان این مقاله از مؤسسه عالی آموزشی و پژوهشی طب انتقال خون برای تصویب و حمایت مالی از انجام این مرور نظاممند در قالب یک طرح پژوهشی تشکر میکنند.
متن کامل: (621 مشاهده)
تعیین غلظت خونی سرب، جیوه و کادمیوم در اهداکنندگان خون:
یک مرور نظام مند و متاآنالیز
مژگان پورمختار1 ، امیر تیمورپور2 ، سودابه بنازاده3
1- PhD فارماسیوتیکس ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- PhD آمار زیستی- استادیار مرکز تحقیقات فرآورده های بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
3- کارشناس ارشد بیوشیمی ـ دانشکده پزشکی دانشگاه علوم پزشکی تهران - تهران ـ ایران
یک مرور نظام مند و متاآنالیز
1- PhD فارماسیوتیکس ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- PhD آمار زیستی- استادیار مرکز تحقیقات فرآورده های بیولوژیک و سلامت خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
3- کارشناس ارشد بیوشیمی ـ دانشکده پزشکی دانشگاه علوم پزشکی تهران - تهران ـ ایران
http://dx.doi.org/10.61186/bloodj.22.1.76 Citation: Pourmokhtar M, Teimourpour A, Banazadeh S. Determination of Blood Concentrations of Lead, Mercury and Cadmium in Blood Donors: A Systematic Review and Meta-Analysis. J Iran Blood Transfus. 2025: 22 (1) : 76-85. نویسنده مسئول: دکتر مژگان پورمختار. استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران صندوق پستی: 1157-14665 E-mail:
|
چکیده سابقه و هدف مواجهه با سرب، جیوه و کادمیوم تهدیدی جدی برای افراد محسوب می شود. از طرفی انتقال خون، منبعی پنهان و بالقوه برای مواجهه با این فلزات میباشد. لذا این مطالعه با هدف تعیین غلظت خونی فلزات مذکور در اهداکنندگان خون انجام شد. مواد و روشها این مرور نظاممنـد، بـا جستجـوی کلیـد واژههـای Lead, Mercury, Cadmium, Pb, Hg, Cd و “blood donor” ، در پایگاههای اطلاعاتی PubMed، Scopus ، Web of Science و ProQuest تـا پایان ژوئیه 2023 انجام شد. پس از غربالگری و انتخاب مقالههای مرتبط براساس معیارهای ورود و خروج ، دادهها استخراج شدند. به منظور ادغام نتایج مطالعههای اولیه و محاسبه میانگین نهایی از مدل اثر تصادفی (Random-Effects Model) استفاده شد و میانگین و انحراف معیار به عنوان اندازه اثر در نظر گرفته شدند. بـه منظور ارزیابی میزان ناهمگنی نتایج مطالعههای اولیه، از شاخصهای I2 و Q و برای بررسی روند تغییرات در طی زمان از تحلیل متارگرسیون استفاده شد. گزارش و خلاصه سازی نتایج به صورت جدول و توسط نمودار Funnel plot و محاسبات آماری توسط نرمافزار R و پکیج meta انجام شدند. یافتهها میانگین غلظت خونی سرب، جیوه و کادمیوم در اهداکنندگان خون در سطح جهان، به ترتیب (mg/dL) 85/4، (mg/dL) 154/0 و (mg/dL) 0595/0 بودند. همچنین براساس نتایج متارگرسیون، زمان انجام مطالعه عاملی مهم و تاثیرگذار در تبیین میانگین غلظت خونی سرب در اهداکنندگان خون درسطح جهان تشخیص داده شد (0018/0 p=). به گونهای که از سال 1985 تا سال 2023 میانگین غلظت خونی سرب در اهداکنندگان خون در سطح جهان، به طور متوسط سالانه به میزان (mg/dL) 27/2 کاهش نشان داد. در حالی که در خصوص تأثیر زمان انجام مطالعه در میانگین غلظت خونی فلز کادمیوم در اهداکنندگان خون در سطح جهان، روند معناداری مشاهده نشد. نتیجه گیری اگر چه بر اساس نتایج این مرور نظاممند، میانگین غلظت خونی فلز سرب در اهداکنندگان بالاتر از میزان مجاز اعلام شده توسط WHO بود، تصمیمگیری درخصوص ضرورت غربالگری اهداکنندگان خون از نظر سرب، همچنان نیازمند انجام مطالعههای اولیه بیشتر به ویژه در اهداکنندگان مناطق پرخطر یا مشاغل خاص میباشد. در حالی که این غربالگری برای کادمیوم و جیوه ضروری به نظر نمیرسد. کلمات کلیدی: سرب، جیوه، کادمیوم، اهداکنندگان خون |
مقدمه
آلایندههای محیطی سرب، جیوه و کادمیوم، تهدیدی جدی برای افراد به ویژه گروههای آسیبپذیر همچون نوزادان نارس، کودکان و زنان باردار و چالشی بزرگ در حوزه بهداشت عمومی میباشند. زیرا مواجهههای طولانی مدت با این فلزات سنگین در نتیجه عوامل شغلی یا محیطی، سبب بروز مواردی چون اختلال در فرآیندهای عصبی، شناختی و متابولیکی، بینظمی در سیستم ایمنی و یا سرطانزایی میشوند. همچنین سقط خود به خودی، زایمان زودرس، آسیبهای برگشتناپذیر مغزی و ناهنجاریهای مادرزادی از دیگر پیامدهای مواجهه با این آلایندههای محیطی در دوران بارداری، جنینی و یا کودکی میباشند. لذا محدود کردن این مواجهه از اهمیت ویژهای برخوردار است (27-1).
بر اساس پارهای از مطالعههای انجام شده، علاوه بر مشاغل پر خطر، عادات غذایی خاص، استعمال دخانیات و سکونت در مناطق آلوده که از جمله مهمترین منابع شناخته شده مواجهه با سرب، جیوه و کادمیوم میباشند، غلظت خونی این فلزات سنگین در درصد قابل توجهی از اهداکنندگان خون نیز بالا و نگرانکننده بوده است (30-28). بنابراین مواجهههای طولانی مدت (ناشی از آلودگی محل سکونت دائمی اهداکنندگان) یا کوتاه مدت (ناشی از آلودگی محل قرارگیری مراکز خونگیری و تأثیر آن بر واحدهای اهدایی در مدت نگهداری)، سبب میشوند که انتقال خون و فرآوردههای خونی نیز، به عنوان منبعی پنهان و بالقوه برای مواجهه با این فلزات محسوب شوند. به عنوان مثال مشخص شده است که بین غلظت سرب در فرآورده گلبول قرمز (pRBCs) و سطوح خونی سرب (BLL) در نوزادان نارس، متعاقب تزریق فرآورده، رابطه میزان مصرف ـ پاسخ (Dose-Response) وجود دارد. به علاوه شدت مسمومیت با سرب با سطح خونی آن ارتباط دارد (34-31). بنابراین با توجه به تبعات و عواقب نامطلوب مواجهه با فلزات سنگین به ویژه در گروههای آسیبپذیر، به نظر میرسد سنجش غلظت خونی آنها در اهداکنندگان خون، به خصوص ساکنین مناطق مشکوک به آلودگی و یا در معرض مواجهه محیطی حائز اهمیت باشد (45-35).
به گونهای که بر اساس دستورالعمل WHO ، غلظت خونی مجاز سرب در اهداکنندگان mg/dL 80/1 میباشد. این در حالی است که سازمان ایمنی غذایی اروپا (EFSA : European Food Safety Authority) حد مجاز جیوه را در خون اهداکنندگانmg/dL 475/0 و آژانس حفاظت محیط زیست ایالات متحده آمریکا (EPA : US Environmental Protection Agency) میزان مجاز کادمیوم در خون اهداکنندگان را معادل mg/dL 18/0 اعلام کردهاند (28).
در حال حاضر با وجود تأکید بسیاری از مطالعههای انجام شده به اهمیت انجام غربالگری خون اهداکنندگان از نظر وجود فلزات سنگین، هنوز این غربالگری در مراکز انتقال خون به صورت معمول و روتین انجام نمیگردد (49-46). لذا این پژوهش با هدف مرور نظاممند مطالعههای بررسیکننده غلظت خونی سرب، جیوه و کادمیوم در اهداکنندگان خون و استفاده از نتایج حاصله، برای کمک به تصمیمگیری درخصوص ضرورت انجام غربالگری خون اهداکنندگان از نظر وجود این فلزات سنگین، استفاده از پرسشنامههای مرتبط و در صورت لزوم معاف نمودن اهداکنندگان متعلق به جوامع مستعد از نظر مواجهه با این آلایندههای محیطی، با هدف دستیابی به فرآوردههای ایمنتر و با کیفیتتر به ویژه برای تزریق به گروههای آسیبپذیر انجام شد.
از مزایای این پژوهش نسبت به مطالعههای مرور نظاممند قبلی در این زمینه، میتوان به مواردی همچون جستجو در پایگاههای اطلاعاتی بیشتر و معتبرتر شامل PubMed ، Web of Science ، Scopus و ProQuest ، پوشش زمانی بیشتر مطالعهها (تا پایان ژوئیه 2023) و عدم محدودیت در نوع مطالعههای مورد بررسی اشاره کرد.
مواد و روشها
برای انجام پژوهش حاضر، از یک مرور نظاممند جهت بررسی غلظت خونی فلزات سنگین سرب، جیوه و کادمیوم در اهداکنندگان خون در سطح جهان استفاده شد. به این منظور پس از طرح سؤال و تعیین عنوان پژوهش، پروتکلی مشتمل بر معیارهای ورود و خروج، راهبرد جستجو، نحوه جمعآوری، استخراج و تجزیه و تحلیل دادهها و ارزیابی کیفیت و سوگیری مطالعهها تدوین شد. پروتکل مذکور براساس مدل POLIS (با در نظر گرفتن شرکتکنندگان، پیامد، محل، شاخص و طراحی مطالعه)، مطابق با بیانیه هلسینکی و با پیروی از رهنمودهای دستورالعمل PRISMA-P یاPreferred Reporting Items for Systematic Reviews and Meta-analysis Protocols تدوین شد (50).
سپس پایگاههای اطلاعاتیPubMed ، Scopus ، Web of Science و ProQuest براساس راهبرد جستجوی تعریف شـده، بـه طور جامع و با توجه به کلید واژه های انگلیسی Cd ، Hg ، Pb ، Cadmium ، Mercury ، Lead و "blood donor" به صورت آنلاین، بدون محدودیت زبانی و تا پایان ژوئیه 2023 جستجو شدند. همه مقالاتی که طی جستجوی اولیه دارای کلید واژههای مورد نظر در قسمت عنوان، خلاصه و کلمات کلیدی بودند، وارد مطالعه شدند. سپس به دنبال غربالگری منابع به دست آمده براساس معیارهای ورود و خروج در نظر گرفته شده و با استخراج متن کامل آنها، مقالات مرتبط انتخاب شدند. معیارهای ورود شامل گزارش غلظت خونی فلزات سنگین سرب، جیوه و کادمیوم (پیامد) در نمونه خون کامل وریدی اهداکنندگان خون (شرکتکنندگان) بودند. از طرفی مطالعههای تکراری، نمونههایی غیر از خون کامل وریدی و نمونههای خونی متعلق به افرادی غیر از اهداکنندگان خون از جمله معیارهای خروج در نظر گرفته شدند.
هنگام استخراج دادهها، ابتدا دو داور به صورت مستقل مطالعههای انتخاب شده را مورد ارزیابی کامل قرار دادند و به منظور دستیابی به یک نتیجه واحد، هرگونه اختلاف نظر بین داوران از طریق توافق و یا متعاقب مشورت با داور سوم مستقل رفع گردید. سپس با توجه به نظرات دو داور و با استفاده از یک فرم استاندارد و هدفمند، اطلاعات لازم پس از استخراج مورد بحث قرار گرفتند. در نهایت دادهها با توجه به چک لیست نهایی مورد توافق دو داور، استخراج و ثبت شدند. به منظور ادغام نتایج مطالعههای اولیه و محاسبه میانگین نهایی و فاصله اطمینان 95% از مدل اثر تصادفی (Random effect model) یا روش برآورد REML استفاده شد. میانگین و انحراف معیار به عنوان اندازه اثر در این مطالعه در نظر گرفته شدند. به منظور ارزیابی میزان ناهمگنی نتایج مطالعههای اولیه، از شاخصهای I2 و Q و برای بررسی روند تغییرات در طی زمان از تحلیل متارگرسیون استفاده شد. گزارش و خلاصهسازی نتایج به صورت جدول و توسط نمودار Funnel plot و محاسبات آماری توسط نرمافزار R و پکیج meta انجام شدند.
یافتهها
نتایج مرور نظاممند:
از مجموع 17 مطالعه مورد بررسی در این مرور نظاممند، 14 مورد حاوی اطلاعات مورد نظر برای سرب، 3 مورد حاوی اطلاعات مورد نظر برای جیوه و 9 مورد حاوی اطلاعات مورد نظر برای کادمیوم بودند (شکل 1).
نتایج فراتحلیل:
غلظت سرب در خون اهداکنندگان:
بر اساس مرور نظاممند انجام شده و مطابق با معیارهای ورود و خروج، در نهایت تعداد 14 مطالعه وارد مرحله فراتحلیل گردید. تعداد کل نمونهها برابر 7959 نمونه بود. مقدار شاخص 9/99% = 2I نشاندهنده وجود هتروژنیته میان مطالعهها بود. با استفاده از مدل اثر تصادفی (Random effect) برای ادغام نتایج 14 مطالعه، در نهایت میانگین و فاصله اطمینان 95% غلظت خونی فلز سرب در اهداکنندگان خون در سطح جهان برابر mg/dL 85/4 (56/7؛ 14/2 CI: 95%) محاسبه گردید. اطلاعات مربوط به هر مطالعه و مقدار شاخص میانگین ادغام شده به وسیله مدل اثر تصادفی و نتایج فرا تحلیل برآورد غلظت خونی سرب در اهداکنندگان خون در نمودار گزارش شدهاند (نمودار 1). بر اساس نتایج متارگرسیون، زمان انجام مطالعه یک عامل مهم و تاثیرگذار در تبیین میانگین غلظت خونی سرب در اهداکنندگان خون در سطح جهان بود (0018/0 p=). بـه گونـهای کـه از سال 1985 تا سال 2023 میانگین غلظت خونی سرب در اهداکنندگان خون در سطح جهان، بهطور متوسط سالانه به میزان µg/dL 27/2 (12/0- ؛42/0- : CI 95%) کاهـش یافته است (نمـودار 2) (0018/0 p=).
.jpg)



غلظت جیوه در خون اهداکنندگان:
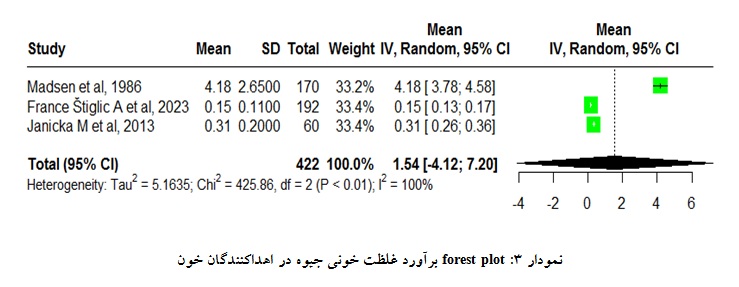
بر اساس مرور نظاممند انجام شده و مطابق با معیارهای ورود و خروج در نهایت تعداد 3 مطالعه برای برآورد غلظت جیوه وارد مطالعه شدند. تعداد کل نمونهها در سه مطالعه برابر 422 نمونه و مقدار میانگین غلظت خونی جیوه در اهداکنندگان خون در سطح جهان و فاصله اطمینان 95% برابر (20/7؛ 12/4- CI: 95%) mg/dL 154/0 و مقدار شاخص 2I برابر 5/99% بود. اطلاعات مربوط به هر مطالعه و مقدار شاخص میانگین ادغام شده به وسیله مدل اثر تصادفی و نتایج فراتحلیل برآورد غلظت خونی جیوه در اهداکنندگان خون در نمودار گزارش شدهاند (نمودار 3).
غلظت خونی کادمیوم در اهداکنندگان خون در سطح جهان:
بر اساس مرور نظاممند انجام شده و مطابق با معیارهای ورود و خروج در نهایت تعداد 9 مطالعه وارد مرحله فرا تحلیل شدند. تعداد کل نمونهها برابر 2765 نمونه بود. مقدار شاخص 7/98% = 2I و نشاندهنده وجود هتروژنیته میان مطالعهها بود. با استفاده از مدل اثر تصادفی (Random effect) برای ادغام نتایج 9 مطالعه، در نهایت میانگین و فاصله اطمینان 95% غلظت خونی فلز کادمیوم در اهداکنندگان خون در سطح جهان برابر µg/dL 0595/0 (0823/0؛0366/0 CI: 95%) محاسبه گردید. اطلاعات مربوط به هر مطالعه و مقدار شاخص میانگین ادغام شده به
غلظت خونی کادمیوم در اهداکنندگان خون در سطح جهان:
بر اساس مرور نظاممند انجام شده و مطابق با معیارهای ورود و خروج در نهایت تعداد 9 مطالعه وارد مرحله فرا تحلیل شدند. تعداد کل نمونهها برابر 2765 نمونه بود. مقدار شاخص 7/98% = 2I و نشاندهنده وجود هتروژنیته میان مطالعهها بود. با استفاده از مدل اثر تصادفی (Random effect) برای ادغام نتایج 9 مطالعه، در نهایت میانگین و فاصله اطمینان 95% غلظت خونی فلز کادمیوم در اهداکنندگان خون در سطح جهان برابر µg/dL 0595/0 (0823/0؛0366/0 CI: 95%) محاسبه گردید. اطلاعات مربوط به هر مطالعه و مقدار شاخص میانگین ادغام شده به

بحث
با توجه به این که هدف اصلی مراکز انتقال خون، تأمین به موقع و کافی خون و فرآوردههای خونی سالم و بیخطر میباشد، انتخاب بهینه اهداکنندگان به منظور اطمینان از سلامت واحدهای اهدایی آنها جهت تزریق بیخطر به گیرندگان و تضمین ایمنی فرآوردههای خونی از اهمیت بالایی برخوردار است (52، 51).
مواجهه با فلزات سنگین سـرب، جیوه و کادمیوم، سبب
سمیت سیستمیک و ایجاد آسیبهای متعدد در اندامها میشود (53). به علاوه آژانس حفاظت از محیط زیست ایالات متحده آمریکا (USEPA) و آژانس بینالمللی تحقیقات سرطان (IARC) فلزات مذکور را به عنوان مواد سرطانزای بالقوه طبقهبندی کرده و آنها را تهدیدی جدی برای انسان در نظر میگیرند (56-54). لذا محدود کردن مواجهه با این فلزات به ویژه در نوزادان نارس، کودکان و زنان باردار به عنوان گروههای آسیبپذیر ضروری میباشد.
از طرفی بر اساس برخی از مطالعههای منتشر شده، انتقال خون و فرآوردههای خونی منبعی پنهان و بالقوه برای مواجهه با فلزات سنگین سرب، جیوه و کادمیوم میباشند (49-28). بنابراین مرور نظاممند مطالعههای اندازهگیری کننده غلظت خونی فلزات مورد اشاره در اهداکنندگان خون و استخراج دادههای مربوطه میتواند به تصمیمگیری درخصوص ضرورت غربالگری اهداکنندگان خون از نظر وجود این فلزات سنگین، به منظور انتخاب فرآوردههای خونی ایمنتر برای تزریق به گروههای آسیبپذیر و جلوگیری از تبعات و عواقب نامطلوب مواجهه با آنها کمک کند.
بر اساس نتایج این مرور نظاممند، میانگین غلظت خونی فلز سرب در اهداکنندگان mg/dL 85/4 و بالاتر از mg/dL 80/1 (میزان مجاز اعلام شده توسط WHO ) بود (28). با این توضیح که زمان انجام مطالعه، عاملی مهم و تأثیرگذار در میانگین غلظت خونی فلز سرب در اهداکنندگان بود (0018/0 p=). به گونهای که این میانگین در بازه زمانی 2023-1985 میلادی، به طور متوسط سالانه mg/dL 27/2 کاهش نشان داد. این کاهش قابل توجه غلظتهای خونی سرب اهداکنندگان در طول زمان را میتوان با کاهش تدریجی استفاده از سرب در بنزین، رنگ، لحیم کاری، لولهکشی و ... در سطح جهانی مرتبط دانست (58، 57). اگر چه این میانگین همچنان بالاتر از غلظت خونی مجاز سرب در اهداکنندگان خون است و تلاشهای بیشتری جهت کاهش استفاده از سرب و انتشار آن و همچنین کاهش مواجهههای محیطی و شغلی با آن لازم میباشد. به عنوان مثال آورینا و همکاران و دلاژ و همکاران، غلظت خونی سرب را به ترتیب در 18% از اهداکنندگان نروژی و 5/15% از اهداکنندگان کانادایی بالاتر از حد مجاز برآورد کردند (30، 28).
از طرفی بر اساس نتایج این مرور نظاممند، میانگین غلظت خونی کادمیوم در اهداکنندگان mg/dL 0595/0 و کمتر از سقف مجاز اعلام شده توسط EPA یعنی mg/dL 18/0 بود (28). به علاوه در بررسی تأثیر زمان انجام مطالعه بر میانگین غلظت خونی کادمیوم در اهداکنندگان، روند معناداری مشاهده نشد. میانگین غلظت خونی جیوه نیز در این مرور نظاممند mg/dL 154/0 و کمتر از mg/dL 475/0 که سقف مجاز اعلام شده توسط EFSA بود، برآورد شد (28).
به این ترتیب بر اساس نتایج این مرور نظاممند و با توجه به محدودیت تعداد مطالعههای اولیه در این خصوص، و هم چنین تأثیر احتمالی عواملی همچون سن، جنسیت، محل سکونت و محل اشتغال اهداکنندگان با مشاغل خاص و در مناطق پرخطر بر غلظت خونی فلزات سنگین پیشنهاد میشود برای تصمیمگیری جهت ضرورت غربالگری سرب در اهداکنندگان خون، مطالعههای اولیه جدید و بیشتر به ویژه در اهداکنندگان مناطق پرخطر یا مشاغل خاص انجام شوند. ضمن آن که این غربالگری فعلاً برای کادمیوم و جیوه ضرورت ندارد.
از مزایای این مطالعه میتوان به متدولوژی دقیق و داوری پروتکل آن در PROSPERO اشاره کرد که خطر سوگیری را کاهش داده و منجر به شفافسازی فرآیند شد. ضمن آن که شواهد مفید حاصل از این مرور نظاممند، امکان سیاستگذاری و تصمیمگیری بهتر در زمینه غربالگری اهداکنندگان خون از نظر فلزات سنگین سرب، جیوه و کادمیوم را به منظور انتخاب بهینه اهداکنندگان، دستیابی به فرآوردههای ایمنتر و جلوگیری از تبعات و عواقب نامطلوب انتقال خون فراهم مینماید.
البته با توجه به هتروژنیته بالای نتایج مطالعه به علت تفاوت در زمان انجام مطالعههای مورد بررسی، پیشنهاد میشود در آینده برای چنین مرور نظاممندی از مطالعههایی که در بازههای زمانی مشابه و نزدیک به هم انجام شدهاند، جهت مقایسه نتایج استفاده شود.
نتیجهگیری
بـا تـوجـه بـه نتایـج ایــن مرور نظاممند، تصمیمگیری
درخصوص ضرورت غربالگری اهداکنندگان خون از نظر سرب، همچنان نیازمند انجام مطالعههای اولیه بیشتر به ویژه در اهداکنندگان مناطق پرخطر یا مشاغل خاص میباشد. در حالی که به نظر میرسد در شرایط فعلی این امر برای کادمیوم و جیوه ضرورت نداشته باشد.
حمایت مالی
این مرور نظاممند با حمایت مالی مؤسسه عالی آموزشی و پژوهشی طب انتقال خون انجام شد.
ملاحظات اخلاقی
این مرور نظاممند بر اساس پروتکل شماره PROSPERO 2023 CRD42023352397 ثبت شده در سامانه PROSPERO و مطابق با بیانیه هلسینکی انجام شد و کلیه موازین اخلاقی توسط نویسندگان رعایت شدند.
عدم تعارض منافع
نویسندگان در انجام این مرور نظاممند هیچگونه منافع تجاری نداشتند.
نقش نویسندگان
دکتر مژگان پورمختار: پیشنهاد و طراحی مرور نظاممند، تدوین و ثبت پروتکل در سامانه PROSPERO ، جستجو در پایگاههای اطلاعاتی، غربالگری منابع و انتخاب مقالات مرتبط، استخراج دادهها، نگارش مقاله
دکتر امیر تیمورپور: تجزیه و تحلیل دادهها، متاآنالیز و تفسیر نتایج
سودابه بنازاده: جستجو در پایگاههای اطلاعاتی، غربالگری منابع و انتخاب مقالات مرتبط، استخراج دادهها
تشکر و قدردانی
نویسندگان این مقاله از مؤسسه عالی آموزشی و پژوهشی طب انتقال خون برای تصویب و حمایت مالی از انجام این مرور نظاممند در قالب یک طرح پژوهشی تشکر میکنند.
نوع مطالعه: مرور سیستماتیک |
موضوع مقاله:
اهدا خون
فهرست منابع
1. Odland JØ, Donaldson S, Dudarev A, Carlsen A. AMAP assessment 2015: human health in the Arctic. Int J Circumpolar Health 2016; 75: 33949. [DOI:10.3402/ijch.v75.33949] [PMID] []
2. EPA US. Persistent organic pollutants: a global issue. A global response; 2014. Available from: https://www.epa.gov/international-cooperation/persistent-organic-pollutants-global-issue-global-response.
3. WHO. Air pollution. 2019; Available from: ttps://www.who.int/airpollution/en/.
4. EEA. Consumption of hazardous chemicals; 2018, Available from: https://www.eea.europa.eu /airs/ 2018 / environment-and-health/production-ofhazardous-chemicals.
5. Grandjean P, Landrigan PJ. Neurobehavioural effects of developmental toxicity. Lancet Neurol 2014; 13(3): 330-8. [DOI:10.1016/S1474-4422(13)70278-3] [PMID]
6. Hassan L, Moser A, Rorman E, Groisman L, Naor Y, Shinar E, et al. Human biologic monitoring based on blood donations to the National Blood Services. BMC Public Health 2020; 20(1): 469. [DOI:10.1186/s12889-020-08588-7] [PMID] []
7. Aliomrani M, Sahraian MA, Shirkhanloo H, Sharifzadeh M, Khoshayand MR, Ghahremani MH. Blood concentrations of cadmium and lead in multiple sclerosis patients from Iran. IJPR 2016; 15(4): 825-33.
8. Iarc Monographs On The Identification Of Carcinogenic Hazards To Humans. [Online] International Agency for Reserach on Cancer, September 23, 2019. [Cited: October 2, 2019.] Available from: https:// monographs. iarc. fr/ agentsclassified-by-the-iarc/.
9. Nemsadze K, Sanikidze T, Ratiani L, Gabunia L, Sharashenidze T. Mechanisms of lead-induced poisoning. Georgian Med News 2009; (172-173): 92-6.
10. National Toxicology Program. NTP monograph on health effects of low-level lead. NTP Monogr 2012; (1):xiii, xv-148.
11. Bellinger DC. Prenatal exposures to environmental chemicals and children's neurodevelopment: an update. Saf Health Work 2013; 4: 1-11. [DOI:10.5491/SHAW.2013.4.1.1] [PMID] []
12. Hong YS, Kim YM, Lee KE. Methylmercury exposure and health effects. J Prev Med Public Health 2012; 45: 353. [DOI:10.3961/jpmph.2012.45.6.353] [PMID] []
13. Nigg JT, Knottnerus GM, Martel MM, Nikolas M, Cavanagh K, Karmaus W, et al. Low blood lead levels associated with clinically diagnosed attention-deficit/hyperactivity disorder and mediated by weak cognitive control. Biol Psychiatry 2008; 63(3): 325-31. [DOI:10.1016/j.biopsych.2007.07.013] [PMID] []
14. Banerjee TD, Middleton F, Faraone SV. Environmental risk factors for attention‐deficit hyperactivity disorder. Acta Paediatr 2007; 96(6): 69-74. [DOI:10.1111/j.1651-2227.2007.00430.x] [PMID]
15. Frye RE, Casanova MF, Fatemi SH, Folsom TD, Reutiman TJ, Brown GL, et al. Neuropathological mechanisms of seizures in autism spectrum disorder. Front Neurosci 2016; 10: 192. [DOI:10.3389/fnins.2016.00192]
16. Sanders T, Liu Y, Buchner V, Tchounwou PB. Neurotoxic effects and biomarkers of lead exposure: a review. Rev Environ Health 2009; 24: 15-45. [DOI:10.1515/REVEH.2009.24.1.15] [PMID] []
17. Khanna MM. Boys, not girls, are negatively affected on cognitive tasks by lead exposure: a pilot study. J Environ Health 2015; 77: 72-7.
18. Patrick L. Lead toxicity, a review of the literature. Part I:exposure, evaluation, and treatment. Altern Med Rev 2006; 11(1): 2-23.
19. Rempel D. The lead-exposed worker. JAMA 1989; 262(4): 532-4. [DOI:10.1001/jama.1989.03430040104034]
20. Bellinger D, Leviton A, Waternaux C, Needleman H, Rabinowitz M. Longitudinal analyses of prenatal and postnatal lead exposure and early cognitive development. N Engl J Med 1987; 316: 1037-43. [DOI:10.1056/NEJM198704233161701] [PMID]
21. Hu H, Téllez-Rojo MM, Bellinger D, Smith D, Ettinger AS, Lamadrid-Figueroa H, et al. Fetal lead exposure at each stage of pregnancy as a predictor of infant mental development. Environ Health Perspect 2006; 114(11): 1730-5. [DOI:10.1289/ehp.9067] [PMID] []
22. Schnur J, John RM. Childhood lead poisoning and the new Centers for Disease Control and Prevention guidelines for lead exposure. J Am Assoc Nurse 2014; 26(5): 238-47. [DOI:10.1002/2327-6924.12112] [PMID]
23. Sowers M, Jannausch M, Scholl T, Li W, Kemp FW, Bogden JD. Blood lead concentrations and pregnancy outcomes. Arch Environ Health 2002; 57(5): 489-95. [DOI:10.1080/00039890209601442] [PMID]
24. Borja-Aburto VH, Hertz-Picciotto I, Lopez MR, Farias P, Rios C, Blanco J. Blood lead levels measured prospectively and risk of spontaneous abortion. Am J Epidemiol 1999; 150(6): 590-7. [DOI:10.1093/oxfordjournals.aje.a010057] [PMID]
25. Cheng L, Zhang B, Huo W, Cao Z, Liu W, Liao J, et al. Fetal exposure to lead during pregnancy and the risk of preterm and early-term deliveries. Int J Hyg Environ Health 2017; 220(6): 984-9. [DOI:10.1016/j.ijheh.2017.05.006] [PMID]
26. Bellinger DC. Teratogen update: lead and pregnancy. Birth Defects Res A Clin Mol Teratol 2005; 73(6): 409-20. [DOI:10.1002/bdra.20127] [PMID]
27. Zhu M, Fitzgerald EF, Gelberg KH, Lin S, Druschel CM. Maternal low-level lead exposure and fetal growth. Environ Health Perspect 2010; 118(10): 12-9. [DOI:10.1289/ehp.0901561] [PMID] []
28. Averina M. Environmental pollutants in blood donors: The multicentre Norwegian donor study. Transfus Med 2020; 30: 201-9. [DOI:10.1111/tme.12662] [PMID]
29. Agyemang V, Acquaye JK, Harrison SBE, Oppong FB, Gyaase S, Asante KP, et al. Blood Lead Levels among Blood Donors and High-Risk Occupational Groups in a Mining Area in Ghana: Implications for Blood Transfusion among Vulnerable Populations. J Trop Med 2020; 2020: 6718985. [DOI:10.1155/2020/6718985] [PMID] []
30. Delage G, Gingras S, Rhainds M. A population-based study on blood lead levels in blood donors. Transfusion 2015; 55: 2633-40. [DOI:10.1111/trf.13199] [PMID]
31. Zubairi H, Visintainer P, Fleming J, Richardson M, Singh R. Lead exposure in preterm infants receiving red blood cell transfusions. Pediatr Res 2015; 77(6): 814-8. [DOI:10.1038/pr.2015.53] [PMID]
32. Elabiad MT, Christensen M. Changes in premature infant mercury and lead blood levels after blood transfusions. Am J Perinatol 2014; 31(10): 863-8. [DOI:10.1055/s-0033-1361936] [PMID]
33. Bearer CF, O'Riordan MA, Powers R. Lead exposure from blood transfusion to premature infants. J Pediatr 2000; 137(4): 549-54. [DOI:10.1067/mpd.2000.108273] [PMID]
34. Bearer CF, Linsalata N, Yomtovian R, Walsh M, Singer L. Blood transfusions: a hidden source of lead exposure. Lancet 2003; 362: 332. [DOI:10.1016/S0140-6736(03)13989-X] [PMID]
35. Dignam T, Kaufmann RB, LeStourgeon L, Brown MJ. Control of lead sources in the United States, 1970-2017: public health progress and current challenges to eliminating lead exposure. JPHMP 2019; 25(Suppl): 13-22. [DOI:10.1097/PHH.0000000000000889] [PMID] []
36. Ghorani-Azam A, Riahi-Zanjani B, Balali-Mood M. Effects of air pollution on human health and practical measures for prevention in Iran. J Res Med Sci 2016; 21(5): 1-12. [DOI:10.4103/1735-1995.189646] [PMID] []
37. Han Z, Guo X, Zhang B, Liao J, Nie L. Blood lead levels of children in urban and suburban areas in China (1997-2015): Temporal and spatial variations and influencing factors. Sci Total Environ 2018; 625(12): 1659-66. [DOI:10.1016/j.scitotenv.2017.12.315] [PMID]
38. Oulhote Y, Le Bot B, Poupon J, Lucas J-P, Mandin C, Etchevers A, et al. Identification of sources of lead exposure in French children by lead isotope analysis: a cross-sectional study. J Environ Health 2011; 10(1): 1-12. [DOI:10.1186/1476-069X-10-75] [PMID] []
39. Obeng-Gyasi E. Sources of lead exposure in various countries. Rev Environ Health 2019; 34(1): 25-34. [DOI:10.1515/reveh-2018-0037] [PMID]
40. Pelc W, Pawlas N, Dobrakowski M, Kasperczyk S. Environmental and socioeconomic factors contributing to elevated blood lead levels in children from an industrial area of Upper Silesia. Environ Toxicol Chem 2016; 35(10): 2597-603. [DOI:10.1002/etc.3429] [PMID]
41. Azami M, Tardeh Z, Mansouri A, Soleymani A, Sayehmiri K. Mean blood lead level in Iranian workers: A systematic and meta-analysis. Iran Red Crescent Med J 2018; 20(1): 1-8. [DOI:10.5812/ircmj.64172]
42. Rashid A, Bhat RA, Qadri H, Mehmood MA. Environmental and socioeconomic factors induced blood lead in children: an investigation from Kashmir, India. Environ Monit Assess 2019; 191(2): 76. [DOI:10.1007/s10661-019-7220-y] [PMID]
43. Ericson B, Hu H, Nash E, Ferraro G, Sinitsky J, Taylor MP. Blood lead levels in low-income and middle-income countries: a systematic review. Lancet Planet Health 2021; 5(3): e145-e53. [DOI:10.1016/S2542-5196(20)30278-3] [PMID]
44. Andrews J. The time has come to mitigate the risk of lead exposure from blood transfusions. Pediatr Res 2019; 85(1): 7-8. [DOI:10.1038/s41390-018-0218-2] [PMID]
45. World Health Organization, Childhood Lead Poisoning: World Health Organization, 2010; Available from: http:// www. who. int/ceh/ publications/ leadguidance.pdf.
46. Falck AJ, Sundararajan S, Al-Mudares F, Contag SA, Bearer CF. Fetal exposure to mercury and lead from intrauterine blood transfusions. Pediatr Res 2019; 86(4): 510-4. [DOI:10.1038/s41390-019-0463-z] [PMID]
47. Gehrie E, Keiser A, Dawling S, Travis J, Strathmann FG, Booth GS. Primary prevention of pediatric lead exposure requires new approaches to transfusion screening. J Pediatr 2013; 163(3): 855-9. [DOI:10.1016/j.jpeds.2013.03.003] [PMID] []
48. Janicka M, Binkowski ŁJ, Błaszczyk M, Paluch J, Wojtaś W, Massanyi P, et al. Cadmium, lead and mercury concentrations and their influence on morphological parameters in blood donors from different age groups from southern Poland. J Trace Elem Med Biol 2015; 29: 342-6. [DOI:10.1016/j.jtemb.2014.10.002] [PMID]
49. Elabiad MT, Hook RE. Lead content of blood transfusions for extremely low-birth-weight infants. Am J Perinatol 2013; 30(9): 765-9. [DOI:10.1055/s-0032-1332803] [PMID]
50. Shamseer L, Moher D, Clarke M, Ghersi D, Liberati A, Petticrew M, et al. Preferred reporting items for systematic review and meta-analysis protocols (PRISMA-P) 2015: elaboration and explanation. BMJ 2015; 4(1): 1-9. [DOI:10.1136/bmj.g7647] [PMID]
51. WHO, World Health Organization. Blood donor selection: guidelines on assessing donor suitability for blood donation. Available from: http://www.who.int/bloodsafety/publications/bts_guideline1/en/index.html; 2012. [accessed 01 June 2020].
52. Chassé M, McIntyre L, English SW, Tinmouth A, Knoll G, Wolfe D, et al. Effect of Blood Donor Characteristics on Transfusion Outcomes: A Systematic Review and Meta-Analysis. Transfus Med Rev 2016; 30(2): 69-80. [DOI:10.1016/j.tmrv.2016.01.002] [PMID]
53. Maximova N, Zanon D, Pascolo L, Zennaro F, Gregori M, Grosso D, et al. Metal accumulation in the renal cortex of a pediatric patient with sickle cell disease: A case report and review of the literature. J Pediatr Hematol Oncol 2015; 37: 311-4. [DOI:10.1097/MPH.0000000000000322] [PMID]
54. Agency for Toxic Substances and Disease Registry. Toxicological Profile for Nickel (Update). Atlanta, GA: US Department of Public Health and Human Services, Public Health Service. Available from: http:/www.atsdr.cdc.gov; 2005.
55. Chervona Y, Arita A, Costa M. Carcinogenic metals and the epigenome: understanding the effect of nickel, arsenic, and chromium. Metallomics 2012; 4: 619-27. [DOI:10.1039/c2mt20033c] [PMID] []
56. WHO (2020). Global elimination of lead paint: why and how countries should take action: technical brief. Available from: https://apps.who.int/iris/handle/10665/333840.
57. Public health impact of chemicals: knowns and unknowns-2021 data addendum Available from: https://www.who.int/publications/i/item/WHO-HEP-ECH-EHD-21.01.
58. UN Environment Program. Final review of scientific information on lead [Internet]. 2010. Available from: http://www.cms.int/sites/default/files/document/UNEP_GC26_INF_11_Add_1_Final_UNEP_Lead_review_and_apppendix_Dec_2010.pdf [Accessed 2017 May 23].
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







