جلد 20، شماره 3 - ( پاییز 1402 )
جلد 20 شماره 3 صفحات 224-214 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Foroughi Ardakan R, Hanachi P, Azarkeivan A, Arab Khazaeli A. ]nvestigating hypothyroidism in beta thalassemia patients receiving blood and determining its relationship with iron overload and iron removal treatment. bloodj 2023; 20 (3) :214-224
URL: http://bloodjournal.ir/article-1-1500-fa.html
URL: http://bloodjournal.ir/article-1-1500-fa.html
فروغی اردکان راشین، حناچی پریچهر، آذرکیوان آزیتا، عرب خزائلی علی. بررسی هیپوتیروئیدی در بیماران بتا تالاسمی دریافتکننده خون و تعیین ارتباط آن با میزان بار آهن و درمان آهنزدایی. فصلنامه پژوهشی خون. 1402; 20 (3) :214-224
دانشیار گروه بیوتکنولوژی دانشکده علوم زیستی دانشگاه الزهرا
متن کامل [PDF 523 kb]
(766 دریافت)
| چکیده (HTML) (1885 مشاهده)
مقدمه
بتا تالاسمی از شایعترین بیماریهای ژنتیکی در ایران است که به صورت اتوزوم مغلوب به ارث میرسد و 83/4% از جمعیت جهان را درگیر کرده است (2، 1). این بیماری یکی از اختلالات ساخت هموگلوبین به شمار میآید که در آن به دلیل رخداد یک موتاسیون در ژن کروموزوم 11، با کاهش سنتز زنجیره بتا و یا فقدان کامل آن روبهرو هستیم (3). کمبود زنجیره بتا باعث افزایش نسبی ساخت زنجیره آلفا میشود که در داخل سلولهای پیشساز رده اریتروئیدی رسوب میکنند. این گلبولهای قرمز به واسطه عدم توازن زنجیرهای، قبل از رسیدن به خون محیطی در داخل طحال از بین میروند (4). این عارضه منجر به عمر کوتاه گلبولهای قرمز و در نتیجه خونسازی غیر مؤثر میشود (5).
اولین و بهترین خط درمانی در این بیماری، تزریق خون مکرر و منظم است[A4] . اگر چه تزریق خون برای این بیماران حیاتبخش محسوب میشود اما عوارض متعددی هم به دنبال دارد (6). در بدن یک فرد تالاسمی به دلیل افزایش تحریک خونسازی (هر چند غیر مؤثر)، جذب آهن از دستگاه گوارش افزایش مییابد (7)، از طرفی یک بیمار تالاسمی به طور متوسط در طول یک سال 18 واحد تزریق خون خواهد داشت که هر واحد کیسه خون با حجم متوسط 450 میلیلیتر، حدود 200 میلیگرم آهن دارد و این در حالی است که هر فرد روزانه تنها به 25-20 میلیگرم آهن برای سنتز هموگلوبین نیاز دارد (1). در نتیجه با توجه به این که تزریق خون یک درمان مادامالعمر برای بیمار محسوب میشود، بروز اضافه بار آهن یک عارضه قابل انتظار و مسئلهساز در بین این افراد خواهد بود (8). در بدن فردی که دچار اضافه بار آهن شده است، ترانسفرین به صورت کامل اشباع میشود، در نتیجه بخش زیادی از آهن به صورت آزاد در پلاسما ظاهر خواهد شد که این پدیده موجب تسریع تشکیل رادیکالهای آزاد هیدروکسیل و افزایش میزان ذخیرهسازی و رسوب آهن در ارگانها و اختلال در عملکرد آنها میگردد. یکی از ارگانهای تحت تأثیر این عارضه، غدد اندوکرین مخصوصاً غده تیروئید است (9). از آن جایی که برخی از مواد معدنی و عناصر مثل آهن، ید، سلنیوم و روی، برای متابولیسم طبیعی هورمونهای تیروئیدی، حیاتی و ضروری هستند، تغییر در سطح این املاح میتواند منجر به تغییر در سطح هورمونهای تیروئیدی و در نتیجه هیپوتیروئیدیسم شود (10، 7). به دلیل این که در بدن انسان هیچ راه دفع مؤثری برای آهن وجود ندارد، تنها راه کمک به این مسئله استفاده از شلاتهکنندههای آهن است که آهن اضافی را از طریق ادرار یا مدفوع دفع میکنند (11).
به طور کلی مشخص شده است که فریتین سرم با ذخایر آهن بدن ارتباط دارد. با این حال، به عنوان یک پارامتر منفرد، همیشه قابل اعتماد نیست، زیرا به عنوان یک واکنشدهنده فاز حاد، تحت تأثیر عوامل دیگری مانند اختلالات التهابی، بیماری کبدی و انواع بدخیمی قرار دارد (12). در سالهای اخیر، روشهای تصویربرداری رزونانس مغناطیسی هستهای (MRI) برای ارزیابی بار آهن در کبد و قلب معرفی شدهاند. پارامترهای R2 و T2* برای غلظت آهن کبد تایید شده است )11). مطالعهها نشان دادند تخمین غلظت آهن کبدی به واسطه این روش به طور قابل اعتمادی با کل ذخایر آهن بدن ارتباط دارد (13).
هدف ما از این مطالعه بررسی شیوع کمکاری تیروئید، در بیماران بتا تالاسمی دریافتکننده خون و ارتباط آن با میزان بار آهن و درمان آهنزدایی بود به طوری که علاوه بر فریتین، از نتایج MRI قلبی و کبدی به عنوان یک روش نوین تشخیص رسوب آهن استفاده کردهایم. چرا که امید داریم با تعیین عوامل مؤثر بر این عارضه و درمان آهنزدایی به موقع، بتوان به جلوگیری یا بهبود این عارضه کمک کرد.
مواد و روشها
این مطالعه مقطعی بر روی بیماران بتا تالاسمی ماژور و اینترمدیا مراجعهکننده به درمانگاه تالاسمی بزرگسالان ظفر تهران که تحت تزریق مکرر خون بودند، انجام شد. تشخیص بیماری تالاسمی بر اساس جواب آزمایش ژنتیک، شرح حال و سابقه بالینی بیماران بوده است.
اطلاعات دموگرافیک بیماران از طریق یک پرسشنامه و با رضایت آگاهانه آنان ثبت گردید. معیارهای ورود به این مطالعه شامل بیماران بتا تالاسمی بالای 18 سال، بیمارانی که به طور منظم خون دریافت کردهاند و بیمارانی که در طول یک سال اخیر سابقه انجام MRI قلبی و کبدی داشتند و در پرونده پزشکی آنان ثبت شده، بود. معیارهای خروج از مطالعه شامل: بیماران بتا تالاسمی با سابقه ژنتیکی کم کاری تیروئید، بیماران با سابقه ابتلا به بیماری خود ایمنی تیروئید و یا زنان باردار، بود. سپس از 232 بیماری که شرایط ورود به مطالعه را داشتند، به اندازه 8 میلیلیتر نمونه خون کامل جهت انجام آزمایشهای Ferritin ، TSH ، T4 و T3 درون لوله لخته فاقد ضد انعقاد جمعآوری و حداکثر تا یک ساعت پس از نمونهگیری در شرایط دمایی 2 تا 8 درجه سانتیگراد به آزمایشگاه منتقل شد. جهت تعیین میزان تمامی این پارامترها از کیت تشخیصی شرکت پیشتاز طب و دستگاه الایزا ریدر Vira VA2154 طبق دستورالعمل شرکت سازنده استفاده شد. اساس اندازهگیری کیت برای آزمایش Ferritin و TSH به روش ساندویچ و برای آزمایش T3 و T4به روش رقابتی با استفاده از آنتیبادیهای مونوکلونال علیه این مولکولها در ته چاهکها طراحی شدهاست. لازم به ذکر است که مقادیر طبیعی فریتین با توجه به کیت الایزا شرکت پیشتاز طب، برای زنان ng/mL 200-10 و برای مردان ng/mL 300-20 و مقادیر طبیعی برای سطح هورمونهای TSH، T4 و T3 به ترتیب mIU/L 2/5-32/0 ، μg/dL 5/12-7/4 و ng/mL 1/2-6/0 تعیین شد.
بر اساس راهنمای فدراسیون بینالمللی تالاسمی، فریتین بالاتر از ng/mL 1000 به عنوان سرباری آهن در نظر گرفته شده است و بر همین مبنا درمان آهنزدایی آغاز میشود. همچنین فریتین بالاتر از ng/mL 2500 به عنوان سرباری شدید آهن برای شروع درمان ترکیبی داروی L1 و دسفرال در نظر گرفته میشود (14).
بیماران مورد مطالعه، در چهار گروه سنی 18 تا 30 سال، 31 تا 40 سال، 41 تا 50 سال و بالای 50 سال گروهبندی شدند. بر اساس سطح هورمونهای تیروئیدیشان نیز در دو گروه مبتلا به کمکاری تیروئید و غیر مبتلا به کمکاری تیروئید طبقهبندی شدند و کلیه آزمونها و مقایسه ارتباطها بر همین مبنا انجام شد. به طوری که افراد با سطح TSH بالاتر از mIU/L 2/5 و سطح T3 و T4 پایینتر از محدوده طبیعی مشخص شده توسط کیت و یا بیمارانی که قرص لووتیروکسین مصرف میکردند، به عنوان افراد مبتلا به کمکاری تیروئید در نظر گرفته شدند.
در این مطالعه شلاتهکنندههای آهن، به سه دسته خوراکی، تزریقی و ترکیبی از این دو تقسیمبندی شد. به طوری که قرص L1 ، Jadenu ، Nanojade ، Osveral و Exjade در دسته داروهای خوراکی و Desferal و Desfonak در دسته داروهای تزریقی قرار گرفتند.
کلیه محاسبات آماری توسط نرمافزار 26 SPSS انجام شد. به منظور مقایسه میانگین متغیرهای کمی از آزمون تی مستقل و در صورت طبیعی نبودن توزیع دادهها از آزمون منویتنی[p5] [A6] و کروسکال والیس استفاده شد. همچنین برای ارزیابی رابطه بین متغیرهای کیفی از آزمون کایدو2) χ( و در صورت لزوم از آزمون دقیق فیشر استفاده شد. سطح معناداری آزمونها 05/0 p<در نظر گرفته شد و به منظور بررسی طبیعی بودن توزیع اطلاعات از آزمون شاپیرو ویلکس استفاده شد. در رابطه با حجم نمونه، برای پیدا کردن اندازه اثر بزرگ بر مبنای نظر متخصصین و مرجع، خطای نوع اول 01/0 و قدرت 95/0 در نرمافزار G*Power محاسبه شد (15).
یافتهها
در این مطالعه 232 بیمار در محدوده سنی 18 تا 76 سال[p7] [A8] و با میانگین سنی 02/9 ± 79/40 سال بررسی شدند. در مجموع 145 نفر (5/62%) زن و 87 نفر (5/37%) مرد بودند. میانگین شاخص توده بدنی (BMI) بیماران 87/2 ± 93/21 بود. بیماران در چهار گروه سنی تقسیمبندی شدند که نشان میدهد گروه سنی 31 تا 40 سال بیشترین فراوانی معادل 107 نفر (1/46%) را شامل میشد و همواره در تمامی گروهها، تعداد زنان از مردان بیشتر بود.
از بیـن 232 بیمـار بتـا تالاسمی ماژور و اینترمدیا مورد مطالعه، 64 نفر (6/27%) مبتلا به کمکاری تیروئید بودند که 36 نفر از آنان زن و 28 نفر مرد بودند. همچنین اطلاعات نشان داد که بین ابتلا به کمکاری تیروئید و جنسیت ارتباط
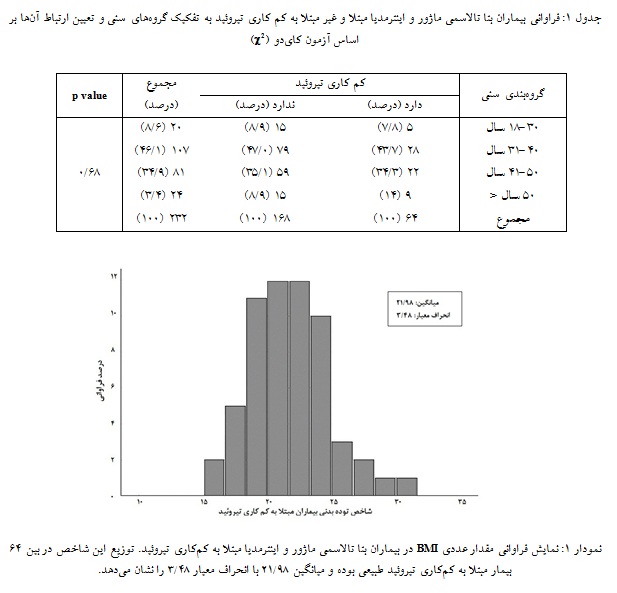
معناداری وجود نداشت. ابتلا به این عارضه در تمامی گروههای سنی نیز با آزمون کایدو بررسی و تفاوت معناداری در هیچ یک از گروهها مشاهده نشد. در هر دو گروه بیمار تالاسمی مبتلا و غیر مبتلا به کمکاری تیروئید، نزدیک به نیمی از آنان در گروه سنی 31 تا 40 سال قرار دارند، به طوری که 28 نفر از بیماران مبتلا به کمکاری تیروئید، معادل 7/43%، در این گروه سنی جای گرفتند (جدول 1). مقایسه میانگین BMI در هر دو گروه بیمار، هیچ ارتباط معناداری میان بیماران مبتلا و غیر مبتلا به کمکاری تیروئید و مقدار عددی BMI آنها نشان نداد و این نتیجه حاکی از آن است که بیماران به طور میانگیـن در
بحث
در مطالعه حاضر درصد فراوانی هیپوتیروئیدی در بیماران بتا تالاسمی ماژور و اینترمدیا ، 6/27% به دست آمد و نسبت شیوع آن در خانمها به آقایان 42/1 بود. در مقایسه میزان فریتین سرم در دو گروه مبتلا و غیر مبتلا به کمکاری تیروئید، نشان داده شد که هیچ ارتباط معنــاداری
بین میزان کنونی فریتین سرم و اختلال عملکرد غده تیروئید یافت نشد. به طوری که از کل بیماران با سربــاری
شدید آهن، بیشترین فراوانی متعلق به گـروه غیـر مبتلا به کمکاری تیروئید بوده است. علاوه بر این، سطح فریتین سرم بین زنان و مردان متفاوت نبود. در مطالعه ما هیچ ارتباط معناداری میان بیماران مبتلا و غیر مبتـلا به کمکاری
تیروئید و رسوب آهن قلبی و کبدی یافت نشد و حتی میتوان گفت که فراوانی افراد با رسوب شدید آهن کبدی، در گروه غیر مبتلا به کمکاری تیروئید بیشتر از گروه مبتلا به این عارضه بوده است. همچنین بیشترین درصد از بیماران در هر دو گروه از لحاظ اضافه بار آهن قلبی در شرایط طبیعی بودند.
مالیک و همکاران هیپوتیروئیدی اولیه را در 18 نفر (7/25%) از 70 بیمار گزارش کردهاند که تقریباً با نتیجه ما همخوانی دارد (16). همچنین در مطالعه کاشانچی و پورهروی، فراوانی بیماریهای غددی را در 206 بیمار تالاسمی ماژور بررسی کردند، شیوع هیپوتیروئیدی 65/20% با نسبت 71/1 زن به مرد گزارش شد (17). در حالی که در مطالعه مهرور و همکاران فراوانی هیپوتیروئیدی از بین 437 بیمار تالاسمی ماژور و اینترمدیا، 2/2% گزارش شد و نسبت زن به مرد 4/1 بود (18). که این نتیجه نسبت به مطالعه حاضر شیوع پایینتری را نشان میدهد. بر اساس گزارش فدراسیون بینالمللی تالاسمی، فراوانی کمکاری تیروئید در بیماران تالاسمی ماژور بین 6 تا 30 درصد است و این گستره متفاوت به دلیل تفاوتهای ژنتیکی، قومیتی، سن و درمانهای مختلف است (19).
در مطالعه لکزایی و همکاران در شهرستان زابل، از 117 بیمار مورد بررسی، 88/41% فریتین کمتر از μg/L 1000 و 12/58% فریتین بین μg/L 2000-1000 داشتند که از این نظر تقریباً مشابه نتایج ما بود ولی بین میانگین طیف فریتین زنان و مردان تفاوت معناداری بود (002/0 =p)(20). اشراقی و همکارانش سال 2011 در بابل، در مطالعهای که ارتباط عملکرد تیروئید کودکان با قد آنان و درمان آهنزدایی را بررسی میکرد، اعلام کردند بین کمکاری تیروئید و سطح فریتین سرم ارتباط معنادار پیدا نشد (3). دکتر طباطبائی و همکاران نیز، تفاوتی بین سطح سرمی فریتین در بیماران تالاسمی که اختلال غدد درونریز داشتند و عدهای که نداشتند مشاهده نکردند (21). گزارشهای ضد و نقیضی در مورد تاثیر آهن در بیماران تالاسمی ماژور بر روی عملکرد غده تیروئید وجود دارد و برخی از محققان بین سطح سرمی فریتین و عملکرد غده تیروئید رابطه مستقیمی را گزارش کردند. این موضوع شاید بدین علت باشد که فریتین سرم مقدار انباشتگی آهن در 3 ماه گذشته را نشان میدهد، در حالی که ایجاد اختلالات غددی نیازمند تماس طولانی با آهن اضافی است. دلیل دیگر، احتمالاً اختلاف در روش اندازهگیری فریتین سرم، اختلاف نژادی، تفاوت در رژیم غذایی، اختلاف در مکان و زمان انجام مطالعه است (22). با بهبود روشهای درمانی در بیماران تالاسمی ماژور، یعنی تزریق مکرر و منظم خون از یک طرف و درمان شدید و منظم آهنزدایی از طرف دیگر، امید به زندگی در بیماران تالاسمیک افزایش یافته است که به همین علت تماس طولانیتر آهن انباشته بدن با غدد درونریز، شانس اختلال عملکرد این ارگانها را افزایش داده است (23). به غیر از اضافه بار آهن، عوامل دیگری از جمله هایپوکسی مزمن ناشی از کمخونی میتواند مسئول آسیب به اندامها باشد و ممکن است سمیت رسوب آهن در غدد درونریز را تشدید کند (7). [A9]
طاهر و سالیبا در 2017 اعلام کردند، روش T2*MIR و R2 یک روش غیر تهاجمی و مناسب برای تعیین میزان غلظت آهن به جای بیوپسی کبد است. از طرفی فریتین سرم توانایی محدودی برای تعیین اضافه بار آهن قلب دارد، اما میتواند به طور قابل اعتمادی سیدروز قلبی و بیماری غدد درون ریز را پیشبینی کند. از این رو توصیه میشود در صورت دسترسی امکانات، در کنار فریتین از روشهای رزونانس هستهای جهت تعیین اضافه بار آهن و برنامهریزی برای دوز داروی شلاتهکننده آهن مصرفی استفاده شود (12). در مطالعه مقطعی که آتماکوسوما و همکارانش در 2021 بر روی 62 بیمار بتا تالاسمی ماژور وابسته به تزریق خون انجام دادند، ارتباط ضعیفی بین فریتین سرم با سمیت آهن قلب و عملکرد سیستولیک قلب گزارش شد. این محققان اظهار داشتند که مسمومیت قلبی در بیماران تالاسمی تحت تأثیر عوامل دیگری به غیر از مسمومیت با آهن است و باید عوامل بییشتری در مطالعهها در نظر گرفته شود (2).
نتیجهگیری
بـه نظـر مـیرسد اضافه بار آهن اعم از فریتین بالا و یا
رسوب آهن در ارگانها، میتواند تا حدودی در ابتلا به کمکاری تیروئید مؤثر باشد اما لزوماً بیمارانی که اضافه بار آهن دارند، کمکاری تیروئید ندارند. همچنین علیرغم درمان آهنزدایی، اضافه بار آهن هنوز یکی از عوارض اصلی تالاسمی به شمار میآید. با توجه به افزایش فراوانی هیپوتیروئیدی با افزایش سن و اثر مستقیمی که هیپوتیروئیدی بر عملکرد قلب دارد، اقدامات پیشگیرانه از جمله کنترل منظم عملکرد غده تیروئید با آزمایشهای دورهای اندازهگیری TSH و T4 سرم، قدم مهمی در تشخیص زودرس بیماری و کنترل و درمان آن میباشد.
پیشنهاد میشود به منظور دستیابی به نتایج دقیقتر، در مطالعههای بعدی نقطه صفر شروع کمکاری تیروئید در بیماران را در نظر گرفته و میزان بار آهن و درمان آهنزدایی در زمان قبل و بعد از بروز عارضه بررسی شود. هـم چنیـن بهتـر اسـت مطالعههـای بعـدی روی گستـره محدودتر سنی و تعداد برابر زنان و مردان انجام شود.
حمایت مالی
این مطالعه حاصل پایاننامه کارشناسی ارشد رشته بیوشیمی است و با حمایت معاونت پژوهشی دانشگاه
الزهرا به انجام رسیده است.
ملاحظات اخلاقی
در اجرای این پروژه کلیه موازین اخلاقی رعایت شده و اطلاعات دموگرافیک بیماران از طریق یک پرسشنامه و با رضایت آگاهانه آنها جمعآوری شده است. این پروژه دارای کد اخلاق IR.ALZAHRA.REC.1401.110 از دانشگاه الزهرا میباشد.
عدم تعارض منافع
نویسندگان این مقاله اعلام میدارند که در نگارش مقاله، هیچگونه تعارضی در منافع نبوده است.
تشکر و قدردانی
این مطالعه حاصل پایاننامه کارشناسی ارشد رشته بیوشیمی دانشگاه الزهرا است و بدین وسیله از مدیریت و پرسنل درمانگاه تالاسمی و بیماران تالاسمی عزیز که ما را در پیشبرد و تحقق این هدف یاری نمودند، کمال تشکر را داریم.
متن کامل: (857 مشاهده)
بررسی هیپوتیروئیدی در بیماران بتا تالاسمی دریافتکننده خون و تعیین ارتباط آن با میزان بار آهن و درمان آهنزدایی
راشین فروغی اردکان1، پریچهر حناچی2، آزیتا آذرکیوان3، علی عرب خزائلی4
چکیده
سابقه و هدف
تزریق خون به عنوان درمان حیاتبخش بیماری تالاسمی، عوارضی هم چون انباشته شدن آهن در غدد درونریز را به دنبال دارد. در بدن هیچ راه دفع مؤثری برای آهن اضافی وجود ندارد، در نتیجه استفاده از شلاتهکنندههای آهن ضروری است. هدف این مطالعه، بررسی شیوع هیپوتیروئیدی و ارتباط آن با میزان بار آهن و نتایج MRI قلبی و کبدی [A1] به عنوان روش نوین تشخیص رسوب آهن و درمان آهنزدایی بود.
مواد و روشها
این مطالعه مقطعی روی 232 بیمار بتا تالاسمی ماژور و اینترمدیا درمانگاه تالاسمی بزرگسال تهران در سال 1400 که به روش نمونهگیری آسان انتخاب شدند، [A2] انجام شد. مقایسه سطح سرمی هورمونهای تیروئیدی و فریتین با آزمونهای کایدو، تی مستقل، منویتنی[A3] و کروسکال والیس، توسط نرمافزار 26 SPSS انجام شد.
یافتهها
شیوع هیپوتیروئیدی در بیماران با میانگین سنی 02/9 ± 79/40 سال، 6/27% به دست آمد و هیچ ارتباط معناداری میان ابتلا به هیپوتیروئیدی و فریتین و همچنین رسوب آهن قلبی و کبدی یافت نشد. سطح هورمون TSH در مردان به طور معناداری بالاتر از زنان بود (01/0 p=). اکثر بیماران از داروهای آهنزدای ترکیبی استفاده میکردند ولی نوع دارو در هیچ یک از دو گروه بیمار تفاوت معناداری نداشت.
نتیجه گیری
به نظر میرسد اضافه بار آهن در ابتلا به هیپوتیروئیدی مؤثر باشد اما لزوماً موجب آن نمیشود. علیرغم درمان آهنزدایی، این عارضه هنوز یکی از مشکلات اساسی است. پیشنهاد میشود در مطالعههای بعدی میزان بار آهن و درمان آهنزدایی، قبل و بعد از شروع کمکاری تیروئید در نظر گرفته شود.
کلمات کلیدی: هیپوتیروئیدی، تالاسمی، اضافه بار آهن، عناصر آهنزدا
تاریخ دریافت: 24/03/1402
تاریخ پذیرش : 18/05/1402
1- دانشجوی کارشناسی ارشد بیوشیمی ـ دانشکده علوم زیستی دانشگاه الزهرا ـ تهران ـ ایران
2- مؤلف مسئول: PhD بیوشیمی ـ دانشیار گروه بیوتکنولوژی دانشکده علوم زیستی دانشگاه الزهرا ـ تهران ـ ایران ـ کد پستی: 1916799553
3- فوق تخصص خون و هماتولوژی کودکان ـ استاد مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
4- PhD آمار و اپیدمیولوژی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
راشین فروغی اردکان1، پریچهر حناچی2، آزیتا آذرکیوان3، علی عرب خزائلی4
چکیده
سابقه و هدف
تزریق خون به عنوان درمان حیاتبخش بیماری تالاسمی، عوارضی هم چون انباشته شدن آهن در غدد درونریز را به دنبال دارد. در بدن هیچ راه دفع مؤثری برای آهن اضافی وجود ندارد، در نتیجه استفاده از شلاتهکنندههای آهن ضروری است. هدف این مطالعه، بررسی شیوع هیپوتیروئیدی و ارتباط آن با میزان بار آهن و نتایج MRI قلبی و کبدی [A1] به عنوان روش نوین تشخیص رسوب آهن و درمان آهنزدایی بود.
مواد و روشها
این مطالعه مقطعی روی 232 بیمار بتا تالاسمی ماژور و اینترمدیا درمانگاه تالاسمی بزرگسال تهران در سال 1400 که به روش نمونهگیری آسان انتخاب شدند، [A2] انجام شد. مقایسه سطح سرمی هورمونهای تیروئیدی و فریتین با آزمونهای کایدو، تی مستقل، منویتنی[A3] و کروسکال والیس، توسط نرمافزار 26 SPSS انجام شد.
یافتهها
شیوع هیپوتیروئیدی در بیماران با میانگین سنی 02/9 ± 79/40 سال، 6/27% به دست آمد و هیچ ارتباط معناداری میان ابتلا به هیپوتیروئیدی و فریتین و همچنین رسوب آهن قلبی و کبدی یافت نشد. سطح هورمون TSH در مردان به طور معناداری بالاتر از زنان بود (01/0 p=). اکثر بیماران از داروهای آهنزدای ترکیبی استفاده میکردند ولی نوع دارو در هیچ یک از دو گروه بیمار تفاوت معناداری نداشت.
نتیجه گیری
به نظر میرسد اضافه بار آهن در ابتلا به هیپوتیروئیدی مؤثر باشد اما لزوماً موجب آن نمیشود. علیرغم درمان آهنزدایی، این عارضه هنوز یکی از مشکلات اساسی است. پیشنهاد میشود در مطالعههای بعدی میزان بار آهن و درمان آهنزدایی، قبل و بعد از شروع کمکاری تیروئید در نظر گرفته شود.
کلمات کلیدی: هیپوتیروئیدی، تالاسمی، اضافه بار آهن، عناصر آهنزدا
تاریخ دریافت: 24/03/1402
تاریخ پذیرش : 18/05/1402
1- دانشجوی کارشناسی ارشد بیوشیمی ـ دانشکده علوم زیستی دانشگاه الزهرا ـ تهران ـ ایران
2- مؤلف مسئول: PhD بیوشیمی ـ دانشیار گروه بیوتکنولوژی دانشکده علوم زیستی دانشگاه الزهرا ـ تهران ـ ایران ـ کد پستی: 1916799553
3- فوق تخصص خون و هماتولوژی کودکان ـ استاد مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
4- PhD آمار و اپیدمیولوژی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
مقدمه
بتا تالاسمی از شایعترین بیماریهای ژنتیکی در ایران است که به صورت اتوزوم مغلوب به ارث میرسد و 83/4% از جمعیت جهان را درگیر کرده است (2، 1). این بیماری یکی از اختلالات ساخت هموگلوبین به شمار میآید که در آن به دلیل رخداد یک موتاسیون در ژن کروموزوم 11، با کاهش سنتز زنجیره بتا و یا فقدان کامل آن روبهرو هستیم (3). کمبود زنجیره بتا باعث افزایش نسبی ساخت زنجیره آلفا میشود که در داخل سلولهای پیشساز رده اریتروئیدی رسوب میکنند. این گلبولهای قرمز به واسطه عدم توازن زنجیرهای، قبل از رسیدن به خون محیطی در داخل طحال از بین میروند (4). این عارضه منجر به عمر کوتاه گلبولهای قرمز و در نتیجه خونسازی غیر مؤثر میشود (5).
اولین و بهترین خط درمانی در این بیماری، تزریق خون مکرر و منظم است[A4] . اگر چه تزریق خون برای این بیماران حیاتبخش محسوب میشود اما عوارض متعددی هم به دنبال دارد (6). در بدن یک فرد تالاسمی به دلیل افزایش تحریک خونسازی (هر چند غیر مؤثر)، جذب آهن از دستگاه گوارش افزایش مییابد (7)، از طرفی یک بیمار تالاسمی به طور متوسط در طول یک سال 18 واحد تزریق خون خواهد داشت که هر واحد کیسه خون با حجم متوسط 450 میلیلیتر، حدود 200 میلیگرم آهن دارد و این در حالی است که هر فرد روزانه تنها به 25-20 میلیگرم آهن برای سنتز هموگلوبین نیاز دارد (1). در نتیجه با توجه به این که تزریق خون یک درمان مادامالعمر برای بیمار محسوب میشود، بروز اضافه بار آهن یک عارضه قابل انتظار و مسئلهساز در بین این افراد خواهد بود (8). در بدن فردی که دچار اضافه بار آهن شده است، ترانسفرین به صورت کامل اشباع میشود، در نتیجه بخش زیادی از آهن به صورت آزاد در پلاسما ظاهر خواهد شد که این پدیده موجب تسریع تشکیل رادیکالهای آزاد هیدروکسیل و افزایش میزان ذخیرهسازی و رسوب آهن در ارگانها و اختلال در عملکرد آنها میگردد. یکی از ارگانهای تحت تأثیر این عارضه، غدد اندوکرین مخصوصاً غده تیروئید است (9). از آن جایی که برخی از مواد معدنی و عناصر مثل آهن، ید، سلنیوم و روی، برای متابولیسم طبیعی هورمونهای تیروئیدی، حیاتی و ضروری هستند، تغییر در سطح این املاح میتواند منجر به تغییر در سطح هورمونهای تیروئیدی و در نتیجه هیپوتیروئیدیسم شود (10، 7). به دلیل این که در بدن انسان هیچ راه دفع مؤثری برای آهن وجود ندارد، تنها راه کمک به این مسئله استفاده از شلاتهکنندههای آهن است که آهن اضافی را از طریق ادرار یا مدفوع دفع میکنند (11).
به طور کلی مشخص شده است که فریتین سرم با ذخایر آهن بدن ارتباط دارد. با این حال، به عنوان یک پارامتر منفرد، همیشه قابل اعتماد نیست، زیرا به عنوان یک واکنشدهنده فاز حاد، تحت تأثیر عوامل دیگری مانند اختلالات التهابی، بیماری کبدی و انواع بدخیمی قرار دارد (12). در سالهای اخیر، روشهای تصویربرداری رزونانس مغناطیسی هستهای (MRI) برای ارزیابی بار آهن در کبد و قلب معرفی شدهاند. پارامترهای R2 و T2* برای غلظت آهن کبد تایید شده است )11). مطالعهها نشان دادند تخمین غلظت آهن کبدی به واسطه این روش به طور قابل اعتمادی با کل ذخایر آهن بدن ارتباط دارد (13).
هدف ما از این مطالعه بررسی شیوع کمکاری تیروئید، در بیماران بتا تالاسمی دریافتکننده خون و ارتباط آن با میزان بار آهن و درمان آهنزدایی بود به طوری که علاوه بر فریتین، از نتایج MRI قلبی و کبدی به عنوان یک روش نوین تشخیص رسوب آهن استفاده کردهایم. چرا که امید داریم با تعیین عوامل مؤثر بر این عارضه و درمان آهنزدایی به موقع، بتوان به جلوگیری یا بهبود این عارضه کمک کرد.
مواد و روشها
این مطالعه مقطعی بر روی بیماران بتا تالاسمی ماژور و اینترمدیا مراجعهکننده به درمانگاه تالاسمی بزرگسالان ظفر تهران که تحت تزریق مکرر خون بودند، انجام شد. تشخیص بیماری تالاسمی بر اساس جواب آزمایش ژنتیک، شرح حال و سابقه بالینی بیماران بوده است.
اطلاعات دموگرافیک بیماران از طریق یک پرسشنامه و با رضایت آگاهانه آنان ثبت گردید. معیارهای ورود به این مطالعه شامل بیماران بتا تالاسمی بالای 18 سال، بیمارانی که به طور منظم خون دریافت کردهاند و بیمارانی که در طول یک سال اخیر سابقه انجام MRI قلبی و کبدی داشتند و در پرونده پزشکی آنان ثبت شده، بود. معیارهای خروج از مطالعه شامل: بیماران بتا تالاسمی با سابقه ژنتیکی کم کاری تیروئید، بیماران با سابقه ابتلا به بیماری خود ایمنی تیروئید و یا زنان باردار، بود. سپس از 232 بیماری که شرایط ورود به مطالعه را داشتند، به اندازه 8 میلیلیتر نمونه خون کامل جهت انجام آزمایشهای Ferritin ، TSH ، T4 و T3 درون لوله لخته فاقد ضد انعقاد جمعآوری و حداکثر تا یک ساعت پس از نمونهگیری در شرایط دمایی 2 تا 8 درجه سانتیگراد به آزمایشگاه منتقل شد. جهت تعیین میزان تمامی این پارامترها از کیت تشخیصی شرکت پیشتاز طب و دستگاه الایزا ریدر Vira VA2154 طبق دستورالعمل شرکت سازنده استفاده شد. اساس اندازهگیری کیت برای آزمایش Ferritin و TSH به روش ساندویچ و برای آزمایش T3 و T4به روش رقابتی با استفاده از آنتیبادیهای مونوکلونال علیه این مولکولها در ته چاهکها طراحی شدهاست. لازم به ذکر است که مقادیر طبیعی فریتین با توجه به کیت الایزا شرکت پیشتاز طب، برای زنان ng/mL 200-10 و برای مردان ng/mL 300-20 و مقادیر طبیعی برای سطح هورمونهای TSH، T4 و T3 به ترتیب mIU/L 2/5-32/0 ، μg/dL 5/12-7/4 و ng/mL 1/2-6/0 تعیین شد.
بر اساس راهنمای فدراسیون بینالمللی تالاسمی، فریتین بالاتر از ng/mL 1000 به عنوان سرباری آهن در نظر گرفته شده است و بر همین مبنا درمان آهنزدایی آغاز میشود. همچنین فریتین بالاتر از ng/mL 2500 به عنوان سرباری شدید آهن برای شروع درمان ترکیبی داروی L1 و دسفرال در نظر گرفته میشود (14).
بیماران مورد مطالعه، در چهار گروه سنی 18 تا 30 سال، 31 تا 40 سال، 41 تا 50 سال و بالای 50 سال گروهبندی شدند. بر اساس سطح هورمونهای تیروئیدیشان نیز در دو گروه مبتلا به کمکاری تیروئید و غیر مبتلا به کمکاری تیروئید طبقهبندی شدند و کلیه آزمونها و مقایسه ارتباطها بر همین مبنا انجام شد. به طوری که افراد با سطح TSH بالاتر از mIU/L 2/5 و سطح T3 و T4 پایینتر از محدوده طبیعی مشخص شده توسط کیت و یا بیمارانی که قرص لووتیروکسین مصرف میکردند، به عنوان افراد مبتلا به کمکاری تیروئید در نظر گرفته شدند.
در این مطالعه شلاتهکنندههای آهن، به سه دسته خوراکی، تزریقی و ترکیبی از این دو تقسیمبندی شد. به طوری که قرص L1 ، Jadenu ، Nanojade ، Osveral و Exjade در دسته داروهای خوراکی و Desferal و Desfonak در دسته داروهای تزریقی قرار گرفتند.
کلیه محاسبات آماری توسط نرمافزار 26 SPSS انجام شد. به منظور مقایسه میانگین متغیرهای کمی از آزمون تی مستقل و در صورت طبیعی نبودن توزیع دادهها از آزمون منویتنی[p5] [A6] و کروسکال والیس استفاده شد. همچنین برای ارزیابی رابطه بین متغیرهای کیفی از آزمون کایدو2) χ( و در صورت لزوم از آزمون دقیق فیشر استفاده شد. سطح معناداری آزمونها 05/0 p<در نظر گرفته شد و به منظور بررسی طبیعی بودن توزیع اطلاعات از آزمون شاپیرو ویلکس استفاده شد. در رابطه با حجم نمونه، برای پیدا کردن اندازه اثر بزرگ بر مبنای نظر متخصصین و مرجع، خطای نوع اول 01/0 و قدرت 95/0 در نرمافزار G*Power محاسبه شد (15).
یافتهها
در این مطالعه 232 بیمار در محدوده سنی 18 تا 76 سال[p7] [A8] و با میانگین سنی 02/9 ± 79/40 سال بررسی شدند. در مجموع 145 نفر (5/62%) زن و 87 نفر (5/37%) مرد بودند. میانگین شاخص توده بدنی (BMI) بیماران 87/2 ± 93/21 بود. بیماران در چهار گروه سنی تقسیمبندی شدند که نشان میدهد گروه سنی 31 تا 40 سال بیشترین فراوانی معادل 107 نفر (1/46%) را شامل میشد و همواره در تمامی گروهها، تعداد زنان از مردان بیشتر بود.
از بیـن 232 بیمـار بتـا تالاسمی ماژور و اینترمدیا مورد مطالعه، 64 نفر (6/27%) مبتلا به کمکاری تیروئید بودند که 36 نفر از آنان زن و 28 نفر مرد بودند. همچنین اطلاعات نشان داد که بین ابتلا به کمکاری تیروئید و جنسیت ارتباط

معناداری وجود نداشت. ابتلا به این عارضه در تمامی گروههای سنی نیز با آزمون کایدو بررسی و تفاوت معناداری در هیچ یک از گروهها مشاهده نشد. در هر دو گروه بیمار تالاسمی مبتلا و غیر مبتلا به کمکاری تیروئید، نزدیک به نیمی از آنان در گروه سنی 31 تا 40 سال قرار دارند، به طوری که 28 نفر از بیماران مبتلا به کمکاری تیروئید، معادل 7/43%، در این گروه سنی جای گرفتند (جدول 1). مقایسه میانگین BMI در هر دو گروه بیمار، هیچ ارتباط معناداری میان بیماران مبتلا و غیر مبتلا به کمکاری تیروئید و مقدار عددی BMI آنها نشان نداد و این نتیجه حاکی از آن است که بیماران به طور میانگیـن در
وضعیت مطلوبی از نظر وزنی قرار داشتند (نمودار 1).
بین غلظت فریتین و گروههای سنی مختلف بیماران ارتباط معناداری وجود نداشت. هم چنین بین غلظت فریتین در زنان و مردان نیز تفاوت معناداری یافت نشد ولی از کل بیماران با سرباری شدید آهن، 49 نفر (3/65%) را زنان و26 نفر (7/34%) را مردان تشکیل دادند.
28 نفر (7/43%) از بیماران مبتلا به کمکاری تیروئید، فریتین زیر ng/mL 1000 و فقط 16 نفر (25%) از آنان فریتین بالای ng/mL 2500 یا به عبارتی اضافه بار شدید آهن داشتند در حالی که این نرخ در گروه غیر مبتلا به کم کاری تیروئید بیشتر و معادل 59 نفر (35%) بود. با این وجود تفاوت فریتین سرمی در هر دو گروه بیمار مورد بررسی قرار گرفت و هیچ ارتباط معناداری میان بیماران مبتلا و غیر مبتلا به کمکاری تیروئید و فریتین سرمی یافت نشد (جدول 2).
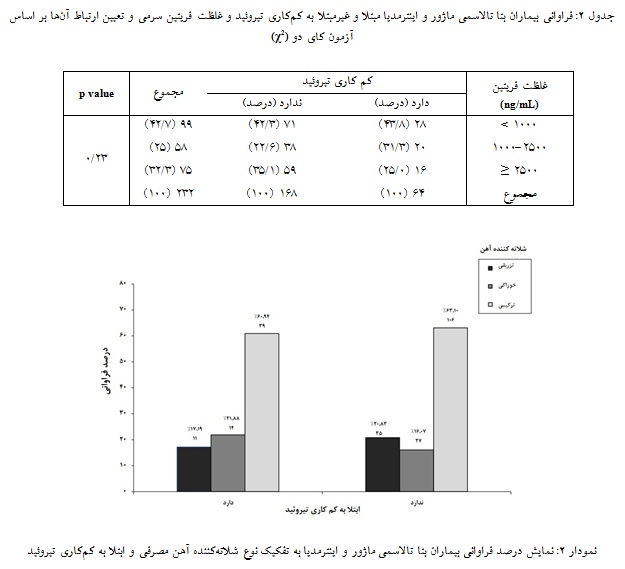
در بررسی شلاتهکننده های آهن، 46 نفر (%8/19) آهنزدا تزریقی، 41 نفر (7/17%) آهنزدا خوراکی و 145 نفر (5/62%) ترکیبی از هر دو را استفاده میکنند که بیشترین فراوانی متعلق به دسته آخر است. ولی هیچ تفاوت معناداری میان بیماران مبتلا و غیر مبتلا به کمکاری تیروئید در مصرف داروهای شلاتهکننده آهن یافت نشد (نمودار 2).
نتایج به دست آمده در این مطالعه نشان داد که بیشترین
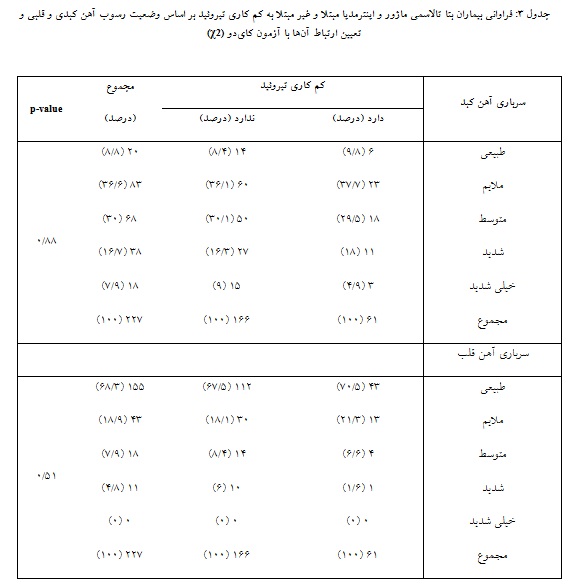
درصد از بیماران مبتلا (7/37%) و غیر مبتلا به کمکاری تیروئید (1/36%) دارای اضافه بار ملایم آهن کبدی هستند. 9% از بیماران غیر مبتلا به کمکاری تیروئید و فقط 9/4% از بیماران مبتلا دارای اضافه بار شدید آهن کبدی هستند. هیچ ارتباط معناداری میان دو گروه بیمار و رسوب آهن کبدی یافت نشد. همچنین بیشترین درصد از بیماران مبتلا (4/70%) و غیر مبتلا به کمکاری تیروئید (4/67%)، از لحاظ اضافه بار آهن قلبی در شرایط طبیعی هستند و در هیچ یک از گروهها سرباری شدید آهن قلبی مشاهده نشد. هیچ ارتباط معناداری میان دو گروه بیمار و رسوب آهن قلبی یافت نشد (جدول 3).
بین غلظت فریتین و گروههای سنی مختلف بیماران ارتباط معناداری وجود نداشت. هم چنین بین غلظت فریتین در زنان و مردان نیز تفاوت معناداری یافت نشد ولی از کل بیماران با سرباری شدید آهن، 49 نفر (3/65%) را زنان و26 نفر (7/34%) را مردان تشکیل دادند.
28 نفر (7/43%) از بیماران مبتلا به کمکاری تیروئید، فریتین زیر ng/mL 1000 و فقط 16 نفر (25%) از آنان فریتین بالای ng/mL 2500 یا به عبارتی اضافه بار شدید آهن داشتند در حالی که این نرخ در گروه غیر مبتلا به کم کاری تیروئید بیشتر و معادل 59 نفر (35%) بود. با این وجود تفاوت فریتین سرمی در هر دو گروه بیمار مورد بررسی قرار گرفت و هیچ ارتباط معناداری میان بیماران مبتلا و غیر مبتلا به کمکاری تیروئید و فریتین سرمی یافت نشد (جدول 2).
در بررسی شلاتهکننده های آهن، 46 نفر (%8/19) آهنزدا تزریقی، 41 نفر (7/17%) آهنزدا خوراکی و 145 نفر (5/62%) ترکیبی از هر دو را استفاده میکنند که بیشترین فراوانی متعلق به دسته آخر است. ولی هیچ تفاوت معناداری میان بیماران مبتلا و غیر مبتلا به کمکاری تیروئید در مصرف داروهای شلاتهکننده آهن یافت نشد (نمودار 2).
نتایج به دست آمده در این مطالعه نشان داد که بیشترین
درصد از بیماران مبتلا (7/37%) و غیر مبتلا به کمکاری تیروئید (1/36%) دارای اضافه بار ملایم آهن کبدی هستند. 9% از بیماران غیر مبتلا به کمکاری تیروئید و فقط 9/4% از بیماران مبتلا دارای اضافه بار شدید آهن کبدی هستند. هیچ ارتباط معناداری میان دو گروه بیمار و رسوب آهن کبدی یافت نشد. همچنین بیشترین درصد از بیماران مبتلا (4/70%) و غیر مبتلا به کمکاری تیروئید (4/67%)، از لحاظ اضافه بار آهن قلبی در شرایط طبیعی هستند و در هیچ یک از گروهها سرباری شدید آهن قلبی مشاهده نشد. هیچ ارتباط معناداری میان دو گروه بیمار و رسوب آهن قلبی یافت نشد (جدول 3).

تجزیه و تحلیل آماری هیچ ارتباط معناداری بین سطح هورمونهای تیروئیدی با گروههای مختلف سنی بیماران نشان نداد. اما نتایج جالبی در این مقایسهها به دست آمد. به طوری که بالاترین سطح هورمون TSH و پایینترین سطح هورمون T4 مربوط به گروه سنی بالای 50 سال و پایینترین سطح هورمون T3 مربوط به گروه سنی 41 تا 50 سال بود که میتواند نشاندهنده این باشد که احتمال ابتلا به کمکاری تیروئید با افزایش سن بیشتر شده است.
سطح هورمون T3 در دو جنس تفاوت معناداری نداشت اما سطح هورمون TSH در مردان به طور معناداری بالاتر از زنان بود (01/0=p) (نمودار 3). در حالی که سطح هورمون T4 در مردان به طور معناداری پایینتر از سطح این هورمون در زنان است (01/0 p<) (نمودار 4). لازم به ذکر است که با توجه به طبیعی نبودن توزیع دادهها، مقایسه هورمونهای تیروئیدی به واسطه گزارش میانه و چارک اول و سوم انجام شده است.
سطح هورمون T3 در دو جنس تفاوت معناداری نداشت اما سطح هورمون TSH در مردان به طور معناداری بالاتر از زنان بود (01/0=p) (نمودار 3). در حالی که سطح هورمون T4 در مردان به طور معناداری پایینتر از سطح این هورمون در زنان است (01/0 p<) (نمودار 4). لازم به ذکر است که با توجه به طبیعی نبودن توزیع دادهها، مقایسه هورمونهای تیروئیدی به واسطه گزارش میانه و چارک اول و سوم انجام شده است.

در مردان میانه:9/2، چارک اول:0/2، چارک سوم:9/4)
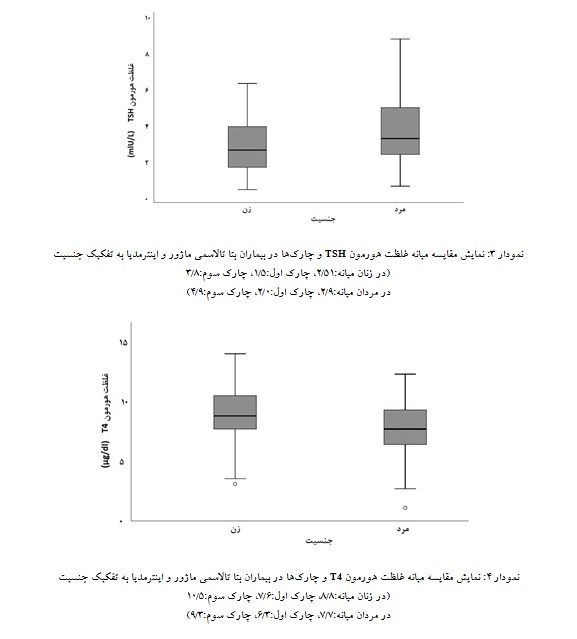
نمودار 4: نمایش مقایسه میانه غلظت هورمون T4 و چارکها در بیماران بتا تالاسمی ماژور و اینترمدیا به تفکیک جنسیت
(در زنان میانه:8/8، چارک اول:6/7، چارک سوم:5/10
در مردان میانه:7/7، چارک اول:3/6، چارک سوم:3/9)

نمودار 4: نمایش مقایسه میانه غلظت هورمون T4 و چارکها در بیماران بتا تالاسمی ماژور و اینترمدیا به تفکیک جنسیت
(در زنان میانه:8/8، چارک اول:6/7، چارک سوم:5/10
در مردان میانه:7/7، چارک اول:3/6، چارک سوم:3/9)
بحث
در مطالعه حاضر درصد فراوانی هیپوتیروئیدی در بیماران بتا تالاسمی ماژور و اینترمدیا ، 6/27% به دست آمد و نسبت شیوع آن در خانمها به آقایان 42/1 بود. در مقایسه میزان فریتین سرم در دو گروه مبتلا و غیر مبتلا به کمکاری تیروئید، نشان داده شد که هیچ ارتباط معنــاداری
بین میزان کنونی فریتین سرم و اختلال عملکرد غده تیروئید یافت نشد. به طوری که از کل بیماران با سربــاری
شدید آهن، بیشترین فراوانی متعلق به گـروه غیـر مبتلا به کمکاری تیروئید بوده است. علاوه بر این، سطح فریتین سرم بین زنان و مردان متفاوت نبود. در مطالعه ما هیچ ارتباط معناداری میان بیماران مبتلا و غیر مبتـلا به کمکاری
تیروئید و رسوب آهن قلبی و کبدی یافت نشد و حتی میتوان گفت که فراوانی افراد با رسوب شدید آهن کبدی، در گروه غیر مبتلا به کمکاری تیروئید بیشتر از گروه مبتلا به این عارضه بوده است. همچنین بیشترین درصد از بیماران در هر دو گروه از لحاظ اضافه بار آهن قلبی در شرایط طبیعی بودند.
مالیک و همکاران هیپوتیروئیدی اولیه را در 18 نفر (7/25%) از 70 بیمار گزارش کردهاند که تقریباً با نتیجه ما همخوانی دارد (16). همچنین در مطالعه کاشانچی و پورهروی، فراوانی بیماریهای غددی را در 206 بیمار تالاسمی ماژور بررسی کردند، شیوع هیپوتیروئیدی 65/20% با نسبت 71/1 زن به مرد گزارش شد (17). در حالی که در مطالعه مهرور و همکاران فراوانی هیپوتیروئیدی از بین 437 بیمار تالاسمی ماژور و اینترمدیا، 2/2% گزارش شد و نسبت زن به مرد 4/1 بود (18). که این نتیجه نسبت به مطالعه حاضر شیوع پایینتری را نشان میدهد. بر اساس گزارش فدراسیون بینالمللی تالاسمی، فراوانی کمکاری تیروئید در بیماران تالاسمی ماژور بین 6 تا 30 درصد است و این گستره متفاوت به دلیل تفاوتهای ژنتیکی، قومیتی، سن و درمانهای مختلف است (19).
در مطالعه لکزایی و همکاران در شهرستان زابل، از 117 بیمار مورد بررسی، 88/41% فریتین کمتر از μg/L 1000 و 12/58% فریتین بین μg/L 2000-1000 داشتند که از این نظر تقریباً مشابه نتایج ما بود ولی بین میانگین طیف فریتین زنان و مردان تفاوت معناداری بود (002/0 =p)(20). اشراقی و همکارانش سال 2011 در بابل، در مطالعهای که ارتباط عملکرد تیروئید کودکان با قد آنان و درمان آهنزدایی را بررسی میکرد، اعلام کردند بین کمکاری تیروئید و سطح فریتین سرم ارتباط معنادار پیدا نشد (3). دکتر طباطبائی و همکاران نیز، تفاوتی بین سطح سرمی فریتین در بیماران تالاسمی که اختلال غدد درونریز داشتند و عدهای که نداشتند مشاهده نکردند (21). گزارشهای ضد و نقیضی در مورد تاثیر آهن در بیماران تالاسمی ماژور بر روی عملکرد غده تیروئید وجود دارد و برخی از محققان بین سطح سرمی فریتین و عملکرد غده تیروئید رابطه مستقیمی را گزارش کردند. این موضوع شاید بدین علت باشد که فریتین سرم مقدار انباشتگی آهن در 3 ماه گذشته را نشان میدهد، در حالی که ایجاد اختلالات غددی نیازمند تماس طولانی با آهن اضافی است. دلیل دیگر، احتمالاً اختلاف در روش اندازهگیری فریتین سرم، اختلاف نژادی، تفاوت در رژیم غذایی، اختلاف در مکان و زمان انجام مطالعه است (22). با بهبود روشهای درمانی در بیماران تالاسمی ماژور، یعنی تزریق مکرر و منظم خون از یک طرف و درمان شدید و منظم آهنزدایی از طرف دیگر، امید به زندگی در بیماران تالاسمیک افزایش یافته است که به همین علت تماس طولانیتر آهن انباشته بدن با غدد درونریز، شانس اختلال عملکرد این ارگانها را افزایش داده است (23). به غیر از اضافه بار آهن، عوامل دیگری از جمله هایپوکسی مزمن ناشی از کمخونی میتواند مسئول آسیب به اندامها باشد و ممکن است سمیت رسوب آهن در غدد درونریز را تشدید کند (7). [A9]
طاهر و سالیبا در 2017 اعلام کردند، روش T2*MIR و R2 یک روش غیر تهاجمی و مناسب برای تعیین میزان غلظت آهن به جای بیوپسی کبد است. از طرفی فریتین سرم توانایی محدودی برای تعیین اضافه بار آهن قلب دارد، اما میتواند به طور قابل اعتمادی سیدروز قلبی و بیماری غدد درون ریز را پیشبینی کند. از این رو توصیه میشود در صورت دسترسی امکانات، در کنار فریتین از روشهای رزونانس هستهای جهت تعیین اضافه بار آهن و برنامهریزی برای دوز داروی شلاتهکننده آهن مصرفی استفاده شود (12). در مطالعه مقطعی که آتماکوسوما و همکارانش در 2021 بر روی 62 بیمار بتا تالاسمی ماژور وابسته به تزریق خون انجام دادند، ارتباط ضعیفی بین فریتین سرم با سمیت آهن قلب و عملکرد سیستولیک قلب گزارش شد. این محققان اظهار داشتند که مسمومیت قلبی در بیماران تالاسمی تحت تأثیر عوامل دیگری به غیر از مسمومیت با آهن است و باید عوامل بییشتری در مطالعهها در نظر گرفته شود (2).
نتیجهگیری
بـه نظـر مـیرسد اضافه بار آهن اعم از فریتین بالا و یا
رسوب آهن در ارگانها، میتواند تا حدودی در ابتلا به کمکاری تیروئید مؤثر باشد اما لزوماً بیمارانی که اضافه بار آهن دارند، کمکاری تیروئید ندارند. همچنین علیرغم درمان آهنزدایی، اضافه بار آهن هنوز یکی از عوارض اصلی تالاسمی به شمار میآید. با توجه به افزایش فراوانی هیپوتیروئیدی با افزایش سن و اثر مستقیمی که هیپوتیروئیدی بر عملکرد قلب دارد، اقدامات پیشگیرانه از جمله کنترل منظم عملکرد غده تیروئید با آزمایشهای دورهای اندازهگیری TSH و T4 سرم، قدم مهمی در تشخیص زودرس بیماری و کنترل و درمان آن میباشد.
پیشنهاد میشود به منظور دستیابی به نتایج دقیقتر، در مطالعههای بعدی نقطه صفر شروع کمکاری تیروئید در بیماران را در نظر گرفته و میزان بار آهن و درمان آهنزدایی در زمان قبل و بعد از بروز عارضه بررسی شود. هـم چنیـن بهتـر اسـت مطالعههـای بعـدی روی گستـره محدودتر سنی و تعداد برابر زنان و مردان انجام شود.
حمایت مالی
این مطالعه حاصل پایاننامه کارشناسی ارشد رشته بیوشیمی است و با حمایت معاونت پژوهشی دانشگاه
الزهرا به انجام رسیده است.
ملاحظات اخلاقی
در اجرای این پروژه کلیه موازین اخلاقی رعایت شده و اطلاعات دموگرافیک بیماران از طریق یک پرسشنامه و با رضایت آگاهانه آنها جمعآوری شده است. این پروژه دارای کد اخلاق IR.ALZAHRA.REC.1401.110 از دانشگاه الزهرا میباشد.
عدم تعارض منافع
نویسندگان این مقاله اعلام میدارند که در نگارش مقاله، هیچگونه تعارضی در منافع نبوده است.
تشکر و قدردانی
این مطالعه حاصل پایاننامه کارشناسی ارشد رشته بیوشیمی دانشگاه الزهرا است و بدین وسیله از مدیریت و پرسنل درمانگاه تالاسمی و بیماران تالاسمی عزیز که ما را در پیشبرد و تحقق این هدف یاری نمودند، کمال تشکر را داریم.
[A1]نوع ام آر آی مشخص شد
[A2]نحوه انتخاب نمونه تصحیح شد
[A3]اصلاح نگارشی انجام شد
[A4]جمله تصحیح و مختصر شد.
[p5]مان ویتنی
[A6]اصلاح نگارشی انجام شد
[A8]مطالعه روی بیماران بتا تالاسمی تحت تزریق خون مکرر( اعم از ماژور و اینترمدیا) انجام شده است. بیمار 76 ساله خانم مبتلا به بتا تالاسمی اینترمدیا و متولد 1325 بوده است.بیماران اینترمدیا اغلب طول عمر طولانی تری خواهند داشت.
[A9]با توجه به عنوان مقاله، هدف اصلی ما بررسی ارتباط آهن و ابتلا به هیپوتیروئیدی بوده است که الزام بحث در مورد آن را توجیه میکند!!!!
نوع مطالعه: پژوهشي |
موضوع مقاله:
اندوكرينولوژي
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |






