جلد 18، شماره 2 - ( تابستان 1400 )
جلد 18 شماره 2 صفحات 104-97 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Milani S, Yari F. Alloimmune lymphocytes proliferation in presence of Mixed Lymphocyte Culture and cyclosporine. Sci J Iran Blood Transfus Organ 2021; 18 (2) :97-104
URL: http://bloodjournal.ir/article-1-1409-fa.html
URL: http://bloodjournal.ir/article-1-1409-fa.html
میلانی سعیده، یاری فاطمه. تکثیر سلولهای لنفوسیتی آلوایمن در حضور کشت مخلوط لنفوسیتی و سیکلوسپورین. فصلنامه پژوهشی خون. 1400; 18 (2) :97-104
استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون
متن کامل [PDF 649 kb]
(1142 دریافت)
| چکیده (HTML) (2277 مشاهده)
مقدمه
کشت لنفوسیت مخلوط(MLC ؛ Mixed Lymphocyte Cultures) روشی است که جهت مطالعه میانکنشهای سلول ـ سلول بین زیر گروههای لنفوسیتی و تولید ترکیبات ناشی از این میانکنشها به کار میرود. جهت انجام آزمایش MLC ، دو روش مورد استفاده قرار میگیرد. روش اول، روش یک طرفه یا ONE WAY و روش دوم دو طرفه یا TWO WAY نام دارد که در نوع اول تنها یکی از دو گروه لنفوسیتی قادر به تکثیر هستند و در حالت دوم هر دو گروه لنفوسیت تکثیر مییابند(1). MLC دو طرفه اولین بار توسط بین و همکارانش معرفی شد و چندی بعد برای اندازهگیری سازگاری بافتی بین دو فرد مختلف مورد استفاده قرار گرفت(2). استفاده از واکنشهایMLC امکان انجام مطالعههای دقیقتر در مورد پاسخهای ایمنی در برابر سلولهای آلوژنیک را امکانپذیر میسازد(3).
سلولهای تک هستهای خون محیطی حاوی سلولهای ایمنی از جمله لنفوسیتهای B و T میباشند. یکی از راههای تهیه لنفوسیتهای B ، استفاده از خون محیطی است. تولید آنتیبادی در لنفوسیتهای B نیازمند تکثیر طولانی مدت این سلولها میباشد. مطالعههای قبلی نشان دادهاند که تکثیر لنفوسیتهای B در محیط MLC به علت فعالشدن لنفوسیتهای T کمکی در این محیط و اثر آنها بر لنفوسیتهای B ، افزایش مییابد(5، 4). سیتوکاینهای مختلفی همچون اینترلوکین 2، 4، 6، 10 و اینترفرون گاما بر اثر فعال شدن لنفوسیتهای T ناشی از تحریک سلولهای کوچک تک هستهای ایجاد میشوند که میتوانند در تکثیر لنفوسیتهای B اثرگذار باشند(6).
سیکلوسپورین A متابولیت قارچی است که بر روی سیستم ایمنی موثر بوده و میتواند به عنوان عامل مهار کننده سیستم ایمنی به کار رود. این ترکیب با جلوگیری از رونویسی برخی از ژنهای سیتوکاینی، میتواند فعالیت سلول T لنفوسیتی را مهار کند(7). سیکلوسپورین میتواند به طور مستقیم سلولهای B انسانی را با مکانیسمی مشابه عملکرد آن در لنفوسیتهای T مهار کرده و از ورود سلول به چرخه سلولی جلوگیری کند(8). از طرف دیگر سیکلوسپوریـن قـادر بـه مهـار آپوپتوز ناشی از فعال شدن
لنفوسیتها میباشد(9).
زمانی که سلولهای لنفوسیتی در معرض آنتیژن بیگانه قرار میگیرند، تکثیر لنفوسیتهای B و متعاقب آن تولید آنتیبادی ضد عامل تحریککننده آغاز میگردد. در این فرآیند لنفوسیتهای T کمکی، به لنفوسیتهای B کمک میکنند(10). لنفوسیتهای ایمن شده قادر به تولید آنتیبادی ضد آنتیژن مربوطه میباشند(11). آلوایمونیزاسیون ناشی از انتقال خون به علت دریافت مکرر خون حاوی آنتیژنهای گلبول قرمز بیگانه که در سطح گلبولهای قرمز فرد گیرنده وجود ندارند، ایجاد میگردد (13، 12). این فرآیند باعث تحریک لنفوسیتهای B فرد گیرنده میشود(14). این لنفوسیتها بعدها میتوانند به عنوان منبعی جهت تولید آنتیبادی ضد آنتیژن تحریکی مورد استفاده قرار بگیرند. از آنجایی که طول عمر این لنفوسیتها کم است، در مرحله بعد بایستی این سلولها نامیرا گردند تا امکان تولید مداوم آنتیبادی در آنها فراهم باشد. در کنار عوامل نامیرا کننده، حضور ترکیباتی که بتوانند به افزایش تکثیر سلولهای لنفوسیتی کمک کنند بسیار ضروری است(17-15). مطالعهها نشان دادهاند که سیتوکاینها میتوانند سبب افزایش فعالیت تکثیری و افزایش میزان آنتیبادی تولیدی توسط لنفوسیتهای B نامیرا گردند. این سیتوکاینها میتوانند طی واکنش MLC ایجاد شوند(18). بر این اساس، هدف اول این مطالعه، تولید MLC به عنوان منبع سیتوکاین، طی واکنش دو مرحله ای با در معرض قرار دادن گلبولهای قرمز خون فرد حاوی آنتیژن RhD با لنفوسیتهای خون محیطی فاقد این آنتیژن بود. از طرف دیگر استفاده از ترکیباتی که منجر به تکثیر جمعیت سلولهای خون محیطی میشود، میتواند در رشد و تکثیر لنفوسیتهای B به عنوان یکی از گروههای سلولی حاضر در این جمعیت نیز مؤثر باشد. در نتیجه، هدف بعدی این مطالعه، بررسی اثرات کلی MLC تولیدی بر تکثیر جمعیت سلولهای لنفوسیتی نمونه خون دارای پاسخ آلوایمنی با بررسی میکروسکوپی و روش رنگآمیزی سلولی با تریپانبلو بود. اثر داروی سرکوبکننده سیستم ایمنی سیکلوسپورین نیز بر تکثیر لنفوسیتها در حضور و یا عدم حضور MLC مورد مطالعه
قرار گرفت.
مواد و روشها
تهیه لنفوسیتهای خون محیطی:
مطالعه انجام شده از نوع تجربی بود؛ دو عدد کیسه خون کامل که یکی از آنها حاوی آنتیژن RhD (RhD مثبت) و دیگری فاقد آن (RhD منفی) بود از اهداکنندگانی که به پایگاه انتقال خون وصال تهران مراجعه کرده بودند و فرم رضایتنامه کتبی جهت انجام مطالعه بر روی نمونههای اهدایی را پر کرده بودند، دریافت گردید. لنفوسیتهای خون محیطی نمونهها به کمک فایکول(ایران، بهار افشان) و با استفاده از سانتریفیوژ شیب گرادیان جداسازی گردید. به طور خلاصه 3 میلیلیتر نمونه خونRhD مثبت و 3 میلیلیتر نمونه خون RhD منفی در لولههای هپارینه مجزا جمعآوری شدند. هر لوله خون به نسبت ۱: ۲ با نمک بافر فسفات استریل( (PBSرقیق و در لوله کاملاً مخلوط گردید و نمونهها در× g ۴۰۰ به مدت ۳۰ دقیقه در دمای اتاق سانتریفیوژ شدند. لنفوسیتهای هر دو نمونه دو بار با PBS در x g۱۰۰ به مدت ۱۰ دقیقه شستشو داده شدند. بعد از شستن سلولها، سلولها در حجم مناسب PBS مجدداً معلق وتعداد سلولها در هر دو نمونه با لام نئوبار شمارش گردیدند.
تهیه MLC:
پس از شمارش سلولی، تعداد مساوی لنفوسیت به میزان 106× 4/0 از هر دو گروه به داخل حفرههای چاهک 24 تایی منتقل گردید و پس از رساندن حجم پلیتها به 1 میلیلیتر به وسیله محیط RPMI(بیوراد، ایران) حاوی 10% آلبومین سرم گاوی، پلیتها به انکوباتور دارای 5% CO2 و دمای 37 درجه سانتیگراد منتقل گردیدند.
پس از یک هفته، سوپرناتانت رویی سلولها با سمپلر کشیده شده و پس از انتقال به فالکنهای 15 میلیلیتر، نمونهها در دور rpm 1900 به مدت 10 دقیقه سانتریفیوژ گردیدند. سوپ رویی مجدداً برداشته شد و پس از فیلتر کردن در داخل میکروتیوب منتقل و تا زمان استفاده در داخل فریزر قرار داده شد.
بررسی اثر MLC بر تکثیر سلولی:
دو عدد کیسه خون کامل از دو بیمار تالاسمی مراجعهکننده به مرکز درمان تالاسمی که در پرونده آنها فرم مربوط به رضایتنامه آگاهانه جهت انجام پژوهش بر روی نمونههای خون موجود در این مرکز وجود داشت، دریافت گردید. سوابق بیمار نشان میداد که در سرم وی آنتیبادی ضد آنتیژن RhE مشاهده شده و پاسخ آلوایمنی در بدن وی ایجاد گردیده است. لنفوسیتهای موجود در خون بیمار با روش فایکول مطابق با مراحل موجود در مرحله 1 روش کار جداسازی گردید. پس از شمارش سلولی با رنگآمیزی تریپان بلو، تعداد40000 سلول در حجم 50 میکرولیتر در داخل هر یک از حفرههای پلیت 96 حفره اضافه گردید.
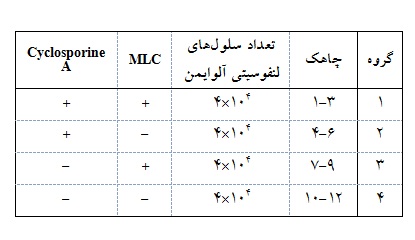
تمامی مراحل کار به صورت تکرار سه تایی انجام شد. به سه چاهک اول هر ردیف، MLC و سیکلوسپورین (کانادا، کایمن) به طور همزمان، به 3 چاهک بعدی فقط MLC ، به سه چاهک فقط سیکلوسپورین و به 3 چاهک آخر به عنوان کنترل چیزی اضافه نشد. حجم MLCمورد استفاده 50 میکرولیتر و سیکلوسپورین ng/mL 100 بود(19، 1). در نهایت حجم همه چاهکها با محیط RPMI 10% به 200 میکرولیتر رسید و سلولها به انکوباتور منتقل شدند(جدول 1).
جدول 1: تعداد سلولهای لنفوسیتی و ترکیب چاهکها جهت تیمار با MLC و سیکلوسپورین
بررسی میکروسکوپی چاهکها به مدت یک هفته با میکروسکوپ معکوس انجام گردید(شکل 1). همچنین زمانـی کـه تـراکم سلولهـا در چاهکهـا به بالاتر از 70% رسید، سلولها جهت بررسی میزان تکثیر با رنگآمیزی سلولی تریپانبلو و با استفاده از لام نئوبار شمارش شدند.
آنالیز آماری:
برای تحلیل دادههای حاصل از تکثیر سلولهای لنفوسیتی، میانگین و انحراف معیار بین گروههای دریافتکننده MLC و یا سیکلوسیورین و گروه کنترل با برنامه اکسل محاسبه شد. مقایسه میانگینها نیز با استفاده از نرمافزار Graphpad prism8 و انجام تست t جفت شده انجام گردید. سطح معناداری 05/0 p< در نظر گرفته شد.
یافتهها
با شمارش سلولی، میانگین تعداد سلولهای زنده در گروه 1 (دریافتکننده MLC و سیکلوسپورین) به 440000 سلول، در گروه 2 (دریافتکننده سیکلوسپورین) 300000، گروه 3 دریافتکنندهMLC)) 310000 و در گروه آخر (بدون MLC و سیکلوسپورین) 160000 سلول بود(جدول 2 و نمودار 1). هر چند اختلاف میانگینها بین گروههای دریافتکننده MLC و یا سیکلوسپورین و کنترل به لحاظ آماری معنادار نبود. تصاویر گروه 2 و 3 به علت مشابهت کلی توده سلولی با گروه 1، ارائه نشدهاند.
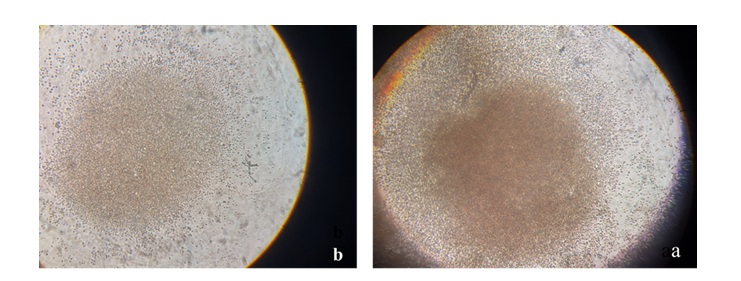
شکل 1: تصویر میکروسکوپی سلولهای تیمار شده با MLC و سیکلوسپورین. شکل a توده سلولهای دریافتکننده MLC و سیکلوسپورین (گروه 1) و شکل b سلولهای گروه کنترل(گروه 4) که هیچ یک از این دو تیمار را دریافت نکردهاند را نشان میدهد.

نمودار 1: نمودار میانگین تعداد سلولهای زنده در گروههای مختلف دریافتکنندهMLC و سیکلوسپورین، نشاندهنده تأثیر توأم MLC و سیکلوسپورین A در تکثیر بیشتر لنفوسیتهای به دست آمده از خون محیطی میباشد.
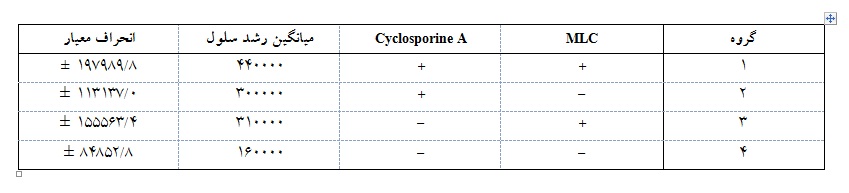
جدول 2: میانگین و انحراف معیار حاصل از رشد سلولهای لنفوسیتی پس از تیمار با MLC و سیکلوسپورین
بحث
عمدهترین یافته این مطالعه، افزایش تکثیر و زندهماندن سلولهای لنفوسیتی افراد آلوایمن بعد از در معرض قرار گرفتن با MLC بود. این یافته با مطالعههای قبلی انجام شده که در آن تعداد سلولهای زنده لنفوسیتی بعد از در معرض قرار گرفتن با MLC افزایش پیدا کرده بود مطابقت دارد (20، 19). از طرف دیگر با وجودی که از سیکلوسپورین به عنوان ترکیب مؤثر در مهار سیستم ایمنی یاد میشود، در مطالعه ما حضور سیکلوسپورین باعث افزایش تکثیر و زندهماندن لنفوسیتهای خون محیطی در مقایسه با گروه کنترل گردید. شاید یکی از دلایل آن، تداخل سیکلوسپورین با لنفوسیتهای T سیتوتوکسیک باشد که طی فرآیند آلوایمیونیزاسیون و تحریک لنفوسیتها ضد آنتیژن بیگانه ایجاد میگردد(21). در مقابل، این امر باعث فعال شدن و تکثیر لنفوسیتهای Tکمکی CD4+ میگردد که در نهایت به تکثیر لنفوسیتهای B و تمایز آنها به پلاسما سلها میانجامد(22). دلیل دیگر میتواند اثر مهارکنندگی سیکلوسپورین بر روی فرآیند آپوپتوز باشد که منجر به افزایش تعداد لنفوسیتها میشود(23). اثر بازدارنگی سیکلوسپورین بر روی آپوپتوز در حضور MLC در برخی مطالعهها اثبات شده است. لنفوسیتهایCD8+ سیتوتوکسیک باعث مهار تکثیر لنفوسیتهای B آلوایمن و سوق دادن آنها به سمت آپوپتوز در محیط In vitro میگردند در نتیجه مهار آنها میتواند به افزایش ماندگاری و تکثیر لنفوسیتهای B کمک کند(24). یکی از راههای تولید آنتیبادیهای مونوکلونال، افزایش تکثیر و القای نامیرایی در لنفوسیتهای محیطی تحریک شده با آنتیژن بیگانه، در محیط In vitro میباشد. در سال ۲۰۰۳، پاشا و همکـاران از لنفوسیـتهای خـون محیطـی خانمـی که در
دوران بارداری علیه آنتیژنهای Rh D وRh C ایمیونیزه شده بود، استفاده کرده و با استفاده از روش EBV Transformation ، موفق به تولید آنتیبادی علیه این آنتیژنها شدند(25). مشابه این کار در سال ۲۰۰۹ با استفاده از لنفوسیتهای افراد دارای Anti-D انجام شد که منجر به تولید آنتیبادی Anti-D گردید(26). بر طبق مطالعههای انجام شده، لنفوسیتهای B آلوایمن شده به عنوان سلولهای تولیدکننده آنتیبادی ضد آنتیژن تحریکی، نیاز به نامیرا شدن با عوامل نامیرا کننده جهت تولید مداوم آنتیبادی دارند. لذا استفاده از ترکیبات ادجوانتی همچون انواع سیتوکاینها با هدف کمک به تکثیر لنفوسیتهای Bو افزایش کارآیی ترانسفورماسیون همواره توصیه میگردد(28، 27). در این مطالعه اثرMLC به عنوان ترکیب حاوی سیتوکاینها و ادجوانتهای مختلف بر میزان تکثیر سلولهای لنفوسیتی خون محیطی نمونههای آلو ایمن شده به لحاظ بررسی میکروسکوپی و محاسبه زندهمانی سلولها پس از تیمار با رنگآمیزی حیاتی و استفاده از رنگ تریپانبلو بررسی گردید.
نتیجه مطالعه نشان داد که MLC و سیکلوسپورین در افزایش تکثیر و ماندگاری لنفوسیتهای خون محیطی مؤثر هستند. در این مطالعه افزایش تکثیر سلولی در سلولهایی که تحت تیمار MLC و سیکلوسپورین به طور همزمان بودند، از گروهی که فقط تیمار MLC یا فقط سیکلوسپورین دریافت کرده بودند بالاتر بود. به نظر میرسد استفاده از سیکلوسپورین به علت مهار اثر لنفوسیتهای T سیتوتوکسیک بتواند به تکثیر لنفوسیتهای B آلوآنتیژن و لنفوسیتهای T CD4+کمک کند. این اثر بخشی بایستی با آزمایشهای ایمونولوژی و سرولوژی اختصاصی، مورد بررسیهای بیشتر قرار بگیرد.
نتیجهگیری
MLC و سیکلوسپورین به تکثیر سلولهای لنفوسیتی کمک مینماید. با توجه به قابلیت استفاده از لنفوسیتهای B آلو ایمن به عنوان منبعی جهت تولید آنتیبادی، بررسی اثر MLC بر میزان تولید آنتیبادی در این سلولها در مقایسه با نمونه کنترل، با آزمایش سرولوژیکی الایزا به عنوان مرحله تکمیلی توصیه میگردد. به علت شرایط تولید آسان MLC و سهولت دسترسی به آن، در صورت تأیید این ترکیب با آزمایشهای تکمیلی بر روی نمونههای بیشتر
و دفعات بالاتر و همچنین تعیین این که چقدر از جمعیت سلولی تکثیر شده لنفوسیتهای B بودهاند، پتانسیل MLC و همین طور سیکلوسپورین به عنوان ترکیبات کمککننده در تکثیر و همچنین ایجاد شرایط مستعد جهت نامیرایی بعدی لنفوسیتهای B وتولید آنتیبادی در آنها بیشتر آشکار خواهد شد. این مطالعه حاصل بخشی از نتایج مربوط به طرح تحقیقاتی مصوب مؤسسه آموزشی و پژوهشی طب انتقال خون، با کد اخلاق IR.TMI.REC.1399.016 میباشد.
متن کامل: (2052 مشاهده)
تکثیر سلولهای لنفوسیتی آلوایمن در حضور کشت مخلوط لنفوسیتی و سیکلوسپورین
سعیده میلانی1، فاطمه یاری2
چکیده
سابقه و هدف
کشت لنفوسیتی مخلوط ((MLC جهت مطالعه میانکنش بین جمعیتهای لنفوسیتی و ترکیبات ناشی از این میانکنشها به کار میرود. تکثیر لنفوسیتها در محیط MLC، به علت ترشح سیتوکاینها در این محیط افزایش مییابد. سیکلوسپورین A به عنوان مهارکننده سیستم ایمنی به کار میرود. تزریق مکرر خون، باعث آلوایمیونیزاسیون لنفوسیتهای B میگردد. یکی از روشهای تولید آنتیبادی، نامیراسازی لنفوسیتهای B میباشد. سیتوکاینها با افزایش تکثیر لنفوسیت B به نامیراسازی کمک میکنند. با توجه به نقش MLC در تولید سیتوکاین، هدف این مطالعه، تولید MLC و بررسی آن در تکثیر سلولهای آلوایمن در حضور و عدم حضور سیکلوسپورین بود.
مواد و روشها
در یک مطالعه تجربی، لنفوسیتهای خون محیطی دو فرد که یکی حاوی آنتیژن RhD و دیگری فاقد آن بود با روش فایکول جداسازی و جهت تولید MLC در معرض هم قرار گرفتند. اثرMLC تولیدی و سیکلوسپورین بر تکثیر لنفوسیتهای آلوایمن با میکروسکوپ و رنگآمیزی تریپانبلو بررسی شد و نتایج با نرمافزار prism و مقایسه میانگینها با آزمون t-test جفت شده بررسی گردید(05/0 p<).
یافتهها
MLC و سیکلوسپورین باعث افزایش تکثیر لنفوسیتها با میانگین و انحراف معیار8/197989 ± 440000 در مقایسه با کنترل 8/84852 ± 160000 گردیدند.
نتیجه گیری
MLC و سیکلوسپورین به تکثیر سلولهای لنفوسیتی کمک میکنند. با تأیید آزمایشهای تکمیلی،MLC و سیکلوسپورین میتوانند در تکثیر لنفوسیتهای B به عنوان یکی از گروههای سلولی لنفوسیتی، جهت تولید آنتیبادی مؤثر واقع گردند.
کلمات کلیدی: سیکلوسپورینA ، کشت مخلوط لنفوسیتی، انتقال خون
تاریخ دریافت: 20/02/1400
تاریخ پذیرش: 09/03 /1400
1- مؤلف مسئول: PhD بیوتکنولوژی پزشکی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران ـ صندوق پستی: 1157-14665
2- PhD ایمونولوژی ـ استاد مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
سعیده میلانی1، فاطمه یاری2
چکیده
سابقه و هدف
کشت لنفوسیتی مخلوط ((MLC جهت مطالعه میانکنش بین جمعیتهای لنفوسیتی و ترکیبات ناشی از این میانکنشها به کار میرود. تکثیر لنفوسیتها در محیط MLC، به علت ترشح سیتوکاینها در این محیط افزایش مییابد. سیکلوسپورین A به عنوان مهارکننده سیستم ایمنی به کار میرود. تزریق مکرر خون، باعث آلوایمیونیزاسیون لنفوسیتهای B میگردد. یکی از روشهای تولید آنتیبادی، نامیراسازی لنفوسیتهای B میباشد. سیتوکاینها با افزایش تکثیر لنفوسیت B به نامیراسازی کمک میکنند. با توجه به نقش MLC در تولید سیتوکاین، هدف این مطالعه، تولید MLC و بررسی آن در تکثیر سلولهای آلوایمن در حضور و عدم حضور سیکلوسپورین بود.
مواد و روشها
در یک مطالعه تجربی، لنفوسیتهای خون محیطی دو فرد که یکی حاوی آنتیژن RhD و دیگری فاقد آن بود با روش فایکول جداسازی و جهت تولید MLC در معرض هم قرار گرفتند. اثرMLC تولیدی و سیکلوسپورین بر تکثیر لنفوسیتهای آلوایمن با میکروسکوپ و رنگآمیزی تریپانبلو بررسی شد و نتایج با نرمافزار prism و مقایسه میانگینها با آزمون t-test جفت شده بررسی گردید(05/0 p<).
یافتهها
MLC و سیکلوسپورین باعث افزایش تکثیر لنفوسیتها با میانگین و انحراف معیار8/197989 ± 440000 در مقایسه با کنترل 8/84852 ± 160000 گردیدند.
نتیجه گیری
MLC و سیکلوسپورین به تکثیر سلولهای لنفوسیتی کمک میکنند. با تأیید آزمایشهای تکمیلی،MLC و سیکلوسپورین میتوانند در تکثیر لنفوسیتهای B به عنوان یکی از گروههای سلولی لنفوسیتی، جهت تولید آنتیبادی مؤثر واقع گردند.
کلمات کلیدی: سیکلوسپورینA ، کشت مخلوط لنفوسیتی، انتقال خون
تاریخ دریافت: 20/02/1400
تاریخ پذیرش: 09/03 /1400
1- مؤلف مسئول: PhD بیوتکنولوژی پزشکی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران ـ صندوق پستی: 1157-14665
2- PhD ایمونولوژی ـ استاد مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
مقدمه
کشت لنفوسیت مخلوط(MLC ؛ Mixed Lymphocyte Cultures) روشی است که جهت مطالعه میانکنشهای سلول ـ سلول بین زیر گروههای لنفوسیتی و تولید ترکیبات ناشی از این میانکنشها به کار میرود. جهت انجام آزمایش MLC ، دو روش مورد استفاده قرار میگیرد. روش اول، روش یک طرفه یا ONE WAY و روش دوم دو طرفه یا TWO WAY نام دارد که در نوع اول تنها یکی از دو گروه لنفوسیتی قادر به تکثیر هستند و در حالت دوم هر دو گروه لنفوسیت تکثیر مییابند(1). MLC دو طرفه اولین بار توسط بین و همکارانش معرفی شد و چندی بعد برای اندازهگیری سازگاری بافتی بین دو فرد مختلف مورد استفاده قرار گرفت(2). استفاده از واکنشهایMLC امکان انجام مطالعههای دقیقتر در مورد پاسخهای ایمنی در برابر سلولهای آلوژنیک را امکانپذیر میسازد(3).
سلولهای تک هستهای خون محیطی حاوی سلولهای ایمنی از جمله لنفوسیتهای B و T میباشند. یکی از راههای تهیه لنفوسیتهای B ، استفاده از خون محیطی است. تولید آنتیبادی در لنفوسیتهای B نیازمند تکثیر طولانی مدت این سلولها میباشد. مطالعههای قبلی نشان دادهاند که تکثیر لنفوسیتهای B در محیط MLC به علت فعالشدن لنفوسیتهای T کمکی در این محیط و اثر آنها بر لنفوسیتهای B ، افزایش مییابد(5، 4). سیتوکاینهای مختلفی همچون اینترلوکین 2، 4، 6، 10 و اینترفرون گاما بر اثر فعال شدن لنفوسیتهای T ناشی از تحریک سلولهای کوچک تک هستهای ایجاد میشوند که میتوانند در تکثیر لنفوسیتهای B اثرگذار باشند(6).
سیکلوسپورین A متابولیت قارچی است که بر روی سیستم ایمنی موثر بوده و میتواند به عنوان عامل مهار کننده سیستم ایمنی به کار رود. این ترکیب با جلوگیری از رونویسی برخی از ژنهای سیتوکاینی، میتواند فعالیت سلول T لنفوسیتی را مهار کند(7). سیکلوسپورین میتواند به طور مستقیم سلولهای B انسانی را با مکانیسمی مشابه عملکرد آن در لنفوسیتهای T مهار کرده و از ورود سلول به چرخه سلولی جلوگیری کند(8). از طرف دیگر سیکلوسپوریـن قـادر بـه مهـار آپوپتوز ناشی از فعال شدن
لنفوسیتها میباشد(9).
زمانی که سلولهای لنفوسیتی در معرض آنتیژن بیگانه قرار میگیرند، تکثیر لنفوسیتهای B و متعاقب آن تولید آنتیبادی ضد عامل تحریککننده آغاز میگردد. در این فرآیند لنفوسیتهای T کمکی، به لنفوسیتهای B کمک میکنند(10). لنفوسیتهای ایمن شده قادر به تولید آنتیبادی ضد آنتیژن مربوطه میباشند(11). آلوایمونیزاسیون ناشی از انتقال خون به علت دریافت مکرر خون حاوی آنتیژنهای گلبول قرمز بیگانه که در سطح گلبولهای قرمز فرد گیرنده وجود ندارند، ایجاد میگردد (13، 12). این فرآیند باعث تحریک لنفوسیتهای B فرد گیرنده میشود(14). این لنفوسیتها بعدها میتوانند به عنوان منبعی جهت تولید آنتیبادی ضد آنتیژن تحریکی مورد استفاده قرار بگیرند. از آنجایی که طول عمر این لنفوسیتها کم است، در مرحله بعد بایستی این سلولها نامیرا گردند تا امکان تولید مداوم آنتیبادی در آنها فراهم باشد. در کنار عوامل نامیرا کننده، حضور ترکیباتی که بتوانند به افزایش تکثیر سلولهای لنفوسیتی کمک کنند بسیار ضروری است(17-15). مطالعهها نشان دادهاند که سیتوکاینها میتوانند سبب افزایش فعالیت تکثیری و افزایش میزان آنتیبادی تولیدی توسط لنفوسیتهای B نامیرا گردند. این سیتوکاینها میتوانند طی واکنش MLC ایجاد شوند(18). بر این اساس، هدف اول این مطالعه، تولید MLC به عنوان منبع سیتوکاین، طی واکنش دو مرحله ای با در معرض قرار دادن گلبولهای قرمز خون فرد حاوی آنتیژن RhD با لنفوسیتهای خون محیطی فاقد این آنتیژن بود. از طرف دیگر استفاده از ترکیباتی که منجر به تکثیر جمعیت سلولهای خون محیطی میشود، میتواند در رشد و تکثیر لنفوسیتهای B به عنوان یکی از گروههای سلولی حاضر در این جمعیت نیز مؤثر باشد. در نتیجه، هدف بعدی این مطالعه، بررسی اثرات کلی MLC تولیدی بر تکثیر جمعیت سلولهای لنفوسیتی نمونه خون دارای پاسخ آلوایمنی با بررسی میکروسکوپی و روش رنگآمیزی سلولی با تریپانبلو بود. اثر داروی سرکوبکننده سیستم ایمنی سیکلوسپورین نیز بر تکثیر لنفوسیتها در حضور و یا عدم حضور MLC مورد مطالعه
قرار گرفت.
مواد و روشها
تهیه لنفوسیتهای خون محیطی:
مطالعه انجام شده از نوع تجربی بود؛ دو عدد کیسه خون کامل که یکی از آنها حاوی آنتیژن RhD (RhD مثبت) و دیگری فاقد آن (RhD منفی) بود از اهداکنندگانی که به پایگاه انتقال خون وصال تهران مراجعه کرده بودند و فرم رضایتنامه کتبی جهت انجام مطالعه بر روی نمونههای اهدایی را پر کرده بودند، دریافت گردید. لنفوسیتهای خون محیطی نمونهها به کمک فایکول(ایران، بهار افشان) و با استفاده از سانتریفیوژ شیب گرادیان جداسازی گردید. به طور خلاصه 3 میلیلیتر نمونه خونRhD مثبت و 3 میلیلیتر نمونه خون RhD منفی در لولههای هپارینه مجزا جمعآوری شدند. هر لوله خون به نسبت ۱: ۲ با نمک بافر فسفات استریل( (PBSرقیق و در لوله کاملاً مخلوط گردید و نمونهها در× g ۴۰۰ به مدت ۳۰ دقیقه در دمای اتاق سانتریفیوژ شدند. لنفوسیتهای هر دو نمونه دو بار با PBS در x g۱۰۰ به مدت ۱۰ دقیقه شستشو داده شدند. بعد از شستن سلولها، سلولها در حجم مناسب PBS مجدداً معلق وتعداد سلولها در هر دو نمونه با لام نئوبار شمارش گردیدند.
تهیه MLC:
پس از شمارش سلولی، تعداد مساوی لنفوسیت به میزان 106× 4/0 از هر دو گروه به داخل حفرههای چاهک 24 تایی منتقل گردید و پس از رساندن حجم پلیتها به 1 میلیلیتر به وسیله محیط RPMI(بیوراد، ایران) حاوی 10% آلبومین سرم گاوی، پلیتها به انکوباتور دارای 5% CO2 و دمای 37 درجه سانتیگراد منتقل گردیدند.
پس از یک هفته، سوپرناتانت رویی سلولها با سمپلر کشیده شده و پس از انتقال به فالکنهای 15 میلیلیتر، نمونهها در دور rpm 1900 به مدت 10 دقیقه سانتریفیوژ گردیدند. سوپ رویی مجدداً برداشته شد و پس از فیلتر کردن در داخل میکروتیوب منتقل و تا زمان استفاده در داخل فریزر قرار داده شد.
بررسی اثر MLC بر تکثیر سلولی:
دو عدد کیسه خون کامل از دو بیمار تالاسمی مراجعهکننده به مرکز درمان تالاسمی که در پرونده آنها فرم مربوط به رضایتنامه آگاهانه جهت انجام پژوهش بر روی نمونههای خون موجود در این مرکز وجود داشت، دریافت گردید. سوابق بیمار نشان میداد که در سرم وی آنتیبادی ضد آنتیژن RhE مشاهده شده و پاسخ آلوایمنی در بدن وی ایجاد گردیده است. لنفوسیتهای موجود در خون بیمار با روش فایکول مطابق با مراحل موجود در مرحله 1 روش کار جداسازی گردید. پس از شمارش سلولی با رنگآمیزی تریپان بلو، تعداد40000 سلول در حجم 50 میکرولیتر در داخل هر یک از حفرههای پلیت 96 حفره اضافه گردید.
تمامی مراحل کار به صورت تکرار سه تایی انجام شد. به سه چاهک اول هر ردیف، MLC و سیکلوسپورین (کانادا، کایمن) به طور همزمان، به 3 چاهک بعدی فقط MLC ، به سه چاهک فقط سیکلوسپورین و به 3 چاهک آخر به عنوان کنترل چیزی اضافه نشد. حجم MLCمورد استفاده 50 میکرولیتر و سیکلوسپورین ng/mL 100 بود(19، 1). در نهایت حجم همه چاهکها با محیط RPMI 10% به 200 میکرولیتر رسید و سلولها به انکوباتور منتقل شدند(جدول 1).
جدول 1: تعداد سلولهای لنفوسیتی و ترکیب چاهکها جهت تیمار با MLC و سیکلوسپورین

بررسی میکروسکوپی چاهکها به مدت یک هفته با میکروسکوپ معکوس انجام گردید(شکل 1). همچنین زمانـی کـه تـراکم سلولهـا در چاهکهـا به بالاتر از 70% رسید، سلولها جهت بررسی میزان تکثیر با رنگآمیزی سلولی تریپانبلو و با استفاده از لام نئوبار شمارش شدند.
آنالیز آماری:
برای تحلیل دادههای حاصل از تکثیر سلولهای لنفوسیتی، میانگین و انحراف معیار بین گروههای دریافتکننده MLC و یا سیکلوسیورین و گروه کنترل با برنامه اکسل محاسبه شد. مقایسه میانگینها نیز با استفاده از نرمافزار Graphpad prism8 و انجام تست t جفت شده انجام گردید. سطح معناداری 05/0 p< در نظر گرفته شد.
یافتهها
با شمارش سلولی، میانگین تعداد سلولهای زنده در گروه 1 (دریافتکننده MLC و سیکلوسپورین) به 440000 سلول، در گروه 2 (دریافتکننده سیکلوسپورین) 300000، گروه 3 دریافتکنندهMLC)) 310000 و در گروه آخر (بدون MLC و سیکلوسپورین) 160000 سلول بود(جدول 2 و نمودار 1). هر چند اختلاف میانگینها بین گروههای دریافتکننده MLC و یا سیکلوسپورین و کنترل به لحاظ آماری معنادار نبود. تصاویر گروه 2 و 3 به علت مشابهت کلی توده سلولی با گروه 1، ارائه نشدهاند.

شکل 1: تصویر میکروسکوپی سلولهای تیمار شده با MLC و سیکلوسپورین. شکل a توده سلولهای دریافتکننده MLC و سیکلوسپورین (گروه 1) و شکل b سلولهای گروه کنترل(گروه 4) که هیچ یک از این دو تیمار را دریافت نکردهاند را نشان میدهد.

نمودار 1: نمودار میانگین تعداد سلولهای زنده در گروههای مختلف دریافتکنندهMLC و سیکلوسپورین، نشاندهنده تأثیر توأم MLC و سیکلوسپورین A در تکثیر بیشتر لنفوسیتهای به دست آمده از خون محیطی میباشد.

جدول 2: میانگین و انحراف معیار حاصل از رشد سلولهای لنفوسیتی پس از تیمار با MLC و سیکلوسپورین
بحث
عمدهترین یافته این مطالعه، افزایش تکثیر و زندهماندن سلولهای لنفوسیتی افراد آلوایمن بعد از در معرض قرار گرفتن با MLC بود. این یافته با مطالعههای قبلی انجام شده که در آن تعداد سلولهای زنده لنفوسیتی بعد از در معرض قرار گرفتن با MLC افزایش پیدا کرده بود مطابقت دارد (20، 19). از طرف دیگر با وجودی که از سیکلوسپورین به عنوان ترکیب مؤثر در مهار سیستم ایمنی یاد میشود، در مطالعه ما حضور سیکلوسپورین باعث افزایش تکثیر و زندهماندن لنفوسیتهای خون محیطی در مقایسه با گروه کنترل گردید. شاید یکی از دلایل آن، تداخل سیکلوسپورین با لنفوسیتهای T سیتوتوکسیک باشد که طی فرآیند آلوایمیونیزاسیون و تحریک لنفوسیتها ضد آنتیژن بیگانه ایجاد میگردد(21). در مقابل، این امر باعث فعال شدن و تکثیر لنفوسیتهای Tکمکی CD4+ میگردد که در نهایت به تکثیر لنفوسیتهای B و تمایز آنها به پلاسما سلها میانجامد(22). دلیل دیگر میتواند اثر مهارکنندگی سیکلوسپورین بر روی فرآیند آپوپتوز باشد که منجر به افزایش تعداد لنفوسیتها میشود(23). اثر بازدارنگی سیکلوسپورین بر روی آپوپتوز در حضور MLC در برخی مطالعهها اثبات شده است. لنفوسیتهایCD8+ سیتوتوکسیک باعث مهار تکثیر لنفوسیتهای B آلوایمن و سوق دادن آنها به سمت آپوپتوز در محیط In vitro میگردند در نتیجه مهار آنها میتواند به افزایش ماندگاری و تکثیر لنفوسیتهای B کمک کند(24). یکی از راههای تولید آنتیبادیهای مونوکلونال، افزایش تکثیر و القای نامیرایی در لنفوسیتهای محیطی تحریک شده با آنتیژن بیگانه، در محیط In vitro میباشد. در سال ۲۰۰۳، پاشا و همکـاران از لنفوسیـتهای خـون محیطـی خانمـی که در
دوران بارداری علیه آنتیژنهای Rh D وRh C ایمیونیزه شده بود، استفاده کرده و با استفاده از روش EBV Transformation ، موفق به تولید آنتیبادی علیه این آنتیژنها شدند(25). مشابه این کار در سال ۲۰۰۹ با استفاده از لنفوسیتهای افراد دارای Anti-D انجام شد که منجر به تولید آنتیبادی Anti-D گردید(26). بر طبق مطالعههای انجام شده، لنفوسیتهای B آلوایمن شده به عنوان سلولهای تولیدکننده آنتیبادی ضد آنتیژن تحریکی، نیاز به نامیرا شدن با عوامل نامیرا کننده جهت تولید مداوم آنتیبادی دارند. لذا استفاده از ترکیبات ادجوانتی همچون انواع سیتوکاینها با هدف کمک به تکثیر لنفوسیتهای Bو افزایش کارآیی ترانسفورماسیون همواره توصیه میگردد(28، 27). در این مطالعه اثرMLC به عنوان ترکیب حاوی سیتوکاینها و ادجوانتهای مختلف بر میزان تکثیر سلولهای لنفوسیتی خون محیطی نمونههای آلو ایمن شده به لحاظ بررسی میکروسکوپی و محاسبه زندهمانی سلولها پس از تیمار با رنگآمیزی حیاتی و استفاده از رنگ تریپانبلو بررسی گردید.
نتیجه مطالعه نشان داد که MLC و سیکلوسپورین در افزایش تکثیر و ماندگاری لنفوسیتهای خون محیطی مؤثر هستند. در این مطالعه افزایش تکثیر سلولی در سلولهایی که تحت تیمار MLC و سیکلوسپورین به طور همزمان بودند، از گروهی که فقط تیمار MLC یا فقط سیکلوسپورین دریافت کرده بودند بالاتر بود. به نظر میرسد استفاده از سیکلوسپورین به علت مهار اثر لنفوسیتهای T سیتوتوکسیک بتواند به تکثیر لنفوسیتهای B آلوآنتیژن و لنفوسیتهای T CD4+کمک کند. این اثر بخشی بایستی با آزمایشهای ایمونولوژی و سرولوژی اختصاصی، مورد بررسیهای بیشتر قرار بگیرد.
نتیجهگیری
MLC و سیکلوسپورین به تکثیر سلولهای لنفوسیتی کمک مینماید. با توجه به قابلیت استفاده از لنفوسیتهای B آلو ایمن به عنوان منبعی جهت تولید آنتیبادی، بررسی اثر MLC بر میزان تولید آنتیبادی در این سلولها در مقایسه با نمونه کنترل، با آزمایش سرولوژیکی الایزا به عنوان مرحله تکمیلی توصیه میگردد. به علت شرایط تولید آسان MLC و سهولت دسترسی به آن، در صورت تأیید این ترکیب با آزمایشهای تکمیلی بر روی نمونههای بیشتر
و دفعات بالاتر و همچنین تعیین این که چقدر از جمعیت سلولی تکثیر شده لنفوسیتهای B بودهاند، پتانسیل MLC و همین طور سیکلوسپورین به عنوان ترکیبات کمککننده در تکثیر و همچنین ایجاد شرایط مستعد جهت نامیرایی بعدی لنفوسیتهای B وتولید آنتیبادی در آنها بیشتر آشکار خواهد شد. این مطالعه حاصل بخشی از نتایج مربوط به طرح تحقیقاتی مصوب مؤسسه آموزشی و پژوهشی طب انتقال خون، با کد اخلاق IR.TMI.REC.1399.016 میباشد.
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |






