جلد 18، شماره 3 - ( پاییز 1400 )
جلد 18 شماره 3 صفحات 214-205 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Baban َ, Keshavarzi F, Nikkhoo B. Association of rs855791TMPRSS6 polymorphism with iron deficiency anemia. Sci J Iran Blood Transfus Organ 2021; 18 (3) :205-214
URL: http://bloodjournal.ir/article-1-1405-fa.html
URL: http://bloodjournal.ir/article-1-1405-fa.html
بابان آناهیتا، کشاورزی فاطمه، نیکخو بهرام. ارتباط پلیمورفیسم rs855791 TMPRSS6 با آنمی فقر آهن. فصلنامه پژوهشی خون. 1400; 18 (3) :205-214
دانشیار گروه زیست شناسی، واحد سنندج، دانشگاه آزاد سنندج
متن کامل [PDF 580 kb]
(841 دریافت)
| چکیده (HTML) (1555 مشاهده)
مقدمه
از آن جایی که تمام سلولهای بدن انسان برای زنده ماندن به اکسیژن وابستهاند، کمبود آن باعث هیپوکسی شده و گستره وسیعی از مشکلات را به همراه دارد(5-1).
کم خونی میتواند در تمامی مراحل زندگی رخ دهد اما بیشتر در دوران بارداری و سنین پایین و یا افراد مسن خود را نشان میدهد(2). کم خونی انواع گوناگونی دارد که هر یک علت خاص خود را دارند. این بیماری بر اساس گوناگونی ریختشناسی گلبولهای قرمز و مکانیسمهای اتیولوژیک طبقهبندی میشود. سه علت اصلی آن از دست رفتن حجم زیادی از خون(خونریزیهای حاد یا مزمن)، از بین رفتن سلولهای خونی(همولیز) و کمبود تولید سلولهای خونی است. از علل کاهش تولید سلولهای خونی؛ کمبود آهن، کمبود ویتامین B12، تالاسمی و تعدادی نئوپلاسم مغز استخوان میباشد. علل افزایش همولیز شامل تعدادی شرایط ژنتیکی مانند کم خونی داسی شکل، عفونت مانند مالاریا و برخی از بیماریهای خود ایمنی است(3).
عموماً آزمایش شمارش کامل خون را جزو آزمایشهای نخستین برای تشخیص کم خونی، درنظر میگیرند. علاوه بر شمارش گلبول های قرمز و مقدار هموگلوبین، دستگاه خودکار شمارنده، اندازه گلبولهای قرمز را با فلوسیتومتری اندازه میگیرند که یک عامل مهم در افتراق میان علل گوناگون کم خونی میباشد. برای مردان بالغ هموگلوبین کمتر از gr/dL 13، نشانه کم خونی است و برای زنان بالغ این مقدار gr/dL 12 میباشد(5، 4).
علاوه بر عوامل تغذیهای و بیماریهای عفونی که از مهمترین عوامل بیماری کم خونی فقر آهن هستند، جهشهای ژنتیکی نیز در کم خونی فقر آهن مؤثرند. جهش در ژنهای کد کننده زیر واحدهای هموگلوبین که منجر به تالاسمی و جهش در ژن Serine 6 (TMPRSS6) ، Transmembrane protease که باعث کمخونی فقر آهن میشود، از آن جمله است(1). در انسان محصول ژن TMPRSS6 پروتئینی به نام ماتریپتاز 2 است که تنظیم کننده پروتئین دیگری به نام هپسیدین میباشد. هپسیدیـن تنظیمکننــده کلیــدی تعــادل آهــن در بــدن
است(1).
ژن TMPRSS6 از 18 اگزون تشکیل شده است، که این اگزونها کدکننده دومینهای پروتئین ماتریپتاز2 هستند، دومین سرین پروتئازی پروتئین توسط اگزونهای 15 تا 18 کد میشوند(3). ماتریپتاز 2 ، سرین پروتئاز سطح سلولی با ساختار نوسانی است که به عنوان تنظیمکننده منفی بیان هپسیدین میباشد(4). این هورمون به عنوان اصلیترین تنظیمکننده آهن خون در انسان و سایر پستانداران شناخته شده است(6، 1).
فعال شدن هپسیدین باعث کمبود شدید آهن در موش و انسان میگردد در حالی که بیان بالای هپسیدین باعث کم خونی فقر آهن میشود(6). جهشهای ژن TMPRSS6 تا حد زیادی میزان عملکرد ماتریپتاز 2 را کاهش میدهد. کمبود ماتریپتاز 2 سطح بسیار بالایی از هپسیدین را به وجود میآورد که این منجر به مهار جذب آهن در رژیم غذایی و ایجاد فنوتیپ کمخونی فقرآهن شدید میشود. بنابراین ماتریپتاز 2 بهعنوان یک تنظیمکننده منفی بیان ژن هپسیدین مشخص شده است(1).
مطالعههای مرتبط با ژنوم چندین پلیمورفیسم تک نوکلئوتیدی SNP) ، Single Nucleotide polymorphism) را که بر فنوتیپ سلولهای خونی مؤثرند، نشان داده است. همه این پلیمورفیسمهای شناسایی شده مربوط به ژن TMPRSS6 است که در میان آنهـا rs855791 بیشتـرین ارتباط را با سطح هموگلوبین داشته است(7، 6).
در سال 2018 ، باتار و همکاران ، نقش برخی از انواع پلیمورفیسمهای این ژن را در پارامترهای خون مرتبط با آهن در بیماران ترک با کم خونی فقر آهن بررسی کردند و دریافتند کـه تغییرات rs855791 بـا افزایــش RBC و TIBC در این بیماران همراه است(8). در سال 2019، کاکماکلی و همکـاران طیـف جهــشهای ژن TMPRSS6 را در کم خونی فقر آهن با گزارش یک حذف 374 جفت بازی هموزیگوت در اگزون 15 ژن گزارش دادند(9). در آفریقای جنوبی سال 2019 ، نالادو شناسایی و ارتباط بین چند شکلی rs855791 را با افزایش حساسیت به کم خونــی فقـر آهن در بیماران مبتلا بــه نارسایی مزمن کلیه بدون دیالیز انجام داد(10).
پلیمورفیسم تک نوکلئوتیدی rs855791 بر روی کروموزوم 22، اگزون 17 بخش عملکردی ژن TMPRSS6 را به نام V736A شناخته است. در موقعیت 736 این ژن یک تغییرتک نوکلئوتیدی منجر به جایگرینی آمینو اسید آلانین به جای والین شده و لذا توانایی آنزیم برای مهار رونویسی هپسیدین کاهش یافته است(12، 11). یافتهها نشان میدهد که این جایگزینی ممکن است باعث تغییر در ساختار پروتئین شده و باعث کاهش دسترسی به جایگاه فعالسازی پیش آنزیم TMPRSS6 گردد(13).
لذا هدف از این مطالعه بررسی ارتباط پلیمورفیسم rs855791 TMPRSS6 با آنمی فقرآهن در افراد مبتلا در شهر سنندج بود.
مواد و روشها
تحقیق حاضر یک مطالعه شاهد- موردی بود. این بررسی در قالب یک پایاننامه کارشناسی ارشد توسط شورای پژوهشی دانشگاه آزاد اسلامی ـ واحد علوم و تحقیقات کردستان از لحاظ اخلاقی و پژوهشی تایید شد. نمونهگیری به صورت تصادفی بدون محدودیت سن و جنس و فقط بر اساس نتایج آزمایشهای کم خونی در یک فاصله زمانی 3 ماهه در بهار سال 1394 و با همکاری آزمایشگاههای خصوصی در سطح شهر سنندج انجام شد. در مجموع 120 نفر با رضایت شخصی و به صورت تصادفی انتخاب شده و در این مطالعه شرکت کردند. تشخیص کم خونی بر اساس معیارهای سازمان بهداشت جهانی یعنی آزمایشهای CBC ، اندازه گلبولهای قرمز (27< MCH & 80 MCV<)، هماتوکریت، هموگلوبین (برای مردان بالغ کمتر از gr/dL 13 و برای زنان بالغ کمتر gr/dL 12) و آزمایش فریتین(کمتر از 15 نانوگرم بر میلیلیتر با حساسیت 59% و ویژگی 99%) صورت گرفت. از این تعداد با توجه به نتایج آزمایشها و بر اساس تائید پزشک، 40 نفر از افراد با آنمی فقر آهن، و 80 نفر کنترل سالم بودند. 5 میلیلیتر نمونه خون از همه شرکتکنندگان در لولههای CBC حاوی ماده ضد انعقاد جمعآوری شـد و بعـد از چنـد بار اینورت کردن در فریزر 20- درجه سانتیگراد تا زمان انجام آزمایش قرار گرفت.
استخراج DNA :
استخراج DNA از خون با کیت استخراج High Yirld DNA Purification Kit محصول شرکت سیناژن (سیناژن: تهران، ایران) و بر اساس دستورالعمل کیت انجام شد. در ادامه با استفاده از جذب نوری در اسپکتروفتومتر و الکتروفورز بر روی ژل آگارز 1% ، تعیین کمیت و کیفیت DNA های استخراج شده، صورت گرفت. DNA جداسازی شده در میکروتیوبهای جداگانه در دمای 20- درجه سانتیگراد تا زمان انجام PCR نگهداری شد.
تعیین ژنوتیپها:
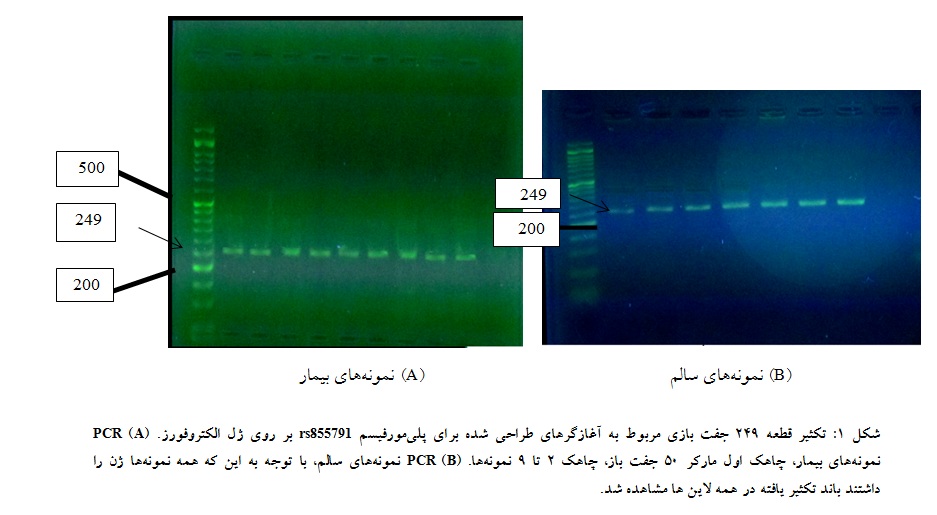
توالی آغازگرها از مطالعههای پیشین، بعد از انجام بلاست تایید و به شرکت سیناژن سفارش داده شد(1) (جدول 1). فرآیند PCR در حجم نهایی µL 20 با استفاده از کیت PCR شرکت سیناژن و توسط دستگاه سیکلوترون Rotor-Gene Q(Corbett Life Science) انجام شد(جدول 2). برای اطمینان از تکثیر درست قطعه مورد نظر، محصول PCR بر روی ژل آگارز 8/1 درصد بارگذاری و تعیین کیفیت گردید(شکل 1).
جهت مشاهده پلیمورفیسم طبق دستورالعمل، 1 میکرولیتر از آنزیم محدود کننده Stu l به 10 میکرولیتر محصول PCR اضافه شد و سپس به آن 2 میکرولیتر بافر اضافه گردید. سپس حجم نهایی توسط 27 میکرولیتر آب مقطر دوبار تقطیر به 40 میکرولیتر رسید و به مدت 10 تا 20 دقیقه در دمای 37 درجه سانتیگراد دستگاه بن ماری انکوبه شد. پس از انکوبه کردن، محصول حاصله دوباره الکتروفورز گردید(شکل 2).
برای برش ناحیه مورد نظر، آنزیم Stu l جایگاه تشخیص آن در rs855791 به صورت توالی پالیندرومیک AGGCCT میباشد و در نتیجه در صورت وجود آلل C در جایگاه پلیمورف آنزیم قطعه را برش میدهد و در صورت وجود آلل T قطعه برش نمی خورد. با توجه به این که اگر فرد سالم باشد آنزیم Stu l آلل وحشی را که C میباشد برش میدهد، لذا 2 باند در 123 و 126 داریم و با توجه به این که این طول قطعهها به هم نزدیک هستند، هنگـام الکتروفـورز محصـول روی ژل فقـط یـک باند در


نزدیک ناحیه 125 میبینیم، یعنی هر دو آلل آن فرد سالم بوده (هموزیگوت) و به صورت CC میباشد. مشاهده یک باند 249 جفت بازی بر روی ژل نشاندهنده پلیمورفیسم میباشد با توجه به این که آنزیم آلل C را برش میدهد، در این حالت جایگاه برش آنزیم Stu l نمیباشد و در حین run کردن بر روی ژل در ناحیه 249 تک باند داریم که به صورت TT است. در صورتی که سه باند در الکتروفورز مشاهده گردد، ژنوتیپ به صورت TC قابل مشاهده میباشد. یک باند در ناحیه 249 و دو باند در ناحیه 123 و 126 باید داشته باشیم که به علت نزدیک بودن، باند را در ناحیه نزدیک 125 میبینیم.
تحلیل آماری:
آنالیز آماری دادهها با استفاده از نرمافزار 32/1 popgene و 19 SPSS و در سطح معنادار(05/0 p<) انجام شد.
یافتهها
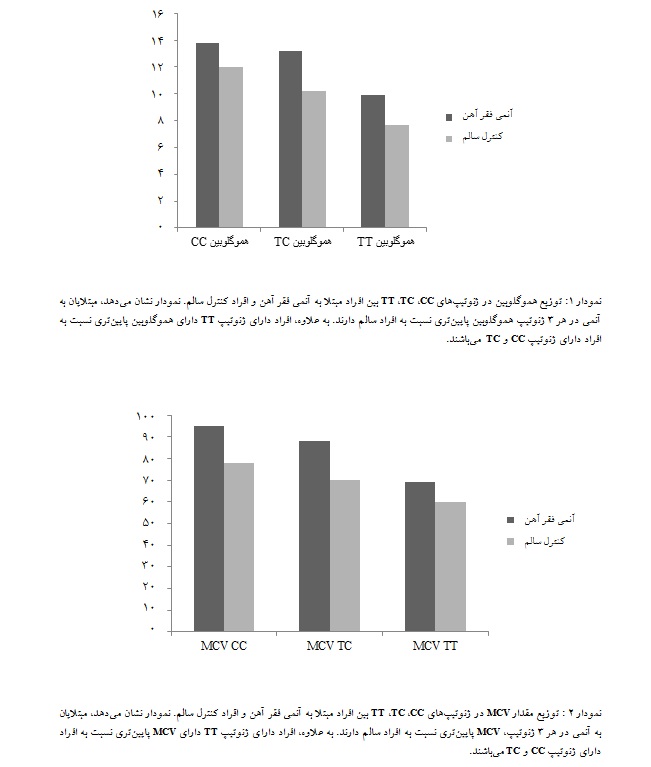
نتایج تجزیه و تحلیل آماری توزیع ژنوتیپ rs855791 در جدول آمده است(جدول 3). همان طور که مشاهده میشود فراوانی ژنوتیپهای CC، CT و TT در بین 40 بیمار و 80 نفر کنترل سالم به ترتیب 15، 5/37 ، 5/47 و 75/33، 5/42 و 75/23 درصد بوده است(نمودار 1). فراوانی TT در افراد بیمار بالا (5/47%) و فراوانی آن در افراد سالم تا حدودی بالا(75/23%) بود. با توجه به نتایج به دست آمده ارتباط معناداری وجود دارد(01/0 p=). با توجه به جدول 3 ، تجزیه و تحلیل دادههای ژنوتیپ CC نشان میدهد که چون 035/0 p= و 346/0 OR= است و همچنین فراوانی ژنوتیپ CC در افراد سالم از بیمار بیشتر است که این نشان دهنده غالب بودن ژنوتیپ CC در افراد سالم نسبت به افراد بیمار میباشد، در نتیجه احتمال بروز ایجاد کم خونی فقرآهن در افراد سالم که دارای ژنوتیپ CC میباشند کم است.
همچنبن در ارتباط با ژنوتیپ CT، مشاهده می شود که p معنادار نمیباشد و هم چنین فراوانی بیشتر CT در گروه کنترل نسبت به گروه بیمار، نشان میدهد که احتمال ابتلا به کم خونی فقر آهن در افرادی با ژنوتیپ CT کمتر است. طبق نتایج به دست آمده 010/0 p= و 905/2 OR= ، رابطه معناداری بین ژنوتیپ TT و ابتلا به بیماری کم خونی فقرآهن در افراد بیمار نسبت به افراد سالم وجود دارد که نشاندهنده غالب بودن ژنوتیپ TT در بین افراد بیمار میباشد و هم چنین با توجه به 905/2 OR= به دست آمده میتوان نتیجه گرفت در افراد سالمی که دارای ژنوتیپ TT میباشند، احتمـال ابتـلا بـه کـم خونـی فقر آهن بالا است.

همچنین نمودارهای 1 تا 3 ارتباط بین پلیمورفیسمهای rs855791 و سطح فاکتورهای خونی هموگلوبین، حجم متوسط گلبول قرمز خون و میزان فریتین بیماران و افراد کنترل را با توجه به بررسی پرونده بیماران و پرسشنامههای پر شده نشان میدهد. نتایج ارتباط معناداری بین پایین بودن Hb ،MCV و Ferritin و ژنوتیپ را نشان میدهد، به طوری که افراد دارای ژنوتیپ TT دارای Hb ،MCV وFerritin پایینتر نسبت به افراد دارای ژنوتیپ CC و TC میباشند.

بحث
در تحقیق حاضر ارتباط بین پلیمورفیسم T/C rs855791 و آنمی فقر آهن در 40 فرد مبتلا به آنمی فقر آهن و 80 فرد سالم در سنندج بررسی شده است. فراوانی ژنوتیپهای CC ، CT و TT در بین 40 بیمار و 80 نفر کنترل سالم به ترتیب 15، 5/37 ، 5/47 و 75/33، 5/42 و 75/23 درصد بود. با توجه به نتایج آماری، رابطه معناداری بین ژنوتیپ TT و ابتلا به بیماری وجود داشت(010/0 p= و 905/2 OR=). همچنین بین فراوانی ژنوتیپ CC و عدم ابتلا به کم خونی فقر آهن رابطه معناداری مشاهده شد(035/0 p=و 346/0 OR=). فراوانی بیشتر CT در گروه کنترل نسبت به گروه بیمار، نشان داد که احتمال ابتلا به کم خونی فقر آهن در افرادی با ژنوتیپ CT کمتر است. هم چنین در بررسیهای صورت گرفته بر روی ارتباط پلیمورفیسم تک نوکلئوتیدی rs855791 با سطح فاکتورهای Hb ، MCV و فریتین، نتایج نشان داد که این پلیمورفیسم احتمال خطر ابتلا به کم خونی فقرآهن را در بین افـرادی بـا ژنوتیـپ TT بـالا برده و فاکتورهای کمبود
هموگلوبین، فریتین و MCV این خطر را تا حدود زیادی بالا میبرد.
بنیامین و همکاران در سال 2009 بر روی 2516 نوجوان استرالیایی، ارتباط میان سطح فاکتورهای خونی MCV و هموگلوبین با پلیمورفیسم rs855791 را مورد مطالعه قرار دادند. نتایج نشان داد که پایین بودن سطح هموگلوبین رابطه معناداری با پیش آگهی و افزایش خطر ابتلا به همراه دارد(6)(008/0 p=).
در مطالعهای که جان چمبرز و همکارانش در سال 2009 بر روی 5187 نفر اروپایی و 6721 نفر آسیایی (هندی) انجام دادند، مشخص شد که ارتباط معناداری بین تغییر نوکلئوتیدی والین به آلانین در ناحیه 736 پلیمورفیسم تک نوکلئوتیدی rs855791 با سطح هموگلوبین و شدت بیماری وجود دارد(001/0 p=). همچنین مطالعه نشان داد، در مناطقی با فقر تغذیهای، کم خونی فقر آهن به صورت چشمگیری افزایش یافته و سطح هموگلوبین و آهن ذخیرهای بدن کاهش مییابد(7).
در مطالعهای که پائلو دلبینی و همکـاران در سال 2010
در میلان ایتالیا بر روی 16 فرد بیمار انجام دادند، اثر پلیمورفیسمهای rs855791 بر مسیر سیگنالینگ پروتئین ماتریپتاز 2 و اختلال در تولید هپسیدین بررسی شد. نتایج نشان داد در افراد بیماری با ژنوتیپ TT ، سطح هموگلوبین به طور چشمگیری پایین بوده و بین این پلیمورفیسم و سطح هموگلوبین رابطه معناداری وجود دارد(001/0 p= ، 18/5 OR=). همچنین این مطالعه نشان داد که پلیمورفیسمهای تک نوکلئوتیدی بد معنی(rs855791) باعث ایجاد تغییر در ناحیه دومین سرین پروتئازی پروتئین ماتریپتاز 2 شده، در نتیجه عملکرد کاتالیتیکی این پروتئین دچار اختلال میشود(14).
گان و همکاران در سال 2012 با بررسی 1574 فرد چینی، ارتباط پلیمورفیسمهای ژن TMPRSS6 با فریتین، هموگلوبین و خطر ابتلا به دیابت نوع دوم را مطالعه کردند. نتایج آنها نشان داد که پلیمورفیسم rs855791 با کاهش هموگلوبین و هم چنین فریتین پلاسما خطر افزایش بار آهن را در بدن بالا برده و احتمال خطر ابتلا به دیابت نوع 2 را نیز بالا خواهد برد(031/0 p=)(15).
سال 2014 پی و همکاران ارتباط پلیمورفیسم rs855791 با کم خونی فقر آهن را بر روی 67 مبتلا و 107 نفر داوطلب سالم به روش PCR-RFLP بررسی نمودند. نتایج نشان داد همه شاخصهای گلبول قرمز، پلاکت، هموگلوبین، فریتین و حجم متوسط گلبولهای قرمز به طور قابل توجهی بین دو گروه متفاوت است(03/0 p=)، که با نتایج این مطالعه همخوانی دارد(16).
در مطالعه شینتا و همکاران سال 2019 در لومبوک شرقی و اندونزی بر روی کودکان 6 تا 17 ماهه هیچ ارتباطی بین پلیمورفیسم rs855791 با گیرنده ترانسفرین محلول (sTfR)و غلظت هموگلوبین سرم به دست نیامد(17).
در مطالعهای در سال 2020 توسط آلامر روی 108 دانشجوی دختر 18 تا 25 سال در پادشاهی عربستان سعودی، پلیمورفیسمrs855791 با وضعیت آهن دارای ارتباط معناداری بود(11).
کم خونی همچنان به عنوان یک مشکل بهداشت جهانی گسترده و قابل توجه باقی مانده است که باید به طور کافی مورد بررسی قرار گیرد. اگر چه آنمی فقر آهن در اکثر مناطق دلیل اصلی کم خونی است، اما تحقیقهای اخیر نشان میدهد که علت کم خونی پیچیده و مختص به هر منطقهای است. برای درک بیشتر چگونگی کمک به دلایل اصلی کم خونی، از جمله آنمی فقر آهن و سایر کمبودهای تغذیهای، بیماریها و اختلالات Hb ، در کم خونی لازم است تلاش شود تا مداخلات مناسب در شرایط خاص قابل اجرا باشد. همچنین مطالعههای بیشتر در مقیاس بیماران بیشتر برای شناسایی هاپلوتیپهای بالقوه و چند شکلیهای مسئول پاسخ کم به درمان خوراکی آهن ضروری است و ممکن است برای برنامهریزی یک مکمل صحیح آهن مفید باشد. سؤال دیگری که در این بررسیها باید به آن پاسخ داد این است که آیا تجویز مکمل غذایی آهن به کودکان، باید بر اساس مشخصات ژنتیکی باشد، به ویژه برای کودکانی که در TMPRSS6 جهش دارند؟
نتیجهگیری
بالا بودن فراوانی ژنوتیپ TT در بین افراد مبتلا به کم خونی فقرآهن(5/47%)، در جمعیت مورد بررسی نشان میدهد خطر ابتلا به بیماری با ژنوتیپ TT رابطه معناداری دارد(010/0 p= و 905/2 OR=). هم چنین رابطه معناداری بین ژنوتیپ TT و سطح پایین فاکتورهای خونی هموگلوبین، فریتین و حجم متوسط گلبولهای قرمز وجود داشت.
تشکر و قدردانی
بدینوسیله نویسندگان مقاله از همکاری پرسنل زحمتکش آزمایشگاه پاتولوژی نور، تشکر و قدردانی مینمایند.
متن کامل: (1718 مشاهده)
ارتباط پلیمورفیسم rs855791 TMPRSS6 با آنمی فقر آهن
آناهیتا بابان1، فاطمه کشاورزی2، بهرام نیکخو3
چکیده
سابقه و هدف
بر اساس مطالعههای گذشته، میان پلیمورفیسمهای TMPRSS6 گزارش شده مرتبط با آنمی فقر آهن، rs855791 بیشترین ارتباط را با سطح هموگلوبین و شدت بیماری دارد. هدف از این مطالعه، بررسی ارتباط rs855791 با آنمی فقر آهن در سنندج بود.
مواد و روشها
در این مطالعه مورد - شاهدی مربوط به بهار سال 1394 ، فراوانی پلیمورفیسم rs855791 TMPRSS6 در 40 بیمار مبتلا به کم خونی فقر آهن و80 فرد سالم با انتخاب تصادفی و بدون محدودیت سن و جنس توسط روش PCR-RFLP بررسی شد. سپس ارتباط rs855791و سطح هموگلوبین، فریتین و MCV در افراد بیمار و سالم با نرم افزار آماری 19 SPSS مطالعه گردید.
یافتهها
فراوانی CC ، CT و TT در بین 40 بیمار و 80 فرد سالم به ترتیب 15، 5/37 ، 5/47 و 75/33، 5/42 و 75/23 درصد بود. لذا رابطه معناداری بین ژنوتیپ TT و ابتلا به بیماری وجود داشت(010/0 =p). همچنین بین فراوانی CC و عدم ابتلا به بیماری رابطه معناداری مشاهده شد(035/0 p= ، 34/0 OR=). فراوانی بیشتر CT در گروه کنترل نسبت به بیمار، نشان دهنده احتمال ابتلای کمتر افرادی با ژنوتیپ CT است. نتایج ارتباط معناداری بین پایین بودن Hb ، MCV ، Ferritin و ژنوتیپ را نشان داد، به طوری که افراد دارای ژنوتیپ TT دارای Hb ،MCV وFerritin پایینتر نسبت به افراد دارای ژنوتیپ CC و TC بودند.
نتیجه گیری
پلیمورفیسم rs855791 TMPRSS6 در بیماران مورد بررسی مبتلا به کم خونی فقرآهن در شهر سنندج مؤثر بود.
کلمات کلیدی: آنمی فقر آهن، فریتین، هموگلوبین
تاریخ دریافت: 11/02/1400
تاریخ پذیرش: 19/03/1400
1- کارشناس ارشد زیستشناسی سلولی و مولکولی، گروه زیستشناسی، واحد سنندج، دانشگاه آزاد اسلامی، سنندج، ایران
2- مؤلف مسئول: دکترای ژنتیک مولکولی، دانشیار گروه زیستشناسی، واحد سنندج، دانشگاه آزاد سنندج، سنندج، ایران، کد پستی: 6616935391
3- متخصص آسیب شناسی، دانشیار گروه پاتولوژی، دانشکده پزشکی، دانشگاه علوم پزشکی کردستان، سنندج، ایران
آناهیتا بابان1، فاطمه کشاورزی2، بهرام نیکخو3
چکیده
سابقه و هدف
بر اساس مطالعههای گذشته، میان پلیمورفیسمهای TMPRSS6 گزارش شده مرتبط با آنمی فقر آهن، rs855791 بیشترین ارتباط را با سطح هموگلوبین و شدت بیماری دارد. هدف از این مطالعه، بررسی ارتباط rs855791 با آنمی فقر آهن در سنندج بود.
مواد و روشها
در این مطالعه مورد - شاهدی مربوط به بهار سال 1394 ، فراوانی پلیمورفیسم rs855791 TMPRSS6 در 40 بیمار مبتلا به کم خونی فقر آهن و80 فرد سالم با انتخاب تصادفی و بدون محدودیت سن و جنس توسط روش PCR-RFLP بررسی شد. سپس ارتباط rs855791و سطح هموگلوبین، فریتین و MCV در افراد بیمار و سالم با نرم افزار آماری 19 SPSS مطالعه گردید.
یافتهها
فراوانی CC ، CT و TT در بین 40 بیمار و 80 فرد سالم به ترتیب 15، 5/37 ، 5/47 و 75/33، 5/42 و 75/23 درصد بود. لذا رابطه معناداری بین ژنوتیپ TT و ابتلا به بیماری وجود داشت(010/0 =p). همچنین بین فراوانی CC و عدم ابتلا به بیماری رابطه معناداری مشاهده شد(035/0 p= ، 34/0 OR=). فراوانی بیشتر CT در گروه کنترل نسبت به بیمار، نشان دهنده احتمال ابتلای کمتر افرادی با ژنوتیپ CT است. نتایج ارتباط معناداری بین پایین بودن Hb ، MCV ، Ferritin و ژنوتیپ را نشان داد، به طوری که افراد دارای ژنوتیپ TT دارای Hb ،MCV وFerritin پایینتر نسبت به افراد دارای ژنوتیپ CC و TC بودند.
نتیجه گیری
پلیمورفیسم rs855791 TMPRSS6 در بیماران مورد بررسی مبتلا به کم خونی فقرآهن در شهر سنندج مؤثر بود.
کلمات کلیدی: آنمی فقر آهن، فریتین، هموگلوبین
تاریخ دریافت: 11/02/1400
تاریخ پذیرش: 19/03/1400
1- کارشناس ارشد زیستشناسی سلولی و مولکولی، گروه زیستشناسی، واحد سنندج، دانشگاه آزاد اسلامی، سنندج، ایران
2- مؤلف مسئول: دکترای ژنتیک مولکولی، دانشیار گروه زیستشناسی، واحد سنندج، دانشگاه آزاد سنندج، سنندج، ایران، کد پستی: 6616935391
3- متخصص آسیب شناسی، دانشیار گروه پاتولوژی، دانشکده پزشکی، دانشگاه علوم پزشکی کردستان، سنندج، ایران
مقدمه
از آن جایی که تمام سلولهای بدن انسان برای زنده ماندن به اکسیژن وابستهاند، کمبود آن باعث هیپوکسی شده و گستره وسیعی از مشکلات را به همراه دارد(5-1).
کم خونی میتواند در تمامی مراحل زندگی رخ دهد اما بیشتر در دوران بارداری و سنین پایین و یا افراد مسن خود را نشان میدهد(2). کم خونی انواع گوناگونی دارد که هر یک علت خاص خود را دارند. این بیماری بر اساس گوناگونی ریختشناسی گلبولهای قرمز و مکانیسمهای اتیولوژیک طبقهبندی میشود. سه علت اصلی آن از دست رفتن حجم زیادی از خون(خونریزیهای حاد یا مزمن)، از بین رفتن سلولهای خونی(همولیز) و کمبود تولید سلولهای خونی است. از علل کاهش تولید سلولهای خونی؛ کمبود آهن، کمبود ویتامین B12، تالاسمی و تعدادی نئوپلاسم مغز استخوان میباشد. علل افزایش همولیز شامل تعدادی شرایط ژنتیکی مانند کم خونی داسی شکل، عفونت مانند مالاریا و برخی از بیماریهای خود ایمنی است(3).
عموماً آزمایش شمارش کامل خون را جزو آزمایشهای نخستین برای تشخیص کم خونی، درنظر میگیرند. علاوه بر شمارش گلبول های قرمز و مقدار هموگلوبین، دستگاه خودکار شمارنده، اندازه گلبولهای قرمز را با فلوسیتومتری اندازه میگیرند که یک عامل مهم در افتراق میان علل گوناگون کم خونی میباشد. برای مردان بالغ هموگلوبین کمتر از gr/dL 13، نشانه کم خونی است و برای زنان بالغ این مقدار gr/dL 12 میباشد(5، 4).
علاوه بر عوامل تغذیهای و بیماریهای عفونی که از مهمترین عوامل بیماری کم خونی فقر آهن هستند، جهشهای ژنتیکی نیز در کم خونی فقر آهن مؤثرند. جهش در ژنهای کد کننده زیر واحدهای هموگلوبین که منجر به تالاسمی و جهش در ژن Serine 6 (TMPRSS6) ، Transmembrane protease که باعث کمخونی فقر آهن میشود، از آن جمله است(1). در انسان محصول ژن TMPRSS6 پروتئینی به نام ماتریپتاز 2 است که تنظیم کننده پروتئین دیگری به نام هپسیدین میباشد. هپسیدیـن تنظیمکننــده کلیــدی تعــادل آهــن در بــدن
است(1).
ژن TMPRSS6 از 18 اگزون تشکیل شده است، که این اگزونها کدکننده دومینهای پروتئین ماتریپتاز2 هستند، دومین سرین پروتئازی پروتئین توسط اگزونهای 15 تا 18 کد میشوند(3). ماتریپتاز 2 ، سرین پروتئاز سطح سلولی با ساختار نوسانی است که به عنوان تنظیمکننده منفی بیان هپسیدین میباشد(4). این هورمون به عنوان اصلیترین تنظیمکننده آهن خون در انسان و سایر پستانداران شناخته شده است(6، 1).
فعال شدن هپسیدین باعث کمبود شدید آهن در موش و انسان میگردد در حالی که بیان بالای هپسیدین باعث کم خونی فقر آهن میشود(6). جهشهای ژن TMPRSS6 تا حد زیادی میزان عملکرد ماتریپتاز 2 را کاهش میدهد. کمبود ماتریپتاز 2 سطح بسیار بالایی از هپسیدین را به وجود میآورد که این منجر به مهار جذب آهن در رژیم غذایی و ایجاد فنوتیپ کمخونی فقرآهن شدید میشود. بنابراین ماتریپتاز 2 بهعنوان یک تنظیمکننده منفی بیان ژن هپسیدین مشخص شده است(1).
مطالعههای مرتبط با ژنوم چندین پلیمورفیسم تک نوکلئوتیدی SNP) ، Single Nucleotide polymorphism) را که بر فنوتیپ سلولهای خونی مؤثرند، نشان داده است. همه این پلیمورفیسمهای شناسایی شده مربوط به ژن TMPRSS6 است که در میان آنهـا rs855791 بیشتـرین ارتباط را با سطح هموگلوبین داشته است(7، 6).
در سال 2018 ، باتار و همکاران ، نقش برخی از انواع پلیمورفیسمهای این ژن را در پارامترهای خون مرتبط با آهن در بیماران ترک با کم خونی فقر آهن بررسی کردند و دریافتند کـه تغییرات rs855791 بـا افزایــش RBC و TIBC در این بیماران همراه است(8). در سال 2019، کاکماکلی و همکـاران طیـف جهــشهای ژن TMPRSS6 را در کم خونی فقر آهن با گزارش یک حذف 374 جفت بازی هموزیگوت در اگزون 15 ژن گزارش دادند(9). در آفریقای جنوبی سال 2019 ، نالادو شناسایی و ارتباط بین چند شکلی rs855791 را با افزایش حساسیت به کم خونــی فقـر آهن در بیماران مبتلا بــه نارسایی مزمن کلیه بدون دیالیز انجام داد(10).
پلیمورفیسم تک نوکلئوتیدی rs855791 بر روی کروموزوم 22، اگزون 17 بخش عملکردی ژن TMPRSS6 را به نام V736A شناخته است. در موقعیت 736 این ژن یک تغییرتک نوکلئوتیدی منجر به جایگرینی آمینو اسید آلانین به جای والین شده و لذا توانایی آنزیم برای مهار رونویسی هپسیدین کاهش یافته است(12، 11). یافتهها نشان میدهد که این جایگزینی ممکن است باعث تغییر در ساختار پروتئین شده و باعث کاهش دسترسی به جایگاه فعالسازی پیش آنزیم TMPRSS6 گردد(13).
لذا هدف از این مطالعه بررسی ارتباط پلیمورفیسم rs855791 TMPRSS6 با آنمی فقرآهن در افراد مبتلا در شهر سنندج بود.
مواد و روشها
تحقیق حاضر یک مطالعه شاهد- موردی بود. این بررسی در قالب یک پایاننامه کارشناسی ارشد توسط شورای پژوهشی دانشگاه آزاد اسلامی ـ واحد علوم و تحقیقات کردستان از لحاظ اخلاقی و پژوهشی تایید شد. نمونهگیری به صورت تصادفی بدون محدودیت سن و جنس و فقط بر اساس نتایج آزمایشهای کم خونی در یک فاصله زمانی 3 ماهه در بهار سال 1394 و با همکاری آزمایشگاههای خصوصی در سطح شهر سنندج انجام شد. در مجموع 120 نفر با رضایت شخصی و به صورت تصادفی انتخاب شده و در این مطالعه شرکت کردند. تشخیص کم خونی بر اساس معیارهای سازمان بهداشت جهانی یعنی آزمایشهای CBC ، اندازه گلبولهای قرمز (27< MCH & 80 MCV<)، هماتوکریت، هموگلوبین (برای مردان بالغ کمتر از gr/dL 13 و برای زنان بالغ کمتر gr/dL 12) و آزمایش فریتین(کمتر از 15 نانوگرم بر میلیلیتر با حساسیت 59% و ویژگی 99%) صورت گرفت. از این تعداد با توجه به نتایج آزمایشها و بر اساس تائید پزشک، 40 نفر از افراد با آنمی فقر آهن، و 80 نفر کنترل سالم بودند. 5 میلیلیتر نمونه خون از همه شرکتکنندگان در لولههای CBC حاوی ماده ضد انعقاد جمعآوری شـد و بعـد از چنـد بار اینورت کردن در فریزر 20- درجه سانتیگراد تا زمان انجام آزمایش قرار گرفت.
استخراج DNA :
استخراج DNA از خون با کیت استخراج High Yirld DNA Purification Kit محصول شرکت سیناژن (سیناژن: تهران، ایران) و بر اساس دستورالعمل کیت انجام شد. در ادامه با استفاده از جذب نوری در اسپکتروفتومتر و الکتروفورز بر روی ژل آگارز 1% ، تعیین کمیت و کیفیت DNA های استخراج شده، صورت گرفت. DNA جداسازی شده در میکروتیوبهای جداگانه در دمای 20- درجه سانتیگراد تا زمان انجام PCR نگهداری شد.
تعیین ژنوتیپها:
توالی آغازگرها از مطالعههای پیشین، بعد از انجام بلاست تایید و به شرکت سیناژن سفارش داده شد(1) (جدول 1). فرآیند PCR در حجم نهایی µL 20 با استفاده از کیت PCR شرکت سیناژن و توسط دستگاه سیکلوترون Rotor-Gene Q(Corbett Life Science) انجام شد(جدول 2). برای اطمینان از تکثیر درست قطعه مورد نظر، محصول PCR بر روی ژل آگارز 8/1 درصد بارگذاری و تعیین کیفیت گردید(شکل 1).
جهت مشاهده پلیمورفیسم طبق دستورالعمل، 1 میکرولیتر از آنزیم محدود کننده Stu l به 10 میکرولیتر محصول PCR اضافه شد و سپس به آن 2 میکرولیتر بافر اضافه گردید. سپس حجم نهایی توسط 27 میکرولیتر آب مقطر دوبار تقطیر به 40 میکرولیتر رسید و به مدت 10 تا 20 دقیقه در دمای 37 درجه سانتیگراد دستگاه بن ماری انکوبه شد. پس از انکوبه کردن، محصول حاصله دوباره الکتروفورز گردید(شکل 2).
برای برش ناحیه مورد نظر، آنزیم Stu l جایگاه تشخیص آن در rs855791 به صورت توالی پالیندرومیک AGGCCT میباشد و در نتیجه در صورت وجود آلل C در جایگاه پلیمورف آنزیم قطعه را برش میدهد و در صورت وجود آلل T قطعه برش نمی خورد. با توجه به این که اگر فرد سالم باشد آنزیم Stu l آلل وحشی را که C میباشد برش میدهد، لذا 2 باند در 123 و 126 داریم و با توجه به این که این طول قطعهها به هم نزدیک هستند، هنگـام الکتروفـورز محصـول روی ژل فقـط یـک باند در



نزدیک ناحیه 125 میبینیم، یعنی هر دو آلل آن فرد سالم بوده (هموزیگوت) و به صورت CC میباشد. مشاهده یک باند 249 جفت بازی بر روی ژل نشاندهنده پلیمورفیسم میباشد با توجه به این که آنزیم آلل C را برش میدهد، در این حالت جایگاه برش آنزیم Stu l نمیباشد و در حین run کردن بر روی ژل در ناحیه 249 تک باند داریم که به صورت TT است. در صورتی که سه باند در الکتروفورز مشاهده گردد، ژنوتیپ به صورت TC قابل مشاهده میباشد. یک باند در ناحیه 249 و دو باند در ناحیه 123 و 126 باید داشته باشیم که به علت نزدیک بودن، باند را در ناحیه نزدیک 125 میبینیم.
تحلیل آماری:
آنالیز آماری دادهها با استفاده از نرمافزار 32/1 popgene و 19 SPSS و در سطح معنادار(05/0 p<) انجام شد.
یافتهها
نتایج تجزیه و تحلیل آماری توزیع ژنوتیپ rs855791 در جدول آمده است(جدول 3). همان طور که مشاهده میشود فراوانی ژنوتیپهای CC، CT و TT در بین 40 بیمار و 80 نفر کنترل سالم به ترتیب 15، 5/37 ، 5/47 و 75/33، 5/42 و 75/23 درصد بوده است(نمودار 1). فراوانی TT در افراد بیمار بالا (5/47%) و فراوانی آن در افراد سالم تا حدودی بالا(75/23%) بود. با توجه به نتایج به دست آمده ارتباط معناداری وجود دارد(01/0 p=). با توجه به جدول 3 ، تجزیه و تحلیل دادههای ژنوتیپ CC نشان میدهد که چون 035/0 p= و 346/0 OR= است و همچنین فراوانی ژنوتیپ CC در افراد سالم از بیمار بیشتر است که این نشان دهنده غالب بودن ژنوتیپ CC در افراد سالم نسبت به افراد بیمار میباشد، در نتیجه احتمال بروز ایجاد کم خونی فقرآهن در افراد سالم که دارای ژنوتیپ CC میباشند کم است.
همچنبن در ارتباط با ژنوتیپ CT، مشاهده می شود که p معنادار نمیباشد و هم چنین فراوانی بیشتر CT در گروه کنترل نسبت به گروه بیمار، نشان میدهد که احتمال ابتلا به کم خونی فقر آهن در افرادی با ژنوتیپ CT کمتر است. طبق نتایج به دست آمده 010/0 p= و 905/2 OR= ، رابطه معناداری بین ژنوتیپ TT و ابتلا به بیماری کم خونی فقرآهن در افراد بیمار نسبت به افراد سالم وجود دارد که نشاندهنده غالب بودن ژنوتیپ TT در بین افراد بیمار میباشد و هم چنین با توجه به 905/2 OR= به دست آمده میتوان نتیجه گرفت در افراد سالمی که دارای ژنوتیپ TT میباشند، احتمـال ابتـلا بـه کـم خونـی فقر آهن بالا است.

همچنین نمودارهای 1 تا 3 ارتباط بین پلیمورفیسمهای rs855791 و سطح فاکتورهای خونی هموگلوبین، حجم متوسط گلبول قرمز خون و میزان فریتین بیماران و افراد کنترل را با توجه به بررسی پرونده بیماران و پرسشنامههای پر شده نشان میدهد. نتایج ارتباط معناداری بین پایین بودن Hb ،MCV و Ferritin و ژنوتیپ را نشان میدهد، به طوری که افراد دارای ژنوتیپ TT دارای Hb ،MCV وFerritin پایینتر نسبت به افراد دارای ژنوتیپ CC و TC میباشند.


بحث
در تحقیق حاضر ارتباط بین پلیمورفیسم T/C rs855791 و آنمی فقر آهن در 40 فرد مبتلا به آنمی فقر آهن و 80 فرد سالم در سنندج بررسی شده است. فراوانی ژنوتیپهای CC ، CT و TT در بین 40 بیمار و 80 نفر کنترل سالم به ترتیب 15، 5/37 ، 5/47 و 75/33، 5/42 و 75/23 درصد بود. با توجه به نتایج آماری، رابطه معناداری بین ژنوتیپ TT و ابتلا به بیماری وجود داشت(010/0 p= و 905/2 OR=). همچنین بین فراوانی ژنوتیپ CC و عدم ابتلا به کم خونی فقر آهن رابطه معناداری مشاهده شد(035/0 p=و 346/0 OR=). فراوانی بیشتر CT در گروه کنترل نسبت به گروه بیمار، نشان داد که احتمال ابتلا به کم خونی فقر آهن در افرادی با ژنوتیپ CT کمتر است. هم چنین در بررسیهای صورت گرفته بر روی ارتباط پلیمورفیسم تک نوکلئوتیدی rs855791 با سطح فاکتورهای Hb ، MCV و فریتین، نتایج نشان داد که این پلیمورفیسم احتمال خطر ابتلا به کم خونی فقرآهن را در بین افـرادی بـا ژنوتیـپ TT بـالا برده و فاکتورهای کمبود
هموگلوبین، فریتین و MCV این خطر را تا حدود زیادی بالا میبرد.
بنیامین و همکاران در سال 2009 بر روی 2516 نوجوان استرالیایی، ارتباط میان سطح فاکتورهای خونی MCV و هموگلوبین با پلیمورفیسم rs855791 را مورد مطالعه قرار دادند. نتایج نشان داد که پایین بودن سطح هموگلوبین رابطه معناداری با پیش آگهی و افزایش خطر ابتلا به همراه دارد(6)(008/0 p=).
در مطالعهای که جان چمبرز و همکارانش در سال 2009 بر روی 5187 نفر اروپایی و 6721 نفر آسیایی (هندی) انجام دادند، مشخص شد که ارتباط معناداری بین تغییر نوکلئوتیدی والین به آلانین در ناحیه 736 پلیمورفیسم تک نوکلئوتیدی rs855791 با سطح هموگلوبین و شدت بیماری وجود دارد(001/0 p=). همچنین مطالعه نشان داد، در مناطقی با فقر تغذیهای، کم خونی فقر آهن به صورت چشمگیری افزایش یافته و سطح هموگلوبین و آهن ذخیرهای بدن کاهش مییابد(7).
در مطالعهای که پائلو دلبینی و همکـاران در سال 2010
در میلان ایتالیا بر روی 16 فرد بیمار انجام دادند، اثر پلیمورفیسمهای rs855791 بر مسیر سیگنالینگ پروتئین ماتریپتاز 2 و اختلال در تولید هپسیدین بررسی شد. نتایج نشان داد در افراد بیماری با ژنوتیپ TT ، سطح هموگلوبین به طور چشمگیری پایین بوده و بین این پلیمورفیسم و سطح هموگلوبین رابطه معناداری وجود دارد(001/0 p= ، 18/5 OR=). همچنین این مطالعه نشان داد که پلیمورفیسمهای تک نوکلئوتیدی بد معنی(rs855791) باعث ایجاد تغییر در ناحیه دومین سرین پروتئازی پروتئین ماتریپتاز 2 شده، در نتیجه عملکرد کاتالیتیکی این پروتئین دچار اختلال میشود(14).
گان و همکاران در سال 2012 با بررسی 1574 فرد چینی، ارتباط پلیمورفیسمهای ژن TMPRSS6 با فریتین، هموگلوبین و خطر ابتلا به دیابت نوع دوم را مطالعه کردند. نتایج آنها نشان داد که پلیمورفیسم rs855791 با کاهش هموگلوبین و هم چنین فریتین پلاسما خطر افزایش بار آهن را در بدن بالا برده و احتمال خطر ابتلا به دیابت نوع 2 را نیز بالا خواهد برد(031/0 p=)(15).
سال 2014 پی و همکاران ارتباط پلیمورفیسم rs855791 با کم خونی فقر آهن را بر روی 67 مبتلا و 107 نفر داوطلب سالم به روش PCR-RFLP بررسی نمودند. نتایج نشان داد همه شاخصهای گلبول قرمز، پلاکت، هموگلوبین، فریتین و حجم متوسط گلبولهای قرمز به طور قابل توجهی بین دو گروه متفاوت است(03/0 p=)، که با نتایج این مطالعه همخوانی دارد(16).
در مطالعه شینتا و همکاران سال 2019 در لومبوک شرقی و اندونزی بر روی کودکان 6 تا 17 ماهه هیچ ارتباطی بین پلیمورفیسم rs855791 با گیرنده ترانسفرین محلول (sTfR)و غلظت هموگلوبین سرم به دست نیامد(17).
در مطالعهای در سال 2020 توسط آلامر روی 108 دانشجوی دختر 18 تا 25 سال در پادشاهی عربستان سعودی، پلیمورفیسمrs855791 با وضعیت آهن دارای ارتباط معناداری بود(11).
کم خونی همچنان به عنوان یک مشکل بهداشت جهانی گسترده و قابل توجه باقی مانده است که باید به طور کافی مورد بررسی قرار گیرد. اگر چه آنمی فقر آهن در اکثر مناطق دلیل اصلی کم خونی است، اما تحقیقهای اخیر نشان میدهد که علت کم خونی پیچیده و مختص به هر منطقهای است. برای درک بیشتر چگونگی کمک به دلایل اصلی کم خونی، از جمله آنمی فقر آهن و سایر کمبودهای تغذیهای، بیماریها و اختلالات Hb ، در کم خونی لازم است تلاش شود تا مداخلات مناسب در شرایط خاص قابل اجرا باشد. همچنین مطالعههای بیشتر در مقیاس بیماران بیشتر برای شناسایی هاپلوتیپهای بالقوه و چند شکلیهای مسئول پاسخ کم به درمان خوراکی آهن ضروری است و ممکن است برای برنامهریزی یک مکمل صحیح آهن مفید باشد. سؤال دیگری که در این بررسیها باید به آن پاسخ داد این است که آیا تجویز مکمل غذایی آهن به کودکان، باید بر اساس مشخصات ژنتیکی باشد، به ویژه برای کودکانی که در TMPRSS6 جهش دارند؟
نتیجهگیری
بالا بودن فراوانی ژنوتیپ TT در بین افراد مبتلا به کم خونی فقرآهن(5/47%)، در جمعیت مورد بررسی نشان میدهد خطر ابتلا به بیماری با ژنوتیپ TT رابطه معناداری دارد(010/0 p= و 905/2 OR=). هم چنین رابطه معناداری بین ژنوتیپ TT و سطح پایین فاکتورهای خونی هموگلوبین، فریتین و حجم متوسط گلبولهای قرمز وجود داشت.
تشکر و قدردانی
بدینوسیله نویسندگان مقاله از همکاری پرسنل زحمتکش آزمایشگاه پاتولوژی نور، تشکر و قدردانی مینمایند.
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |






