جلد 18، شماره 3 - ( پاییز 1400 )
جلد 18 شماره 3 صفحات 186-180 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Amiri Hezave Y, Sharifi Z, Ranjbar kermani F, Shahabi M, Kheirandish M. Lack of the association between single nucleotide polymorphism in programmed cell death 1 gene) PD-1(and susceptibility to human lymphotropic virus infection type 1(HTLV-1) in the Iranian population. bloodj 2021; 18 (3) :180-186
URL: http://bloodjournal.ir/article-1-1381-fa.html
URL: http://bloodjournal.ir/article-1-1381-fa.html
امیری هزاوه یلدا، شریفی زهره، رنجبر کرمانی فهیمه، شهابی مجید، خیراندیش مریم. فقدان ارتباط بین پلیمورفیسم تک نوکلئوتیدی ژن مرگ برنامهریزی شده 1 سلولی و استعداد آلودگی به ویروس لنفوتروپیک تیپ یک انسانی در جمعیت ایرانی. فصلنامه پژوهشی خون. 1400; 18 (3) :180-186
استاد مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون
متن کامل [PDF 558 kb]
(996 دریافت)
| چکیده (HTML) (2500 مشاهده)
مقدمه
10-5 میلیون نفر از مردم جهان به ویروس لنفوتروپیک سلول T انسانی نوع یک(HTLV-1) آلوده هستند. این ویروس در برخی مناطق جهان از جمله ژاپن، تایوان، جنوب و مرکز آفریقا و شمال شرقی ایران آندمیک است به طوری که میزان آلودگی با ویروس HTLV-1 در اهداکنندگان خون در مشهد ۲۸/۰% است(1). HTLV-1 توسط تغذیه با شیر مادر، ارتباط جنسی، تزریق فرآوردههای خونی آلوده و استفاده از سوزن آلوده منتقل میشود(2). تعداد کپی بالای ویروس، یک عامل مؤثر در انتقال ویروس توسط تغذیه با شیر مادر است(3). در انتقال ویروس HTLV-1 به دنبال تزریق فرآوردههای خونی، کاهش لکوسیت سبب کاهش خطر انتقال HTLV-1 میشود که طبق استاندارد، لکوسیت کمتر از 106×5 در هر واحد RBC یا پلاکت، فرآورده خونی کم لکوسیت است که میتواند ایمن باشد اما اگر اهداکنندهای باشد که تعداد کپی بالایی از ویروس را داشته باشد، با وجود کاهش لکوسیت هنوز امکان انتقال وجود دارد(4). 5% از افراد آلوده به ویروس HTLV-1 به سمت بیماری لوسمی سلول T بالغین(ATL : Acute T Cell Leukemia) و 4% از افراد آلوده به سمت بیماری فلج سفت گرمسیری ( HAM/TSP)پیشرفت میکنند(5). فاکتورهای ژنتیک میزبان، تعداد کپی ویروس و پاسخ سیستم ایمنی میزبان میتوانند در پیشرفت افراد آلوده به سمت بیماریهای ATL و(HAM/TSP : HTLV-1 Associatedc Myelopathy/Tropical Spastic Paraparesis) کمککننده باشند(6). همچنین مطالعهها نشان دادند که در گسترده شدن عفونت مزمن، مکانیسمهای مختلف ایمنی مثل تولید سیتوکاینهای ضد التهابی، القای سلولهای T تنظیمکننده(Treg) و بیان مولکولهای Immune checkpoint درگیر هستند(7). در عفونتهای مزمن مانند HIV ، هپاتیت B ، هپاتیت CوHTLV-1 ، بیان پروتئین مرگ برنامهریزی شده یک (PD-1) که یک مولکول Immune checkpointاست، افزایش مییابد و به دنبال آن تکثیر سلولهای T CD8+ و تولید سایتوکاین آنها مختل میشود و حالت خستگی برای سلولهای Tایجاد میشود که عفونت پایدار میگردد(9، 8). ژن PD-1 بر روی کروموزوم 2 در موقعیت q37.3 با KDal55 و 228 اسید آمینه است(10). PD-1 (که CD279نیز نامیده میشود) یک پروتئین تراغشایی از خانواده B7/CD28 و سوپرخانواده ایمنوگلوبولین است که بر روی سلولهای T (CD4+ ، CD8+)، سلولهای NK1 ، لنفوسیتهای B و مونوسیتهای فعال شده بیان میشود(11).
در عفونت HTLV-1 ، با افزایش بیان PD-1 ، تعداد کپی ویروس افزایش و عملکرد لنفوسیتهای سیتوتوکسیک کاهش مییابد(12). پلیمورفیسمrs36084323 در جایگاه 606 در ناحیه پروموتور ژن PD-1 قرار دارد که میتواند در فعالیت پروموتور اثرگذار باشد(13). با توجه به نقش PD-1 در عفونت HTLV-1 و تاثیر آن در عملکرد سلولهای T ، این مطالعه به منظور بررسی ارتباط بین پلیمورفیسم rs36084323دراهداکنندگان خون آلوده به ویروس HTLV-1 بدون علامت در مقایسه با افراد سالم انجام شد، که میتواند اطلاعات مفیدی را در مورد تاثیر پلیمورفیسمrs36084323 در پایداری عفونت ویروسی و انتقال ویروس HTLV-1 به افراد سالم فراهم آورد.
مواد و روشها
این مطالعه از نوع مورد- شاهدی بود که بر روی نمونه خون 81 اهداکننده خون آلوده به ویروس HTLV-1 که علامتی از بیماری را نداشتند(65 مرد و16 زن با میانگین و انحراف معیار سنی 55/10 ± 36/40 سال) و 162 اهدا کننده خون سالم(154 مرد و 8 زن با میانگین و انحراف معیار سنی 009/0 ± 37/61 سال) انجام شد. نمونههای استفاده شده در این مطالعه از اهداکنندگان خون استان خراسان رضوی بود که پس از دریافت رضایتنامه آگاهانه جمعآوری گردید. افراد آلوده به ویروس HTLV-1 توسط آزمایش الایزا و کیت(سنگاپور، HTLV-I/II ELISA 4.0) تشخیص داده شده بودند و آزمایش وسترنبلات با کیت (سنگاپور، HTLV Blot 2.4) به منظور تایید آلودگی انجام شده بود .به علاوه تمامی نمونهها از نظر آلودگیهای ویروسی HIV ، HBV و HCV منفی بودند. نمونه خون افراد به منظور جداسازی بافیکوت و پلاسما سانتریفیوژ گردید و از نمونههای بافیکوت، DNA ژنومی با استفاده از کیت یکتا تجهیز استخراج گردید و برای انجام مراحل بعد در فریزر 70- درجه سانتیگراد نگهداری شد. پلیمورفیسم rs36084323 با استفاده از روشPCR- RFLP تعیین ژنوتیپ گردید. آغازگرهای به کار رفته در واکنش زنجیرهای پلیمراز (PCR) عبارت بودند از: آغازگر مستقیم (AAGAAGGTCAAGGCTGGAAGGGG3′′5)، آغازگر معکوس3′) ATTCTGTCGGAGCCTCTGGGAG′5) (جدول 1).

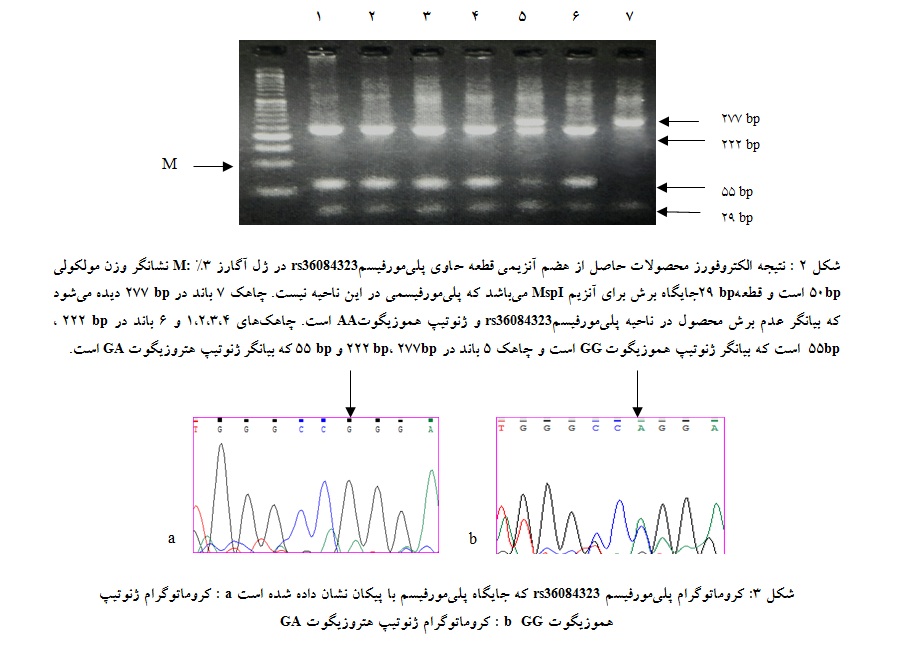
محصول حاصل از PCR که قطعه ۳۰۶ جفت باز بود، بر روی ژل آگارز ۲ درصد الکتروفورز و توسط رنگآمیزی با رنگ Green viewer درمقابل نور فرابنفش آشکارسازی شد. پس از آن ۱۰میکرولیتر از محصول PCR جهت هضم آنزیمی توسط U/µL ۵ آنزیم محدودالاثر MspI و۲ میکرولیتر بافر آنزیم ده برابر غلظت به مدت ۱۶-۱۲ ساعت(overnight) در دمای ۳۷ درجه سانتیگراد انکوبه گردید .محصول هضم آنزیمی با الکتروفورز بر روی ژل آگارز 3% به همراه نشانگر وزن مولکولی ۵۰ جفت بازی آشکار شد. قطعه تکثیر شده دارای دو جایگاه برش آنزیم MspIاست که یک جایگاه سبب برش قطعه ۲۹ جفت بازی میشود که در زیر نشانگر وزن ملکولی ۵۰ جفت باز قرار میگیرد. اگر در جایگاه
برش آنزیم MspIپلیمورفیسم، آلل G باشد، به دنبال برش قطعه bp ۲۷۷ و اگر آلل A باشد، قطعات ۲۲۲و ۵۵ جفت بازی به دست میآید. جهت تایید نتایج ژنوتایپینگ، ۱۰% از محصولات PCR به روش سنگر یا خاتمه زنجیره جهت توالییابی به شرکت پیشگام ارسال شد.
تحلیل آماری نتایج با استفاده از نرمافزای آماری SPSS نسخه ۲۲ انجام شد و دادههای ژنوتیپی براساس آزمون مربع کای مورد مقایسه قرار گرفت. مقدار p-value کمتر از ۰۵/۰ معنادار در نظر گرفته شد.
یافتهها
با انجام PCR و الکتروفورز محصولی با طول ۳۰۶ جفت باز مشاهده شد(شکل ۱). پس از هضم آنزیمی محصول PCR درافراد هموزیگوت GG ، سه قطعه ۲۹، ۵۵، ۲۲۲ جفت بازی در افراد هموزیگوت AA ، دو قطعه۲۹، ۲۷۷ جفت بازی و در افراد هتروزیگوت GA ، چهار قطعه ۲۹ ، ۵۵ ، ۲۲۲ و ۲۷۷ جفت باز مشاهده گردید(شکل ۲).
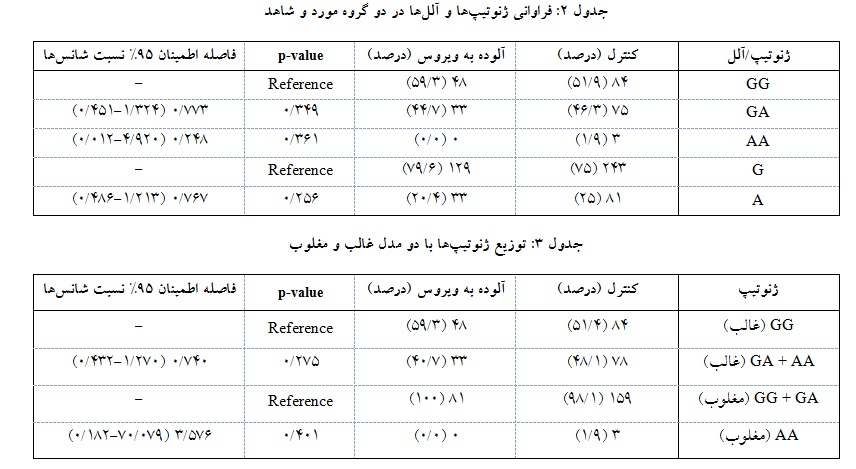
نتایج حاصل از تعیین توالی، تاییدکننده نتایج PCR-RFLP بود(شکل ۳) . در کلیه محاسبات آماری انجام شده فاصله اطمینان 95% بود. در دو گروه مورد مطالعه فراوانی ژنوتیپها به شرح: GG (۹/۵۱%) ، GA (۳/۴۶%) و AA (۹/۱%) برای گروه شاهد و GG (۳/۵۹%) ، GA (۷/۴۴%) و AA (00/0%) برای گروه مورد بود. محاسبات آماری نشان داد که با مرجع در نظر گرفتن ژنوتیپ GG ، میزان p-value برای ژنوتیپها GA و AA به ترتیب ۳۴۹/۰ و ۳۶۱/۰ بود . با مرجع در نظرگرفتن آلل رفرنس G میزان p-value برای آلل A برابر۲۵۶/۰ بود(جدول 2). نتایج تعیین ژنوتیپ براساس دو مدل غالب و مغلوب با استفاده از آزمون آماری مربعکای نشان میدهد در مدل غالب، p معنادار نبود (جدول 3).

بحث
در این مطالعه ارتباط بین پلیمورفیسم rs36084323با استعداد آلودگی به ویروس HTLV-1 در اهداکنندگان خون استان خراسان رضوی بررسی شد. مقایسه فراوانی آللها و ژنوتیپها بر اساس نتایج آماری حاصله در دو گروه مورد و شاهد نشان داد که اختلاف معناداری بین این دو گروه وجود ندارد که بیانگر عدم هم بستگی این پلیمورفیسم با شانس آلودگی ویروس HTLV-1 در جمعیت مورد مطالعه است . مطالعه حاضر نشان داد که فراوانی ژنوتیپ AA پلیمورفیسمrs36084323 درجمعیت ایرانی کم است. مطالعه دیگری که درجمعیت ایرانی بر روی پلیمورفیسم rs36084323 انجام شده بود، با نتایج ما همسو است و نشان داد که آلل G پلیمورفیسم rs36084323 ، آلل شایع در جمعیت ایرانی است که از لحاظ فراوانی تقریباً مشابه جمعیت اروپایی و آفریقایی میباشد. این درحالی است که در جمعیت چینی، مکزیکی و هندی آلل A این پلیمورفیسم غالب است(14). تفاوت در شیوع آللهای پلیمورفیسم rs36084323 در جمعیتهای مختلف میتواند درآندمیک بودن بیماریها در برخی جمعیتها اثرگذار باشد. با اتصال گیرنده PD-1 به لیگاندهایش، تولید سیتوکاین و فعال شدن سلول T سرکوب میشود که منجر به سرکوب تکثیر و القای آپوپتوزسلول های T و تمایز آنها به سلولهای T تنظیمی میشود. مطالعهها نشان داده که بیان PD-1 در عفونتهای مزمن افزایش مییابد و درپاسخهای ضد ویروسی اختلال ایجاد میکند(15). پلیمورفیسم rs36084323 که در ناحیه پروموتور این ژن است، میتواند در اتصال فاکتور رونویسی و ایجاد موتیف خاص اثرگذار باشد و سبب اختلال در فعال شدن ژن و شروع رونویسی از ژنPD-1 شود. جالب است که فراوانی آلل A در پلیمورفیسم rs36084323 در مواردی که جهش در P53 وجود دارد، بالاتر است. پیشنهاد شده که در سرطانها جهش P53 که به عنوان مارکری برای پیشرفت بیماری است، سبب پیش آگهی ضعیف و عدم پاسخ به درمان میشود(16). ویروس HTLV-1 از جمله ویروسهایی است که در گسترش سرطان در جهان دارای نقش میباشد(17). از طرف دیگر تنها 5% از افراد آلوده به ویروس به سمت بیماری ATL پیشرفت میکنند(5). همچنین درمان ایمونوتراپی در بیماران ATL تنها در تعدادی از بیماران موفقیتآمیز بوده است بنابراین منطقی است که تجویز ایمونوتراپی بدون دانستن زمینه ژنتیکی بیماران مورد تجدید نظر قرار گیرد و لازم است تاثیر آلل A پلیمورفیسم rs36084323 در پیشرفت افراد آلوده به ویروس HTLV-1 به سمت بیماری و پاسخ به درمانهای ایمونوتراپی در بیماران ATL مورد بررسی بیشتر قرار گیرد(18).
بنابراین با توجه به نقش PD-1 ، پلیمورفیسمهای این ژن میتوانند با تغییر در میزان بیان PD-1 در فرار ویروس از پاسخهای ایمنی و افزایش تعداد سلول آلوده اثرگذار باشند و با افزایش تعداد سلول آلوده، احتمال انتقال این ویروس به دنبال تزریق فرآوردههای خونی و تغذیه با شیر مادر افزایش مییابد. مطالعهای بر روی بیماران روماتوئید آرتریت نشان داد که آلل G و ژنوتیپ GG پلیمورفیسم rs36084323 ، با افزایش میزان بیان mRNA PD-1 همراه است و ژنوتیپ AA این پلیمورفیسم یک فاکتور محافظتکننده در برابر روماتوئید آرتریت است. در مطالعهای دیگر بر روی بیماران روماتوئید آرتریت نشان داده شد که آلل A پلیمورفیسم rs36084323 ، دارای فراوانی بیشتری در بیماران روماتوئید آرتریت درجمعیت ایرانی است(14).
به علاوه مطالعهها بر روی سرطان پستان نشان داده شده است که ژنوتیپ GG این پلیمورفیسم، یک فاکتور محافظتکننده در برابر سرطان پستان است(19). مطالعه بر روی بیماران مبتلا به هپاتیت B نشان داد که ترکیب ژنوتیپ GA یا GG پلیمورفیسم rs10204525به همراه ژنوتیپ GG پلیمورفیسم rs36084323در بیماران مبتلا به هپاتیت B فراوانی کمی دارد(20). نتایج مطالعه حاضر نشان میدهد که فراوانی ژنوتیپ GG در گروه سالم (۹/۵۱%) و در گروه مورد(۳/۵۹%) بالا است و با توجه به این که گروه مورد در این مطالعه افراد آلوده به ویروس HTLV-1 هست که علامتی از بیماری را نداشتهاند، بنابراین مطالعه حاضر میتواند با نتایج مطالعه قبل همسو باشد و ژنوتیپ GG این پلیمورفیسم میتواند نقش محافظتکننده
در افراد آلوده به ویروس در پیشرفت بـه سمـت بیمـاری
داشته باشد.
نتیجهگیری
نتایج این مطالعه نشان داد ارتباطی بین پلیمورفیسم تک نوکلئوتیدیrs36084323 با استعداد آلودگی به ویروس HTLV-1 در جمعیت ایرانی وجود ندارد و ژنوتیپ GG این پلیمورفیسم میتواند نقش محافظتکننده علیه ویروس HTLV-1 داشته باشد. از آن جا که شیوع پلیمورفیسم rs36084323 درجوامع مختلف متفاوت است، این موضوع میتواند دلیلی برای آندمیک بودن برخی بیماریها در
جمعیتها و نژادهای مختلف باشد، لازم است این پلیمورفیسم در کنار سایر عوامل اثرگذار بر روی تعداد بیشتری افراد آلوده به ویروس، بیماران HAM/TSP و بیماران ATL و پاسخ آنها به درمان ایمونوتراپی مورد بررسی قرار گیرد.
تشکر و قدردانی
این تحقیق موضو ع کارشناسی ارشد رشته بیوتکنولوژی پزشکی با کد اخلاقIR.TIM.REC.1398.025 است که هزینه آن توسط مؤسسه عالی آموزشی و پژوهشی طب انتقال خون تامین شده است.
متن کامل: (1483 مشاهده)
فقدان ارتباط بین پلیمورفیسم تک نوکلئوتیدی ژن مرگ برنامهریزی شده 1 سلولی
و استعداد آلودگی به ویروس لنفوتروپیک تیپ یک انسانی در جمعیت ایرانی
یلدا امیری هزاوه1، زهره شریفی2، فهیمه رنجبر کرمانی3، مجید شهابی4، مریم خیراندیش5
چکیده
سابقه و هدف
ویروس لنفوتروپیک سلول T انسانی نوع یک(HTLV-1) به ارتباط سلول به سلول برای ایجاد آلودگی نیازمند است و افزایش تعداد سلول آلوده به ویروس، احتمال انتقال ویروس و پیشرفت به سمت بیماری را افزایش میدهد. پاسخهای سیستم ایمنی و ژنتیک میزبان میتواند در استعداد آلودگی افراد به ویروس اثرگذار باشد، لذا در این مطالعه برای نخستین بار پلیمورفیسم ناحیه پروموتور ژن PD-1 که در تنظیم منفی پاسخهای ایمنی مؤثراست، در افراد آلوده به ویروس HTLV-1 فاقد علائم و افراد سالم درسال 1399 در جمعیت ایرانی بررسی گردید.
مواد و روشها
در این مطالعه که به صورت مورد ـ شاهدی انجام شد، DNA ژنومی 81 اهداکننده خون آلوده به ویروس HTLV-1 فاقد علائم و162 اهداکننده خون سالم در استان خراسان رضوی استخراج و ژنوتیپ پلیمورفیسم تک نوکلئوتیدی rs36084323 با روشRFLP-PCR تعیین گردید. جهت تایید نتایج تعیین ژنوتیپ، محصولات PCR توالییابی شدند. نتایج با استفاده از نرمافزار آماری 22 SPSS و براساس آزمون مربع کای تجزیه و تحلیل گردید.
یافتهها
فراوانی آللهای G وA پلیمورفیسم rs36084323 به ترتیب 75% و25% در گروه شاهد و 6/79% و 4/20% در گروه مورد بود و هیچگونه اختلاف معناداری بین گروه مورد و شاهد با مرجع در نظر گرفتن آلل وحشی G مشاهده نشد.
نتیجه گیری
نتایج این مطالعه نشان داد که ارتباطی بین پلیمورفیسم تک نوکلئوتیدی rs36084323 G/A با استعداد آلودگی به ویروس HTLV-1 در جمعیت ایرانی وجود ندارد.
کلمات کلیدی: HTLV-1 ، چند شکلی ژنی، PCR
تاریخ دریافت: 21/08/1399
تاریخ پذیرش: 09/12/1399
1- دانشجوی کارشناسی ارشد بیوتکنولوژی پزشکی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- مؤلف مسئول: PhD ویروسشناسی ـ استاد مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران ـ صندوق پستی: 1157-14665
3- PhD خونشناسی آزمایشگاهی و علوم انتقال خون ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
4- PhD بیوتکنولوژی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
5- PhD ایمونولوژی ـ دانشیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
و استعداد آلودگی به ویروس لنفوتروپیک تیپ یک انسانی در جمعیت ایرانی
یلدا امیری هزاوه1، زهره شریفی2، فهیمه رنجبر کرمانی3، مجید شهابی4، مریم خیراندیش5
چکیده
سابقه و هدف
ویروس لنفوتروپیک سلول T انسانی نوع یک(HTLV-1) به ارتباط سلول به سلول برای ایجاد آلودگی نیازمند است و افزایش تعداد سلول آلوده به ویروس، احتمال انتقال ویروس و پیشرفت به سمت بیماری را افزایش میدهد. پاسخهای سیستم ایمنی و ژنتیک میزبان میتواند در استعداد آلودگی افراد به ویروس اثرگذار باشد، لذا در این مطالعه برای نخستین بار پلیمورفیسم ناحیه پروموتور ژن PD-1 که در تنظیم منفی پاسخهای ایمنی مؤثراست، در افراد آلوده به ویروس HTLV-1 فاقد علائم و افراد سالم درسال 1399 در جمعیت ایرانی بررسی گردید.
مواد و روشها
در این مطالعه که به صورت مورد ـ شاهدی انجام شد، DNA ژنومی 81 اهداکننده خون آلوده به ویروس HTLV-1 فاقد علائم و162 اهداکننده خون سالم در استان خراسان رضوی استخراج و ژنوتیپ پلیمورفیسم تک نوکلئوتیدی rs36084323 با روشRFLP-PCR تعیین گردید. جهت تایید نتایج تعیین ژنوتیپ، محصولات PCR توالییابی شدند. نتایج با استفاده از نرمافزار آماری 22 SPSS و براساس آزمون مربع کای تجزیه و تحلیل گردید.
یافتهها
فراوانی آللهای G وA پلیمورفیسم rs36084323 به ترتیب 75% و25% در گروه شاهد و 6/79% و 4/20% در گروه مورد بود و هیچگونه اختلاف معناداری بین گروه مورد و شاهد با مرجع در نظر گرفتن آلل وحشی G مشاهده نشد.
نتیجه گیری
نتایج این مطالعه نشان داد که ارتباطی بین پلیمورفیسم تک نوکلئوتیدی rs36084323 G/A با استعداد آلودگی به ویروس HTLV-1 در جمعیت ایرانی وجود ندارد.
کلمات کلیدی: HTLV-1 ، چند شکلی ژنی، PCR
تاریخ دریافت: 21/08/1399
تاریخ پذیرش: 09/12/1399
1- دانشجوی کارشناسی ارشد بیوتکنولوژی پزشکی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- مؤلف مسئول: PhD ویروسشناسی ـ استاد مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران ـ صندوق پستی: 1157-14665
3- PhD خونشناسی آزمایشگاهی و علوم انتقال خون ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
4- PhD بیوتکنولوژی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
5- PhD ایمونولوژی ـ دانشیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
مقدمه
10-5 میلیون نفر از مردم جهان به ویروس لنفوتروپیک سلول T انسانی نوع یک(HTLV-1) آلوده هستند. این ویروس در برخی مناطق جهان از جمله ژاپن، تایوان، جنوب و مرکز آفریقا و شمال شرقی ایران آندمیک است به طوری که میزان آلودگی با ویروس HTLV-1 در اهداکنندگان خون در مشهد ۲۸/۰% است(1). HTLV-1 توسط تغذیه با شیر مادر، ارتباط جنسی، تزریق فرآوردههای خونی آلوده و استفاده از سوزن آلوده منتقل میشود(2). تعداد کپی بالای ویروس، یک عامل مؤثر در انتقال ویروس توسط تغذیه با شیر مادر است(3). در انتقال ویروس HTLV-1 به دنبال تزریق فرآوردههای خونی، کاهش لکوسیت سبب کاهش خطر انتقال HTLV-1 میشود که طبق استاندارد، لکوسیت کمتر از 106×5 در هر واحد RBC یا پلاکت، فرآورده خونی کم لکوسیت است که میتواند ایمن باشد اما اگر اهداکنندهای باشد که تعداد کپی بالایی از ویروس را داشته باشد، با وجود کاهش لکوسیت هنوز امکان انتقال وجود دارد(4). 5% از افراد آلوده به ویروس HTLV-1 به سمت بیماری لوسمی سلول T بالغین(ATL : Acute T Cell Leukemia) و 4% از افراد آلوده به سمت بیماری فلج سفت گرمسیری ( HAM/TSP)پیشرفت میکنند(5). فاکتورهای ژنتیک میزبان، تعداد کپی ویروس و پاسخ سیستم ایمنی میزبان میتوانند در پیشرفت افراد آلوده به سمت بیماریهای ATL و(HAM/TSP : HTLV-1 Associatedc Myelopathy/Tropical Spastic Paraparesis) کمککننده باشند(6). همچنین مطالعهها نشان دادند که در گسترده شدن عفونت مزمن، مکانیسمهای مختلف ایمنی مثل تولید سیتوکاینهای ضد التهابی، القای سلولهای T تنظیمکننده(Treg) و بیان مولکولهای Immune checkpoint درگیر هستند(7). در عفونتهای مزمن مانند HIV ، هپاتیت B ، هپاتیت CوHTLV-1 ، بیان پروتئین مرگ برنامهریزی شده یک (PD-1) که یک مولکول Immune checkpointاست، افزایش مییابد و به دنبال آن تکثیر سلولهای T CD8+ و تولید سایتوکاین آنها مختل میشود و حالت خستگی برای سلولهای Tایجاد میشود که عفونت پایدار میگردد(9، 8). ژن PD-1 بر روی کروموزوم 2 در موقعیت q37.3 با KDal55 و 228 اسید آمینه است(10). PD-1 (که CD279نیز نامیده میشود) یک پروتئین تراغشایی از خانواده B7/CD28 و سوپرخانواده ایمنوگلوبولین است که بر روی سلولهای T (CD4+ ، CD8+)، سلولهای NK1 ، لنفوسیتهای B و مونوسیتهای فعال شده بیان میشود(11).
در عفونت HTLV-1 ، با افزایش بیان PD-1 ، تعداد کپی ویروس افزایش و عملکرد لنفوسیتهای سیتوتوکسیک کاهش مییابد(12). پلیمورفیسمrs36084323 در جایگاه 606 در ناحیه پروموتور ژن PD-1 قرار دارد که میتواند در فعالیت پروموتور اثرگذار باشد(13). با توجه به نقش PD-1 در عفونت HTLV-1 و تاثیر آن در عملکرد سلولهای T ، این مطالعه به منظور بررسی ارتباط بین پلیمورفیسم rs36084323دراهداکنندگان خون آلوده به ویروس HTLV-1 بدون علامت در مقایسه با افراد سالم انجام شد، که میتواند اطلاعات مفیدی را در مورد تاثیر پلیمورفیسمrs36084323 در پایداری عفونت ویروسی و انتقال ویروس HTLV-1 به افراد سالم فراهم آورد.
مواد و روشها
این مطالعه از نوع مورد- شاهدی بود که بر روی نمونه خون 81 اهداکننده خون آلوده به ویروس HTLV-1 که علامتی از بیماری را نداشتند(65 مرد و16 زن با میانگین و انحراف معیار سنی 55/10 ± 36/40 سال) و 162 اهدا کننده خون سالم(154 مرد و 8 زن با میانگین و انحراف معیار سنی 009/0 ± 37/61 سال) انجام شد. نمونههای استفاده شده در این مطالعه از اهداکنندگان خون استان خراسان رضوی بود که پس از دریافت رضایتنامه آگاهانه جمعآوری گردید. افراد آلوده به ویروس HTLV-1 توسط آزمایش الایزا و کیت(سنگاپور، HTLV-I/II ELISA 4.0) تشخیص داده شده بودند و آزمایش وسترنبلات با کیت (سنگاپور، HTLV Blot 2.4) به منظور تایید آلودگی انجام شده بود .به علاوه تمامی نمونهها از نظر آلودگیهای ویروسی HIV ، HBV و HCV منفی بودند. نمونه خون افراد به منظور جداسازی بافیکوت و پلاسما سانتریفیوژ گردید و از نمونههای بافیکوت، DNA ژنومی با استفاده از کیت یکتا تجهیز استخراج گردید و برای انجام مراحل بعد در فریزر 70- درجه سانتیگراد نگهداری شد. پلیمورفیسم rs36084323 با استفاده از روشPCR- RFLP تعیین ژنوتیپ گردید. آغازگرهای به کار رفته در واکنش زنجیرهای پلیمراز (PCR) عبارت بودند از: آغازگر مستقیم (AAGAAGGTCAAGGCTGGAAGGGG3′′5)، آغازگر معکوس3′) ATTCTGTCGGAGCCTCTGGGAG′5) (جدول 1).

محصول حاصل از PCR که قطعه ۳۰۶ جفت باز بود، بر روی ژل آگارز ۲ درصد الکتروفورز و توسط رنگآمیزی با رنگ Green viewer درمقابل نور فرابنفش آشکارسازی شد. پس از آن ۱۰میکرولیتر از محصول PCR جهت هضم آنزیمی توسط U/µL ۵ آنزیم محدودالاثر MspI و۲ میکرولیتر بافر آنزیم ده برابر غلظت به مدت ۱۶-۱۲ ساعت(overnight) در دمای ۳۷ درجه سانتیگراد انکوبه گردید .محصول هضم آنزیمی با الکتروفورز بر روی ژل آگارز 3% به همراه نشانگر وزن مولکولی ۵۰ جفت بازی آشکار شد. قطعه تکثیر شده دارای دو جایگاه برش آنزیم MspIاست که یک جایگاه سبب برش قطعه ۲۹ جفت بازی میشود که در زیر نشانگر وزن ملکولی ۵۰ جفت باز قرار میگیرد. اگر در جایگاه
برش آنزیم MspIپلیمورفیسم، آلل G باشد، به دنبال برش قطعه bp ۲۷۷ و اگر آلل A باشد، قطعات ۲۲۲و ۵۵ جفت بازی به دست میآید. جهت تایید نتایج ژنوتایپینگ، ۱۰% از محصولات PCR به روش سنگر یا خاتمه زنجیره جهت توالییابی به شرکت پیشگام ارسال شد.
تحلیل آماری نتایج با استفاده از نرمافزای آماری SPSS نسخه ۲۲ انجام شد و دادههای ژنوتیپی براساس آزمون مربع کای مورد مقایسه قرار گرفت. مقدار p-value کمتر از ۰۵/۰ معنادار در نظر گرفته شد.
یافتهها
با انجام PCR و الکتروفورز محصولی با طول ۳۰۶ جفت باز مشاهده شد(شکل ۱). پس از هضم آنزیمی محصول PCR درافراد هموزیگوت GG ، سه قطعه ۲۹، ۵۵، ۲۲۲ جفت بازی در افراد هموزیگوت AA ، دو قطعه۲۹، ۲۷۷ جفت بازی و در افراد هتروزیگوت GA ، چهار قطعه ۲۹ ، ۵۵ ، ۲۲۲ و ۲۷۷ جفت باز مشاهده گردید(شکل ۲).
نتایج حاصل از تعیین توالی، تاییدکننده نتایج PCR-RFLP بود(شکل ۳) . در کلیه محاسبات آماری انجام شده فاصله اطمینان 95% بود. در دو گروه مورد مطالعه فراوانی ژنوتیپها به شرح: GG (۹/۵۱%) ، GA (۳/۴۶%) و AA (۹/۱%) برای گروه شاهد و GG (۳/۵۹%) ، GA (۷/۴۴%) و AA (00/0%) برای گروه مورد بود. محاسبات آماری نشان داد که با مرجع در نظر گرفتن ژنوتیپ GG ، میزان p-value برای ژنوتیپها GA و AA به ترتیب ۳۴۹/۰ و ۳۶۱/۰ بود . با مرجع در نظرگرفتن آلل رفرنس G میزان p-value برای آلل A برابر۲۵۶/۰ بود(جدول 2). نتایج تعیین ژنوتیپ براساس دو مدل غالب و مغلوب با استفاده از آزمون آماری مربعکای نشان میدهد در مدل غالب، p معنادار نبود (جدول 3).



بحث
بنابراین با توجه به نقش PD-1 ، پلیمورفیسمهای این ژن میتوانند با تغییر در میزان بیان PD-1 در فرار ویروس از پاسخهای ایمنی و افزایش تعداد سلول آلوده اثرگذار باشند و با افزایش تعداد سلول آلوده، احتمال انتقال این ویروس به دنبال تزریق فرآوردههای خونی و تغذیه با شیر مادر افزایش مییابد. مطالعهای بر روی بیماران روماتوئید آرتریت نشان داد که آلل G و ژنوتیپ GG پلیمورفیسم rs36084323 ، با افزایش میزان بیان mRNA PD-1 همراه است و ژنوتیپ AA این پلیمورفیسم یک فاکتور محافظتکننده در برابر روماتوئید آرتریت است. در مطالعهای دیگر بر روی بیماران روماتوئید آرتریت نشان داده شد که آلل A پلیمورفیسم rs36084323 ، دارای فراوانی بیشتری در بیماران روماتوئید آرتریت درجمعیت ایرانی است(14).
به علاوه مطالعهها بر روی سرطان پستان نشان داده شده است که ژنوتیپ GG این پلیمورفیسم، یک فاکتور محافظتکننده در برابر سرطان پستان است(19). مطالعه بر روی بیماران مبتلا به هپاتیت B نشان داد که ترکیب ژنوتیپ GA یا GG پلیمورفیسم rs10204525به همراه ژنوتیپ GG پلیمورفیسم rs36084323در بیماران مبتلا به هپاتیت B فراوانی کمی دارد(20). نتایج مطالعه حاضر نشان میدهد که فراوانی ژنوتیپ GG در گروه سالم (۹/۵۱%) و در گروه مورد(۳/۵۹%) بالا است و با توجه به این که گروه مورد در این مطالعه افراد آلوده به ویروس HTLV-1 هست که علامتی از بیماری را نداشتهاند، بنابراین مطالعه حاضر میتواند با نتایج مطالعه قبل همسو باشد و ژنوتیپ GG این پلیمورفیسم میتواند نقش محافظتکننده
در افراد آلوده به ویروس در پیشرفت بـه سمـت بیمـاری
داشته باشد.
نتیجهگیری
نتایج این مطالعه نشان داد ارتباطی بین پلیمورفیسم تک نوکلئوتیدیrs36084323 با استعداد آلودگی به ویروس HTLV-1 در جمعیت ایرانی وجود ندارد و ژنوتیپ GG این پلیمورفیسم میتواند نقش محافظتکننده علیه ویروس HTLV-1 داشته باشد. از آن جا که شیوع پلیمورفیسم rs36084323 درجوامع مختلف متفاوت است، این موضوع میتواند دلیلی برای آندمیک بودن برخی بیماریها در
جمعیتها و نژادهای مختلف باشد، لازم است این پلیمورفیسم در کنار سایر عوامل اثرگذار بر روی تعداد بیشتری افراد آلوده به ویروس، بیماران HAM/TSP و بیماران ATL و پاسخ آنها به درمان ایمونوتراپی مورد بررسی قرار گیرد.
تشکر و قدردانی
این تحقیق موضو ع کارشناسی ارشد رشته بیوتکنولوژی پزشکی با کد اخلاقIR.TIM.REC.1398.025 است که هزینه آن توسط مؤسسه عالی آموزشی و پژوهشی طب انتقال خون تامین شده است.
نوع مطالعه: پژوهشي |
موضوع مقاله:
ويروس شناسي
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |






