جلد 18، شماره 1 - ( بهار 1400 )
جلد 18 شماره 1 صفحات 69-60 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Darbandi A, Yari F, Sharifi Z, Rezaei N. Comparison of different techniques for loading doxorubicin in platelets microparticles. Sci J Iran Blood Transfus Organ 2021; 18 (1) :60-69
URL: http://bloodjournal.ir/article-1-1363-fa.html
URL: http://bloodjournal.ir/article-1-1363-fa.html
دربندی آرزو، یاری فاطمه، شریفی زهره، رضایی نگار. مقایسه روشهای مختلف بارگذاری داروی دوکسوروبیسین در میکروپارتیکلهای پلاکتی. فصلنامه پژوهشی خون. 1400; 18 (1) :60-69
استاد مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون
متن کامل [PDF 573 kb]
(1194 دریافت)
| چکیده (HTML) (2229 مشاهده)
مقدمه
میکروپارتیکل پلاکتی(platelet Microparticles) یا به اختصارPMP ، از پلاکت آزاد میشود و حاوی انواع مختلفی از پروتئینها، میکروRNA و DNA است. این PMP ، میتوانند مارکر بسیاری از بیماریها باشند(1). در شرایط فیزیولوژیک بدن، میکروپارتیکلها از پلاکتهای فعال شده جوانه میزنند. PMPها در مواردی که نشاندهنده بیماری هستند، مارکرهای اختصاصی سطح غشایی آنها مانند فسفاتیدیل سرین دچار تغییرات بعد از ترجمه مانند سیترولیناسیون میشوند(2). PMPفراوانترین(90-70 درصد) میکروپارتیکلهای خون است که از پلاکتهای ذخیره شده در بانک خون نیز آزاد میشود(3). روشهای متعددی برای تشخیص و بررسی خصوصیات میکروپارتیکلها وجود دارد که فلوسیتومتری Gold standard آنها است(4). سلولها در پاسخ به فعالسازی، وزیکولهای غشای پلاسمایی را آزاد میکنند. اگرچه میکروپارتیکل در خون افراد سالم وجود دارد اما بالا رفتن سطح آن با اختلالاتی از جمله سرطان، آترواسکلروز و غیره همراه میشود(3). سیستمهای دارو رسانی(Drug Delivery System) شامل تکنولوژی و سیستمهایی است که بر پایه نانوذرات استوار است و میتواند ترکیبات دارویی را در بدن حمل کند(5). امروزه استفاده از این پارتیکلها میتواند محدودیتهای استفاده از روشهای پیشین دارو رسانی مانند توزیع و هدفگذاری غیر اختصاصی دارو را حل کند. نانو پارتیکلها قادر هستند مدت زمان بیشتری در خون بمانند و محتویات خود را در اختیار سلولهای توموری قرار دهند. یکی از عوامل مهم که میتواند باعث مقاومت دارویی شود، شناسایی ذرههای دارویی توسط گلیکو پروتئینهای p است. این عامل وقتی از پارتیکلهای سازگار با بدن استفاده شود، میتواند به حداقل برسد. در نهایت میتواند در برداشتن گامی جدید در درمان انواع بیماریها و سرطانها به صورت درمان دارویی شخص محور بسیار حائز اهمیت باشد(6). دوکسوروبیسین از داروهای شیمی درمانی موجود برای درمان بسیاری از سرطانها است. این دارو در خانواده آنتیبیوتیکی آنتراسایکلین قرار میگیرد و در حال حاضر برای دستهای از بیماریهای نئوپلاستیک توسط سازمان غذا و داروی آمریکا تائید شده است. این دارو که حالت محلول آن دوکسوروبیسین هیدروکلراید نامیده میشود، به دلیل وجود گروه کروموفور آنتراسیکلین مرکزی، دارای خاصیت فلوئورسنت بوده و میتوان با روشهای تصویربرداری فلوئورسنت آنها را در بافتها ردیابی کرد(8، 7).
پپتیدهای نفوذکننده به سلول CPP (Cell Penetrating Peptides) پپتیدهایی به شدت کاتیونیک هستند و غالباً غنی از آمینواسیدهای لیزین و آرژنین میباشند و خیلی سریع به هر سلولی نفوذ میکنند. انواع مختلفی از این پپتیدها وجود دارد که در 5 کلاس دستهبندی میشوند. از شایعترین آنها کلاس کاتیونیک است(10، 9).
مواد و روشها
نوع این مطالعه تجربی بوده و نمونه های کنستانتره پلاکتی به صورت تصادفی از اهداکنندگان انتخاب و پس از 5 روز قرار گرفتن بر روی انکوباتور شیکر در دمای 20 الی 24 درجه سانتیگراد، از سازمان انتقال خون ایران دریافت شدند.
تهیه میکروپارتیکلهای پلاکتی:
کیسههای کنستانتره پلاکتی در روز پنجم پس از خونگیری از اهداکننده، برای جداسازی میکروپارتیکلها استفاده شد. میکروپارتیکلهای پلاکتی در روز 3 تا 5 نگهداری کیسههای کنستانتره پلاکتی به مقدار زیادی در کیسهها تجمع پیدا میکنند. محتویات کیسههای کنستانتره پلاکتی در زیر هود کلاس دو و تحت شرایط استریل به درون لولههای فالکون منتقل شدند و جهت رسوب و جداسازی پلاکتها و گلبولهای قرمز و سفید، لولههای فالکون به مدت 15 دقیقه در دور g 1200 و طی دو مرحله در دمای محیط سانتریفیوژ(مدل اپندورف) شدند. سپس سوپرناتانت به لولههای مخصوص اولتراسانتریفیوژ منتقل و در دور g16000 طی سه مرحله در دمای یخچال (10 درجه سانتیگراد) سانتریفیوژ شد که بین هر مرحله میکروپارتیکلهای رسوب شده با بافر PBS (Phosphate Buffer Saline) استریل شسته شدند. رسوب نهایی در PBS حل شده و جهت تعیین غلظت، ویژگی، سایز، مواجهه با دارو و سلول در فریزر 70- درجه سانتیگراد نگهداری شدند.
تعیین غلظت میکروپارتیکلها با استفاده از روش برادفورد:
اتصال پروتئین به رنگ کوماسی، فرم آبی رنگ را تثبیت و منجر به تغییر رنگ متناسب با میزان پروتئین میشود.
برای خوانش میزان جذب نوری رنگها در روش برادفورد، از طول موج nm595 استفاده میشود. برای مواجهه مؤثر و مطلوب میکروپارتیکلها با داروها و ردههای سلولی، تعیین غلظت میکروپارتیکلها انجام شد. برای تعیین غلظت از استانداردهای با غلظت مشخص BSA(Bovine serum albumin) استفاده گردید. غلظتهای µg/mL1500، µg/mL 750 ،µg/mL 375 ،µg/mL 5/187 ، µg/mL 75/93 ، µg/mL 87/46 ، µg/mL 43/23 و µg/mL 71/11 از BSA تهیه شد. 200میکرولیتر از معرف برادفورد در چاهکها ریخته شد و متعاقب آن 10 میکرولیتر از رقتهای استاندارد تهیه شده و میکروپارتیکلهای جدا شده به چاهکها اضافه شد.
تعیین سایز میکروپارتیکلها با استفاده از میکروبیدهای کونژوگه با فلوئورسنت:
برای این آزمایش از میکروبیدهای فلوئورسنت (برند molecular probes، کشور آمریکا) با اندازه 1 میکرومتر استفاده شد. به نمونههای میکروپارتیکل با غلظت µg/ml 100 ، 5 میکرولیتر از محلول 500 بار رقیق شده میکروبیدهای فلوئورسنت اضافه شد و سپس این نمونهها جهت بررسی اندازه با استفاده از دستگاه فلوسیتومتری (partec CyFlow) استفاده شد.
تعیین منشاء و خصوصیات میکروپارتیکلهای پلاکتی:
برای تایید منشا میکروپارتیکلها از مارکرهای سطحی و اختصاصی پلاکتها استفاده گردید. CD41 (از شرکت بیولژند کشور آمریکا و کونژوگه به ماده فلوئورسنت FITC) و CD61 (از شرکت داکو کشور دانمارک و کونژوگه به ماده فلوئورسنت FITC)، یکی از بهترین گزینههاست. برای این کار غلظت میکروپارتیکلها را به µg/mL100 رسانده و 3 میکرولیتر از آنتیبادی ضد CD41 وCD61 کونژوگه شده با فلوئورسنت به آن اضافه شد و نیم ساعت در یخچال انکوباسیون انجام شد. سپس با استفاده از دستگاه فلوسیتومتری تایید منشا انجام گرفت. برای اطمینان و کنترل این که آنتیبادی استفاده شده به صورت اختصاصی به مارکر سطحی چسبیده است و چسبندگی غیر اختصاصی با ناحیهFC مارکر نداشته، از isotype control استفاده شد.
بارگذاری داروی دوکسوروبیسین در میکروپارتیکل پلاکتی:
دوکسوروبیسین برند Tocris از کشور انگلستان خریداری شد و غلظتهای مختلف میکروپارتیکل (µg/mL 50 ، µg/mL 100 ، µg/mL 150 ، µg/mL 200 و µg/mL 250 ) با غلظتهای مختلف دوکسوروبیسین (µg/mL 20 ، µg/mL 10، µg/mL 5 ، µg/mL 1) با روشهای مختلف به شرح زیر با هم مواجه شدند. در این مرحله غلظت بهینه شده برای مواجهه دارو با میکروپارتیکل مشخص گردید که در هر سه روش ثابت بوده و در ادامه توضیحات هرروش ذکر شده است.
بارگذاری دارو با روش انکوباسیون:
استفاده از این روش از رایجترین روشهای مورد استفاده برای بارگذاری دارو بر روی پارتیکلها و ذرات مختلف میباشد. میکروپارتیکلهای پلاکتی با غلظت µg/mL 150 با دوکسوروبیسین با غلظت µg/mL 10 به مدت 2 ساعت در 37 درجه سانتیگراد و در تاریکی و با دور rpm 100 انکوبه شدند. سپس نمونهها با دور g 16000 و به مدت 15 دقیقه در 10 درجه سانتیگراد سانتریفیوژ شدند و مایع رویی خارج شد و با PBS شستشو شد. پلت نهایی برای بررسی فلوسیتومتری جمعآوری شد.
بارگذاری دارو با روش CPP :
محلول CPP
برای ساخت پلیمر آرژنین حاوی مولکولهای داروی
دوکسوروبیسین، 30 میلیگرم آرژنین که وزن مولکولی 2/174 داشت را در 6 میلیلیتر PBS حل کرده و مقدار 5 میکرولیتر گلوتارآلدئید به آن اضافه کرده و 5/1 ساعت در تاریکی با هم مخلوط شدند و بعد در کیسههای دیالیز 3000 دالتون دیالیز گردیدند و محیط آن دو بار تعویض شد که مونومرهای موجود در کیسه دیالیز خارج شود و تنها پلیمرهای آرژنین باقی ماندند. در ادامه، 25 میکرولیتر از محلول داروی دوکسوروبیسین با غلظت µg/mL500 را اضافه کرده و سپس مقدار 2 میلیگرم از پودر گلایسین اضافه شده و انکوباسیون، دیالیز انجام گردید.
میکروپارتیکلهای پلاکتی با غلظت µg/mL 150 با داروی کونژوگه شده به CPP به مدت 2 ساعت در 37 درجه سانتیگراد و در تاریکی و با دور rpm 100 مواجه شدند. سپس نمونهها با دور g 16000 و به مدت 15 دقیقه سانتریفیوژ شدند و مایع رویی خارج شد و PBS ریخته و یک بار با همان شرایط ذکر شده شستشو و سانتریفیوژ انجام شد. پلت نهایی برای بررسی فلوسیتومتری جمع آوری گردید.
بارگذاری دارو با روش سونیکاسیون :
میکروپارتیکلهای پلاکتی با غلظت µg/mL 150 با دوکسوروبیسین با غلظت µg/mL 10، 6 چرخه 20% آمپلیتیود که هر چرخه 3 دقیقه (30 ثانیه روشن/30 ثانیه خاموش) طول میکشد، سونیکه شدند و بین هر چرخه 2 دقیقه زمان کولینگ در نظر گرفته شد و پس از آن نمونه سونیکه شده 1 ساعت در 37 درجه سانتیگراد انکوبه شد. در ادامه نمونهها با دور g 16000 و به مدت 15 دقیقه سانتریفیوژ شدند و مایع رویی خارج شد و PBS ریخته و یک بار با همان شرایط ذکر شده شستشو و سانتریفیوژ شد. پلـت نهایـی بـرای بـررسی فلـوسیتومتری جمعآوری شد.
نحوه جمعآوری و تجزیه و تحلیل دادهها:
تمامی آزمایشها حداقل 3 بار تکرار شده و نتایج حاصل از بررسیهای اصلی پروژه شامل فلوسیتومتری بـرای ثبت میزان نور فلوئورسنت ساطع شده، جمعآوری و
به صورت میانگین ± انحراف معیار گزارش شدند.
تحلیل آماری با استفاده از نرمافزار SPSS26 انجام شد و طبیعی بودن توزیع متغیرها با استفاده از آزمون کلموگروف - اسمیرنوف محاسبه شد. جهت تحلیل و مقایسه میانگین دادهها در بیشتر از دو گروه از آزمونOne Way Anova و Tukey Post Hoc Test استفاده شد. ضمناً 05/0 p≤ معنادار در نظر گرفته شد.
یافتهها
نمودار استاندارد از خواندن جذب نوری رقتهای مختلف BSA تهیه شده و در ادامه با استفاده از این نمودار، غلظت میکروپارتیکلهای جدا شده بر حسب میکروگرم در هر میلیلیتر محاسبه شد. غلظت میکروپارتیکلهای پلاکتی که از 7 کیسه کنستانتره پلاکتی جدا شده بود،µg/mL 1800،µg/mL 1500، µg/mL700، µg/mL3000، µg/mL 2500، µg/mL1000 وµg/mL 4500 تعیین شد (نمودار 1).
در ادامه برای تعیین سایز میکروپارتیکلها با استفاده از میکروبیدهای کونژوگه با فلوئورسنت، قسمت R1 ، میکروپارتیکلهای به دست آمده از کنسانتره پلاکتی میباشد که 95% کل جمعیت میکروپارتیکلها از لحاظ سایز از میکروبیدهای فلوئورسنت که در قسمت R1 مشخص شده است، کوچکتر است و در محدوده پایینتر از یک میکرومتر قرار گرفته است(نمودار 2). در این مطالعه از کل جمعیت میکروپارتیکل پلاکتی استفاده شده و اقدام به جداسازی اندازه خاصی از آنها نشد.
در ادامه، میکروپارتیکلهای پلاکتی با آنتیبادی ضد CD41 و CD61 تیمار شدند. در مقایسه با آنتیبادی ایزوتایپ کنترل، 39/92% و 03/80% از آنها به ترتیب دارای این آنتیژن پلاکتی بودند. در نمودار 3 قسمت A ، R1 نشاندهنده جمعیت میکروپارتیکلهای پلاکتی بوده و شکل C و D به ترتیب نشاندهنده جمعیت میکروپارتیکلهای پلاکتی رنگ شده با Anti CD41 وAnti CD61 میباشد که با ماده فلوئورسنت FITC کونژوگه شدهاند.
در روش انکوباسیـون برای بـررسی میـزان بـارگـذاری داروی دوکسـوروبیسیــن در میکـروپـــارتیکـلهــای در پلاکتی، 5 بـار مـواجهه در دوزهای مختلف صورت گرفت

نمودار 6 : میزان بارگذاری دارو در روش CPPقسمت A نشاندهنده گیت جمعیتی و قسمت B نشاندهنده میزان نور فلوئورسنت ساطع شده (97/85%) داروی بارگذاری شده با روش CPP در یکی از نمونههای میکروپارتیکل پلاکتی میباشد.

نمودار 7: مقایسه روشهای لود دارو در میکروپارتیکلهای پلاکتی نشاندهنده مؤثرتر بودن روش انکوباسیون در مقایسه با دو روش سونیکاسیون و CPP میباشد.
بحث
شباهت ساختاری و عملکردی میکروپارتیکلهای مشتق از سلول از قبیل میکروپارتیکلهای پلاکتی با نانو ساختارهای سنتتیک و پلیمری که در دارو رسانی استفاده میشوند، این ایده را ایجاد کرد که بتوان از این میکروپارتیکلها برای دارو رسانی در بیماریهای مختلف مانند سرطان و عفونتهای ویروسی استفاده نمود. طبیعی بودن منشاء ایـن میکـروپارتیکلها میتواند بسیاری از اثرات جانبی و سمیتهای سیستمهای دارو رسانی سنتتیک و پلیمـری را بـرطرف کنـد. ایـن مطالعـه جهـت بــررسی
کاربرد استفاده از میکروپارتیکلهای پلاکتی به عنوان حامل داروی دوکسوروبیسین با روشهای مختلف بارگذاری شامل: انکوباسیون، سونیکاسیون و CPP انجام گردید. با توجه به نتایج به دست آمده از فلوسیتومتری، میزان شدت نور فلوئورسنت داروی دوکسوروبیسین در روشهای انکوباسیون، سونیکاسیون و CPP به ترتیب 37/11 ± 09/79 درصد، 12/25 ± 48/47 درصد و 23/24 ± 69/56 درصد گزارش شدند.
برای مقایسه این 3 روش مختلف لود دارو با استفاده از آزمایـش آمـاری Anova مـیتوان گفـت، به طور کلی میان
روشهای مختلف انجام شده اختلاف معناداری وجود دارد(005/0 p≤). استفاده از روش انکوباسیون برای لود دارو به دلیل بالاتر بودن درصد میانگین به دست آمده از فلوسیتومتری، میتواند روش مؤثرتری باشد.
نتایج حاصل از مطالعههایی که در آن از ذرههای پلاکتی به عنوان حامل داروی دوکسوروبیسین استفاده شده است نشان داده که استفاده از پلاکت به عنوان حامل این دارو توانایی توکسیسیتی بالاتر برای بافت و سلولهای سرطانی و در عین حال کاردیوتوکسیسیتی کمتر برای بیماران را دارد(13-11). مطالعههایی نیز از پلاکت به عنوان حامل دارو استفاده کردند که برای اختصاصی تر شدن تحویل دارو به سلولهای سرطانی و بافت هدف، پلاکتها را با آنتیبادی ضد CD22 کونژوگه نمودند(14). در مطالعههای جدیدی که انجام شده، میکروپارتیکلهای پلاکتی به عنوان فاکتور مهم در بازسازی کبد استفاده شده که میکروپارتیکلهای پلاکتی با تنظیم مسیر اتوفاژی و افزایش تکثیر سلولهای هپاتوسیت، در این مسیر نقش خود را ایفا میکنند(15). در مطالعههای دیگری که اخیراً انجام داده شده، برای کنترل عوارض انفارکتوس حاد میوکاردی که در آن اینترلوکین-1ß نقش اصلی را در آسیب و مرگ سلولهای میوکاردی دارد، از میکروپارتیکلهای پلاکتی همراه با آنتی بادی ضد IL-1ß استفاده کردند و نشان دادند که این میکروپارتیکلها میتوانند عامل مهمی در سمزدایی و ترمیم سلولی در زمان انفارکتوس حاد میوکاردی باشند(16). در این مطالعه برای اولین بار مقایسه روشهای مختلف لود دارو در میکروپارتیکلهای پلاکتی به منظور یافتن روش مؤثرتر برای بارگذاری دارو، انجام شد. در مطالعههای پیشین بیشتر مواقع از روش انکوباسیون برای لود دارو استفاده شده است و مواردی نیز گزارش شده که
از سایر روشهای لودینگ مانند استفاده از پلیاتیلن گلیکول، الکتروپوریشن و غیره برای لود دارو بر روی میکروپارتیکلها استفاده شده است(18، 17). نتایج مطالعههای انجام شده در این مقاله در مقایسه با روشی که از پلاکت به عنوان حامل و از روش انکوباسیون برای بارگذاری دارو استفاده شده بود، در یک راستا قرار داشتند(19، 14، 11). اگر چه در مطالعهای که از میکروپارتیکلهای پلاکتی به عنوان حامل داروهای ضد ویروسی HIV-1 استفاده شد، روش سونیکاسیون در بارگذاری آن داروها دارای اثرگذاری بالاتری بوده است(20). در توجیه این اختلاف میتوان بیان کرد که با توجه به این که از سل لاینها و داروهای متفاوت استفاده شده است، میزان لود شدن دارو در میکروپارتیکلها میتواند متفاوت باشد.
نتیجهگیری
در نهایت مطالعه صورت گرفته نشان میدهد که استفاده از روش انکوباسیون میتواند روش مؤثرتری برای لود داروی دوکسوروبیسین در میکروپارتیکلهای پلاکتی باشد. پیشنهاد میشود که استفاده از این روش در مطالعههای بالینی و آزمایشگاهی بر روی سایر داروها با همراهی با میکروپارتیکلهای پلاکتی جهت اثرگذاری بیشتر، مورد بررسی قرار گیرند.
تشکر و قدردانی
این مقاله حاصل از پایاننامه ارشد کارشناسی ارشد آرزو دربندی با کد اخلاق IR.timi.rec.1397.036 میباشد که در مرکز تحقیقات انتقال خون، مؤسسه عالی آموزشی و پژوهشی طب انتقال خون و با حمایت مالی این مؤسسه انجام شده است.
متن کامل: (2284 مشاهده)
مقایسه روشهای مختلف بارگذاری داروی دوکسوروبیسین در
میکروپارتیکلهای پلاکتی
آرزو دربندی1، فاطمه یاری2، زهره شریفی3، نگار رضایی4
چکیده
سابقه و هدف
میکروپارتیکلهای پلاکتی، میکروذرات مشتق از پلاکت میباشند. امروزه میتوان با استفاده از نانو پارتیکلها، بسیاری از محدودیتهای روشهای پیشین دارو رسانی در درمان سرطانها را کاهش داد. دوکسوروبیسین، داروی شیمی درمانی موجود برای درمان بسیاری از سرطانها است که دارای خاصیت فلوئورسنت بوده و با ویژگی فلوئورسنت آن، شناسایی میشود. هدف از این مطالعه، مقایسه روشهای مختلف بارگذاری دارو در میکروپارتیکل پلاکتی بود.
مواد و روشها
در یک مطالعه تجربی، کنسانتره پلاکتی در روز پنجم از سازمان انتقال خون دریافت گردید. سپس طی چند مرحله سانتریفیوژ، میکروپارتیکل پلاکتی استخراج شد. با استفاده از میکروبیدهای فلوئورسنت یک میکرومتری و آنتیبادی ضد CD41 وCD61 ، میکروپارتیکلها به ترتیب تعیین سایز و هویت گردیدند. µg10 دوکسوـ روبیسین در میکروپارتیکلهای پلاکتی با سه روش انکوباسیون، پپتیدهای نفوذکننده به سلول و سونیکاسیون بارگذاری شد و با استفاده از خاصیت اتو فلوئورسنت دوکسوروبیسین، درصد ورود دارو به میکروپارتیکل با فلوسیتومتری اندازهگیری شد.
یافتهها
95% از جمعیت کل میکروپارتیکلها از نظر سایز در محدوده زیر یک میکرومتر و 39/92% و 03/80% از این میکروپارتیکلها دارای CD41 و CD61 بودند. میزان نور فلوئورسنتی که به طور میانگین در هر کدام از روشهای انکوباسیون، سونیکاسیون و CPP محاسبه گردیدند، به ترتیب 37/11 ± 09/79% ، 12/25 ± 48/47% و 24/23 ± 69/56% تعیین شدند.
نتیجه گیری
روش انکوباسیون با بالاترین میانگین داروی لود شده میتواند روش مؤثرتری باشد. استفاده از این روش برای بارگذاری دارو در پارتیکلها در مطالعههای بالینی میتواند مورد توجه قرار گیرد.
کلمات کلیدی: دوکسوروبیسین، پلاکتها، میکروپارتیکل های مشتق از سلول
تاریخ دریافت: 29/6/99
تاریخ پذیرش: 31/6/99
1- دانشجوی هماتولوژی و بانک خون ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- مؤلف مسئول: PhD ایمونولوژی ـ استاد مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران ـ صندوق پستی: 1157-14665
3- PhD ویروسشناسی ـ استاد مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
4- PhD اپیدمیولوژی ـ استادیار مرکز تحقیقات غدد درونریز متابولیسم ـ پژوهشکده علوم بالینی غدد ـ پژوهشگاه علوم غدد و متابولیسم دانشگاههای علوم پزشکی تهران ـ تهران ـ ایران
میکروپارتیکلهای پلاکتی
آرزو دربندی1، فاطمه یاری2، زهره شریفی3، نگار رضایی4
چکیده
سابقه و هدف
میکروپارتیکلهای پلاکتی، میکروذرات مشتق از پلاکت میباشند. امروزه میتوان با استفاده از نانو پارتیکلها، بسیاری از محدودیتهای روشهای پیشین دارو رسانی در درمان سرطانها را کاهش داد. دوکسوروبیسین، داروی شیمی درمانی موجود برای درمان بسیاری از سرطانها است که دارای خاصیت فلوئورسنت بوده و با ویژگی فلوئورسنت آن، شناسایی میشود. هدف از این مطالعه، مقایسه روشهای مختلف بارگذاری دارو در میکروپارتیکل پلاکتی بود.
مواد و روشها
در یک مطالعه تجربی، کنسانتره پلاکتی در روز پنجم از سازمان انتقال خون دریافت گردید. سپس طی چند مرحله سانتریفیوژ، میکروپارتیکل پلاکتی استخراج شد. با استفاده از میکروبیدهای فلوئورسنت یک میکرومتری و آنتیبادی ضد CD41 وCD61 ، میکروپارتیکلها به ترتیب تعیین سایز و هویت گردیدند. µg10 دوکسوـ روبیسین در میکروپارتیکلهای پلاکتی با سه روش انکوباسیون، پپتیدهای نفوذکننده به سلول و سونیکاسیون بارگذاری شد و با استفاده از خاصیت اتو فلوئورسنت دوکسوروبیسین، درصد ورود دارو به میکروپارتیکل با فلوسیتومتری اندازهگیری شد.
یافتهها
95% از جمعیت کل میکروپارتیکلها از نظر سایز در محدوده زیر یک میکرومتر و 39/92% و 03/80% از این میکروپارتیکلها دارای CD41 و CD61 بودند. میزان نور فلوئورسنتی که به طور میانگین در هر کدام از روشهای انکوباسیون، سونیکاسیون و CPP محاسبه گردیدند، به ترتیب 37/11 ± 09/79% ، 12/25 ± 48/47% و 24/23 ± 69/56% تعیین شدند.
نتیجه گیری
روش انکوباسیون با بالاترین میانگین داروی لود شده میتواند روش مؤثرتری باشد. استفاده از این روش برای بارگذاری دارو در پارتیکلها در مطالعههای بالینی میتواند مورد توجه قرار گیرد.
کلمات کلیدی: دوکسوروبیسین، پلاکتها، میکروپارتیکل های مشتق از سلول
تاریخ دریافت: 29/6/99
تاریخ پذیرش: 31/6/99
1- دانشجوی هماتولوژی و بانک خون ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- مؤلف مسئول: PhD ایمونولوژی ـ استاد مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران ـ صندوق پستی: 1157-14665
3- PhD ویروسشناسی ـ استاد مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
4- PhD اپیدمیولوژی ـ استادیار مرکز تحقیقات غدد درونریز متابولیسم ـ پژوهشکده علوم بالینی غدد ـ پژوهشگاه علوم غدد و متابولیسم دانشگاههای علوم پزشکی تهران ـ تهران ـ ایران
مقدمه
میکروپارتیکل پلاکتی(platelet Microparticles) یا به اختصارPMP ، از پلاکت آزاد میشود و حاوی انواع مختلفی از پروتئینها، میکروRNA و DNA است. این PMP ، میتوانند مارکر بسیاری از بیماریها باشند(1). در شرایط فیزیولوژیک بدن، میکروپارتیکلها از پلاکتهای فعال شده جوانه میزنند. PMPها در مواردی که نشاندهنده بیماری هستند، مارکرهای اختصاصی سطح غشایی آنها مانند فسفاتیدیل سرین دچار تغییرات بعد از ترجمه مانند سیترولیناسیون میشوند(2). PMPفراوانترین(90-70 درصد) میکروپارتیکلهای خون است که از پلاکتهای ذخیره شده در بانک خون نیز آزاد میشود(3). روشهای متعددی برای تشخیص و بررسی خصوصیات میکروپارتیکلها وجود دارد که فلوسیتومتری Gold standard آنها است(4). سلولها در پاسخ به فعالسازی، وزیکولهای غشای پلاسمایی را آزاد میکنند. اگرچه میکروپارتیکل در خون افراد سالم وجود دارد اما بالا رفتن سطح آن با اختلالاتی از جمله سرطان، آترواسکلروز و غیره همراه میشود(3). سیستمهای دارو رسانی(Drug Delivery System) شامل تکنولوژی و سیستمهایی است که بر پایه نانوذرات استوار است و میتواند ترکیبات دارویی را در بدن حمل کند(5). امروزه استفاده از این پارتیکلها میتواند محدودیتهای استفاده از روشهای پیشین دارو رسانی مانند توزیع و هدفگذاری غیر اختصاصی دارو را حل کند. نانو پارتیکلها قادر هستند مدت زمان بیشتری در خون بمانند و محتویات خود را در اختیار سلولهای توموری قرار دهند. یکی از عوامل مهم که میتواند باعث مقاومت دارویی شود، شناسایی ذرههای دارویی توسط گلیکو پروتئینهای p است. این عامل وقتی از پارتیکلهای سازگار با بدن استفاده شود، میتواند به حداقل برسد. در نهایت میتواند در برداشتن گامی جدید در درمان انواع بیماریها و سرطانها به صورت درمان دارویی شخص محور بسیار حائز اهمیت باشد(6). دوکسوروبیسین از داروهای شیمی درمانی موجود برای درمان بسیاری از سرطانها است. این دارو در خانواده آنتیبیوتیکی آنتراسایکلین قرار میگیرد و در حال حاضر برای دستهای از بیماریهای نئوپلاستیک توسط سازمان غذا و داروی آمریکا تائید شده است. این دارو که حالت محلول آن دوکسوروبیسین هیدروکلراید نامیده میشود، به دلیل وجود گروه کروموفور آنتراسیکلین مرکزی، دارای خاصیت فلوئورسنت بوده و میتوان با روشهای تصویربرداری فلوئورسنت آنها را در بافتها ردیابی کرد(8، 7).
پپتیدهای نفوذکننده به سلول CPP (Cell Penetrating Peptides) پپتیدهایی به شدت کاتیونیک هستند و غالباً غنی از آمینواسیدهای لیزین و آرژنین میباشند و خیلی سریع به هر سلولی نفوذ میکنند. انواع مختلفی از این پپتیدها وجود دارد که در 5 کلاس دستهبندی میشوند. از شایعترین آنها کلاس کاتیونیک است(10، 9).
مواد و روشها
نوع این مطالعه تجربی بوده و نمونه های کنستانتره پلاکتی به صورت تصادفی از اهداکنندگان انتخاب و پس از 5 روز قرار گرفتن بر روی انکوباتور شیکر در دمای 20 الی 24 درجه سانتیگراد، از سازمان انتقال خون ایران دریافت شدند.
تهیه میکروپارتیکلهای پلاکتی:
کیسههای کنستانتره پلاکتی در روز پنجم پس از خونگیری از اهداکننده، برای جداسازی میکروپارتیکلها استفاده شد. میکروپارتیکلهای پلاکتی در روز 3 تا 5 نگهداری کیسههای کنستانتره پلاکتی به مقدار زیادی در کیسهها تجمع پیدا میکنند. محتویات کیسههای کنستانتره پلاکتی در زیر هود کلاس دو و تحت شرایط استریل به درون لولههای فالکون منتقل شدند و جهت رسوب و جداسازی پلاکتها و گلبولهای قرمز و سفید، لولههای فالکون به مدت 15 دقیقه در دور g 1200 و طی دو مرحله در دمای محیط سانتریفیوژ(مدل اپندورف) شدند. سپس سوپرناتانت به لولههای مخصوص اولتراسانتریفیوژ منتقل و در دور g16000 طی سه مرحله در دمای یخچال (10 درجه سانتیگراد) سانتریفیوژ شد که بین هر مرحله میکروپارتیکلهای رسوب شده با بافر PBS (Phosphate Buffer Saline) استریل شسته شدند. رسوب نهایی در PBS حل شده و جهت تعیین غلظت، ویژگی، سایز، مواجهه با دارو و سلول در فریزر 70- درجه سانتیگراد نگهداری شدند.
تعیین غلظت میکروپارتیکلها با استفاده از روش برادفورد:
اتصال پروتئین به رنگ کوماسی، فرم آبی رنگ را تثبیت و منجر به تغییر رنگ متناسب با میزان پروتئین میشود.
برای خوانش میزان جذب نوری رنگها در روش برادفورد، از طول موج nm595 استفاده میشود. برای مواجهه مؤثر و مطلوب میکروپارتیکلها با داروها و ردههای سلولی، تعیین غلظت میکروپارتیکلها انجام شد. برای تعیین غلظت از استانداردهای با غلظت مشخص BSA(Bovine serum albumin) استفاده گردید. غلظتهای µg/mL1500، µg/mL 750 ،µg/mL 375 ،µg/mL 5/187 ، µg/mL 75/93 ، µg/mL 87/46 ، µg/mL 43/23 و µg/mL 71/11 از BSA تهیه شد. 200میکرولیتر از معرف برادفورد در چاهکها ریخته شد و متعاقب آن 10 میکرولیتر از رقتهای استاندارد تهیه شده و میکروپارتیکلهای جدا شده به چاهکها اضافه شد.
تعیین سایز میکروپارتیکلها با استفاده از میکروبیدهای کونژوگه با فلوئورسنت:
برای این آزمایش از میکروبیدهای فلوئورسنت (برند molecular probes، کشور آمریکا) با اندازه 1 میکرومتر استفاده شد. به نمونههای میکروپارتیکل با غلظت µg/ml 100 ، 5 میکرولیتر از محلول 500 بار رقیق شده میکروبیدهای فلوئورسنت اضافه شد و سپس این نمونهها جهت بررسی اندازه با استفاده از دستگاه فلوسیتومتری (partec CyFlow) استفاده شد.
تعیین منشاء و خصوصیات میکروپارتیکلهای پلاکتی:
برای تایید منشا میکروپارتیکلها از مارکرهای سطحی و اختصاصی پلاکتها استفاده گردید. CD41 (از شرکت بیولژند کشور آمریکا و کونژوگه به ماده فلوئورسنت FITC) و CD61 (از شرکت داکو کشور دانمارک و کونژوگه به ماده فلوئورسنت FITC)، یکی از بهترین گزینههاست. برای این کار غلظت میکروپارتیکلها را به µg/mL100 رسانده و 3 میکرولیتر از آنتیبادی ضد CD41 وCD61 کونژوگه شده با فلوئورسنت به آن اضافه شد و نیم ساعت در یخچال انکوباسیون انجام شد. سپس با استفاده از دستگاه فلوسیتومتری تایید منشا انجام گرفت. برای اطمینان و کنترل این که آنتیبادی استفاده شده به صورت اختصاصی به مارکر سطحی چسبیده است و چسبندگی غیر اختصاصی با ناحیهFC مارکر نداشته، از isotype control استفاده شد.
بارگذاری داروی دوکسوروبیسین در میکروپارتیکل پلاکتی:
دوکسوروبیسین برند Tocris از کشور انگلستان خریداری شد و غلظتهای مختلف میکروپارتیکل (µg/mL 50 ، µg/mL 100 ، µg/mL 150 ، µg/mL 200 و µg/mL 250 ) با غلظتهای مختلف دوکسوروبیسین (µg/mL 20 ، µg/mL 10، µg/mL 5 ، µg/mL 1) با روشهای مختلف به شرح زیر با هم مواجه شدند. در این مرحله غلظت بهینه شده برای مواجهه دارو با میکروپارتیکل مشخص گردید که در هر سه روش ثابت بوده و در ادامه توضیحات هرروش ذکر شده است.
بارگذاری دارو با روش انکوباسیون:
استفاده از این روش از رایجترین روشهای مورد استفاده برای بارگذاری دارو بر روی پارتیکلها و ذرات مختلف میباشد. میکروپارتیکلهای پلاکتی با غلظت µg/mL 150 با دوکسوروبیسین با غلظت µg/mL 10 به مدت 2 ساعت در 37 درجه سانتیگراد و در تاریکی و با دور rpm 100 انکوبه شدند. سپس نمونهها با دور g 16000 و به مدت 15 دقیقه در 10 درجه سانتیگراد سانتریفیوژ شدند و مایع رویی خارج شد و با PBS شستشو شد. پلت نهایی برای بررسی فلوسیتومتری جمعآوری شد.
بارگذاری دارو با روش CPP :
محلول CPP
برای ساخت پلیمر آرژنین حاوی مولکولهای داروی
دوکسوروبیسین، 30 میلیگرم آرژنین که وزن مولکولی 2/174 داشت را در 6 میلیلیتر PBS حل کرده و مقدار 5 میکرولیتر گلوتارآلدئید به آن اضافه کرده و 5/1 ساعت در تاریکی با هم مخلوط شدند و بعد در کیسههای دیالیز 3000 دالتون دیالیز گردیدند و محیط آن دو بار تعویض شد که مونومرهای موجود در کیسه دیالیز خارج شود و تنها پلیمرهای آرژنین باقی ماندند. در ادامه، 25 میکرولیتر از محلول داروی دوکسوروبیسین با غلظت µg/mL500 را اضافه کرده و سپس مقدار 2 میلیگرم از پودر گلایسین اضافه شده و انکوباسیون، دیالیز انجام گردید.
میکروپارتیکلهای پلاکتی با غلظت µg/mL 150 با داروی کونژوگه شده به CPP به مدت 2 ساعت در 37 درجه سانتیگراد و در تاریکی و با دور rpm 100 مواجه شدند. سپس نمونهها با دور g 16000 و به مدت 15 دقیقه سانتریفیوژ شدند و مایع رویی خارج شد و PBS ریخته و یک بار با همان شرایط ذکر شده شستشو و سانتریفیوژ انجام شد. پلت نهایی برای بررسی فلوسیتومتری جمع آوری گردید.
بارگذاری دارو با روش سونیکاسیون :
میکروپارتیکلهای پلاکتی با غلظت µg/mL 150 با دوکسوروبیسین با غلظت µg/mL 10، 6 چرخه 20% آمپلیتیود که هر چرخه 3 دقیقه (30 ثانیه روشن/30 ثانیه خاموش) طول میکشد، سونیکه شدند و بین هر چرخه 2 دقیقه زمان کولینگ در نظر گرفته شد و پس از آن نمونه سونیکه شده 1 ساعت در 37 درجه سانتیگراد انکوبه شد. در ادامه نمونهها با دور g 16000 و به مدت 15 دقیقه سانتریفیوژ شدند و مایع رویی خارج شد و PBS ریخته و یک بار با همان شرایط ذکر شده شستشو و سانتریفیوژ شد. پلـت نهایـی بـرای بـررسی فلـوسیتومتری جمعآوری شد.
نحوه جمعآوری و تجزیه و تحلیل دادهها:
تمامی آزمایشها حداقل 3 بار تکرار شده و نتایج حاصل از بررسیهای اصلی پروژه شامل فلوسیتومتری بـرای ثبت میزان نور فلوئورسنت ساطع شده، جمعآوری و
به صورت میانگین ± انحراف معیار گزارش شدند.
تحلیل آماری با استفاده از نرمافزار SPSS26 انجام شد و طبیعی بودن توزیع متغیرها با استفاده از آزمون کلموگروف - اسمیرنوف محاسبه شد. جهت تحلیل و مقایسه میانگین دادهها در بیشتر از دو گروه از آزمونOne Way Anova و Tukey Post Hoc Test استفاده شد. ضمناً 05/0 p≤ معنادار در نظر گرفته شد.
یافتهها
نمودار استاندارد از خواندن جذب نوری رقتهای مختلف BSA تهیه شده و در ادامه با استفاده از این نمودار، غلظت میکروپارتیکلهای جدا شده بر حسب میکروگرم در هر میلیلیتر محاسبه شد. غلظت میکروپارتیکلهای پلاکتی که از 7 کیسه کنستانتره پلاکتی جدا شده بود،µg/mL 1800،µg/mL 1500، µg/mL700، µg/mL3000، µg/mL 2500، µg/mL1000 وµg/mL 4500 تعیین شد (نمودار 1).
در ادامه برای تعیین سایز میکروپارتیکلها با استفاده از میکروبیدهای کونژوگه با فلوئورسنت، قسمت R1 ، میکروپارتیکلهای به دست آمده از کنسانتره پلاکتی میباشد که 95% کل جمعیت میکروپارتیکلها از لحاظ سایز از میکروبیدهای فلوئورسنت که در قسمت R1 مشخص شده است، کوچکتر است و در محدوده پایینتر از یک میکرومتر قرار گرفته است(نمودار 2). در این مطالعه از کل جمعیت میکروپارتیکل پلاکتی استفاده شده و اقدام به جداسازی اندازه خاصی از آنها نشد.
در ادامه، میکروپارتیکلهای پلاکتی با آنتیبادی ضد CD41 و CD61 تیمار شدند. در مقایسه با آنتیبادی ایزوتایپ کنترل، 39/92% و 03/80% از آنها به ترتیب دارای این آنتیژن پلاکتی بودند. در نمودار 3 قسمت A ، R1 نشاندهنده جمعیت میکروپارتیکلهای پلاکتی بوده و شکل C و D به ترتیب نشاندهنده جمعیت میکروپارتیکلهای پلاکتی رنگ شده با Anti CD41 وAnti CD61 میباشد که با ماده فلوئورسنت FITC کونژوگه شدهاند.
در روش انکوباسیـون برای بـررسی میـزان بـارگـذاری داروی دوکسـوروبیسیــن در میکـروپـــارتیکـلهــای در پلاکتی، 5 بـار مـواجهه در دوزهای مختلف صورت گرفت
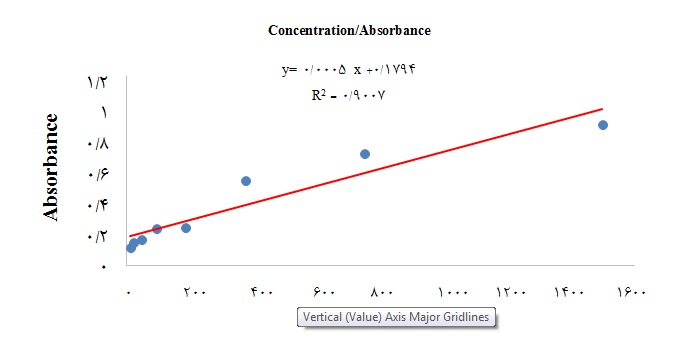 نمودار 1: نمودار استاندارد رقتهای محلول BSA  نمودار 2 : محدوده R1 میکروبیدهای فلوئورسنت را نشان میدهد و محدوده R2 میکروپارتیکلهایی که از نظر سایز زیر یک میکرومتر هستند نشان داده شده است.  نمودار 3 : تعیین منشاء میکروپارتیکلهای پلاکتی با فلوسیتومتری. شکل A نشاندهنده گیت جمعیت میباشد، شکل B نمونه ایزوتایپ کنترل را نشان میدهد و شکل C میکروپارتیکلهای پلاکتی که با آنتی CD41 همراه است، شکل D میکروپارتیکلهای پلاکتی که با آنتی CD61 همراه است و محدوده مثبت مشخص نموده است.  نمودار 4 : میزان بارگذاری دارو در روش انکوباسیون. قسمت A نشاندهنده گیت جمعیتی و B نشاندهنده میزان نور فلوئورسنت ساطع شده (63/86%) داروی بارگذاری شده با روش انکوباسیون در یکی از نمونههای میکروپارتیکل پلاکتی میباشد.  نمودار 5 : میزان بارگذاری دارو در روش سونیکاسیون. قسمت A: نشاندهنده گیت جمعیتی و شکل B نشاندهنده میزان نور فلوئورسنت ساطع شده(03/62%) داروی بارگذاری شده با روش سونیکاسیون در یکی از نمونههای میکروپارتیکل پلاکتی میباشد. |
که میزان نور فلوئورسنت در مقایسه با نمونه میکروپارتیکلی که هیچ دارویی نداشته، سنجیده شد که میانگین نتایج 37/11 ± 09/79 بود. نور فلوئورسنت ساطع شده در یکی از نمونههای مورد مطالعه در شکل نشان داده شده(نمودارهای 4، 5 و 6). در روش سونیکاسیون برای بررسی میزان بارگذاری داروی دوکسوروبیسین در میکروپارتیکلهای پلاکتی، 5 بار مواجهه در دوزهای مختلف صورت گرفت که میزان نور فلوئورسنت در مقایسه با نمونه میکروپارتیکلی که هیچ دارویی نداشته، سنجیده شد و میانگین نتایج 12/25 ± 48/47 بود. در روش CPP ، برای بررسی میزان بارگذاری داروی دوکسوروبیسین در میکروپارتیکلهای پلاکتی، 5 بار مواجهه در دوزهای مختلف صورت گرفت و میزان نور فلوئورسنت در مقایسه با نمونه میکروپارتیکلی که هیچ دارویی نداشته، سنجیده شد و میانگین نتایج 24/23 ± 69/56 بود.
میانگین داروی بارگذاری شده در سه روش گفته شده به صورت نمایش داده شده در نمودار زیر میباشد(نمودار 7). به ترتیب بالاترین میزان داروی بارگذاری شده در روش انکوباسیون، سپس CPP و در نهایت روش سونیکاسیون است.
میانگین داروی بارگذاری شده در سه روش گفته شده به صورت نمایش داده شده در نمودار زیر میباشد(نمودار 7). به ترتیب بالاترین میزان داروی بارگذاری شده در روش انکوباسیون، سپس CPP و در نهایت روش سونیکاسیون است.

نمودار 6 : میزان بارگذاری دارو در روش CPPقسمت A نشاندهنده گیت جمعیتی و قسمت B نشاندهنده میزان نور فلوئورسنت ساطع شده (97/85%) داروی بارگذاری شده با روش CPP در یکی از نمونههای میکروپارتیکل پلاکتی میباشد.

نمودار 7: مقایسه روشهای لود دارو در میکروپارتیکلهای پلاکتی نشاندهنده مؤثرتر بودن روش انکوباسیون در مقایسه با دو روش سونیکاسیون و CPP میباشد.
بحث
شباهت ساختاری و عملکردی میکروپارتیکلهای مشتق از سلول از قبیل میکروپارتیکلهای پلاکتی با نانو ساختارهای سنتتیک و پلیمری که در دارو رسانی استفاده میشوند، این ایده را ایجاد کرد که بتوان از این میکروپارتیکلها برای دارو رسانی در بیماریهای مختلف مانند سرطان و عفونتهای ویروسی استفاده نمود. طبیعی بودن منشاء ایـن میکـروپارتیکلها میتواند بسیاری از اثرات جانبی و سمیتهای سیستمهای دارو رسانی سنتتیک و پلیمـری را بـرطرف کنـد. ایـن مطالعـه جهـت بــررسی
کاربرد استفاده از میکروپارتیکلهای پلاکتی به عنوان حامل داروی دوکسوروبیسین با روشهای مختلف بارگذاری شامل: انکوباسیون، سونیکاسیون و CPP انجام گردید. با توجه به نتایج به دست آمده از فلوسیتومتری، میزان شدت نور فلوئورسنت داروی دوکسوروبیسین در روشهای انکوباسیون، سونیکاسیون و CPP به ترتیب 37/11 ± 09/79 درصد، 12/25 ± 48/47 درصد و 23/24 ± 69/56 درصد گزارش شدند.
برای مقایسه این 3 روش مختلف لود دارو با استفاده از آزمایـش آمـاری Anova مـیتوان گفـت، به طور کلی میان
روشهای مختلف انجام شده اختلاف معناداری وجود دارد(005/0 p≤). استفاده از روش انکوباسیون برای لود دارو به دلیل بالاتر بودن درصد میانگین به دست آمده از فلوسیتومتری، میتواند روش مؤثرتری باشد.
نتایج حاصل از مطالعههایی که در آن از ذرههای پلاکتی به عنوان حامل داروی دوکسوروبیسین استفاده شده است نشان داده که استفاده از پلاکت به عنوان حامل این دارو توانایی توکسیسیتی بالاتر برای بافت و سلولهای سرطانی و در عین حال کاردیوتوکسیسیتی کمتر برای بیماران را دارد(13-11). مطالعههایی نیز از پلاکت به عنوان حامل دارو استفاده کردند که برای اختصاصی تر شدن تحویل دارو به سلولهای سرطانی و بافت هدف، پلاکتها را با آنتیبادی ضد CD22 کونژوگه نمودند(14). در مطالعههای جدیدی که انجام شده، میکروپارتیکلهای پلاکتی به عنوان فاکتور مهم در بازسازی کبد استفاده شده که میکروپارتیکلهای پلاکتی با تنظیم مسیر اتوفاژی و افزایش تکثیر سلولهای هپاتوسیت، در این مسیر نقش خود را ایفا میکنند(15). در مطالعههای دیگری که اخیراً انجام داده شده، برای کنترل عوارض انفارکتوس حاد میوکاردی که در آن اینترلوکین-1ß نقش اصلی را در آسیب و مرگ سلولهای میوکاردی دارد، از میکروپارتیکلهای پلاکتی همراه با آنتی بادی ضد IL-1ß استفاده کردند و نشان دادند که این میکروپارتیکلها میتوانند عامل مهمی در سمزدایی و ترمیم سلولی در زمان انفارکتوس حاد میوکاردی باشند(16). در این مطالعه برای اولین بار مقایسه روشهای مختلف لود دارو در میکروپارتیکلهای پلاکتی به منظور یافتن روش مؤثرتر برای بارگذاری دارو، انجام شد. در مطالعههای پیشین بیشتر مواقع از روش انکوباسیون برای لود دارو استفاده شده است و مواردی نیز گزارش شده که
از سایر روشهای لودینگ مانند استفاده از پلیاتیلن گلیکول، الکتروپوریشن و غیره برای لود دارو بر روی میکروپارتیکلها استفاده شده است(18، 17). نتایج مطالعههای انجام شده در این مقاله در مقایسه با روشی که از پلاکت به عنوان حامل و از روش انکوباسیون برای بارگذاری دارو استفاده شده بود، در یک راستا قرار داشتند(19، 14، 11). اگر چه در مطالعهای که از میکروپارتیکلهای پلاکتی به عنوان حامل داروهای ضد ویروسی HIV-1 استفاده شد، روش سونیکاسیون در بارگذاری آن داروها دارای اثرگذاری بالاتری بوده است(20). در توجیه این اختلاف میتوان بیان کرد که با توجه به این که از سل لاینها و داروهای متفاوت استفاده شده است، میزان لود شدن دارو در میکروپارتیکلها میتواند متفاوت باشد.
نتیجهگیری
در نهایت مطالعه صورت گرفته نشان میدهد که استفاده از روش انکوباسیون میتواند روش مؤثرتری برای لود داروی دوکسوروبیسین در میکروپارتیکلهای پلاکتی باشد. پیشنهاد میشود که استفاده از این روش در مطالعههای بالینی و آزمایشگاهی بر روی سایر داروها با همراهی با میکروپارتیکلهای پلاکتی جهت اثرگذاری بیشتر، مورد بررسی قرار گیرند.
تشکر و قدردانی
این مقاله حاصل از پایاننامه ارشد کارشناسی ارشد آرزو دربندی با کد اخلاق IR.timi.rec.1397.036 میباشد که در مرکز تحقیقات انتقال خون، مؤسسه عالی آموزشی و پژوهشی طب انتقال خون و با حمایت مالی این مؤسسه انجام شده است.
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |






