جلد 15، شماره 4 - ( زمستان 1397 )
جلد 15 شماره 4 صفحات 286-272 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Shamsi M, Salimi A, Ghallasi M, Halabian R. Effect of synthetic biologically activated 45S5 glass nanoparticles on osteogenesis differentiation of mesenchymal human bone marrow. bloodj 2018; 15 (4) :272-286
URL: http://bloodjournal.ir/article-1-1209-fa.html
URL: http://bloodjournal.ir/article-1-1209-fa.html
شمس مهدی، سلیمی علی، قلاسی مرضیه، حلبیان راحله. اثرات نانو ذرات شیشه زیست فعال 45S5 سنتزی بر رشد و تمایز سلولهای بنیادی مزانشیمی مغز استخوان انسان به بافت استخوانی در محیط برون تن. فصلنامه پژوهشی خون. 1397; 15 (4) :272-286
مهدی شمس 
 ، علی سلیمی
، علی سلیمی 

 ، مرضیه قلاسی
، مرضیه قلاسی 
 ، راحله حلبیان*
، راحله حلبیان* 



 ، علی سلیمی
، علی سلیمی 

 ، مرضیه قلاسی
، مرضیه قلاسی 
 ، راحله حلبیان*
، راحله حلبیان* 


استادیار مرکز تحقیقات میکروب شناسی کاربردی ـ مؤسسه زیست شناسی و انستیتو مسمومیت ها ـ دانشگاه علوم پزشکی بقیهاله (عج)
متن کامل [PDF 929 kb]
(2592 دریافت)
| چکیده (HTML) (4456 مشاهده)
مقدمه
برای ترمیم ضایعات و نقـایص اسـتخوانی مـیتـوان از امکانات مهندسی بافت بهره برد. در این ارتباط، بـا طراحـی داربست مناسب و گذاشتن سلولهای دارای پتانسیل تولیـد استخوان بر روی این داربستها و سپس پیوند در محل ضایعه، میتوان قابلیت ترمیم ضایعه را افزایش داد(1). سـرامیکهـای فسفات کلسیمی(از قبیل: شیشه و شیشه- سرامیکهـا) به علت این که سـاختاری مشـابه بـا بخـش غیر آلی ترکیب استخوان دارند، به عنوان داربسـت سـلولی مورد استفاده قرار گرفتهاند. این شیشهها در برابر محلول شبیهسازی شده بدن تشکیل هیدروکسی کربنات آپاتیت میدهند و در بسیاری از موارد بالینی که نیاز به تولید و ترمیم استخوان است، میتوانند کاربرد داشته باشند(3، 2). شیشههـای زیـستی هنگامی که در بدن قرار میگیرند، به راحتی با سیالهای فیزیولوژیکی واکنش داده و تشکیل یک پیونـد قـوی بـا بافـتهـای نـرم و سخت در حین فعالیت سلولی میدهند(4). اولین ترکیبی که بیشترین مطالعهها بر روی آن انجام شده است، شیشه 5S45 ساخته شده بـه روش ذوبـی میباشد که ترکیب آن بر حسب درصد وزنی اجزا شامل: 45 درصد اکسید سیلسیم، 5/24 درصد اکسید سدیم، 4/24 درصد اکسید کلسیم و 6 درصد پنتوکسید فسفر است(5). شیشههای زیست فعال را میتوان به دو روش ذوبی و سل ژل تهیه نمود(7، 6). ساخت شیشه 5S45 در مقیاس نانو بسیار دشوار است، استفاده از روش سل- ژل نیز برای ساخت این نوع شیشه، به دلیل وجود سدیم در ترکیب خود، امکانپذیر نیست چراکه سدیم باعث سمیت و مرگ سلولی می شود. بنابراین روش ذوبی برای ساخت این نوع نانوذره بهترین گزینه است، لازم به ذکر است روش ساخت ذوبی، باعث تولید ذرات با ساختار میکرو میشود.
سـلولهـای بنیـادی مزانشـیمال سلولهـای بنیـادی چنـد قوهای بـوده که دارای قدرت تکثیر و خود نوسازی بالا و هم چنین پتانسیل تمـایز بــه ردههــای مختلــف ســلولی از جملــه ســلولهــای استئوبلاست، هندروسیـت، آدیپوسـیت، سلولهای اندوتلیال، سلولهای
عصبی، سلولهای میوسـیت قلبـی، سـلولهـای هپاتوسیت و سلولهای پانکراس میباشند(11-8).
کارآیی این سلولها در درمان بیماری ژنتیکی استئوژنزیس امپرفکتا(Osteogensis Imperfecta)، بهبود خونسازی در بیماران سرطانی تحت درمان، بازسازی استخوان، ترمیم بافت نکروز شده در بیماران انفارکتوس قلبی و درمان بیماریهای مفصلی به خوبی نشان داده شده است (13، 12). سه منبع اصلی برای جداسازی ســلولهــای بنیــادی مزانشـیمی، برای مطالعهها و درمان بیماریها وجود دارد که میتوان به مغز استخوان، بند ناف و بافت چربی اشاره کرد. سلولهای بنیادی مشتق شده از مغز استخوان انسان مشابه مورفولوژی و فنوتیپ حاصل از بافت چربی هستند(15، 14).
محیط کشت مورد استفاده نیز عامل مهمی در توانایی تمایز استئوژنیک است. استفاده از محیطهای پایه از قبیل؛ DMEM+ Low DMEM+ High, DMEM+ F, و افزودن فاکتورهای رشد فیبروبلاست، دگزامتازون، اسید اسکوربیک و گلیسرول فسفات به محیط پایه از عواملی هستند که تاثیر به سزایی در تمایز استخوانی دارند(18-16، 14).
از موارد دیگری که بر تمایز سلولهای بنیادی مزانشیمی تاثیر دارد؛ اتصال سلول به ماتریکس(داربست) خارج سلولی است. این ماتریکس(داربست) از مواد آلی و غیر آلی از قبیل کلاژن I و نمکهای کلسیم به فرم شیشه زیست فعال، هیدروکسی آپاتیت، نمکهای فلورید، فسفات و سیترات تشکیل یافته است(20، 19).
در تحقیقات صورت گرفته، شیشه زیست فعال را معمولاً به عنوان فاز دوم(تقویتکننده زیست فعال) در ساخت کامپوزیتها و داربستها استفاده کردهاند که تمامی این مطالعهها، شیشه 5S45 را با ساختار میکرو مورد بررسی قرار دادهاند(27-21). علاوه بر آن پژوهشی در زمینه تاثیر اندازه ذرات شیشه فوقالذکر با اندازه ذره 9-750 میکرومتر در رشد، تکثیر و تمایز سلولهای بنیادی مورد بررسی قرار گرفته است. نتایج آن ثابت کرد که هرچه اندازه ذرات ریزتر باشد، تاثیر به سزایی در رشد و تمایز سلولها خواهد داشت(28).
با توجه به مباحث شرح داده شده در مقدمه و اهمیت
نانو مواد در تمایز سلولهای بنیادی، هدف از این پژوهش، سنتز نانوذرات شیشه زیست فعال5S45 و بررسی خواص زیست فعالی و تاثیر آن در تکثیر و تمایز سلولهای بنیادی مزانشیمی مغز استخوان انسان به سلولهای استخوانی در محیط برون تن بود. بـا وجـود آن کـه گزارشهایی مبنی بر ساخت شیشههای زیست فعال 5S45 و بررسی سلولی آن گزارش شده است، اما تاکنون گزارشـی در مـورد ساخت شیشــه زیســت فعــال با این ترکیب و با استفاده از فرآیند آسیاب سیارهای برای ساخت این شیشه در مقیاس نانو و بررسی تکتیر و تمایز سلولهای بنیادی مزانشیمی بیان نشده است. بنابراین ما در این پژوهش سعی در ساخت نانو ذره شیشه فوق با استفاده از آسیاب سیاره کردیم و با چندین مرتبه آسیاب و انجام آزمایشهای متعدد، اندازه ذرات را به مقیاس نانو رساندیم.
نتایج آزمایشها ثابت کرد که با استفاده از آسیاب سیارهای میتوان ساختار نانویی این نوع شیشه را تولید کرد. استفاده از این نوع نانوذرات شیشه به واسطه افزایش نسبت سطح به حجم و یون های زیست فعال، سبب واکنشپذیری بهتر این نوع فاز در تکثیر و تمایز سلولها خواهد شد. از مزیتها و کاربرد نانوذرات تولید شده، میتوان به حل مشکلات کار با داربست و استفاده آن در ارتوپدیها و بیمارستانها جهت بهبود درمان ضایعات استخوانی اشاره کرد.
مواد و روشها
ساخـت و مشخصهیابـی نانو ذرات شیشـه زیست فعال 5S 45:
در این پژوهش تجربی، شیشه زیست فعال به روش ذوبی ساخت و مشخصهیابی شد. برای ساخت شیشه زیست فعال 5S45 ، 07/22 گرم SiO2 و 88/5 گرم P2O5، 45/21 گرم CaCO3 (مرک، آلمان) و در نهایت 6/20 گرم NaCO3 (مرک، آلمان) با هم ترکیب و سپس توسط هاون عقیق، آسیاب گردید. در ادامه با استفاده از ظرف پلیاتیلنی دربدار با چند عدد گلوله پلیاتیلنی مجدداً مخلوط کردن مواد کاملتر انجام شد. مواد فوق با استفاده از دستگاه پرس(تأسیسات صارم ـ ایران ـ T-35) به شکل قرصهای دایرهای با قطر10 میلیمتر، پرس گردید. قرصهای حاصل درون کوره(F11L ، آذرفورناس، ایران) قرار داده شد. تغییرات دمایی کوره بدین صورت تنظیم گردید که ابتدا افزایش دما تا 900 درجه سانتیگراد با سرعت 10 درجه در دقیقه و ماندن در دمای فوق به مدت 5/2 ساعت و مجدداً افزایش دما از 900 به 1400 درجه سانتیگراد با نرخ 10 درجه در دقیقه و قرار دادن در دمای 1400 درجه سانتیگراد به مدت 3 ساعت. در نهایت پس از عملیات مذاب، مواد ذوب شده حاصل از کوره خارج و درون آب مقطر کوینچ شد. شیشه حاصل سپس با استفاده از آون(مرک، آلمان) در دمای 80 درجه سانتیگراد به مدت 5 ساعت خشک گردید. در نهایت با استفاده از آسیاب سیارهای با کاپ زیرکونیا(Petch PM400، آلمان) به مدت 6 ساعت آسیاب گردید. مجدداً، شیشه زیست فعال طی چند مرحله و در مجموع به مدت 60 ساعت، آسیاب شد تا به ساختار نانو تبدیل گردد.
ارزیابی زیست فعالی:
برای ارزیابی زیست فعالی، از مایع شبیهسازی شده بدن طبق دستورالعمل کوکوبو(KoKubo) بهره گرفته شد. در این آزمایش نانوذرات شیشه زیست فعال در بازههای زمانی7 و14 روز به صورت مجزا در 10 میلیلیتر مایع شبیهسازی شده بدن غوطه ور و در دمای 37 درجه سانتیگراد درون انکوباتور(INC 108 ، ممرت، آلمان)، قرار داده شد. پس از آن محلول مایع شبیهسازی شده بدن، خارج و نمکها و سایر اضافات چسبیده به نمونهها، با آب مقطر شستشو داده و خشک گردید.
طیف سنجی مادون قرمز:
برای شناسایی پیوندها و گروههای شیمیایی نانو ذرات شیشه قبل و بعد از غوطهوری در مایع شبیهسازی شده بدن، از آزمون طیفسنجی مادون قرمز(FTIR)(Spectrum 400 ، پرکین المر، آمریکا) در محدوده 400-400 بر سانتیمتر در حالت عبوری استفاده شد.
میکروسکوپ الکترونی روبشی:
به منظور مطالعه مورفولوژی نانوذرات شیشه قبل و بعد از غوطهوری در مایع شبیهسازی شده بدن، از میکروسکوب الکترونی روبشی (SEM)(کره، SEM South، سرون تکنولوژی) با ولتاژ 20 کیلوولت، استفاده شد. به علت هدایت الکتریکی ضعیف نمونهها، سطح مقطع آنها قبل از انجام آزمایش، با لایهای بسیار نازک از طلا به روش کندوپاش پوشانده شد.
ارزیابی رشد و تکثیر سلولهای بنیادی مزانشیمی:
جهت بررسی قابلیت رشد و تکثیر سلولهای بنیادی مزانشیمی، سلولها را در فلاسک کشت سلول 75 ریخته و با استفاده از 12 میلیلیتر محیط کشت با گلوکز بالا(DMEM-High G) به همراه 5 درصد محلول سرم جنین گاوی(FBS) و آنتیبیوتیک(پنیسیلین و استرپتوماسین)(جیبکو، آلمان) 1 درصد کشت داده شد. سپس فلاسک به درون انکوباتور(GmibH, MMM-Group، آلمان) با گاز 5 درصد CO2 در دمای 37 درجه سانتیگراد به همراه رطوبت منتقل گردید. هر 2 روز یک بار، محیط کشت تعویض گردید. طی 6 روز که سلولها رشد پیدا کرده و به تراکم 90 درصد رسیده بودند، پاساژ داده شدند. مراحل انجام پاساژ بدین صورت بود که ابتدا سلولها را درون فلاسک با محلول بافر فسفات سالین(PBS) شستشو داده و سپس با محلول تریپسین/ EDTA (جیبکو، آلمان) 2/0 درصد از کف فلاسک جدا شدند.
در ادامه پس از جدا شدن سلولها از کف فلاسک و معلق شدن، مقدار 3 میلیلیتر محیط کشت به منظور خنثی کردن اثر تریپسین به فلاسک اضافه گردید. سپس سوسپانسیون سلولهـا را بـه داخـل فالکـون 15 انتقـال و سانتریفیوژ (2-16PK ، سیگما، آلمان) با 1200 دور در دقیقه به مدت 5 دقیقه در دمای محیط انجام شد. پس از سانتریفیوژ، محلول رویی خالی و مجدداً 4 میلیلیتر محیط کشت درون فالکون افزوده و به منظور جدا شدن و معلق شدن سلولها، چندین بار پیپت انجام شد. سپس به داخل فلاسک کشت سلول انتقال داده شد.
برای انجام آزمایشهای سلولی باید نمونهها استریل باشند. از این جهت، نمونهها در زیر هود کشت سلولی ((ایران، Jal tajhiz Production ، JTLV C2) با محلول فسفات بافر سالین(PBS) شستشو و به مدت ۲۰ دقیقه تحت اشعه فرابنفش قرار گرفت.
در ادامه آن سلولهای بنیادی مزانشیمی شمارش و بر روی نمونههای درون چاهکها انتقال داده شد. برای شمارش از لام نئوبار استفاده شد. نمونه کنترل نیز استفاده گردید از این جهت سلولها در کف پلیت کشت سلولی، کشت داده شدند.
بـررسی سمیـت سلولی با استفاده از آزمایش سنجش MTT :
برای انجام آزمونMTT حدود 104× 3 هزار سلول به هر چاهک در پلیت 24 خانهای حاوی نمونههای استریل شده انتقال داده شده و 300 میکرولیتر محیط کشت به هر چاهک اضافه گردید. این آزمون در فواصل زمانی 1، 3 ،5 و 7 روز در حضور نانو ذرات شیشه زیست فعال بررسی گردید و محیط کشت هر 2 روز یک بار تعویض شد. در این آزمایش پس از اتمام هر دوره، محیط رویی سلولها خارج و با فسفات بافر سالین شتسشو داده و به مقدار 200 میکرولیتر محیط کشت با گلوکز بالا (DMEM-High G) حاوی20 میکرولیتر محلول MTT (آمریکا، سیگما، آلدریچ) اضافه گردید. سپس سلولها، به مدت 4 ساعت درون انکوباتور 37 درجه سانتیگراد و رطوبت 98 درصد و میزان رطوبت 5 درصد گاز 2 COدر تاریکی قرار داده شدند.
س از 4 ساعت انکوباسیون، مجدداً محیط رویی، خارج و میزان 100 میکرولیتر دی متیل سولفوکساید (DMSO)(آمریکا، سیگما، آلدریچ) اضافه گردید تا کریستالهای فورمازان حل شده و یک محلول بنفش رنگ به دست آید. در نهایت میزان جذب نوری (OD) رنگ حاصله که رابطه مستقیم با تعداد سلولهای فعال از نظر متابولیکی دارد، به وسیله دستگاه الایزا ریدر(اتریش، Sunrise-basic tecan) با طول موج 570 نانومتر، اندازهگیری شد.
قابلیت زنده ماندن سلول ها با آزمون آکریدین اورنج (Acridin Orang):
قابلیت زندهماندن سلولها با رنگآمیزی آکریدین اورنج بعد از 5 روز کشت سلول مورد بررسی قرار گرفت. در این آزمایش محلول رنگآمیزی فلورسنت دوگانه به مقدار 1 میکرولیتر اتیدیوم بروماید(آمریکا، سیگما، آلدریچ) حاوی 100 میکروگرم بر میلیلیتر محلول آکریدین اورنج(آمریکا، سیگما، آلدریچ)به هر چاهک افزوده و سپس با فسفات بافر سالین شستشو داده شد. در ادامه با استفاده از میکروسکوپ فلورسنت(آلمان، Leica 090-135002) با بزرگنمایی 100میکرومتر تصویربرداری شد.
بررسی تمایز سلولهای بنیادی مزانشیمی به سلولهای استخوانی:
جهت بررسی تمایز استخوانی باید از محیط تمایزی استفاده شود. از این جهت، سلولها را بر روی نمونهها کشت داده و پس از 2 روز به اندازهای که سلولها رشد کرده بودند، محیط کشت رویی خارج گردید. سپس نمونهها و سلول را با فسفات بافر سالین شستشو و محیط تمایزی اضافه شد. محیط تمایزی از 45 میلیلیتر محیط کشت((DMEM-High G، 5 میلیلیتر سرم جنین گاوی(FBS) و 500 میکرولیتر بتا گلیسرول، 55 میکرولیتر آسکوربیک اسید و 3 میکرولیتر دگزامتازون (آمریکا، سیگما، آلدریچ) ساخته شد. محیط تمایزی هر 2 روز یک بار تعویض گردید.
ارزیابی فعالیت آلکالین فسفاتاز(ALP) :
این آزمون در فواصل زمانی 7 و14روز بررسی شد. پس از اتمام هر دوره، 200 میکرولیتر بافر ریپا به درون چاهک افزوده شد. در ادامه ویالها، 4 بار و هر 5 دقیقه یک بار به مدت 20 دقیقه ورتکس گردید. برای جدا کردن پروتئینها از بقایای سلولها و داربست، این محلول به مدت 15 دقیقه با 15000 دور بر دقیقه در دمای 4 درجه سانتیگراد، سانتریفیوژ شد. از این جهت 50 میکرو لیتر از عصاره بالایی را درون پلیت 96 خانهای انتقال داده و 150 میکرولیتر کیت آلکالین فسفاتاز با نسبت 4 به 1 محلول به آن اضافه گردید(پارس آزمون، ایران). در نهایت با استفاده از دستگاه الایزا ریدر با طول موج 450 نانومتر، مقدار فعالیت آلکالین فسفاتاز هر نمونه اندازهگیری شد.
ارزیابی رسوب کلسیم به روش آلیزارین قرمز(Alizarin red):
برای بررسی تمایز استخوانی نمونهها، از رنگآمیزی آلیزارین قرمز استفاده شد. رنگآمیزی در روزهای 7 و 14 تمایز، بر روی نمونهها صورت گرفت. به این منظور، محیط کشت تمایزی را برداشته و سلولها با محلول فسفات بافر سالین شستشو داده شدند. سپس سلولها به مدت 20 دقیقه در فرمالدئید 4 درصد(مرک، آلمان) قرار گرفتند. مجدداً، سلولها با محلول فسفات بافر سالین شستشو داده و با رنگ آلیزارین قرمز(مرک، آلمان) 1 درصد به مدت 5 دقیقه رنگآمیزی شدند. رنگهای اضافی خارج و چندین بار با آب مقطر شستشو داده و در نهایت با استفاده از میکروسکوپ نوری، از سلولهای استخوانی رنگ شده که نشاندهنده رسوب کلسیم است، تصویربرداری شد.
آنالیز بیان ژن (Real time-PCR):
سلولهای تمایز یافته از نظر بیان ژنهای اختصاصی استخوان: آلکالین فسفاتاز، استئوکلسین، کلاژن I، استئونکتین، Runx 2 مورد بررسی قرار گرفتند. جهت نرمالیز(یکسانسازی نتایج) از ژن خانهدارHPRT استفاده شد. در این آزمایش ابتدا RNAکل موجود پس از 7 و 14 روز از تمایز استخراج شدند. نمونههای RNA استخراج شده تحت تیمار با آنزیمDNase 1 قرار گرفتند تا آلودگی احتمالی مربوط به DNA حذف گردد. سپس خلوص و غلظت RNA استخراج شده با روش اسپکتروفتومتری (نانودراپ) تعیین گردید. در ادامه cDNA ساخته شد. از این جهت 5 میکرولیتر RNA را برداشته و با استفاده از کیت سنتز cDNA (Thermo Scientific ، آمریکا) در واکنش رونویسی معکوس با استفاده از آغازگرهای رندوم هگزامر و آنزیم ترانس کریپتاز(Revers transcriptaz) معکوس مطابق دستورالعمل کیت cDNA، سنتز گردید. پس از آن روی cDNA به دست آمده PCR Real time-صورت گرفت. بدین منظور 1 میکرولیتر از cDNA ، 10 میکرولیتر low rox Master mix real time (آمپلیکون، دانمارک) و 1 میکرولیتر از آغازگر جلوبرنده و معکوس (آلکالین فسفاتاز، استئوکلسین، استئونکتین، کلاژن I، Runx 2) را داخل ویالهای Real time -PCR ریخته و در نهایت با استفاده از آب دوبار تقطیر حجم آن به 20 میکرولیتر رسانده شد. ژن HPRT به عنوان کنترل داخلی استفاده گردید. دمای PCR با استفاده از دستگاه RT-PCR (Rotor Gene Q ، آلمان) به صورت زیر تنظیم گردید: دمای 95 درجه سانتیگراد به مدت 15 دقیقه، 40 چرخه شامل: دمای 95 درجه سانتیگراد به مدت 20 ثانیه، دمای آنیلینگ 59 درجه سانتیگراد به مدت 30 ثانیه و در نهایت در دمای72 درجه سانتیگراد به مدت 30 ثانیه.
آنالیز آماری:
در این پژوهش تمامی آزمایشها برای هر نمونه، 3 بار تکرار گردید و میانگین نتایج به صورت ± انحراف معیار گزارش شد. از نرمافزار SPSS نسخه 11 برای تجزیه و تحلیل واریانس یک طرفه جهت تعیین میزان معنادار بودن استفاده شد. 05/0 p≤ مرز معنادار بودن تغییرات در نظر گرفته شد. برای رسم نمودارها از نرمافزار اکسل مایکروسافت آفیس 2010 استفاده شد.
یافتهها
طیف سنجی مادون قرمز:
در الگوی شیشه زیست فعال 5S45 ، پیکهای ظاهر شده عبارت بودند از؛ عدد موج 497 و 1030بر سانتیمتر مربوط به ارتعاشات کششی متقارن و نامتقارن پیوندهای Si-O-Si (شکل 1). باند ظاهر شده در عدد موج 696 بر سانتیمتر مربوط به ارتعاشات خمشی P-O و باند 930 بر سانتیمتر مربوط به پیوندهای Si-O است. باند با عدد موج 1456 بر سانتیمتر نیز مربوط به باند کربنات2-3Ca -میباشد. پیکهای ظاهر شده در الگوی نانوذرات شیشه زیست فعال بعد از غوطهوری در مایع شبیهسازی شده بدن، وجود باندهای فسفات P-Oکه نشاندهنده تشکیل لایه هیدروکسی آپاتیت(HA) میباشد را در طول موج 615-590 بر سانتیمتر نشان میدهند. با بررسی و مقایسه الگوها با هم ملاحظه میشود که قلههای مربوط به آپاتیت در روز 14 نسبت به روز 7، از شدت بیشتری برخوردار است و بیانگر این است که مقدار آپاتیت بیشتری تشکیل شده و میتوان گفت نانوذرات ساخته شده، از زیست فعالی بالایی برخوردار است. لازم به ذکر است بقیه باندها نیز مربوط به گروهها و پیوندهای شیشه میباشد که به آنها اشاره گردید.
ارزیابی کیفیت نانو ذرات شیشه زیست فعال توسط میکروسکوپ الکترونی:
تصاویر میکروسکوپ الکترونی روبشی، نانو ذرات شیشه زیست فعال، قبل و بعد از غوطه وری در مایع شبیهسازی شده بدن را نشان میدهد(شکل 2). همان طور که مشخص است، مورفولوژی و اندازه دانههای شیشه ساخته شده در مقیاس نانو میباشد و میانگین اندازه دانهها کمتر از 800 نانومتر است. شکلهای b2 و C2 آپاتیت تشکیل شده بر روی نانوذرات شیشه پس از غوطهوری در مایع شبیهسازی شده بدن در مدت زمانهای 7 و 14 روز
را نشان میدهد. همان طور که مشاهده میشود خوشههای آپاتیت بر روی نانوذرات شیشه زیست فعال تشکیل شده و در تمام سطح به طور یکنواخت و پیوسته رشد پیدا کرده است.
بررسی عدم سمیت سلولی نانوذرات شیشه با آزمایش سنجش MTT :
نتایج، بیشترین حیـات سلولـی، مربـوط بـه نمونه نانوذرات شیشه زیست فعال را گزارش میدهد(شکل 3). این روند در همه فواصل زمانی مورد آزمایش بدین ترتیب بوده است. نتایج حاکی از این است که نانوذرات شیشه زیست فعال ساخته شده، هیچگونه سمیت سلولی ندارد.
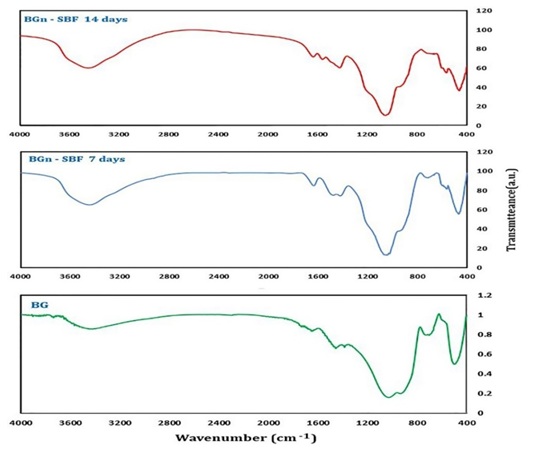
شکل 1: الگوی طیفسنجی مادون قرمز(FTIR) نانو ذرات شیشه زیست فعال 5S45: قبل و بعد از غوطهوری در مایع شبیهسازی شده بدن

شکل 2: تصاویر میکروسکوب الکترونی روبشی(SEM) نانوذرات شیشه زیست فعال 5S45 a) قبل از غوطهوری در مایع شبیهسازی شده بدن
b) بعد از 7 روز غوطهوری و c) بعد از 14 روز غوطهوری

شکل 3: رشد و تکثیر سلولهای بنیادی مزانشیمی مغز استخوان انسان در آزمون MTT بعد از 1، 3، 5 و 7 روز قرارگیری در محیط کشت
(DMEM(h) + FBS + Pen/sterp)؛ نمونه کنترل(CN) و نانوذرات شیشه زیست فعال 5S45(BG)

شکل 4: تصاویر میکروسکوب فلورسنت از سلولهای بنیادی مزانشیمی پس از 3 روز کشت: a) نمونه کنترل و b) نانوذرات شیشه زیست فعال 5S45 (بزرگنمایی تصاویر 100 میکرون میباشد)
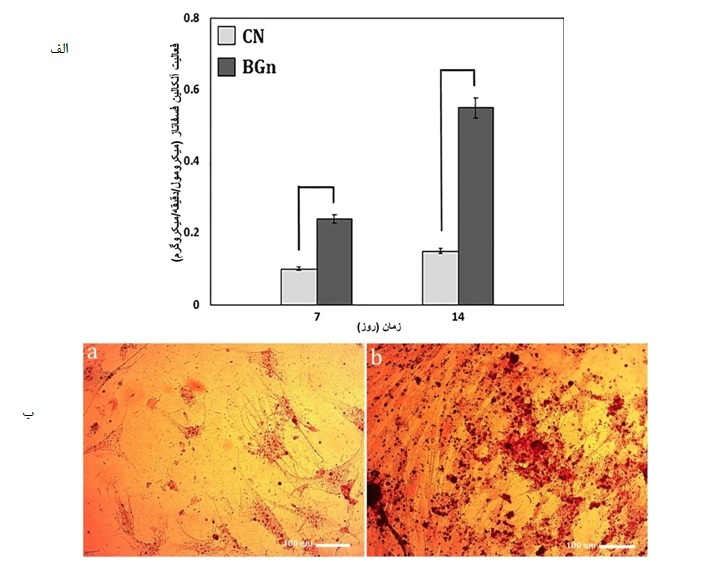
شکل 5 الف: فعالیت آلکالین فسفاتاز(ALP) سلولهای بنیادی مزانشیمی بعد از 7 و 14 روز قرارگیری در محیط تمایزی؛ نمونه کنترل(CN) و نانو ذرات شیشه زیست فعال 5S45 (BG). شکل 5 ب: تصاویر میکروسکوب نوری در آزمون آلیزارین قرمز(Alizarin red) از سلولهای بنیادی مزانشیمی پس از 14 روز قرارگیری در محیط تمایزی: a) نمونه کنترل و b) نانو ذرات شیشه زیست فعال 5S45 (بزرگنمایی تصاویر 100 میکرون میباشد).
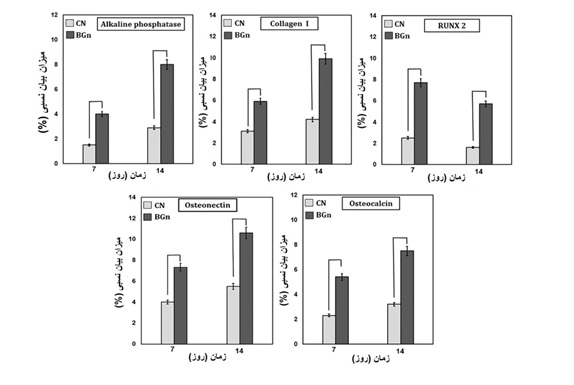
شکل 6 : بیان ژنهای تمایز استخوان با استفاده از Real time-PCR : بیان نسبی ژنهای آلکالین فسفاتاز، استئوکلسین، استئونکتین، کلاژن I و Runx 2 پس از 7 و 14 روز تمایز سلولهای بنیادی مزانشیمی در مجاورت نانو ذرات شیشه زیست فعال 5S45 و نمونه کنترل. نمونه کنترل (CN) و نانو ذرات شیشه زیست فعال 5S45 (BG)
3-7- ارزیابی مقدار بیان ژن:
بیان کمی ژنهای استخوانی(آلکالین فسفاتاز، استئوکلسین، کلاژن I، استئونکتین، Runx 2) cDNA حاصل از تمایز سلولهای مزانشیمی در مجاورت نانو ذارت شیشه 5S45 و نمونه کنترل، در شکل 6 نشان داده شده است. نتایج بیان ژنها مربوط به نانوذرات شیشه در روزهای 7 و 14 تمایز نسبت به نمونه کنترل افزایش قابل ملاحظهای داشته و این در تمامی ژنهای استخوانی به غیر از Runx 2 قابل رؤیت است. این نشاندهنده اثر تحریکی نانوذرات شیشه زیست فعال در تمایز استخوانی میباشد که باعث افزایش بیان ژنها شده است.
بحث
در این پژوهش، نانو ذرات شیشه زیست فعال 5S45 به روش ذوبی ساخته و با استفاده از آسیاب سیارهای به ساختار نانو تبدیل گردید. تصاویر میکروسکوپ الکترونی روبشی و الگوی طیف سنجی مادون قرمز به ترتیب مورفولوژی و اندازه دانهها در مقیاس نانو و پیوندهای مربوط به شیشه را تایید کرد. بررسی زیست فعالی در مایع شبیهسازی شده بدن نیز تشکیل کریستالهای آپاتیت بر روی نانو ذرات را مورد تایید قرار داد. نتایج آزمایشهای سلولی صورت گرفته از قیبل: MTT ، آکریدین اورنج، آلکالین فسفاتاز و آلیزارین قرمز حاکی از عدم سمیت و تاثیر بالقوه این نانو ذرات ساخته شده در رشد و تمایز استخوانی سلولهای بنیادی مزانشیمی بود.
این روش ساخت(روش ذوبی ساخت) مشخص کرد که تبدیل ساختار میکرو شیشه زیست فعال به ساختاری در مقیاس نانو با استفاده از فرآیند آسیاب سیارهای امکانپذیر است.
در سال 2016، تئودور و همکاران نشان دادند که 5S45 میتواند به عنوان یک عامل کمککننده در تمایز استخوان مطرح باشد. اما مشکل این نانو ذره، بزرگ بودن حفرات و عدم پایداری سلول بر روی آن بود. در سال 2011 هیمانشو و همکاران نشان دادند که نانو ذره مذکور، منجر به تمایز استخوانی سلولهای بنیادی میشود. در تحقیقات صورت گرفته، این نوع شیشه را معمولاً به عنوان فاز دوم (تقویتکننده زیست فعال) در ساخت کامپوزیتها و داربستها استفاده کردهاند، تمامی این مطالعهها، شیشه 5S45 را با ساختار میکرو مورد بررسی قرار دادهاند(27-21). علاوه بر آن پژوهشی در زمینه تاثیر اندازه ذرات شیشه فوقالذکر با اندازه ذره 9-750 میکرومتر در رشد، تکثیر و تمایز سلولهای بنیادی مورد بررسی قرار گرفته است. نتایج آن ثابت کرد که هرچه اندازه ذرات ریزتر باشد، تاثیر به سزایی در رشد و تمایز سلولها خواهد داشت(28).
این مطالعه نشان داد که استفاده از نانو ذرات شیشه باعث واکنشپذیری، رشد و تمایز سلولهای بنیادی میشود. نتایج آزمایشهای ارزیابی زیست فعالی نیز مشخص کرد که نانوذرات شیشه زیست فعال ساخته شده، دارای زیست فعالی مناسب بوده به طوری که بعد از 7 روز غوطهوری در مایع شبیهسازی شده بدن، هیدورکسی آپاتیت به خوبی بر روی سطح نانوذرات تشکیل شده و با افزایش زمان غوطه وری به مدت 14 روز، توانایی زیست فعالی آنها حفظ شده است. طول موج 615-590 بر سانتیمتر مربوط به آپاتیت در نمودار شکل 4 ، صحت این موضوع را تایید میکند(32-29).
بنابراین با توجه به نتایج بررسی زیست فعالی و مشابه کارلی در سال 2004، می توان تشکیل فاز هیدروکسی آپاتیت بر روی نانوذرات شیشه فوق را چنین بیان کرد: مراحل تشکیل لایه سطحی هیدروکسیل کربنات آپاتیت (HCA) به طور کلی در سه مرحله لیچینگ، انحلال و رسوب اتفاق میافتد که شامل ایجاد لایه ژل سیلیکاتی و در ادامه هستهزایی و رشد فاز کلسیم فسفات آمورف و تبدیل آن به هیدروکسیل کربنات آپاتیت بالغ با گذشت زمان است. لیچینگ از طریق رهاشدن عناصر قلیـایی، قلیـایی خاکی و مبادله آن ها با کاتیون های H+ و H3O+ انجام مـیشـود. چنین انتشار و تبادل یونی در مدت 1 تا 7 روز غوطهوری باعث افزایش pHدر فصـل مشـترک تا مقادیر بیشتر از 4/7 میشـود اما مجدداً برای مدت 7 الی 24 روز با اشباع این یونها، pHدوباره کاهش مییابد(34-32). در انحلال، شبکه شیشه منجر به تشکیل لایه غنی از سیلیکا و در پی آن رسوب لایه شبه آپاتیتی میشود. لازمه اتصال شیشهها به استخوان، تشکیل لایهای از هیدروکسیل کربنات آپاتیت روی سطح بیومتریال است. کریستالهای هیدروکسیل کربنات آپاتیت با الیاف کلاژن تقویت شده و سپس لایه اتصالدهنده بین ماده زیست فعال و بافتهای زنده تشکیل میشود. مبنای ویژگی اتصال به استخوان شیشههای زیست فعال، واکنش شیمیایی شیشه در حضور سیالات بدن است. توالی از واکنشهای سطحی منجر به تشکیل لایه هیدروکسیل کربنات آپاتیت و پیوند ایمپلنت به بافت میشود(34-32).
نتایج آزمون MTT نیز نشان داد که بیشترین مقدار حیات سلولی مربوط به نانوذرات شیشه زیست فعال بوده است و نانوذره فوق هیچگونه سمیتی ندارد. در آزمون آکریدین اورنج نیز سلولها کاملاً سالم بودند و هیچگونه مرگ سلولی رخ نداده بود. در تصاویر، هسته سلولها سبز بودند که نشاندهنده سلولهای زنده است. نانوذرات شیشه با ایجاد محیطی با ساختارهای نانو و تبادل یونی، باعث رشد و تحریک سلولهای بنیادی مزانشیمی جهت تکثیر میشود(35).
طبق مطالعههای انجام شده نکته مهم در نانوذره زیست فعال این است که در ترکیب شیشههای زیست فعال، وجود اکسید سیلسیوم از اهمیت بالایی برخوردار است چرا که به عنوان شبکهساز در ساختار شیشه عمل میکنند به علاوه گروههای سیلانول (Si-OH) حاصل از فرآیند تبادل یونهای کلسیم(موجود در ساختار شیشه) با هیدرونیوم(H3O+)(موجود در محلول)، مستعد ایجاد مکانهایی برای جوانهزنی کلسیم فسفات هستند(37، 36).
در مطالعه پانزاولتا و همکاران در سال 2008 مشخص شده که وجود سیلسیوم رهایش یافته از ترکیب شیشه به درون محیط کشت سلول میتواند سبب افزایش فعالیت سلولی شود(39، 38). هم چنین فان و همکاران در سال 2003 نشان دادند که اکسید فسفر نیز به جوانهزنی فاز کلسیم فسفات بر روی سطح شیشه کمک میکند(40). در این پژوهش از کلسیم و سیلسیوم با تغییر فرآیند ساخت نانوذرات شیشه استفاده شد که آزمون آلیزارین قرمز تاییدکننده تمایز استخوانی بیشتر نانو ذرات شیشه نسبت به نمونه کنترل بود. طبق تصاویر میتوان این نتیجه را گرفت که نانو ذرات شیشه باعث تشکیل رسوبات کلسیم ناشی از کلسیم و فسفری که در ترکیب خود دارد میشود. رسوب کلسیم شامل ترشحات معدنی سلولهای استئوبلاست به ماتریکس خارج سلولی است و شکلگیری این رسوبات، مشخصه مرحله نهایی تمایز استخوانی است. مطالعهها نشاندهنده این است که حضور این رسوبات، شاخص خوبی از تمایز استخوانی است. این موضوع در تصاویر آلیزارین قرمز به خوبی قابل رؤیت است.
بررسی کمی مقدار بیان ژنهای استخوانی نیز از اثر تحریکی نانوذره شیشه در تمایز استئوژنیک و بیان ژنها دلالت داشت. تشکیل استخوان در سه مرحله اصلی: تمایز استئوبلاست، تشکیل ماتریکس و کانی سازی ماتریکس اتفاق میافتد. کوموری و همکاران در سال 2008 اظهار داشتند که بیان ژن آلکالین فسفاتاز در اوایل و اواسط این مرحلهها است. هم چنین این گروه در مطالعه خود نشان دادند که بیانRunx 2 در طی این سه مرحله متغیر میباشد. آنها نشان دادند کهRunx 2 یک تنظیمکننده اساسی از تمایز استئوبلاست است و در مرحله اولیه تمایز سطح بیان بالایی دارد، اما به تنهایی کافی نیست(41). با توجه به نتایج این پژوهش، میزان بیان ژن آلکالین فسفاتاز نمونه نانوذره شیشه پس از 7 روز کشت نسبت به نمونه کنترل، افزایش قابل ملاحظهای داشته، این روند در روز 14 تمایز نیز به همین صورت بود.Runx 2 پس از 7 روز کشت یعنی در مراحل اولیه بیان ژن سیر صعودی داشت اما در روزهای بعد از روز 14، این روند کاهش پیدا کرده بود. ساندرامورتی و همکاران در سال 2015 نشان دادند که ژنهای استئوکلسین و استئونکتین نقش مهمی در کانیسازی و ایجاد اولیه بلورهای کلسیم ایفا میکنند. استئوکلسین یک پروتئین غیر کلاژنی است که توسط استئوبلاستهای بالغ بیان میشود. این ترکیب از سه اسید کربوکسیگلوتامیک تشکیل شده است که به جذب کلسیم کمک میکند. استئوکلسین مسئول فرآیند استخراج استخوان است(44-42). استئونکتین یک گلیکوپروتئین است که Ca2+ را درگیر میکند، مراحل اولیه رشد کریستال را تنظیم مینماید و نقش حیاتی در کانیسازی دارد(44). در شکل سطوح بیان استئوکلسین و استئونکتین نمونه نانو ذره شیشه زیست فعال در روزهای 7 و14 تمایز نسبت به نمونه کنترل، اختلاف معناداری دارد و تقریباً به یک میزان بیان شدهاند. کلاژن I نیز نقش مهمی در بیومینرالیزاسیون دارد. این ژن نیز در روزهای 7 و14 تمایز استخوانی بیان قابل ملاحظهای داشته است.
نتیجهگیری
در این پژوهش نانوذرات شیشه زیست فعال 5S45 به روش ذوبی ساخت و با استفاده از آسیاب سیارهای به ساختار نانو تبدیل گردید. نتایج نشان داد که با غوطــهوری نانو ذرات شیشــه زیســت فعــال در مــایع شبیهسازی شده بدن، بلورهـای آپاتیـت بـر روی سـطح نانو ذرات شیشه تشکیل شده و با افزایش زمان غوطـهوری، میـزان تشـکیل ذرات آپاتیت نیز افزایش پیدا کـرده است .بررسی رشد و تکثیر سلولی نشان داد نانو ذرات شیشه زیست فعال، باعث افزایش رشد و تکثیر سلولهای بنیادی مزانشیمی میشود. علاوه بر آن، تمایز
سلولهای مزانشیمی به سلولهای استخوانی در حضور نانو ذرات شیشه افزایش پیدا کرده است. استفاده از نانو ذرات شیشه به واسطه دارا بودن عناصر زیست فعال و هم چنین افزایش نسبت سطح به حجم به دلیل ساختار نانویی، واکنشپذیری بهتر و در نتیجه، افزایش کارآیی تکثیر و تمایز سلولهای بنیادی میگردد. پس نانو ذرات شیشه ساخته شده علاوه بر آن که هیچگونه سمیتی نداشته بلکه باعث تحریک و القاء رشد سلول نیز میشود و از آن میتوان جهت درمان و بهبود سریع ضایعات استخوانی استفاده نمود.
تشکر و قدردانی
این پروژه در مرکز تحقیقات بیوتکنولوژی و میکروبیولوژی کاربردی دانشگاه علوم پزشکی بقیهاله (عج) به انجام رسیده است. از صندوق حمایت از پژوهشگران کشور و ستاد نانوتکنولوژی جهت حمایت در انجام پروژه نهایت قدردانی و تشکر به عمل میآید.
متن کامل: (4457 مشاهده)
اثرات نانو ذرات شیشه زیست فعال 45S5 سنتزی بر رشد و تمایز سلولهای
بنیادی مزانشیمی مغز استخوان انسان به بافت استخوانی در محیط برون تن
مهدی شمس1، علی سلیمی2، مرضیه قلاسی3، راحله حلبیان4
چکیده
سابقه و هدف
شیشهها و شیشه – سرامیکها، گروهی از مواد زیستی هستند که در برابر محلول شبیهسازی شده بدن، تشکیل هیدروکسی آپاتیت میدهند و در بسیاری از موارد بالینی که نیاز به تولید و ترمیم استخوان است، میتوانند کاربرد داشته باشند. هدف از این پژوهش، ساخت نانوذرات شیشه زیست فعال 5S45 و بررسی تاثیر آن در رشد، تکثیر و تمایز سلولهای بنیادی مزانشیمی به سلولهای استخوانی بود.
مواد و روشها
در این پژوهش تجربی، شیشه زیست فعال 5S45 به روش ذوبی ساخته شده، با آسیاب سیارهای به ساختار نانو تبدیل و سپس خواص فیزیکوشیمیایی و ساختاری آن بررسی گردید. ویژگی زیست فعالی آن با استفاده از محلول شبیهسازی شده بدن مورد ارزیابی قرار گرفت. قابلیت رشد، تکثیر و تمایز سلولهای بنیادی مزانشیمی در مجاورت نانو ذرات بررسی گردید.
یافتهها
ارزیابی شیشه زیست فعال 5S45، از تشکیل هیدروکسی آپاتیت بر روی نانوذرات پس از غوطهوری در مایع شبیهسازی شده بدن حکایت داشت. آزمایشهای سلولی نیز، عدم سمیت نانو ذرات شیشه، رشد و تمایز سلولهای مزانشیمی به سلولهای استخوانی را تایید کرد. در تمایز استخوانی میزان فعالیت آلکالین فسفاتاز نانوذره شیشه پس از 14 روز تمایز، 07/0 ± 55/0 بیان شد، در حالی که در نمونه کنترل، 03/0 ± 15/0 بود.
نتیجه گیری
با توجه به نتایج میتوان گفت که سلولهای بنیادی مزانشیمی قابلیت تکثیر و رشد بر روی نانو ذرات شیشه زیست فعال ساخته شده را دارند و نانو ذره فوق علاوه بر آن که سمیت نداشته، بلکه باعث تحریک و القاء رشد سلولها میشوند.
کلمات کلیدی: نانوذرهها، سلولهای بنیادی مزانشیمی، شیشه
تاریخ دریافت: 13/4/97
تاریخ پذیرش: 11/6/97
1- کارشناس ارشد نانوتکنولوژی ـ پژوهشکده نانوتکنولوژی و مواد پیشرفته پژوهشگاه مواد و انرژی ـ کرج ـ ایران
2- دکترای نانوتکنولوژی ـ استادیار مرکز تحقیقات نانوتکنولوژی ـ دانشگاه علوم پزشکی بقیهاله(عج) ـ تهران ـ ایران
3- دکترای بیوشیمی ـ استادیار گروه زیستشناسی سلولی مولکولی ـ دانشکده علوم زیستشناسی دانشگاه خوارزمی ـ تهران ـ ایران
4- مؤلف مسئول: دکترای بیوتکنولوژی پزشکی ـ استادیار مرکز تحقیقات میکروبشناسی کاربردی ـ مؤسسه زیستشناسی و انستیتو مسمومیتها ـ دانشگاه علوم پزشکی بقیهاله(عج) ـ تهران ـ ایران ـ صندوق پستی: 44711-14359
بنیادی مزانشیمی مغز استخوان انسان به بافت استخوانی در محیط برون تن
مهدی شمس1، علی سلیمی2، مرضیه قلاسی3، راحله حلبیان4
چکیده
سابقه و هدف
شیشهها و شیشه – سرامیکها، گروهی از مواد زیستی هستند که در برابر محلول شبیهسازی شده بدن، تشکیل هیدروکسی آپاتیت میدهند و در بسیاری از موارد بالینی که نیاز به تولید و ترمیم استخوان است، میتوانند کاربرد داشته باشند. هدف از این پژوهش، ساخت نانوذرات شیشه زیست فعال 5S45 و بررسی تاثیر آن در رشد، تکثیر و تمایز سلولهای بنیادی مزانشیمی به سلولهای استخوانی بود.
مواد و روشها
در این پژوهش تجربی، شیشه زیست فعال 5S45 به روش ذوبی ساخته شده، با آسیاب سیارهای به ساختار نانو تبدیل و سپس خواص فیزیکوشیمیایی و ساختاری آن بررسی گردید. ویژگی زیست فعالی آن با استفاده از محلول شبیهسازی شده بدن مورد ارزیابی قرار گرفت. قابلیت رشد، تکثیر و تمایز سلولهای بنیادی مزانشیمی در مجاورت نانو ذرات بررسی گردید.
یافتهها
ارزیابی شیشه زیست فعال 5S45، از تشکیل هیدروکسی آپاتیت بر روی نانوذرات پس از غوطهوری در مایع شبیهسازی شده بدن حکایت داشت. آزمایشهای سلولی نیز، عدم سمیت نانو ذرات شیشه، رشد و تمایز سلولهای مزانشیمی به سلولهای استخوانی را تایید کرد. در تمایز استخوانی میزان فعالیت آلکالین فسفاتاز نانوذره شیشه پس از 14 روز تمایز، 07/0 ± 55/0 بیان شد، در حالی که در نمونه کنترل، 03/0 ± 15/0 بود.
نتیجه گیری
با توجه به نتایج میتوان گفت که سلولهای بنیادی مزانشیمی قابلیت تکثیر و رشد بر روی نانو ذرات شیشه زیست فعال ساخته شده را دارند و نانو ذره فوق علاوه بر آن که سمیت نداشته، بلکه باعث تحریک و القاء رشد سلولها میشوند.
کلمات کلیدی: نانوذرهها، سلولهای بنیادی مزانشیمی، شیشه
تاریخ دریافت: 13/4/97
تاریخ پذیرش: 11/6/97
1- کارشناس ارشد نانوتکنولوژی ـ پژوهشکده نانوتکنولوژی و مواد پیشرفته پژوهشگاه مواد و انرژی ـ کرج ـ ایران
2- دکترای نانوتکنولوژی ـ استادیار مرکز تحقیقات نانوتکنولوژی ـ دانشگاه علوم پزشکی بقیهاله(عج) ـ تهران ـ ایران
3- دکترای بیوشیمی ـ استادیار گروه زیستشناسی سلولی مولکولی ـ دانشکده علوم زیستشناسی دانشگاه خوارزمی ـ تهران ـ ایران
4- مؤلف مسئول: دکترای بیوتکنولوژی پزشکی ـ استادیار مرکز تحقیقات میکروبشناسی کاربردی ـ مؤسسه زیستشناسی و انستیتو مسمومیتها ـ دانشگاه علوم پزشکی بقیهاله(عج) ـ تهران ـ ایران ـ صندوق پستی: 44711-14359
مقدمه
برای ترمیم ضایعات و نقـایص اسـتخوانی مـیتـوان از امکانات مهندسی بافت بهره برد. در این ارتباط، بـا طراحـی داربست مناسب و گذاشتن سلولهای دارای پتانسیل تولیـد استخوان بر روی این داربستها و سپس پیوند در محل ضایعه، میتوان قابلیت ترمیم ضایعه را افزایش داد(1). سـرامیکهـای فسفات کلسیمی(از قبیل: شیشه و شیشه- سرامیکهـا) به علت این که سـاختاری مشـابه بـا بخـش غیر آلی ترکیب استخوان دارند، به عنوان داربسـت سـلولی مورد استفاده قرار گرفتهاند. این شیشهها در برابر محلول شبیهسازی شده بدن تشکیل هیدروکسی کربنات آپاتیت میدهند و در بسیاری از موارد بالینی که نیاز به تولید و ترمیم استخوان است، میتوانند کاربرد داشته باشند(3، 2). شیشههـای زیـستی هنگامی که در بدن قرار میگیرند، به راحتی با سیالهای فیزیولوژیکی واکنش داده و تشکیل یک پیونـد قـوی بـا بافـتهـای نـرم و سخت در حین فعالیت سلولی میدهند(4). اولین ترکیبی که بیشترین مطالعهها بر روی آن انجام شده است، شیشه 5S45 ساخته شده بـه روش ذوبـی میباشد که ترکیب آن بر حسب درصد وزنی اجزا شامل: 45 درصد اکسید سیلسیم، 5/24 درصد اکسید سدیم، 4/24 درصد اکسید کلسیم و 6 درصد پنتوکسید فسفر است(5). شیشههای زیست فعال را میتوان به دو روش ذوبی و سل ژل تهیه نمود(7، 6). ساخت شیشه 5S45 در مقیاس نانو بسیار دشوار است، استفاده از روش سل- ژل نیز برای ساخت این نوع شیشه، به دلیل وجود سدیم در ترکیب خود، امکانپذیر نیست چراکه سدیم باعث سمیت و مرگ سلولی می شود. بنابراین روش ذوبی برای ساخت این نوع نانوذره بهترین گزینه است، لازم به ذکر است روش ساخت ذوبی، باعث تولید ذرات با ساختار میکرو میشود.
سـلولهـای بنیـادی مزانشـیمال سلولهـای بنیـادی چنـد قوهای بـوده که دارای قدرت تکثیر و خود نوسازی بالا و هم چنین پتانسیل تمـایز بــه ردههــای مختلــف ســلولی از جملــه ســلولهــای استئوبلاست، هندروسیـت، آدیپوسـیت، سلولهای اندوتلیال، سلولهای
عصبی، سلولهای میوسـیت قلبـی، سـلولهـای هپاتوسیت و سلولهای پانکراس میباشند(11-8).
کارآیی این سلولها در درمان بیماری ژنتیکی استئوژنزیس امپرفکتا(Osteogensis Imperfecta)، بهبود خونسازی در بیماران سرطانی تحت درمان، بازسازی استخوان، ترمیم بافت نکروز شده در بیماران انفارکتوس قلبی و درمان بیماریهای مفصلی به خوبی نشان داده شده است (13، 12). سه منبع اصلی برای جداسازی ســلولهــای بنیــادی مزانشـیمی، برای مطالعهها و درمان بیماریها وجود دارد که میتوان به مغز استخوان، بند ناف و بافت چربی اشاره کرد. سلولهای بنیادی مشتق شده از مغز استخوان انسان مشابه مورفولوژی و فنوتیپ حاصل از بافت چربی هستند(15، 14).
محیط کشت مورد استفاده نیز عامل مهمی در توانایی تمایز استئوژنیک است. استفاده از محیطهای پایه از قبیل؛ DMEM+ Low DMEM+ High, DMEM+ F, و افزودن فاکتورهای رشد فیبروبلاست، دگزامتازون، اسید اسکوربیک و گلیسرول فسفات به محیط پایه از عواملی هستند که تاثیر به سزایی در تمایز استخوانی دارند(18-16، 14).
از موارد دیگری که بر تمایز سلولهای بنیادی مزانشیمی تاثیر دارد؛ اتصال سلول به ماتریکس(داربست) خارج سلولی است. این ماتریکس(داربست) از مواد آلی و غیر آلی از قبیل کلاژن I و نمکهای کلسیم به فرم شیشه زیست فعال، هیدروکسی آپاتیت، نمکهای فلورید، فسفات و سیترات تشکیل یافته است(20، 19).
در تحقیقات صورت گرفته، شیشه زیست فعال را معمولاً به عنوان فاز دوم(تقویتکننده زیست فعال) در ساخت کامپوزیتها و داربستها استفاده کردهاند که تمامی این مطالعهها، شیشه 5S45 را با ساختار میکرو مورد بررسی قرار دادهاند(27-21). علاوه بر آن پژوهشی در زمینه تاثیر اندازه ذرات شیشه فوقالذکر با اندازه ذره 9-750 میکرومتر در رشد، تکثیر و تمایز سلولهای بنیادی مورد بررسی قرار گرفته است. نتایج آن ثابت کرد که هرچه اندازه ذرات ریزتر باشد، تاثیر به سزایی در رشد و تمایز سلولها خواهد داشت(28).
با توجه به مباحث شرح داده شده در مقدمه و اهمیت
نانو مواد در تمایز سلولهای بنیادی، هدف از این پژوهش، سنتز نانوذرات شیشه زیست فعال5S45 و بررسی خواص زیست فعالی و تاثیر آن در تکثیر و تمایز سلولهای بنیادی مزانشیمی مغز استخوان انسان به سلولهای استخوانی در محیط برون تن بود. بـا وجـود آن کـه گزارشهایی مبنی بر ساخت شیشههای زیست فعال 5S45 و بررسی سلولی آن گزارش شده است، اما تاکنون گزارشـی در مـورد ساخت شیشــه زیســت فعــال با این ترکیب و با استفاده از فرآیند آسیاب سیارهای برای ساخت این شیشه در مقیاس نانو و بررسی تکتیر و تمایز سلولهای بنیادی مزانشیمی بیان نشده است. بنابراین ما در این پژوهش سعی در ساخت نانو ذره شیشه فوق با استفاده از آسیاب سیاره کردیم و با چندین مرتبه آسیاب و انجام آزمایشهای متعدد، اندازه ذرات را به مقیاس نانو رساندیم.
نتایج آزمایشها ثابت کرد که با استفاده از آسیاب سیارهای میتوان ساختار نانویی این نوع شیشه را تولید کرد. استفاده از این نوع نانوذرات شیشه به واسطه افزایش نسبت سطح به حجم و یون های زیست فعال، سبب واکنشپذیری بهتر این نوع فاز در تکثیر و تمایز سلولها خواهد شد. از مزیتها و کاربرد نانوذرات تولید شده، میتوان به حل مشکلات کار با داربست و استفاده آن در ارتوپدیها و بیمارستانها جهت بهبود درمان ضایعات استخوانی اشاره کرد.
مواد و روشها
ساخـت و مشخصهیابـی نانو ذرات شیشـه زیست فعال 5S 45:
در این پژوهش تجربی، شیشه زیست فعال به روش ذوبی ساخت و مشخصهیابی شد. برای ساخت شیشه زیست فعال 5S45 ، 07/22 گرم SiO2 و 88/5 گرم P2O5، 45/21 گرم CaCO3 (مرک، آلمان) و در نهایت 6/20 گرم NaCO3 (مرک، آلمان) با هم ترکیب و سپس توسط هاون عقیق، آسیاب گردید. در ادامه با استفاده از ظرف پلیاتیلنی دربدار با چند عدد گلوله پلیاتیلنی مجدداً مخلوط کردن مواد کاملتر انجام شد. مواد فوق با استفاده از دستگاه پرس(تأسیسات صارم ـ ایران ـ T-35) به شکل قرصهای دایرهای با قطر10 میلیمتر، پرس گردید. قرصهای حاصل درون کوره(F11L ، آذرفورناس، ایران) قرار داده شد. تغییرات دمایی کوره بدین صورت تنظیم گردید که ابتدا افزایش دما تا 900 درجه سانتیگراد با سرعت 10 درجه در دقیقه و ماندن در دمای فوق به مدت 5/2 ساعت و مجدداً افزایش دما از 900 به 1400 درجه سانتیگراد با نرخ 10 درجه در دقیقه و قرار دادن در دمای 1400 درجه سانتیگراد به مدت 3 ساعت. در نهایت پس از عملیات مذاب، مواد ذوب شده حاصل از کوره خارج و درون آب مقطر کوینچ شد. شیشه حاصل سپس با استفاده از آون(مرک، آلمان) در دمای 80 درجه سانتیگراد به مدت 5 ساعت خشک گردید. در نهایت با استفاده از آسیاب سیارهای با کاپ زیرکونیا(Petch PM400، آلمان) به مدت 6 ساعت آسیاب گردید. مجدداً، شیشه زیست فعال طی چند مرحله و در مجموع به مدت 60 ساعت، آسیاب شد تا به ساختار نانو تبدیل گردد.
ارزیابی زیست فعالی:
برای ارزیابی زیست فعالی، از مایع شبیهسازی شده بدن طبق دستورالعمل کوکوبو(KoKubo) بهره گرفته شد. در این آزمایش نانوذرات شیشه زیست فعال در بازههای زمانی7 و14 روز به صورت مجزا در 10 میلیلیتر مایع شبیهسازی شده بدن غوطه ور و در دمای 37 درجه سانتیگراد درون انکوباتور(INC 108 ، ممرت، آلمان)، قرار داده شد. پس از آن محلول مایع شبیهسازی شده بدن، خارج و نمکها و سایر اضافات چسبیده به نمونهها، با آب مقطر شستشو داده و خشک گردید.
طیف سنجی مادون قرمز:
برای شناسایی پیوندها و گروههای شیمیایی نانو ذرات شیشه قبل و بعد از غوطهوری در مایع شبیهسازی شده بدن، از آزمون طیفسنجی مادون قرمز(FTIR)(Spectrum 400 ، پرکین المر، آمریکا) در محدوده 400-400 بر سانتیمتر در حالت عبوری استفاده شد.
میکروسکوپ الکترونی روبشی:
به منظور مطالعه مورفولوژی نانوذرات شیشه قبل و بعد از غوطهوری در مایع شبیهسازی شده بدن، از میکروسکوب الکترونی روبشی (SEM)(کره، SEM South، سرون تکنولوژی) با ولتاژ 20 کیلوولت، استفاده شد. به علت هدایت الکتریکی ضعیف نمونهها، سطح مقطع آنها قبل از انجام آزمایش، با لایهای بسیار نازک از طلا به روش کندوپاش پوشانده شد.
ارزیابی رشد و تکثیر سلولهای بنیادی مزانشیمی:
جهت بررسی قابلیت رشد و تکثیر سلولهای بنیادی مزانشیمی، سلولها را در فلاسک کشت سلول 75 ریخته و با استفاده از 12 میلیلیتر محیط کشت با گلوکز بالا(DMEM-High G) به همراه 5 درصد محلول سرم جنین گاوی(FBS) و آنتیبیوتیک(پنیسیلین و استرپتوماسین)(جیبکو، آلمان) 1 درصد کشت داده شد. سپس فلاسک به درون انکوباتور(GmibH, MMM-Group، آلمان) با گاز 5 درصد CO2 در دمای 37 درجه سانتیگراد به همراه رطوبت منتقل گردید. هر 2 روز یک بار، محیط کشت تعویض گردید. طی 6 روز که سلولها رشد پیدا کرده و به تراکم 90 درصد رسیده بودند، پاساژ داده شدند. مراحل انجام پاساژ بدین صورت بود که ابتدا سلولها را درون فلاسک با محلول بافر فسفات سالین(PBS) شستشو داده و سپس با محلول تریپسین/ EDTA (جیبکو، آلمان) 2/0 درصد از کف فلاسک جدا شدند.
در ادامه پس از جدا شدن سلولها از کف فلاسک و معلق شدن، مقدار 3 میلیلیتر محیط کشت به منظور خنثی کردن اثر تریپسین به فلاسک اضافه گردید. سپس سوسپانسیون سلولهـا را بـه داخـل فالکـون 15 انتقـال و سانتریفیوژ (2-16PK ، سیگما، آلمان) با 1200 دور در دقیقه به مدت 5 دقیقه در دمای محیط انجام شد. پس از سانتریفیوژ، محلول رویی خالی و مجدداً 4 میلیلیتر محیط کشت درون فالکون افزوده و به منظور جدا شدن و معلق شدن سلولها، چندین بار پیپت انجام شد. سپس به داخل فلاسک کشت سلول انتقال داده شد.
برای انجام آزمایشهای سلولی باید نمونهها استریل باشند. از این جهت، نمونهها در زیر هود کشت سلولی ((ایران، Jal tajhiz Production ، JTLV C2) با محلول فسفات بافر سالین(PBS) شستشو و به مدت ۲۰ دقیقه تحت اشعه فرابنفش قرار گرفت.
در ادامه آن سلولهای بنیادی مزانشیمی شمارش و بر روی نمونههای درون چاهکها انتقال داده شد. برای شمارش از لام نئوبار استفاده شد. نمونه کنترل نیز استفاده گردید از این جهت سلولها در کف پلیت کشت سلولی، کشت داده شدند.
بـررسی سمیـت سلولی با استفاده از آزمایش سنجش MTT :
برای انجام آزمونMTT حدود 104× 3 هزار سلول به هر چاهک در پلیت 24 خانهای حاوی نمونههای استریل شده انتقال داده شده و 300 میکرولیتر محیط کشت به هر چاهک اضافه گردید. این آزمون در فواصل زمانی 1، 3 ،5 و 7 روز در حضور نانو ذرات شیشه زیست فعال بررسی گردید و محیط کشت هر 2 روز یک بار تعویض شد. در این آزمایش پس از اتمام هر دوره، محیط رویی سلولها خارج و با فسفات بافر سالین شتسشو داده و به مقدار 200 میکرولیتر محیط کشت با گلوکز بالا (DMEM-High G) حاوی20 میکرولیتر محلول MTT (آمریکا، سیگما، آلدریچ) اضافه گردید. سپس سلولها، به مدت 4 ساعت درون انکوباتور 37 درجه سانتیگراد و رطوبت 98 درصد و میزان رطوبت 5 درصد گاز 2 COدر تاریکی قرار داده شدند.
س از 4 ساعت انکوباسیون، مجدداً محیط رویی، خارج و میزان 100 میکرولیتر دی متیل سولفوکساید (DMSO)(آمریکا، سیگما، آلدریچ) اضافه گردید تا کریستالهای فورمازان حل شده و یک محلول بنفش رنگ به دست آید. در نهایت میزان جذب نوری (OD) رنگ حاصله که رابطه مستقیم با تعداد سلولهای فعال از نظر متابولیکی دارد، به وسیله دستگاه الایزا ریدر(اتریش، Sunrise-basic tecan) با طول موج 570 نانومتر، اندازهگیری شد.
قابلیت زنده ماندن سلول ها با آزمون آکریدین اورنج (Acridin Orang):
قابلیت زندهماندن سلولها با رنگآمیزی آکریدین اورنج بعد از 5 روز کشت سلول مورد بررسی قرار گرفت. در این آزمایش محلول رنگآمیزی فلورسنت دوگانه به مقدار 1 میکرولیتر اتیدیوم بروماید(آمریکا، سیگما، آلدریچ) حاوی 100 میکروگرم بر میلیلیتر محلول آکریدین اورنج(آمریکا، سیگما، آلدریچ)به هر چاهک افزوده و سپس با فسفات بافر سالین شستشو داده شد. در ادامه با استفاده از میکروسکوپ فلورسنت(آلمان، Leica 090-135002) با بزرگنمایی 100میکرومتر تصویربرداری شد.
بررسی تمایز سلولهای بنیادی مزانشیمی به سلولهای استخوانی:
جهت بررسی تمایز استخوانی باید از محیط تمایزی استفاده شود. از این جهت، سلولها را بر روی نمونهها کشت داده و پس از 2 روز به اندازهای که سلولها رشد کرده بودند، محیط کشت رویی خارج گردید. سپس نمونهها و سلول را با فسفات بافر سالین شستشو و محیط تمایزی اضافه شد. محیط تمایزی از 45 میلیلیتر محیط کشت((DMEM-High G، 5 میلیلیتر سرم جنین گاوی(FBS) و 500 میکرولیتر بتا گلیسرول، 55 میکرولیتر آسکوربیک اسید و 3 میکرولیتر دگزامتازون (آمریکا، سیگما، آلدریچ) ساخته شد. محیط تمایزی هر 2 روز یک بار تعویض گردید.
ارزیابی فعالیت آلکالین فسفاتاز(ALP) :
این آزمون در فواصل زمانی 7 و14روز بررسی شد. پس از اتمام هر دوره، 200 میکرولیتر بافر ریپا به درون چاهک افزوده شد. در ادامه ویالها، 4 بار و هر 5 دقیقه یک بار به مدت 20 دقیقه ورتکس گردید. برای جدا کردن پروتئینها از بقایای سلولها و داربست، این محلول به مدت 15 دقیقه با 15000 دور بر دقیقه در دمای 4 درجه سانتیگراد، سانتریفیوژ شد. از این جهت 50 میکرو لیتر از عصاره بالایی را درون پلیت 96 خانهای انتقال داده و 150 میکرولیتر کیت آلکالین فسفاتاز با نسبت 4 به 1 محلول به آن اضافه گردید(پارس آزمون، ایران). در نهایت با استفاده از دستگاه الایزا ریدر با طول موج 450 نانومتر، مقدار فعالیت آلکالین فسفاتاز هر نمونه اندازهگیری شد.
ارزیابی رسوب کلسیم به روش آلیزارین قرمز(Alizarin red):
برای بررسی تمایز استخوانی نمونهها، از رنگآمیزی آلیزارین قرمز استفاده شد. رنگآمیزی در روزهای 7 و 14 تمایز، بر روی نمونهها صورت گرفت. به این منظور، محیط کشت تمایزی را برداشته و سلولها با محلول فسفات بافر سالین شستشو داده شدند. سپس سلولها به مدت 20 دقیقه در فرمالدئید 4 درصد(مرک، آلمان) قرار گرفتند. مجدداً، سلولها با محلول فسفات بافر سالین شستشو داده و با رنگ آلیزارین قرمز(مرک، آلمان) 1 درصد به مدت 5 دقیقه رنگآمیزی شدند. رنگهای اضافی خارج و چندین بار با آب مقطر شستشو داده و در نهایت با استفاده از میکروسکوپ نوری، از سلولهای استخوانی رنگ شده که نشاندهنده رسوب کلسیم است، تصویربرداری شد.
آنالیز بیان ژن (Real time-PCR):
سلولهای تمایز یافته از نظر بیان ژنهای اختصاصی استخوان: آلکالین فسفاتاز، استئوکلسین، کلاژن I، استئونکتین، Runx 2 مورد بررسی قرار گرفتند. جهت نرمالیز(یکسانسازی نتایج) از ژن خانهدارHPRT استفاده شد. در این آزمایش ابتدا RNAکل موجود پس از 7 و 14 روز از تمایز استخراج شدند. نمونههای RNA استخراج شده تحت تیمار با آنزیمDNase 1 قرار گرفتند تا آلودگی احتمالی مربوط به DNA حذف گردد. سپس خلوص و غلظت RNA استخراج شده با روش اسپکتروفتومتری (نانودراپ) تعیین گردید. در ادامه cDNA ساخته شد. از این جهت 5 میکرولیتر RNA را برداشته و با استفاده از کیت سنتز cDNA (Thermo Scientific ، آمریکا) در واکنش رونویسی معکوس با استفاده از آغازگرهای رندوم هگزامر و آنزیم ترانس کریپتاز(Revers transcriptaz) معکوس مطابق دستورالعمل کیت cDNA، سنتز گردید. پس از آن روی cDNA به دست آمده PCR Real time-صورت گرفت. بدین منظور 1 میکرولیتر از cDNA ، 10 میکرولیتر low rox Master mix real time (آمپلیکون، دانمارک) و 1 میکرولیتر از آغازگر جلوبرنده و معکوس (آلکالین فسفاتاز، استئوکلسین، استئونکتین، کلاژن I، Runx 2) را داخل ویالهای Real time -PCR ریخته و در نهایت با استفاده از آب دوبار تقطیر حجم آن به 20 میکرولیتر رسانده شد. ژن HPRT به عنوان کنترل داخلی استفاده گردید. دمای PCR با استفاده از دستگاه RT-PCR (Rotor Gene Q ، آلمان) به صورت زیر تنظیم گردید: دمای 95 درجه سانتیگراد به مدت 15 دقیقه، 40 چرخه شامل: دمای 95 درجه سانتیگراد به مدت 20 ثانیه، دمای آنیلینگ 59 درجه سانتیگراد به مدت 30 ثانیه و در نهایت در دمای72 درجه سانتیگراد به مدت 30 ثانیه.
آنالیز آماری:
در این پژوهش تمامی آزمایشها برای هر نمونه، 3 بار تکرار گردید و میانگین نتایج به صورت ± انحراف معیار گزارش شد. از نرمافزار SPSS نسخه 11 برای تجزیه و تحلیل واریانس یک طرفه جهت تعیین میزان معنادار بودن استفاده شد. 05/0 p≤ مرز معنادار بودن تغییرات در نظر گرفته شد. برای رسم نمودارها از نرمافزار اکسل مایکروسافت آفیس 2010 استفاده شد.
یافتهها
طیف سنجی مادون قرمز:
در الگوی شیشه زیست فعال 5S45 ، پیکهای ظاهر شده عبارت بودند از؛ عدد موج 497 و 1030بر سانتیمتر مربوط به ارتعاشات کششی متقارن و نامتقارن پیوندهای Si-O-Si (شکل 1). باند ظاهر شده در عدد موج 696 بر سانتیمتر مربوط به ارتعاشات خمشی P-O و باند 930 بر سانتیمتر مربوط به پیوندهای Si-O است. باند با عدد موج 1456 بر سانتیمتر نیز مربوط به باند کربنات2-3Ca -میباشد. پیکهای ظاهر شده در الگوی نانوذرات شیشه زیست فعال بعد از غوطهوری در مایع شبیهسازی شده بدن، وجود باندهای فسفات P-Oکه نشاندهنده تشکیل لایه هیدروکسی آپاتیت(HA) میباشد را در طول موج 615-590 بر سانتیمتر نشان میدهند. با بررسی و مقایسه الگوها با هم ملاحظه میشود که قلههای مربوط به آپاتیت در روز 14 نسبت به روز 7، از شدت بیشتری برخوردار است و بیانگر این است که مقدار آپاتیت بیشتری تشکیل شده و میتوان گفت نانوذرات ساخته شده، از زیست فعالی بالایی برخوردار است. لازم به ذکر است بقیه باندها نیز مربوط به گروهها و پیوندهای شیشه میباشد که به آنها اشاره گردید.
ارزیابی کیفیت نانو ذرات شیشه زیست فعال توسط میکروسکوپ الکترونی:
تصاویر میکروسکوپ الکترونی روبشی، نانو ذرات شیشه زیست فعال، قبل و بعد از غوطه وری در مایع شبیهسازی شده بدن را نشان میدهد(شکل 2). همان طور که مشخص است، مورفولوژی و اندازه دانههای شیشه ساخته شده در مقیاس نانو میباشد و میانگین اندازه دانهها کمتر از 800 نانومتر است. شکلهای b2 و C2 آپاتیت تشکیل شده بر روی نانوذرات شیشه پس از غوطهوری در مایع شبیهسازی شده بدن در مدت زمانهای 7 و 14 روز
را نشان میدهد. همان طور که مشاهده میشود خوشههای آپاتیت بر روی نانوذرات شیشه زیست فعال تشکیل شده و در تمام سطح به طور یکنواخت و پیوسته رشد پیدا کرده است.
بررسی عدم سمیت سلولی نانوذرات شیشه با آزمایش سنجش MTT :
نتایج، بیشترین حیـات سلولـی، مربـوط بـه نمونه نانوذرات شیشه زیست فعال را گزارش میدهد(شکل 3). این روند در همه فواصل زمانی مورد آزمایش بدین ترتیب بوده است. نتایج حاکی از این است که نانوذرات شیشه زیست فعال ساخته شده، هیچگونه سمیت سلولی ندارد.

شکل 1: الگوی طیفسنجی مادون قرمز(FTIR) نانو ذرات شیشه زیست فعال 5S45: قبل و بعد از غوطهوری در مایع شبیهسازی شده بدن

شکل 2: تصاویر میکروسکوب الکترونی روبشی(SEM) نانوذرات شیشه زیست فعال 5S45 a) قبل از غوطهوری در مایع شبیهسازی شده بدن
b) بعد از 7 روز غوطهوری و c) بعد از 14 روز غوطهوری
بررسی تصاویر آکریدین اورنج:
تصاویر میکروسکوپ فلورسنت از مورفولوژی سلولهای بنیادی مزانشیمی بعداز 3 روز کشت در مجاورت نمونهها در شکل ارائه شده است(شکل 4).
در این آزمون سلولهایی که مردهاند رنگ آکریدین اورنج را از خود عبور داده و دارای هسته سبز و سیتوپلاسم قرمز یا نارنجی میباشند، اما در صورتی که هسته و سیتوپلاسم کاملاً سبز باشد، سلولها زنده هستند. مطابق تصاویر مرگ سلولی رخ نداده و هسته و سیتوپلاسم سلولها کاملاً سبز میباشند. وجود این سلولها در نمونه نانوذرات شیشه بـا تراکم بالا به خوبی قابل رؤیت است(شکل b4).
3-5- بررسی نتایج آلکالین فسفاتاز:
آلکالین فسفاتاز به وسیله سلولها تولید میشود و به عنوان شاخصی جهت تفکیک سلولهای استخوانساز به کار میرود. همان طور که از نتایج شکل 5 الف مشخص است، مقدار فعالیت آلکالین فسفاتاز نمونه نانوذرات شیشه زیست فعال 5S45 ، پس از 7 و 14 روز قرارگیری در محیط تمایزی، بالاتر از نمونههای کنترل است. ایــن اختــلاف معنادار اولاً بیانگر تمایز سلولهای مزانشیمی بـه سلولهای استئوبلاست است در ثانی اثر مثبت نانوذرات شیشه در تمایز استخوان زایی سـلولهای بنیادی مزانشیمی را مشخص میکند.
3-6- بررسی نتایج رنگ آلیزارین قرمز:
رنگ آلیزارین قرمز بیانگر رسوبات کلسیم میباشد که تایید کننده حضور سلولهای استخوانی است. بیشترین مقدار رسوب کلسیم که با رنگ قرمز رنگآمیزی شده، مربوط به نمونه نانوذرات شیشه زیست فعال میباشد که حاکی از تمایز سلولهای بنیادی مزانشیمی به رده استئوبلاسـتی است(شکل a5ب). در نمونه کنترل بدون نانو ذره تمایز به مقدار کمتری انجام شده است(شکل b5ب).
تصاویر میکروسکوپ فلورسنت از مورفولوژی سلولهای بنیادی مزانشیمی بعداز 3 روز کشت در مجاورت نمونهها در شکل ارائه شده است(شکل 4).
در این آزمون سلولهایی که مردهاند رنگ آکریدین اورنج را از خود عبور داده و دارای هسته سبز و سیتوپلاسم قرمز یا نارنجی میباشند، اما در صورتی که هسته و سیتوپلاسم کاملاً سبز باشد، سلولها زنده هستند. مطابق تصاویر مرگ سلولی رخ نداده و هسته و سیتوپلاسم سلولها کاملاً سبز میباشند. وجود این سلولها در نمونه نانوذرات شیشه بـا تراکم بالا به خوبی قابل رؤیت است(شکل b4).
3-5- بررسی نتایج آلکالین فسفاتاز:
آلکالین فسفاتاز به وسیله سلولها تولید میشود و به عنوان شاخصی جهت تفکیک سلولهای استخوانساز به کار میرود. همان طور که از نتایج شکل 5 الف مشخص است، مقدار فعالیت آلکالین فسفاتاز نمونه نانوذرات شیشه زیست فعال 5S45 ، پس از 7 و 14 روز قرارگیری در محیط تمایزی، بالاتر از نمونههای کنترل است. ایــن اختــلاف معنادار اولاً بیانگر تمایز سلولهای مزانشیمی بـه سلولهای استئوبلاست است در ثانی اثر مثبت نانوذرات شیشه در تمایز استخوان زایی سـلولهای بنیادی مزانشیمی را مشخص میکند.
3-6- بررسی نتایج رنگ آلیزارین قرمز:
رنگ آلیزارین قرمز بیانگر رسوبات کلسیم میباشد که تایید کننده حضور سلولهای استخوانی است. بیشترین مقدار رسوب کلسیم که با رنگ قرمز رنگآمیزی شده، مربوط به نمونه نانوذرات شیشه زیست فعال میباشد که حاکی از تمایز سلولهای بنیادی مزانشیمی به رده استئوبلاسـتی است(شکل a5ب). در نمونه کنترل بدون نانو ذره تمایز به مقدار کمتری انجام شده است(شکل b5ب).

شکل 3: رشد و تکثیر سلولهای بنیادی مزانشیمی مغز استخوان انسان در آزمون MTT بعد از 1، 3، 5 و 7 روز قرارگیری در محیط کشت
(DMEM(h) + FBS + Pen/sterp)؛ نمونه کنترل(CN) و نانوذرات شیشه زیست فعال 5S45(BG)

شکل 4: تصاویر میکروسکوب فلورسنت از سلولهای بنیادی مزانشیمی پس از 3 روز کشت: a) نمونه کنترل و b) نانوذرات شیشه زیست فعال 5S45 (بزرگنمایی تصاویر 100 میکرون میباشد)

شکل 5 الف: فعالیت آلکالین فسفاتاز(ALP) سلولهای بنیادی مزانشیمی بعد از 7 و 14 روز قرارگیری در محیط تمایزی؛ نمونه کنترل(CN) و نانو ذرات شیشه زیست فعال 5S45 (BG). شکل 5 ب: تصاویر میکروسکوب نوری در آزمون آلیزارین قرمز(Alizarin red) از سلولهای بنیادی مزانشیمی پس از 14 روز قرارگیری در محیط تمایزی: a) نمونه کنترل و b) نانو ذرات شیشه زیست فعال 5S45 (بزرگنمایی تصاویر 100 میکرون میباشد).

شکل 6 : بیان ژنهای تمایز استخوان با استفاده از Real time-PCR : بیان نسبی ژنهای آلکالین فسفاتاز، استئوکلسین، استئونکتین، کلاژن I و Runx 2 پس از 7 و 14 روز تمایز سلولهای بنیادی مزانشیمی در مجاورت نانو ذرات شیشه زیست فعال 5S45 و نمونه کنترل. نمونه کنترل (CN) و نانو ذرات شیشه زیست فعال 5S45 (BG)
3-7- ارزیابی مقدار بیان ژن:
بیان کمی ژنهای استخوانی(آلکالین فسفاتاز، استئوکلسین، کلاژن I، استئونکتین، Runx 2) cDNA حاصل از تمایز سلولهای مزانشیمی در مجاورت نانو ذارت شیشه 5S45 و نمونه کنترل، در شکل 6 نشان داده شده است. نتایج بیان ژنها مربوط به نانوذرات شیشه در روزهای 7 و 14 تمایز نسبت به نمونه کنترل افزایش قابل ملاحظهای داشته و این در تمامی ژنهای استخوانی به غیر از Runx 2 قابل رؤیت است. این نشاندهنده اثر تحریکی نانوذرات شیشه زیست فعال در تمایز استخوانی میباشد که باعث افزایش بیان ژنها شده است.
بحث
در این پژوهش، نانو ذرات شیشه زیست فعال 5S45 به روش ذوبی ساخته و با استفاده از آسیاب سیارهای به ساختار نانو تبدیل گردید. تصاویر میکروسکوپ الکترونی روبشی و الگوی طیف سنجی مادون قرمز به ترتیب مورفولوژی و اندازه دانهها در مقیاس نانو و پیوندهای مربوط به شیشه را تایید کرد. بررسی زیست فعالی در مایع شبیهسازی شده بدن نیز تشکیل کریستالهای آپاتیت بر روی نانو ذرات را مورد تایید قرار داد. نتایج آزمایشهای سلولی صورت گرفته از قیبل: MTT ، آکریدین اورنج، آلکالین فسفاتاز و آلیزارین قرمز حاکی از عدم سمیت و تاثیر بالقوه این نانو ذرات ساخته شده در رشد و تمایز استخوانی سلولهای بنیادی مزانشیمی بود.
این روش ساخت(روش ذوبی ساخت) مشخص کرد که تبدیل ساختار میکرو شیشه زیست فعال به ساختاری در مقیاس نانو با استفاده از فرآیند آسیاب سیارهای امکانپذیر است.
در سال 2016، تئودور و همکاران نشان دادند که 5S45 میتواند به عنوان یک عامل کمککننده در تمایز استخوان مطرح باشد. اما مشکل این نانو ذره، بزرگ بودن حفرات و عدم پایداری سلول بر روی آن بود. در سال 2011 هیمانشو و همکاران نشان دادند که نانو ذره مذکور، منجر به تمایز استخوانی سلولهای بنیادی میشود. در تحقیقات صورت گرفته، این نوع شیشه را معمولاً به عنوان فاز دوم (تقویتکننده زیست فعال) در ساخت کامپوزیتها و داربستها استفاده کردهاند، تمامی این مطالعهها، شیشه 5S45 را با ساختار میکرو مورد بررسی قرار دادهاند(27-21). علاوه بر آن پژوهشی در زمینه تاثیر اندازه ذرات شیشه فوقالذکر با اندازه ذره 9-750 میکرومتر در رشد، تکثیر و تمایز سلولهای بنیادی مورد بررسی قرار گرفته است. نتایج آن ثابت کرد که هرچه اندازه ذرات ریزتر باشد، تاثیر به سزایی در رشد و تمایز سلولها خواهد داشت(28).
این مطالعه نشان داد که استفاده از نانو ذرات شیشه باعث واکنشپذیری، رشد و تمایز سلولهای بنیادی میشود. نتایج آزمایشهای ارزیابی زیست فعالی نیز مشخص کرد که نانوذرات شیشه زیست فعال ساخته شده، دارای زیست فعالی مناسب بوده به طوری که بعد از 7 روز غوطهوری در مایع شبیهسازی شده بدن، هیدورکسی آپاتیت به خوبی بر روی سطح نانوذرات تشکیل شده و با افزایش زمان غوطه وری به مدت 14 روز، توانایی زیست فعالی آنها حفظ شده است. طول موج 615-590 بر سانتیمتر مربوط به آپاتیت در نمودار شکل 4 ، صحت این موضوع را تایید میکند(32-29).
بنابراین با توجه به نتایج بررسی زیست فعالی و مشابه کارلی در سال 2004، می توان تشکیل فاز هیدروکسی آپاتیت بر روی نانوذرات شیشه فوق را چنین بیان کرد: مراحل تشکیل لایه سطحی هیدروکسیل کربنات آپاتیت (HCA) به طور کلی در سه مرحله لیچینگ، انحلال و رسوب اتفاق میافتد که شامل ایجاد لایه ژل سیلیکاتی و در ادامه هستهزایی و رشد فاز کلسیم فسفات آمورف و تبدیل آن به هیدروکسیل کربنات آپاتیت بالغ با گذشت زمان است. لیچینگ از طریق رهاشدن عناصر قلیـایی، قلیـایی خاکی و مبادله آن ها با کاتیون های H+ و H3O+ انجام مـیشـود. چنین انتشار و تبادل یونی در مدت 1 تا 7 روز غوطهوری باعث افزایش pHدر فصـل مشـترک تا مقادیر بیشتر از 4/7 میشـود اما مجدداً برای مدت 7 الی 24 روز با اشباع این یونها، pHدوباره کاهش مییابد(34-32). در انحلال، شبکه شیشه منجر به تشکیل لایه غنی از سیلیکا و در پی آن رسوب لایه شبه آپاتیتی میشود. لازمه اتصال شیشهها به استخوان، تشکیل لایهای از هیدروکسیل کربنات آپاتیت روی سطح بیومتریال است. کریستالهای هیدروکسیل کربنات آپاتیت با الیاف کلاژن تقویت شده و سپس لایه اتصالدهنده بین ماده زیست فعال و بافتهای زنده تشکیل میشود. مبنای ویژگی اتصال به استخوان شیشههای زیست فعال، واکنش شیمیایی شیشه در حضور سیالات بدن است. توالی از واکنشهای سطحی منجر به تشکیل لایه هیدروکسیل کربنات آپاتیت و پیوند ایمپلنت به بافت میشود(34-32).
نتایج آزمون MTT نیز نشان داد که بیشترین مقدار حیات سلولی مربوط به نانوذرات شیشه زیست فعال بوده است و نانوذره فوق هیچگونه سمیتی ندارد. در آزمون آکریدین اورنج نیز سلولها کاملاً سالم بودند و هیچگونه مرگ سلولی رخ نداده بود. در تصاویر، هسته سلولها سبز بودند که نشاندهنده سلولهای زنده است. نانوذرات شیشه با ایجاد محیطی با ساختارهای نانو و تبادل یونی، باعث رشد و تحریک سلولهای بنیادی مزانشیمی جهت تکثیر میشود(35).
طبق مطالعههای انجام شده نکته مهم در نانوذره زیست فعال این است که در ترکیب شیشههای زیست فعال، وجود اکسید سیلسیوم از اهمیت بالایی برخوردار است چرا که به عنوان شبکهساز در ساختار شیشه عمل میکنند به علاوه گروههای سیلانول (Si-OH) حاصل از فرآیند تبادل یونهای کلسیم(موجود در ساختار شیشه) با هیدرونیوم(H3O+)(موجود در محلول)، مستعد ایجاد مکانهایی برای جوانهزنی کلسیم فسفات هستند(37، 36).
در مطالعه پانزاولتا و همکاران در سال 2008 مشخص شده که وجود سیلسیوم رهایش یافته از ترکیب شیشه به درون محیط کشت سلول میتواند سبب افزایش فعالیت سلولی شود(39، 38). هم چنین فان و همکاران در سال 2003 نشان دادند که اکسید فسفر نیز به جوانهزنی فاز کلسیم فسفات بر روی سطح شیشه کمک میکند(40). در این پژوهش از کلسیم و سیلسیوم با تغییر فرآیند ساخت نانوذرات شیشه استفاده شد که آزمون آلیزارین قرمز تاییدکننده تمایز استخوانی بیشتر نانو ذرات شیشه نسبت به نمونه کنترل بود. طبق تصاویر میتوان این نتیجه را گرفت که نانو ذرات شیشه باعث تشکیل رسوبات کلسیم ناشی از کلسیم و فسفری که در ترکیب خود دارد میشود. رسوب کلسیم شامل ترشحات معدنی سلولهای استئوبلاست به ماتریکس خارج سلولی است و شکلگیری این رسوبات، مشخصه مرحله نهایی تمایز استخوانی است. مطالعهها نشاندهنده این است که حضور این رسوبات، شاخص خوبی از تمایز استخوانی است. این موضوع در تصاویر آلیزارین قرمز به خوبی قابل رؤیت است.
بررسی کمی مقدار بیان ژنهای استخوانی نیز از اثر تحریکی نانوذره شیشه در تمایز استئوژنیک و بیان ژنها دلالت داشت. تشکیل استخوان در سه مرحله اصلی: تمایز استئوبلاست، تشکیل ماتریکس و کانی سازی ماتریکس اتفاق میافتد. کوموری و همکاران در سال 2008 اظهار داشتند که بیان ژن آلکالین فسفاتاز در اوایل و اواسط این مرحلهها است. هم چنین این گروه در مطالعه خود نشان دادند که بیانRunx 2 در طی این سه مرحله متغیر میباشد. آنها نشان دادند کهRunx 2 یک تنظیمکننده اساسی از تمایز استئوبلاست است و در مرحله اولیه تمایز سطح بیان بالایی دارد، اما به تنهایی کافی نیست(41). با توجه به نتایج این پژوهش، میزان بیان ژن آلکالین فسفاتاز نمونه نانوذره شیشه پس از 7 روز کشت نسبت به نمونه کنترل، افزایش قابل ملاحظهای داشته، این روند در روز 14 تمایز نیز به همین صورت بود.Runx 2 پس از 7 روز کشت یعنی در مراحل اولیه بیان ژن سیر صعودی داشت اما در روزهای بعد از روز 14، این روند کاهش پیدا کرده بود. ساندرامورتی و همکاران در سال 2015 نشان دادند که ژنهای استئوکلسین و استئونکتین نقش مهمی در کانیسازی و ایجاد اولیه بلورهای کلسیم ایفا میکنند. استئوکلسین یک پروتئین غیر کلاژنی است که توسط استئوبلاستهای بالغ بیان میشود. این ترکیب از سه اسید کربوکسیگلوتامیک تشکیل شده است که به جذب کلسیم کمک میکند. استئوکلسین مسئول فرآیند استخراج استخوان است(44-42). استئونکتین یک گلیکوپروتئین است که Ca2+ را درگیر میکند، مراحل اولیه رشد کریستال را تنظیم مینماید و نقش حیاتی در کانیسازی دارد(44). در شکل سطوح بیان استئوکلسین و استئونکتین نمونه نانو ذره شیشه زیست فعال در روزهای 7 و14 تمایز نسبت به نمونه کنترل، اختلاف معناداری دارد و تقریباً به یک میزان بیان شدهاند. کلاژن I نیز نقش مهمی در بیومینرالیزاسیون دارد. این ژن نیز در روزهای 7 و14 تمایز استخوانی بیان قابل ملاحظهای داشته است.
نتیجهگیری
در این پژوهش نانوذرات شیشه زیست فعال 5S45 به روش ذوبی ساخت و با استفاده از آسیاب سیارهای به ساختار نانو تبدیل گردید. نتایج نشان داد که با غوطــهوری نانو ذرات شیشــه زیســت فعــال در مــایع شبیهسازی شده بدن، بلورهـای آپاتیـت بـر روی سـطح نانو ذرات شیشه تشکیل شده و با افزایش زمان غوطـهوری، میـزان تشـکیل ذرات آپاتیت نیز افزایش پیدا کـرده است .بررسی رشد و تکثیر سلولی نشان داد نانو ذرات شیشه زیست فعال، باعث افزایش رشد و تکثیر سلولهای بنیادی مزانشیمی میشود. علاوه بر آن، تمایز
سلولهای مزانشیمی به سلولهای استخوانی در حضور نانو ذرات شیشه افزایش پیدا کرده است. استفاده از نانو ذرات شیشه به واسطه دارا بودن عناصر زیست فعال و هم چنین افزایش نسبت سطح به حجم به دلیل ساختار نانویی، واکنشپذیری بهتر و در نتیجه، افزایش کارآیی تکثیر و تمایز سلولهای بنیادی میگردد. پس نانو ذرات شیشه ساخته شده علاوه بر آن که هیچگونه سمیتی نداشته بلکه باعث تحریک و القاء رشد سلول نیز میشود و از آن میتوان جهت درمان و بهبود سریع ضایعات استخوانی استفاده نمود.
تشکر و قدردانی
این پروژه در مرکز تحقیقات بیوتکنولوژی و میکروبیولوژی کاربردی دانشگاه علوم پزشکی بقیهاله (عج) به انجام رسیده است. از صندوق حمایت از پژوهشگران کشور و ستاد نانوتکنولوژی جهت حمایت در انجام پروژه نهایت قدردانی و تشکر به عمل میآید.
نوع مطالعه: پژوهشي |
موضوع مقاله:
سلولهاي بنيادي
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |



