جلد 14، شماره 4 - ( زمستان 1396 )
جلد 14 شماره 4 صفحات 271-261 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Yaghoubi R, Shamsasanjan K, Karimi G, Zadsar M. Evaluation of the quality of platelet components in Azarbaijan Sharghi Province: the comparison in the PSL between a blood
center and a hospital . bloodj 2017; 14 (4) :261-271
URL: http://bloodjournal.ir/article-1-1096-fa.html
URL: http://bloodjournal.ir/article-1-1096-fa.html
یعقوبی رضا، شمس اسنجان کریم، کریمی غریب، زادسر مریم. ارزیابی کیفیت فرآوردههای پلاکتی آذربایجان شرقی و مقایسه میزان تغییرات آن در پایگاه و مرکز درمانی طی دوران نگهداری. فصلنامه پژوهشی خون. 1396; 14 (4) :261-271
استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
متن کامل [PDF 432 kb]
(1529 دریافت)
| چکیده (HTML) (6163 مشاهده)
مقدمه
از دهه1950، مشاهده شده که انتقال فرآورده پلاکتی میزان مرگ و میر حاصل از خونریزی در بیماران مبتلا به لوسمی حاد را به طور چشمگیری کاهش میدهد. از آن رو استفاده از فرآوردههای پلاکتی به عنوان بخشی اساسی در درمان بیماریهای سرطانی، بدخیمیهای خونی، نقایص مغز استخوانی، پیوندهای سلول بنیادی خونساز، درمان بیماران ترومبوسایتوپنیک با خطر خونریزی و درمان بیماران با مشکلات خونریزی مربوط به جراحی و تروما پایهگذاری شد(1).
موفقیت در تزریق پلاکت به زیستپذیری، دسترسی و فعالیت هموستاتیک پلاکتهای تزریق شده در شرایط فیزیولوژیک گیرنده بستگی دارد(2). کیسههای پلاکتی تهیه شده با توجه به نحوه و شرایط نگهداری، همواره در معرض آلودگی و افت کارآیی قرار دارند به طوری که میتوانند واکنشهای ایمنی خطرناکی ایجاد کرده و از طرفی عفونتهای کشندهای هم چون عفونتهای باکتریایی را انتقال دهند.
نگهداری این فرآورده در دمای 20 تا 24 درجه سانتیگراد، با کاهش متابولیسم پایه و افزایش عمر پلاکتی، کیفیت فرآورده پلاکتی را از لحاظ تعداد به طور چشمگیری ارتقا داده است(3). لیکن همین امر باعث افزایش احتمال آلودگی این فرآورده نسبت به میکروارگانیسمها شده است. کیفیت کنسانتره پلاکتی، نقش مهمی در درمانهای حمایتی انتقال خون دارد(4). هدف از کنترل کیفی فرآوردهها، دسترسی به پتانسیل هموستاتیک کنسانترههای پلاکتی و کم کردن عوارض مربوط به آن است(1).
مطابق با استانداردهای ملی ایران، فرآوردههای پلاکتی تهیه شده از خون کامل میبایست در پایان روز نگهداری حداقل تعداد پلاکت بیشتر یا مساوی 1010 × 5/5 و pH بیشتر یا مساوی 2/6 در 90 درصد فرآوردههای مورد آزمایش را داشته باشند.
علاوه بر این موارد، طیفی از سایر آزمایشها نیز برای بررسی میزان کیفیت و عملکرد فرآوردههای پلاکتی در پژوهشها به کار گرفته میشود. هیچ کدام از این آزمایشها به طور معمول در مراکز انتقال خون انجام نمیشوند. در حال حاضر تنها مارکر سنجش کیفیت پلاکت که در بیمارستانها و مراکز درمانی در زمان تزریق انجام میشود عبارت است از بررسی ظاهری، تاریخ انقضاء و swirling پلاکت(5). در روشهای پیشرفتهتر ارزیابی کیفیت پلاکتی که در پژوهشها مورد استفاده قرار میگیرند، آزمایشهایی از قبیل اندازهگیری فعالیت پلاکتها به وسیله بیان مارکرهای CD62p و CD63 به روش فلوسیتومتری را میتوان نام برد و تعدادی روشها نیز در کنترل کیفی فرآوردههای پلاکتی انجام میگیرند که میتوان شمارشهای سلولی( پلاکت، لکوسیت، اریتروسیت)، اندازهگیری pH، و بررسی آلودگی باکتریایی به وسیله کشت را برشمرد(4). در پژوهشها در محیط آزمایشگاه، فعالیت پلاکتها به وسیله بیان CD62p و CD63 اندازه گرفته میشود که با pH و swirlingپلاکتی رابطه دارد(6). با توجه به این نکته که نحوه تهیه فرآورده پلاکتی و نیز شرایط نگهداری آن، نه تنها این محصول را بیش از سایر فرآوردههای خونی در معرض خطر آلودگی و انتقال باکتریال قرار میدهند، که کارآمدی فرآورده مذکور را نیز به چالش میکشند، لذا در مطالعه حاضر، تغییرات کیفیت فرآوردههای پلاکت تولیدی در استان آذربایجان شرقی طی دوران نگهداری در پایگاه و مرکز درمانی مورد بررسی قرار گرفت.
مواد و روشها
در یک مطالعه توصیفی از 30 نفر داوطلب اهداکننده خون، که به پایگاه منطقهای انتقال خون استان آذربایجان شرقی مراجعه نموده بودند،450 میلیلیتر خون در کیسههای سهتایی (ماکوفارما) حاوی ضد انعقاد CPDA1 (Citrate phosphate dextrose) جمعآوری گردید. کیسههای خون تهیه شده، در عرض کمتر از 1 ساعت به بخش فرآورده سازمان، انتقال یافت. ابتدا، کیسههای خون را در سانتریفیوژ (ROTO SILENTA 630 RS) قرار داده و به مدت 3 دقیقه با شتاب G2000 و در دمای 20 درجه سانتیگراد سانتریفیوژ شدند. در این مرحله به وسیله دستگاه جداکننده، پلاسمای غنی از پلاکت در کیسههای خون به کیسه جانبی با نشان پلاکت منتقل گردید و کیسههای اصلی حاوی گلبولهای قرمز فشرده به وسیله دستگاه سیلر جدا شدند. در مرحله بعد کیسههای حاوی پلاسمای غنی از پلاکت به مدت 6 دقیقه با شتاب G 5000 و در دمای 20 درجه سانتیگراد سانتریفیوژ شدند. در نهایت پس از سانتریفیوژ، پلاسمای رویی خالی از پلاکت به کیسه جانبی انتقال یافت و رسوب پلاکتی ته نشین شده به صورت فشرده و کنسانتره در کیسههای با نشان پلاکتی باقی ماند. کیسههای پلاکتی تهیه شده به مدت یک ساعت در دمای آزمایشگاه در محدوده 24-20 درجه سانتیگراد به حالت سکون قرار داده شدند تا توده پلاکتی فشرده شده درون پلاسما باز شده و به حالت سیال درآید. فرآوردههای پلاکتی تهیه شده در شرایط نگهداری محصولات پلاکتی پایگاه در دمای 24-20 درجه سانتیگراد با چرخش 60 دور در دقیقه به مدت 24 ساعت جهت انجام آزمایشهای غربالگری قرنطینه شدند. پس از حصول جواب آزمایشهای غربالگری و اطمینان از سلامت محصولات، فرآوردههای پلاکتی برچسبگذاری و آماده پخش به مراکز درمانی گردیدند. این روز به عنوان روز 1 فرآورده پلاکتی در این مطالعه در نظر گرفته شد. تعداد 30 کیسه پلاکتی به صورت تصادفی با استفاده از جدول اعداد تصادفی در روزهای مختلف در مدت سه ماه از اردیبهشت تا مرداد ماه سال 1394 انتخاب شدند. تمامی کیسههای مورد استفاده در این مطالعه، تولیدی شرکت ماکوفارما (فرانسه) با حجم 500 میلیلیتر و دو سال ماندگاری بودند. کیسههای پلاکتی انتخابی پس از اندازهگیری حجم به سه کیسه پلاکتی(1، 2، 3 ) با حجم تقریباً یکسان تقسیم شدند:
ابتدا سطح داخلی هود(BEASAT) به وسیله الکل و گاز استریل به طور کامل ضد عفونی و به مدت نیم ساعت، نور UV و سیستم تهویه هود روشن گردید. به این ترتیب محیط داخلی هود استریل و تمام عوامل مداخلهگر احتمالی موجود در محیط داخلی هود به صورت کامل پاکسازی شد.
در زیر هود و در شرایط استریل با استفاده از وسایل حفاظتی و دستکش، ابتدا ضد انعقاد موجود در کیسه سهتایی ماکوفارما از کیسه اصلی به کیسه جانبی انتقال داده
و به وسیله سیلر، کیسه جانبی جدا شد. با جداسازی کیسه
حاوی ضد انعقاد، دو کیسه خالی باقی ماند و کیسه سه تایی اولیه به کیسه دو تایی تبدیل گردید. در مرحله بعد، فرآورده پلاکتی حاوی پلاکت به خوبی مخلوط شد، سپس سوزن مخصوص کیسه دوتایی از طریق یکی از ورودیهای کیسه پلاکتی، وارد فرآورده پلاکتی گردید و دو سوم محتوای پلاکتی آن به یکی از کیسههای دوتایی منتقل و یک سوم پلاکت در فرآورده پلاکتی باقی گذاشته شد. در مرحله بعد، نصف محتوای پلاکتی موجود در کیسه دوتایی به کیسه جانبی انتقال یافت. به این ترتیب سه کیسه پلاکتی با حجم تقریباً یکسان تهیه شد. در پایان، کیسههای فرآورده پلاکتی با شمارههای 1، 2 و 3 علامتگذاری گردیدند. کیسه شماره 1 به منظور نمونهبرداری در زیر هود باقی گذاشته شد و کیسههای شماره 2 و 3 پانزده فرآورده پلاکتی در شرایط نگهداری فرآوردههای پلاکتی در پایگاه منطقهای انتقال خون آذربایجان شرقی و کیسههای شماره 2 و 3 پانزده فرآورده پلاکتی دیگر در جعبه مخصوص حمل و نقل فرآوردههای پلاکتی با دمای 20 تا 24 درجه سانتیگراد به بیمارستان قاضی تبریز ارسال و در شرایط استاندارد بیمارستان نگهداری شدند. در روزهای 1، 3 و 5 نگهداری، از فرآوردههای پلاکتی نگهداری شده در پایگاه و مرکز درمانی به ترتیب از محتوای پلاکتی داخل کیسههای 1، 2 و 3 به وسیله سرنگ در شرایط استریل و زیر هود، نمونهبرداری جهت انجام آزمایشهای کشت باکتریال، شمارش پلاکتی، شمارش گلبول سفید، MPV، اندازهگیری pH، میزان بیان مارکرهای سطحی CD62P و CD63 به ترتیب بر روی آنها صورت گرفت. به منظور ارزیابی استریلیتی فرآوردههای پلاکتی و پایداری آن طی دوران نگهداری، ابتدا در روز اول و سپس در روزهای 3 و 5 از فرآوردههای پلاکتی نمونهبرداری و به ترتیب زیر مورد بررسی قرار گرفتند: مقدار 1 میلیلیتر از فرآورده پلاکتی را به روی 10 میلیلیتر محیط مایع تایوگلیکولات افزوده و به مدت 7 روز در دمای 37 درجه سانتیگراد نگهداری شد. روزانه محیط مایع تایوگلیکولات از نظر وجود یا عدم وجود کدورت به صورت چشمی مورد بـررسی قـرار گـرفت. پـس از طـی 7 روز و مشاهده عدم
وجود کدورت در محیط مایع تایوگلیکولات، اقدامات زیر
انجام گرفت:
یک لوپ از محیط را برداشته و بر روی لام گسترش تهیه شد. با استفاده از رنگآمیزی گرم، لام تهیه شده مورد بررسی قرار گرفت. یک لوپ(10 میکرولیتر) دیگر از محیط جداگانه بر روی سه محیط بلاد آگار به صورت خطی کشت داده شد. یکی از محیطها در حضور 2CO ، یکی در شرایط هوازی و دیگری در جار بیهوازی در دمای 37 درجه سانتیگراد به مدت 48 ساعت انکوبه گردید، محیطها روزانه از نظر رشد یا عدم رشد باکتری مورد بررسی قرار گرفت.
به منظور ارزیابی pH فرآوردههای پلاکتی، ابتدا دستگاه (JENWay 3320, UK) روشن و به مدت 15 دقیقه جهت رسیدن به دمای مناسب روشن قرار داده شد. سپس دستگاه با استفاده از بافر CentiPURE با 7 pH= کالیبره و سپس میزان pH فرآوردههای پلاکتی مورد ارزیابی قرار گرفت.
جهت محاسبه شمارش پلاکتی، شمارش گلبول سفید و پارامتر MPV ، دستگاه اتوماتیک سیسمکس kx21 روشن، کالیبره و کنترل گردید. پس از اطمینان از صحت عملکرد آن، نمونهها از لحاظ میزان شمارش پلاکتی، گلبول سفید و MPV ارزیابی شدند.
به علاوه به منظور بررسی میزان فعال شدن پلاکتها در زمان نگهداری و ارزیابی تغییرات بیان مارکرهای CD62P و CD63 ، در روزهای 1، 3 و 5 مقدار 500 میکرولیتر نمونه از فرآورده پلاکتی در یک لوله پلاستیکی تمیز قرارداده شد و به منظور شستشو با 1 میلیلیتر بافر فسفاته مخلوط گردید. لوله به مدت 5 دقیقه در دور G1200 سانتریفیوژ شد. محلول رویی سوسپانسیون پلاکتی تخلیه گردید. این عمل شستشو دو بار انجام گرفت. با استفاده از 1 میلیلیتر محلول بافر 1% پارا فرم آلدئید، رسوب پلاکتی تهنشین شده به مدت 5 دقیقه در دور G1200 شستشو داده شد. محلول رویی سوسپانسیون پلاکتی تخلیه و 1 میلیلیتر بافر فسفاته اضافه گردید. سوسپانسیون حاصله به رقت 106 پلاکت در میلیلیتر رسانده شد. مقدار 50 میکرولیتر از سوسپانسیون پلاکتی در چهار لوله به صورت جداگانه قرار داده و به هر کدام از لولهها مقدار 50 میکرولیتر محلول بافر فسفاته حاوی 2% آلبومین سرم گاوی افزوده و به مدت 5 دقیقه در دمای اتاق قرار داده شد. به هر یک از لولهها به صورت جداگانه 5 میکرولیتر از آنتیبادیهای CD62P-PE ، FITC CD63 ، IgG1 PE/FITC (کنترل منفی) و CD61-PE (کنترل مثبت) افزوده و به مدت 25 دقیقه در دمای اتاق و تاریکی انکوبه شد. در پایان مقدار 700 میکرولیتر پارافرم آلدئید 5/0% به لولهها افزوده شد و سوسپانسیون فوق در دستگاه فلوسایتومتری Calibur FACS مورد ارزیابی قرار گرفت. اطلاعات مربوط به فرآوردههای پلاکتی و نتایج آزمایشها به وسیله مسترلیست گردآوری و ثبت گردید. دادههای به دست آمده از آزمایشها با استفاده از برنامه 16 SPSS آنالیزگردیدند. در این پژوهش تمامی دادهها در آزمایشهای پارامتریک با آزمون کولموگروف اسمیرنوف مورد بررسی قرار گرفتند که نتایج به دست آمده برای هر آزمایش مساوی یا بالاتر از 05/0 گزارش گردیدند. این نتایج، نشاندهنده توزیع طبیعی دادهها بودند و در نهایت از آزمون Paired-Samples T Test جهت بررسی معناداری اختـلاف نتایـج در روزهای مختلف در یک مرکز و آزمون t student در ارزیابی اختلاف میانگین پارامترهای مورد مطالعه بین دو مرکز استفاده گردید. حدود معناداری در این پژوهش نیز 05/0 p ≤ در نظر گرفته شد.
یافتهها
میانگین حجم فرآوردههای پلاکتی تولیدی پایگاه 38/56 (68-6/48) میلیلیتر به دست آمد. تمامی فرآوردههای پلاکتی در روز تولید و طی مدت نگهداری 5 روز، از لحاظ آلودگی باکتریایی منفی بودند.
فرآوردههای پلاکتی انتخابی در روز ترخیص(روز 1)، با میانگین و انحراف معیار شمارش پلاکتی در محدوده 103 × 204 ± 1179 در واحد میکرولیتر و با احتساب میانگین حجم فرآوردهها به عبارت 38/56 میلیلیتر به طور متوسط دارای 1010 × 64/6 پلاکت در کیسه بودند که مطابق با استانداردهای ملی لازم برای کیفیت فرآورده پلاکتی گزارش گردید. میـانگین و انحـراف معیار شمارش پلاکتی فرآوردههای پلاکتـی در روز سـوم 103 × 163 ± 1032 در واحد میکرولیتر و در روز پنجم با میانگین و انحراف معیار 103 × 105 ± 914 در واحد میکرولیتر بودند. با احتساب میانگین حجم، شمارش پلاکتی فرآوردهها در روز سوم به طور متوسط برابر با 1010 × 81/5 و در روز پنجم برابر با 1010 × 1/5 بود. با توجه به این نتایج، مشخص گردید فرآوردههای پلاکتی در روزهای 1 و 3 از لحاظ شمارش پلاکتی دارای شرایط استاندارد و کیفیت مناسب بودند لیکن این معیار در روز پنجم به پائینتر از حد استاندارد رسید که فاقد کیفیت تعریف شده در استاندارد ملی برای شمارش پلاکتی بود. میزان شمارش پلاکتی به موازات هم در هر دو شرایط نگهداری مرکز درمانی و پایگاه با گذشت زمان با کاهش معناداری نسبت به شمارش پلاکتی روز اول همراه بودند(001/0 p<). تفاوت معناداری بین نتایج شمارش پلاکتی دو مرکز نسبت به هم مشاهده نگردید.
شمارش لکوسیتی فرآوردههای پلاکتی در روز اول کمتر از 103 × 1 در میکرولیتر بود(جدول 1). روز 3 ، pH فرآوردههای پلاکتی نیز طی دوران نگهداری با کاهش معناداری مواجه گردیدند، لیکن در روز پنجم نیز در محدوده استاندارد تعریف شده قرار داشتند(001/0 p<). با نگهداری فرآوردههای پلاکتی در شرایط نگهداری پایگاه و
مرکز درمانی، میزان MPV در فرآوردههای پلاکتی با افزایش معناداری مواجه گردیده بود(001/0 p<) ولی تفاوت تغییرات بین پایگاه و مرکز درمانی معنادار نبود(جدول 1).
میانگین و انحراف معیار میزان بیان مارکرهای سطحی CD62P و CD63 در فرآوردههای نگهـداری شـده در مرکز درمانی و پایگاه با گذشت زمان در طی دوران نگهداری با افزایـش معنـاداری مواجـه گردیدند(001/0 p<)(جدول 2).
به طور کلی مشاهده گردید تغییرات حاصل از این بررسیها در روزهای مختلف نگهداری نسبت به هم (روز 1 با 3، روز 1 با 5 و نیز 3 با 5 ) معنادار بودند(001/0 p<). لیکن این تغییرات در شرایط نگهداری پایگاه و مرکز درمانی نسبت به هم معنادار نبودند.
در شکل 1 نمونهای از آنالیزهای فلوسایتومتری نشان داده شده است. در این نمونه میزان افزایش بیان مارکرهای CD62P وCD63 به وضوح دیده میشود که نشانگر افت کیفیت فرآوردههای پلاکتی و متعاقباً افت بازده درمانی این محصول میباشد.
جدول 1: نتایج آزمایشهای شمارش پلاکتی، شمارش لکوسیتی MPV و pH فرآوردههای پلاکتی
جدول 2: نتایج حاصل از تغییرات روز به روز میزان بیان مارکرهای CD62P و CD63 در مرکز درمانی و پایگاه.
p value برای تغییرات روزهای 1 با 3، 1 با 5، 3 با 5 برابر با بوده است(001/0 p=).
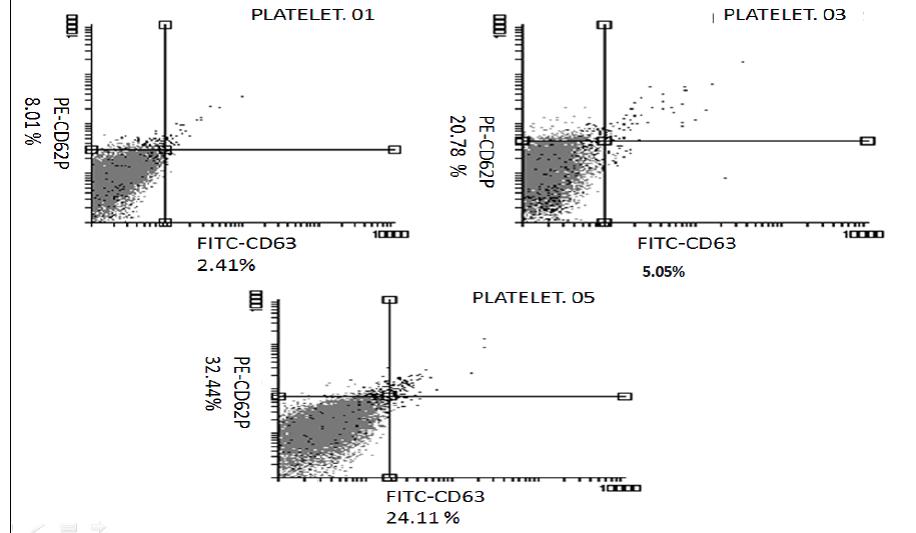
شکل1: نمونهای از آنالیزهای فلوسیتومتری بررسی میزان بیان مارکرهای CD62P وCD63
بحث
از آن جایی که کیفیت فرآوردههای پلاکتی یک ویژگی مهم در انتقال خون درمانی محسوب میگردد و اثر بخشی درمان وابسته به آن است، به علاوه پلاکتها شدیداً نسبت به شرایط ذخیرهسازی آسیبپذیرند، بنابراین نحوه نگهداری پلاکت در مراکز درمانی و انتقال خون بسیار اهمیت دارد. در این مطالعه، ارزیابی فاکتورهای کیفیت پلاکت در زمان ذخیره و نگهداری در پایگاه و مرکز درمانی نشان داد که این فرآورده در زمان تولید، کیفیت مطلوبی دارد ولی با گذشت زمان، افت کیفیت از نظر پارامترهای آلودگی باکتریال، شمارش پلاکت، شمارش گلبول سفید، MPV ، pH و بیان مارکرهای نشانگر فعالشدن پلاکتها در وضعیت نگهداری هم در پایگاه و هم در مرکز درمانی مشهود است و علیرغم این که این پارامترها در روز سوم مورد آزمایش هم چنان در محدوده استاندارد قرار داشتند، در روز پنجم شمارش پلاکتی به مقادیر پایینتر از محدوده استاندارد رسیده بود. هر چند وضعیت تغییرات کیفیت مرکز درمانی نسبت به پایگاه ارجحیت یا نقصانی نداشت و ضایعات ناشی از نگهـداری
فرآورده در این دو وضعیت اختلاف معناداری نشان ندادند.
از عوامل مؤثر بر کیفیت فرآورده پلاکت؛ pH فرآورده و شمارش گلبولهای سفید در آن است. همان طور که میدانیم فرآوردههای پلاکتی در دمای 20 تا 24 درجه سانتیگراد نگهداری میشوند که این دما منجر به افزایش تولید لاکتات به دلیل گلیکولیز و متعاقب آن افت pH میگردد. حضور گلبولهای سفید در فرآورده پلاکتی و هم چنین آلودگی باکتریایی ایجاد رقابت برای اکسیژن موجود میکنند که باعث افت سریع pH میشود(7).
سازمان دارو و غذای آمریکا(FDA) تاکید میکند که فرآوردههای خونی علاوه بر سلامت، میبایست دارای بازده درمانی مطلوب نیز باشند. مطابق استانداردهای ملی، حجم توصیه شده برای فرآوردههای پلاکتی در محدوده 70 - 40 میلیلیتر با دامنه 30 میلیلیتر قرار دارد. با عنایت بر معیار فوق، کلیه فرآوردههای پلاکتی پایگاه از نقطه نظر حجم در محدوده استاندارد قرار داشتند و از لحاظ کیفیت و کنترل کیفی مورد تائید بودند. هم چنین مطابق با استانداردهای ملی سازمان، فرآوردههای پلاکتی تولیدی پایگاه، در روز اول از نظر استریلیتی و عاری بودن از آلودگی باکتریایی سالم و دارای شرایط استاندارد گزارش شدند و این سلامت در دوران نگهداری نیز حفظ شده بود. از این لحاظ تفاوت معناداری بین پایگاه انتقال خون و مرکز درمانی مشاهده نشد. فرآوردههای پلاکتی در دمای اتاق نگهداری میشوند و بنابراین در مقایسه با سایر فرآوردههای خونی در معرض خطر بالای آلودگی باکتریایی قرار دارند. حداکثر مدت نگهداری فرآوردههای پلاکتی در مراکز بانک خون تا 5 روز میباشد.
در برخی مراکز مثل کشورهای اروپایی این مدت تا 7 روز نیز افزایش یافته است و این افزایش زمان مستلزم نظارت پس از ارسال فرآوردهها به مراکز درمانی و انجام آزمایش باکتریایی تمامی فرآوردهها میباشد. رشد باکتری در تیترهای بالای مرتبط با افزایش مدت زمان نگهداری، انجام تحقیقات بیشتر برای پیدا کردن روشهای تضمین کننده سلامت فرآوردههای پلاکتی را الزامی میسازد. طبق آمارهای سال 2016 نشان داده شده است که امروزه در هلند 44/0% کل فرآوردههای پلاکتی تولیدی آلوده میباشند (8). فرآوردههای پلاکتی در پایگاه تبریز حداکثر تا 5 روز نگهداری میشوند و فرآوردههای مورد آزمایش در این مطالعه مطابق با نتایج حاصل شده، طی مدت 5 روز عاری از آلودگی باکتریایی بودند. هر چند با توجه به تعداد نمونه آزمایش شده میتوان نتیجه گرفت که احتمال یافتن آلودگی باکتریال در این مطالعه نیز چندان بالا نبوده است. در هر صورت در این مطالعه؛ هدف بررسی شیوع آلودگی باکتریال به صورت اختصاصی را نیز دنبال نمیکرده است. در این خصوص مطالعههای بعدی با حجم نمونه بیشتر توصیه میشود.
کیفیت فرآوردههای پلاکتی تولیدی در پایگاه در روز اول، تمامی استانداردهای ملی و بینالمللی تعریف شده برای کیفیت یک محصول پلاکتی را داشتند. این کیفیت در طی دوران نگهداری افت معناداری را نشان داد به طوری که pH فرآوردهها همراه با شمارش پلاکتی به طور معناداری در روزهای سوم و پنجم کاهش یافت(001/0 p<). گفتنی است در روز پنجم، کیفیت فرآوردهها افت معناداری را هم نسبت به روز اول و هم نسبت به روز سوم نشان دادند(001/0 p<). در سال 2016 ، ماریا لوزاکورا و همکارانش فرآوردههای پلاکتی تولیدی به روش آفرزیس و بـافیکـوت را از لحـاظ pH بـه منظـور شناسایـی آلودگی
باکتریایی مورد بررسی قرار دادند. در این مطالعه، فرآوردههای پلاکتی را به 2 گروه کنترل و آزمایش تقسیم کرده و نمونه آزمایش را با یکی از 9 گونه باکتری شایع در آلودگی باکتریایی آلوده نمودند. فرآوردهها را به مدت 7 روز در دمای 24-20 درجه سانتیگراد با حرکت ملایم انکوبه کردند. پس از 7 روز مشاهده گردید میزان شدت کاهش در pH با تیتر باکتری رشد کرده رابطه مستقیم دارد. به طوری که شدت کاهش pH در فرآوردههای پلاکتی آلوده نسبت به گروه کنترل بالاتر بود(9).
با عنایت بر عدم وجود آلودگی باکتریایی و این مهم که مطابق استاندارد ملی ایران، pH فرآورده پلاکتی نباید از 2/6 کمتر شود که در این مطالعه نیز چنین بود، pH فرآوردههای پلاکتی مورد استفاده در همه روزهای پژوهش در محدوده قابل قبول قرار داشتند. فرآوردههای پلاکتی طی دوران نگهداری کاهش معناداری در شمارش لکوسیتی نشان دادند. دوران نگهداری، شمارش گلبولهای سفید را به طور معناداری تحت تاثیر قرار میدهد و باعث از بین رفتن گلبولهای سفید در فرآوردههای پلاکتی میگردد. افزایش معنادار میزان بیان مارکر سطحی CD62P که یک پروتئین غشایی وابسته به فعال شدن پلاکتهاست و CD63، طی دوران نگهداری نشاندهنده میزان فعال شدن و افت کیفیت پلاکتهای موجود در فرآوردههای پلاکتی تحت تاثیر نگهداری آنها در شرایط نگهداری پایگاه و مرکز درمانی میباشد. این تفاوتها و تغییرات به موازات هم در هر دو طرف مورد بررسی یعنی پایگاه و مرکز درمانی در مقایسه دادههای روزهای 1 با 3، 1 با 5 و 3 با 5 مشاهده شده ولیکن تفاوت معناداری بین یافتههای مرکز درمانی و پایگاه دیده نشد. این افزایش در میزان بیان مارکرهای فوق نشاندهنده افت کیفیت پلاکتها با افزایش زمان نگهداری میباشند. شرایط نگهداری و سایر عوامل مثل دما، افت pH و افزایش برخورد پلاکتها با گذشت زمان سبب فعال شدن پلاکتها و متعاقب آن افزایش بیان مارکرهای CD62P و CD63 میگردد. در مطالعهای دکتر پورفتح اله و همکاران با استفاده از 24 نمونه نشان دادند که با فعال شدن پلاکتها و افزایش بیان مولکولهای CD62P و CD63 ، توانایی عملکرد پلاکتها به صورت معناداری کاهش مییابد و باعث افت کارایی فرآوردههای پلاکتی در بیماران میشود(10).
هم چنین مطالعههای گذشته نشان دادهاند که با توجه به حجم کم پلاسمای فرآورده پلاکتی، احتمال برخورد پلاکتها با هم و شروع فرآیند فعال شدن و تجمع پلاکتی قبل از تزریق افزایش یافته، بنابراین باعث کاهش تعداد پلاکتها میگردد(11).
در ایران در سال 2015، قزلباش و همکارانش در مطالعهای مشابه تعداد 40 فرآورده پلاکتی تهیه شده به روش PRP در مراکز انتقال خون را به مدت 5 روز از لحاظ pH ، MPV ، بیان مارکر CD62P ، آلودگی باکتریایی و اگریگومتری مورد بررسی قرار دادند. نتایج حاصل نشانگر افت کیفیت پلاکتی بودند به طوری که pH فرآوردهها، مشابه مطالعه حاضر به صورت چشمگیری کاهش یافته بود. قزلباش و همکارانش نشان دادند که فرآوردههای پلاکتی تولیدی مراکز انتقال خون ایران طی مدت 5 روز نگهداری، سلامت خود را از لحاظ آلودگی باکتریایی حفظ میکنند که مشابه مطالعه حاضر میباشد (11). بیان مارکر CD62P طی مدت نگهداری در مطالعه قزلباش و همکاران با وجود اندکی افزایش مشابه یافتههای این مطالعه، تفاوت معناداری در روزهای مطالعه نسبت به هم برخلاف یافتههای مطالعه حاضر نشان نداد. افزایش بیان مارکر CD62P نشان دهنده فعال شدن پلاکتها در طی دوران نگهداری میباشد که متاثر از نحوه نگهداری، دما، شرایط حمل و نقل و بسیاری عوامل دیگر میباشد. به عبارتی میزان افزایش در بیان این مارکر رابطه مستقیمی با عوامل ذکر شده دارد. این میزان تفاوت در نتایج مطالعه قزلباش و همکاران با مطالعه حاضر نشان دهنده افت شرایط نگهداری و حمل و نقل فرآوردههای پلاکتی در پایگاه و مرکز درمانی میباشد که لزوم ارتقای شرایط موجود به منظور حصول معیارهای کیفیتی لازم در نگهداری طولانی مدت را بیش از پیش آشکار میسازد. حساسیت فرآورده پلاکتی به اندک تغییرات در شرایط لازم برای حفظ کیفیت مطلوب این فرآورده با افت فاحش و تغییرات غیر قابل جبران در کیفیت فرآورده پلاکتی روبروست. بنابراین میبایست در تامین و حفظ شرایط مطلوب نگهداری و حمل و نقل فرآورده پلاکتی نهایت دقت و حساسیت مبذول گردد. مطالعههای بعدی در مورد بهبود نحوه حمل و نقل و نگهداری فرآورده پلاکتی به منظور حفظ کیفیت آن توصیه میشود.
افزایش بیان مولکولهای CD62P و CD63 در مطالعه حاضر نشاندهنده فعال شدن پلاکتها طی دوران نگهداری و به موازات آن افت کیفیت فرآوردههای پلاکتی و کاهش بازده درمانی میباشد. در سال 2013 دکتر رحمان و همکارانش با بررسی کیفیت فرآوردههای پلاکتی طی دوران نگهداری به مدت 5 روز، با بررسی شمارش پلاکتی، شمارش گلبولهای سفید و pH، نشان دادند که تمامی پارامترها در روز اول، معیارهای استاندارد بینالمللی را دارند و این پارمترها طی دوران نگهداری به مدت 5 روز با کاهش معناداری مواجه گردیدند، لیکن این پارامترها در روز 5 نیز علیرغم این کاهش معنادار، در محدوده استاندارد بودند. این نتایج نشاندهنده این مطلب بود که شرایط نگهداری فرآوردههای پلاکتی در بیمارستان دانشگاه SAINS در مالزی به مدت 5 روز مناسب میباشد و در انتهای این مدت زمان نگهداری، همچنان محصول پلاکتی با کیفیت مناسب در دسترس است(7).
شرایط نگهداری پلاکتها با توجه به استانداردهای توصیه شده، در حفظ کیفیت و افزایش کارآیی درمانی این فرآوردهها حیاتی است؛ کاوش و بررسی دورهای و مداوم این عوامل در مراکز درمانی و پایگاههای تولید و نگهداری این فرآورده ضروری است.
پلاکتها طی دوران نگهداری از لحاظ متابولیسم فعال بوده و از دو مسیر گلیکولیز و فسفریلاسیون اکسیداتیو به منظور تولید ATP استفاده مینمایند. مسیر گلیکولیز منجر به تولید اسید لاکتیک و کاهش pH و بنابراین افت کیفیت پلاکتها میگردد لیکن مسیر فسفریلاسیون اکسیداتیو، اسید لاکتیک تولید نمیکند. از آن جایی که کیسههای امروزی مورد استفاده برای نگهداری پلاکتها به اکسیژن اجازه نفوذ میدهند، مسیر فسفریلاسیون اکسیداتیو تحریک شده و بنابراین ماندگاری پلاکتها طی دوران نگهداری افزایش مییابد(12). بدیهی است حفظ شرایط استاندارد نگهداری پلاکتها در مکان مناسب و استفاده از کیسههای پلاکتی نفوذپذیر به اکسیژن، باعث افزایش طول مدت نگهداری و هم چنین کیفیت فرآوردههای پلاکتی میشود. در این مطالعه با توجه به رعایت شرایط استاندارد نگهداری در هر دو مرکز درمانی و بیمارستان، تفاوت چندانی در نتایج حاصل از مقایسه این دو مکان دیده نشد.
با عنایت بر مدت مجاز نگهداری و تزریق فرآوردههای پلاکتی در ایران و پایگاه انتقال خون آذربایجان شرقی و بررسی مطالعههای مشابه و مقایسه پایداری کیفیت فرآوردههای پلاکتی میتوان نتیجهگیری کرد که شتاب افت کیفیتی فرآوردههای پلاکتی، در پایگاه انتقال خون آذربایجان شرقی اندکی بالاتر میباشد و این افت کیفیتی به نوبه خود منجر به افت بازده درمانی در بیماران نیز خواهد شد. در سازمانهای انتقال خون به منظور ارتقای کیفیت فرآوردههای پلاکتی و افزایش میزان پایداری آنها، اقدامات گستردهای هم چون مطالعه دکتر پورمختار در بررسی روشهای مختلف تهیه و هم در افزایش پایداری فرآوردههای پلاکتی مداخلاتی هم چون مطالعه دیهیم در بررسی تاثیر افزودن الکارنیتین به فرآوردههای پلاکتی و نیز بررسی وضعیت موجود تهیه و نگهداری آن مثل مطالعههای همدا انجام گرفته است(15-13). امید است در سازمان انتقال خون استان آذربایجان شرقی نیز با بهرهگیری از نتایج مطالعه حاضر در راستای پیگیری و بررسی
وضعیت موجود شرایط نگهداری فرآوردههای پلاکتی، کیفیت و پایداری فرآوردههای پلاکتی تولیدی این مرکز را بیش از پیش ارتقا داد.
نتیجهگیری
مطالعه کیفیت فرآوردههای پلاکتی تولیدی در پایگاه انتقال خون استان آذربایجان شرقی و شرایط نگهداری آنها در پایگاه و مرکز درمانی نشان داد که این فرآوردهها در روز تولید، تمامی استانداردهای لازم ملی را دارند و این کیفیت را تا روز سوم نگهداری حفظ میکنند و لیکن افت کیفیت فرآوردههای پلاکتی در شرایط نگهداری پایگاه و مرکز درمانی نسبتاً شتابنده است. به علاوه مشخص شد تغییرات کیفیت حاصل از شرایط نگهداری فرآوردههای پلاکتی در پایگاه انتقال خون و مرکز درمانی مشابه هم بوده و تفاوت معناداری در کیفیت فرآوردههای نگهداری شده در مرکز درمانی و پایگاه انتقال خون مشاهده نگردید.
تشکر و قدردانی
این مطالعه حاصل تلاش و همکاری ریاست محترم، پرسنل محترم بخش فرآورده و کنترل کیفی سازمان انتقال خون تبریز به ویژه خانمها محمدی، آهنگر و آقایان عبدی و عدالتخواه و هم چنین کمکهای صمیمانه و بیدریغ خانم صالح میباشد. بدینوسیله از این عزیزان و کلیه کارکنان سازمان انتقال خون تبریز تشکر و قدردانی به عمل میآید.
متن کامل: (6276 مشاهده)
ارزیابی کیفیت فرآوردههای پلاکتی آذربایجان شرقی و مقایسه میزان تغییرات آن
در پایگاه و مرکز درمانی طی دوران نگهداری
رضا یعقوبی1، کریم شمس اسنجان2، غریب کریمی3، مریم زادسر4
چکیده
سابقه و هدف
نحوه نگهداری فرآوردههای پلاکتی بر روی اثر بخشی فرآورده پلاکتی تزریقی تاثیری به سزا دارد. نحوه نگهداری فرآورده پلاکت در مراکز انتقال خون مطابق دستورالعملهای سازمان میباشد ولی اطلاع روشنی از وضعیت نگهداری آن در مراکز درمانی و میزانPSL ( platelet storage lesion) ناشی از آن در دست نیست. لذا در این تحقیق قصد داریم تا این مهم را تا روز پنجم نگهداری در شرایط پایگاه و مرکز درمانی بررسی و مقایسه نمائیم.
مواد و روشها
در این مطالعه توصیفی، 30 فرآورده پلاکتی به صورت تصادفی طی 3 ماه از اردیبهشت تا مرداد 1394 انتخاب و در شرایط نگهداری پایگاه و مرکز درمانی قرار گرفتند. آزمایشهای شمارش پلاکتی و گلبولهای سفید، MPV، pH، آلودگی باکتریایی، بیان گلیکوپروتئینهای CD62P و CD63 در روزهای 1، 3، 5 انجام گردید. نتایج ابتدا با روش کولوگروف اسمیرنوف و سپس با استفاده از روشهای آماری paired t-test و t-test مورد ارزیابی قرار گرفتند.
یافتهها
فرآوردههای پلاکتی پایگاه در روز اول تولید، با استانداردهای ملی مطابق بودند. لیکن طی نگهداری کاهش معناداری در شمارش پلاکتی، لکوسیتی و pHو افزایش معناداری درMPV و بیان مارکرهای CD62P و CD63 در هردو مرکز دیده شد(001/0p<). تفاوت بین مرکز درمانی و مرکز انتقال خون معنادار نبود.
نتیجه گیری
مطالعه حاضر نشان داد کیفیت فرآوردههای پلاکتی تولیدی تا روز سوم در محدوده استاندارد قرار داشت، لیکن در روز پنجم، از لحاظ شمارش پلاکتی در محدوده پائینتر از استاندارد قرار گرفت. تفاوت معناداری بین کیفیت فرآوردههای پلاکتی پایگاه و مرکز درمانی یافت نشد.
کلمات کلیدی: تزریق پلاکت،کنترل کیفی، پلاکتهای خون، شمارش پلاکت
تاریخ دریافت: 21/9/95
تاریخ پذیرش: 31/3/96
1- کارشناس ارشد هماتولوژی و بانک خون ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- PhD هماتولوژی آزمایشگاهی و بانک خون ـ استادیار مرکز تحقیقات خون و انکولوژی دانشگاه علوم پزشکی تبریز ـ تبریز ـ ایران
3- متخصص بیماریهای عفونی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
4- مؤلف مسئول: متخصص بیماریهای عفونی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران ـ صندوق پستی: 1157-14665
در پایگاه و مرکز درمانی طی دوران نگهداری
رضا یعقوبی1، کریم شمس اسنجان2، غریب کریمی3، مریم زادسر4
چکیده
سابقه و هدف
نحوه نگهداری فرآوردههای پلاکتی بر روی اثر بخشی فرآورده پلاکتی تزریقی تاثیری به سزا دارد. نحوه نگهداری فرآورده پلاکت در مراکز انتقال خون مطابق دستورالعملهای سازمان میباشد ولی اطلاع روشنی از وضعیت نگهداری آن در مراکز درمانی و میزانPSL ( platelet storage lesion) ناشی از آن در دست نیست. لذا در این تحقیق قصد داریم تا این مهم را تا روز پنجم نگهداری در شرایط پایگاه و مرکز درمانی بررسی و مقایسه نمائیم.
مواد و روشها
در این مطالعه توصیفی، 30 فرآورده پلاکتی به صورت تصادفی طی 3 ماه از اردیبهشت تا مرداد 1394 انتخاب و در شرایط نگهداری پایگاه و مرکز درمانی قرار گرفتند. آزمایشهای شمارش پلاکتی و گلبولهای سفید، MPV، pH، آلودگی باکتریایی، بیان گلیکوپروتئینهای CD62P و CD63 در روزهای 1، 3، 5 انجام گردید. نتایج ابتدا با روش کولوگروف اسمیرنوف و سپس با استفاده از روشهای آماری paired t-test و t-test مورد ارزیابی قرار گرفتند.
یافتهها
فرآوردههای پلاکتی پایگاه در روز اول تولید، با استانداردهای ملی مطابق بودند. لیکن طی نگهداری کاهش معناداری در شمارش پلاکتی، لکوسیتی و pHو افزایش معناداری درMPV و بیان مارکرهای CD62P و CD63 در هردو مرکز دیده شد(001/0p<). تفاوت بین مرکز درمانی و مرکز انتقال خون معنادار نبود.
نتیجه گیری
مطالعه حاضر نشان داد کیفیت فرآوردههای پلاکتی تولیدی تا روز سوم در محدوده استاندارد قرار داشت، لیکن در روز پنجم، از لحاظ شمارش پلاکتی در محدوده پائینتر از استاندارد قرار گرفت. تفاوت معناداری بین کیفیت فرآوردههای پلاکتی پایگاه و مرکز درمانی یافت نشد.
کلمات کلیدی: تزریق پلاکت،کنترل کیفی، پلاکتهای خون، شمارش پلاکت
تاریخ دریافت: 21/9/95
تاریخ پذیرش: 31/3/96
1- کارشناس ارشد هماتولوژی و بانک خون ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- PhD هماتولوژی آزمایشگاهی و بانک خون ـ استادیار مرکز تحقیقات خون و انکولوژی دانشگاه علوم پزشکی تبریز ـ تبریز ـ ایران
3- متخصص بیماریهای عفونی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
4- مؤلف مسئول: متخصص بیماریهای عفونی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران ـ صندوق پستی: 1157-14665
مقدمه
از دهه1950، مشاهده شده که انتقال فرآورده پلاکتی میزان مرگ و میر حاصل از خونریزی در بیماران مبتلا به لوسمی حاد را به طور چشمگیری کاهش میدهد. از آن رو استفاده از فرآوردههای پلاکتی به عنوان بخشی اساسی در درمان بیماریهای سرطانی، بدخیمیهای خونی، نقایص مغز استخوانی، پیوندهای سلول بنیادی خونساز، درمان بیماران ترومبوسایتوپنیک با خطر خونریزی و درمان بیماران با مشکلات خونریزی مربوط به جراحی و تروما پایهگذاری شد(1).
موفقیت در تزریق پلاکت به زیستپذیری، دسترسی و فعالیت هموستاتیک پلاکتهای تزریق شده در شرایط فیزیولوژیک گیرنده بستگی دارد(2). کیسههای پلاکتی تهیه شده با توجه به نحوه و شرایط نگهداری، همواره در معرض آلودگی و افت کارآیی قرار دارند به طوری که میتوانند واکنشهای ایمنی خطرناکی ایجاد کرده و از طرفی عفونتهای کشندهای هم چون عفونتهای باکتریایی را انتقال دهند.
نگهداری این فرآورده در دمای 20 تا 24 درجه سانتیگراد، با کاهش متابولیسم پایه و افزایش عمر پلاکتی، کیفیت فرآورده پلاکتی را از لحاظ تعداد به طور چشمگیری ارتقا داده است(3). لیکن همین امر باعث افزایش احتمال آلودگی این فرآورده نسبت به میکروارگانیسمها شده است. کیفیت کنسانتره پلاکتی، نقش مهمی در درمانهای حمایتی انتقال خون دارد(4). هدف از کنترل کیفی فرآوردهها، دسترسی به پتانسیل هموستاتیک کنسانترههای پلاکتی و کم کردن عوارض مربوط به آن است(1).
مطابق با استانداردهای ملی ایران، فرآوردههای پلاکتی تهیه شده از خون کامل میبایست در پایان روز نگهداری حداقل تعداد پلاکت بیشتر یا مساوی 1010 × 5/5 و pH بیشتر یا مساوی 2/6 در 90 درصد فرآوردههای مورد آزمایش را داشته باشند.
علاوه بر این موارد، طیفی از سایر آزمایشها نیز برای بررسی میزان کیفیت و عملکرد فرآوردههای پلاکتی در پژوهشها به کار گرفته میشود. هیچ کدام از این آزمایشها به طور معمول در مراکز انتقال خون انجام نمیشوند. در حال حاضر تنها مارکر سنجش کیفیت پلاکت که در بیمارستانها و مراکز درمانی در زمان تزریق انجام میشود عبارت است از بررسی ظاهری، تاریخ انقضاء و swirling پلاکت(5). در روشهای پیشرفتهتر ارزیابی کیفیت پلاکتی که در پژوهشها مورد استفاده قرار میگیرند، آزمایشهایی از قبیل اندازهگیری فعالیت پلاکتها به وسیله بیان مارکرهای CD62p و CD63 به روش فلوسیتومتری را میتوان نام برد و تعدادی روشها نیز در کنترل کیفی فرآوردههای پلاکتی انجام میگیرند که میتوان شمارشهای سلولی( پلاکت، لکوسیت، اریتروسیت)، اندازهگیری pH، و بررسی آلودگی باکتریایی به وسیله کشت را برشمرد(4). در پژوهشها در محیط آزمایشگاه، فعالیت پلاکتها به وسیله بیان CD62p و CD63 اندازه گرفته میشود که با pH و swirlingپلاکتی رابطه دارد(6). با توجه به این نکته که نحوه تهیه فرآورده پلاکتی و نیز شرایط نگهداری آن، نه تنها این محصول را بیش از سایر فرآوردههای خونی در معرض خطر آلودگی و انتقال باکتریال قرار میدهند، که کارآمدی فرآورده مذکور را نیز به چالش میکشند، لذا در مطالعه حاضر، تغییرات کیفیت فرآوردههای پلاکت تولیدی در استان آذربایجان شرقی طی دوران نگهداری در پایگاه و مرکز درمانی مورد بررسی قرار گرفت.
مواد و روشها
در یک مطالعه توصیفی از 30 نفر داوطلب اهداکننده خون، که به پایگاه منطقهای انتقال خون استان آذربایجان شرقی مراجعه نموده بودند،450 میلیلیتر خون در کیسههای سهتایی (ماکوفارما) حاوی ضد انعقاد CPDA1 (Citrate phosphate dextrose) جمعآوری گردید. کیسههای خون تهیه شده، در عرض کمتر از 1 ساعت به بخش فرآورده سازمان، انتقال یافت. ابتدا، کیسههای خون را در سانتریفیوژ (ROTO SILENTA 630 RS) قرار داده و به مدت 3 دقیقه با شتاب G2000 و در دمای 20 درجه سانتیگراد سانتریفیوژ شدند. در این مرحله به وسیله دستگاه جداکننده، پلاسمای غنی از پلاکت در کیسههای خون به کیسه جانبی با نشان پلاکت منتقل گردید و کیسههای اصلی حاوی گلبولهای قرمز فشرده به وسیله دستگاه سیلر جدا شدند. در مرحله بعد کیسههای حاوی پلاسمای غنی از پلاکت به مدت 6 دقیقه با شتاب G 5000 و در دمای 20 درجه سانتیگراد سانتریفیوژ شدند. در نهایت پس از سانتریفیوژ، پلاسمای رویی خالی از پلاکت به کیسه جانبی انتقال یافت و رسوب پلاکتی ته نشین شده به صورت فشرده و کنسانتره در کیسههای با نشان پلاکتی باقی ماند. کیسههای پلاکتی تهیه شده به مدت یک ساعت در دمای آزمایشگاه در محدوده 24-20 درجه سانتیگراد به حالت سکون قرار داده شدند تا توده پلاکتی فشرده شده درون پلاسما باز شده و به حالت سیال درآید. فرآوردههای پلاکتی تهیه شده در شرایط نگهداری محصولات پلاکتی پایگاه در دمای 24-20 درجه سانتیگراد با چرخش 60 دور در دقیقه به مدت 24 ساعت جهت انجام آزمایشهای غربالگری قرنطینه شدند. پس از حصول جواب آزمایشهای غربالگری و اطمینان از سلامت محصولات، فرآوردههای پلاکتی برچسبگذاری و آماده پخش به مراکز درمانی گردیدند. این روز به عنوان روز 1 فرآورده پلاکتی در این مطالعه در نظر گرفته شد. تعداد 30 کیسه پلاکتی به صورت تصادفی با استفاده از جدول اعداد تصادفی در روزهای مختلف در مدت سه ماه از اردیبهشت تا مرداد ماه سال 1394 انتخاب شدند. تمامی کیسههای مورد استفاده در این مطالعه، تولیدی شرکت ماکوفارما (فرانسه) با حجم 500 میلیلیتر و دو سال ماندگاری بودند. کیسههای پلاکتی انتخابی پس از اندازهگیری حجم به سه کیسه پلاکتی(1، 2، 3 ) با حجم تقریباً یکسان تقسیم شدند:
ابتدا سطح داخلی هود(BEASAT) به وسیله الکل و گاز استریل به طور کامل ضد عفونی و به مدت نیم ساعت، نور UV و سیستم تهویه هود روشن گردید. به این ترتیب محیط داخلی هود استریل و تمام عوامل مداخلهگر احتمالی موجود در محیط داخلی هود به صورت کامل پاکسازی شد.
در زیر هود و در شرایط استریل با استفاده از وسایل حفاظتی و دستکش، ابتدا ضد انعقاد موجود در کیسه سهتایی ماکوفارما از کیسه اصلی به کیسه جانبی انتقال داده
و به وسیله سیلر، کیسه جانبی جدا شد. با جداسازی کیسه
حاوی ضد انعقاد، دو کیسه خالی باقی ماند و کیسه سه تایی اولیه به کیسه دو تایی تبدیل گردید. در مرحله بعد، فرآورده پلاکتی حاوی پلاکت به خوبی مخلوط شد، سپس سوزن مخصوص کیسه دوتایی از طریق یکی از ورودیهای کیسه پلاکتی، وارد فرآورده پلاکتی گردید و دو سوم محتوای پلاکتی آن به یکی از کیسههای دوتایی منتقل و یک سوم پلاکت در فرآورده پلاکتی باقی گذاشته شد. در مرحله بعد، نصف محتوای پلاکتی موجود در کیسه دوتایی به کیسه جانبی انتقال یافت. به این ترتیب سه کیسه پلاکتی با حجم تقریباً یکسان تهیه شد. در پایان، کیسههای فرآورده پلاکتی با شمارههای 1، 2 و 3 علامتگذاری گردیدند. کیسه شماره 1 به منظور نمونهبرداری در زیر هود باقی گذاشته شد و کیسههای شماره 2 و 3 پانزده فرآورده پلاکتی در شرایط نگهداری فرآوردههای پلاکتی در پایگاه منطقهای انتقال خون آذربایجان شرقی و کیسههای شماره 2 و 3 پانزده فرآورده پلاکتی دیگر در جعبه مخصوص حمل و نقل فرآوردههای پلاکتی با دمای 20 تا 24 درجه سانتیگراد به بیمارستان قاضی تبریز ارسال و در شرایط استاندارد بیمارستان نگهداری شدند. در روزهای 1، 3 و 5 نگهداری، از فرآوردههای پلاکتی نگهداری شده در پایگاه و مرکز درمانی به ترتیب از محتوای پلاکتی داخل کیسههای 1، 2 و 3 به وسیله سرنگ در شرایط استریل و زیر هود، نمونهبرداری جهت انجام آزمایشهای کشت باکتریال، شمارش پلاکتی، شمارش گلبول سفید، MPV، اندازهگیری pH، میزان بیان مارکرهای سطحی CD62P و CD63 به ترتیب بر روی آنها صورت گرفت. به منظور ارزیابی استریلیتی فرآوردههای پلاکتی و پایداری آن طی دوران نگهداری، ابتدا در روز اول و سپس در روزهای 3 و 5 از فرآوردههای پلاکتی نمونهبرداری و به ترتیب زیر مورد بررسی قرار گرفتند: مقدار 1 میلیلیتر از فرآورده پلاکتی را به روی 10 میلیلیتر محیط مایع تایوگلیکولات افزوده و به مدت 7 روز در دمای 37 درجه سانتیگراد نگهداری شد. روزانه محیط مایع تایوگلیکولات از نظر وجود یا عدم وجود کدورت به صورت چشمی مورد بـررسی قـرار گـرفت. پـس از طـی 7 روز و مشاهده عدم
وجود کدورت در محیط مایع تایوگلیکولات، اقدامات زیر
انجام گرفت:
یک لوپ از محیط را برداشته و بر روی لام گسترش تهیه شد. با استفاده از رنگآمیزی گرم، لام تهیه شده مورد بررسی قرار گرفت. یک لوپ(10 میکرولیتر) دیگر از محیط جداگانه بر روی سه محیط بلاد آگار به صورت خطی کشت داده شد. یکی از محیطها در حضور 2CO ، یکی در شرایط هوازی و دیگری در جار بیهوازی در دمای 37 درجه سانتیگراد به مدت 48 ساعت انکوبه گردید، محیطها روزانه از نظر رشد یا عدم رشد باکتری مورد بررسی قرار گرفت.
به منظور ارزیابی pH فرآوردههای پلاکتی، ابتدا دستگاه (JENWay 3320, UK) روشن و به مدت 15 دقیقه جهت رسیدن به دمای مناسب روشن قرار داده شد. سپس دستگاه با استفاده از بافر CentiPURE با 7 pH= کالیبره و سپس میزان pH فرآوردههای پلاکتی مورد ارزیابی قرار گرفت.
جهت محاسبه شمارش پلاکتی، شمارش گلبول سفید و پارامتر MPV ، دستگاه اتوماتیک سیسمکس kx21 روشن، کالیبره و کنترل گردید. پس از اطمینان از صحت عملکرد آن، نمونهها از لحاظ میزان شمارش پلاکتی، گلبول سفید و MPV ارزیابی شدند.
به علاوه به منظور بررسی میزان فعال شدن پلاکتها در زمان نگهداری و ارزیابی تغییرات بیان مارکرهای CD62P و CD63 ، در روزهای 1، 3 و 5 مقدار 500 میکرولیتر نمونه از فرآورده پلاکتی در یک لوله پلاستیکی تمیز قرارداده شد و به منظور شستشو با 1 میلیلیتر بافر فسفاته مخلوط گردید. لوله به مدت 5 دقیقه در دور G1200 سانتریفیوژ شد. محلول رویی سوسپانسیون پلاکتی تخلیه گردید. این عمل شستشو دو بار انجام گرفت. با استفاده از 1 میلیلیتر محلول بافر 1% پارا فرم آلدئید، رسوب پلاکتی تهنشین شده به مدت 5 دقیقه در دور G1200 شستشو داده شد. محلول رویی سوسپانسیون پلاکتی تخلیه و 1 میلیلیتر بافر فسفاته اضافه گردید. سوسپانسیون حاصله به رقت 106 پلاکت در میلیلیتر رسانده شد. مقدار 50 میکرولیتر از سوسپانسیون پلاکتی در چهار لوله به صورت جداگانه قرار داده و به هر کدام از لولهها مقدار 50 میکرولیتر محلول بافر فسفاته حاوی 2% آلبومین سرم گاوی افزوده و به مدت 5 دقیقه در دمای اتاق قرار داده شد. به هر یک از لولهها به صورت جداگانه 5 میکرولیتر از آنتیبادیهای CD62P-PE ، FITC CD63 ، IgG1 PE/FITC (کنترل منفی) و CD61-PE (کنترل مثبت) افزوده و به مدت 25 دقیقه در دمای اتاق و تاریکی انکوبه شد. در پایان مقدار 700 میکرولیتر پارافرم آلدئید 5/0% به لولهها افزوده شد و سوسپانسیون فوق در دستگاه فلوسایتومتری Calibur FACS مورد ارزیابی قرار گرفت. اطلاعات مربوط به فرآوردههای پلاکتی و نتایج آزمایشها به وسیله مسترلیست گردآوری و ثبت گردید. دادههای به دست آمده از آزمایشها با استفاده از برنامه 16 SPSS آنالیزگردیدند. در این پژوهش تمامی دادهها در آزمایشهای پارامتریک با آزمون کولموگروف اسمیرنوف مورد بررسی قرار گرفتند که نتایج به دست آمده برای هر آزمایش مساوی یا بالاتر از 05/0 گزارش گردیدند. این نتایج، نشاندهنده توزیع طبیعی دادهها بودند و در نهایت از آزمون Paired-Samples T Test جهت بررسی معناداری اختـلاف نتایـج در روزهای مختلف در یک مرکز و آزمون t student در ارزیابی اختلاف میانگین پارامترهای مورد مطالعه بین دو مرکز استفاده گردید. حدود معناداری در این پژوهش نیز 05/0 p ≤ در نظر گرفته شد.
یافتهها
میانگین حجم فرآوردههای پلاکتی تولیدی پایگاه 38/56 (68-6/48) میلیلیتر به دست آمد. تمامی فرآوردههای پلاکتی در روز تولید و طی مدت نگهداری 5 روز، از لحاظ آلودگی باکتریایی منفی بودند.
فرآوردههای پلاکتی انتخابی در روز ترخیص(روز 1)، با میانگین و انحراف معیار شمارش پلاکتی در محدوده 103 × 204 ± 1179 در واحد میکرولیتر و با احتساب میانگین حجم فرآوردهها به عبارت 38/56 میلیلیتر به طور متوسط دارای 1010 × 64/6 پلاکت در کیسه بودند که مطابق با استانداردهای ملی لازم برای کیفیت فرآورده پلاکتی گزارش گردید. میـانگین و انحـراف معیار شمارش پلاکتی فرآوردههای پلاکتـی در روز سـوم 103 × 163 ± 1032 در واحد میکرولیتر و در روز پنجم با میانگین و انحراف معیار 103 × 105 ± 914 در واحد میکرولیتر بودند. با احتساب میانگین حجم، شمارش پلاکتی فرآوردهها در روز سوم به طور متوسط برابر با 1010 × 81/5 و در روز پنجم برابر با 1010 × 1/5 بود. با توجه به این نتایج، مشخص گردید فرآوردههای پلاکتی در روزهای 1 و 3 از لحاظ شمارش پلاکتی دارای شرایط استاندارد و کیفیت مناسب بودند لیکن این معیار در روز پنجم به پائینتر از حد استاندارد رسید که فاقد کیفیت تعریف شده در استاندارد ملی برای شمارش پلاکتی بود. میزان شمارش پلاکتی به موازات هم در هر دو شرایط نگهداری مرکز درمانی و پایگاه با گذشت زمان با کاهش معناداری نسبت به شمارش پلاکتی روز اول همراه بودند(001/0 p<). تفاوت معناداری بین نتایج شمارش پلاکتی دو مرکز نسبت به هم مشاهده نگردید.
شمارش لکوسیتی فرآوردههای پلاکتی در روز اول کمتر از 103 × 1 در میکرولیتر بود(جدول 1). روز 3 ، pH فرآوردههای پلاکتی نیز طی دوران نگهداری با کاهش معناداری مواجه گردیدند، لیکن در روز پنجم نیز در محدوده استاندارد تعریف شده قرار داشتند(001/0 p<). با نگهداری فرآوردههای پلاکتی در شرایط نگهداری پایگاه و
مرکز درمانی، میزان MPV در فرآوردههای پلاکتی با افزایش معناداری مواجه گردیده بود(001/0 p<) ولی تفاوت تغییرات بین پایگاه و مرکز درمانی معنادار نبود(جدول 1).
میانگین و انحراف معیار میزان بیان مارکرهای سطحی CD62P و CD63 در فرآوردههای نگهـداری شـده در مرکز درمانی و پایگاه با گذشت زمان در طی دوران نگهداری با افزایـش معنـاداری مواجـه گردیدند(001/0 p<)(جدول 2).
به طور کلی مشاهده گردید تغییرات حاصل از این بررسیها در روزهای مختلف نگهداری نسبت به هم (روز 1 با 3، روز 1 با 5 و نیز 3 با 5 ) معنادار بودند(001/0 p<). لیکن این تغییرات در شرایط نگهداری پایگاه و مرکز درمانی نسبت به هم معنادار نبودند.
در شکل 1 نمونهای از آنالیزهای فلوسایتومتری نشان داده شده است. در این نمونه میزان افزایش بیان مارکرهای CD62P وCD63 به وضوح دیده میشود که نشانگر افت کیفیت فرآوردههای پلاکتی و متعاقباً افت بازده درمانی این محصول میباشد.
جدول 1: نتایج آزمایشهای شمارش پلاکتی، شمارش لکوسیتی MPV و pH فرآوردههای پلاکتی
| روز 1 | روز 3 | روز 5 | ||||
| پایگاه | مرکز درمانی | پایگاه | مرکز درمانی | پایگاه | مرکز درمانی | |
| شمارش پلاکتی × 103 در µL | 219 ± 1156 | 193 ± 1202 | 170 ± 1042 | 162 ± 1021 | 137 ± 936 | 164 ± 914 |
| شمارش لکوسیتی × 103 در µL | 42/0 ± 8/0 | 30/0 ± 8/0 | 26/0 ± 58/0 | 26/0 ± 56/0 | 25/0 ± 52/0 | 16/0 ± 44/0 |
| MPV | 1/1 ± 06/8 | 57/0 ± 53/7 | 17/1 ± 36/8 | 65/0 ± 84/7 | 26/1 ± 76/8 | 03/1 ± 39/8 |
| pH | 14/0 ± 51/7 | 11/0 ± 45/7 | 14/0 ± 38/7 | 21/0 ± 32/7 | 17/0 ± 95/6 | 18/0 ± 89/6 |
جدول 2: نتایج حاصل از تغییرات روز به روز میزان بیان مارکرهای CD62P و CD63 در مرکز درمانی و پایگاه.
p value برای تغییرات روزهای 1 با 3، 1 با 5، 3 با 5 برابر با بوده است(001/0 p=).
| روز 1 | روز 3 | روز 5 | ||||
| پایگاه | مرکز درمانی | پایگاه | مرکز درمانی | پایگاه | مرکز درمانی | |
| CD62P | 66/3 ± 04/12 | 45/2 ± 28/10 | 41/2 ± 43/18 | 17/8 ± 65/16 | 38/7 ± 49/33 | 74/8 ± 28/26 |
| CD63 | 84/1 ± 24/3 | 59/1 ± 04/3 | 24/5 ± 23/6 | 47/4 ± 63/7 | 55/12 ± 58/27 | 90/1 ± 51/18 |

شکل1: نمونهای از آنالیزهای فلوسیتومتری بررسی میزان بیان مارکرهای CD62P وCD63
بحث
از آن جایی که کیفیت فرآوردههای پلاکتی یک ویژگی مهم در انتقال خون درمانی محسوب میگردد و اثر بخشی درمان وابسته به آن است، به علاوه پلاکتها شدیداً نسبت به شرایط ذخیرهسازی آسیبپذیرند، بنابراین نحوه نگهداری پلاکت در مراکز درمانی و انتقال خون بسیار اهمیت دارد. در این مطالعه، ارزیابی فاکتورهای کیفیت پلاکت در زمان ذخیره و نگهداری در پایگاه و مرکز درمانی نشان داد که این فرآورده در زمان تولید، کیفیت مطلوبی دارد ولی با گذشت زمان، افت کیفیت از نظر پارامترهای آلودگی باکتریال، شمارش پلاکت، شمارش گلبول سفید، MPV ، pH و بیان مارکرهای نشانگر فعالشدن پلاکتها در وضعیت نگهداری هم در پایگاه و هم در مرکز درمانی مشهود است و علیرغم این که این پارامترها در روز سوم مورد آزمایش هم چنان در محدوده استاندارد قرار داشتند، در روز پنجم شمارش پلاکتی به مقادیر پایینتر از محدوده استاندارد رسیده بود. هر چند وضعیت تغییرات کیفیت مرکز درمانی نسبت به پایگاه ارجحیت یا نقصانی نداشت و ضایعات ناشی از نگهـداری
فرآورده در این دو وضعیت اختلاف معناداری نشان ندادند.
از عوامل مؤثر بر کیفیت فرآورده پلاکت؛ pH فرآورده و شمارش گلبولهای سفید در آن است. همان طور که میدانیم فرآوردههای پلاکتی در دمای 20 تا 24 درجه سانتیگراد نگهداری میشوند که این دما منجر به افزایش تولید لاکتات به دلیل گلیکولیز و متعاقب آن افت pH میگردد. حضور گلبولهای سفید در فرآورده پلاکتی و هم چنین آلودگی باکتریایی ایجاد رقابت برای اکسیژن موجود میکنند که باعث افت سریع pH میشود(7).
سازمان دارو و غذای آمریکا(FDA) تاکید میکند که فرآوردههای خونی علاوه بر سلامت، میبایست دارای بازده درمانی مطلوب نیز باشند. مطابق استانداردهای ملی، حجم توصیه شده برای فرآوردههای پلاکتی در محدوده 70 - 40 میلیلیتر با دامنه 30 میلیلیتر قرار دارد. با عنایت بر معیار فوق، کلیه فرآوردههای پلاکتی پایگاه از نقطه نظر حجم در محدوده استاندارد قرار داشتند و از لحاظ کیفیت و کنترل کیفی مورد تائید بودند. هم چنین مطابق با استانداردهای ملی سازمان، فرآوردههای پلاکتی تولیدی پایگاه، در روز اول از نظر استریلیتی و عاری بودن از آلودگی باکتریایی سالم و دارای شرایط استاندارد گزارش شدند و این سلامت در دوران نگهداری نیز حفظ شده بود. از این لحاظ تفاوت معناداری بین پایگاه انتقال خون و مرکز درمانی مشاهده نشد. فرآوردههای پلاکتی در دمای اتاق نگهداری میشوند و بنابراین در مقایسه با سایر فرآوردههای خونی در معرض خطر بالای آلودگی باکتریایی قرار دارند. حداکثر مدت نگهداری فرآوردههای پلاکتی در مراکز بانک خون تا 5 روز میباشد.
در برخی مراکز مثل کشورهای اروپایی این مدت تا 7 روز نیز افزایش یافته است و این افزایش زمان مستلزم نظارت پس از ارسال فرآوردهها به مراکز درمانی و انجام آزمایش باکتریایی تمامی فرآوردهها میباشد. رشد باکتری در تیترهای بالای مرتبط با افزایش مدت زمان نگهداری، انجام تحقیقات بیشتر برای پیدا کردن روشهای تضمین کننده سلامت فرآوردههای پلاکتی را الزامی میسازد. طبق آمارهای سال 2016 نشان داده شده است که امروزه در هلند 44/0% کل فرآوردههای پلاکتی تولیدی آلوده میباشند (8). فرآوردههای پلاکتی در پایگاه تبریز حداکثر تا 5 روز نگهداری میشوند و فرآوردههای مورد آزمایش در این مطالعه مطابق با نتایج حاصل شده، طی مدت 5 روز عاری از آلودگی باکتریایی بودند. هر چند با توجه به تعداد نمونه آزمایش شده میتوان نتیجه گرفت که احتمال یافتن آلودگی باکتریال در این مطالعه نیز چندان بالا نبوده است. در هر صورت در این مطالعه؛ هدف بررسی شیوع آلودگی باکتریال به صورت اختصاصی را نیز دنبال نمیکرده است. در این خصوص مطالعههای بعدی با حجم نمونه بیشتر توصیه میشود.
کیفیت فرآوردههای پلاکتی تولیدی در پایگاه در روز اول، تمامی استانداردهای ملی و بینالمللی تعریف شده برای کیفیت یک محصول پلاکتی را داشتند. این کیفیت در طی دوران نگهداری افت معناداری را نشان داد به طوری که pH فرآوردهها همراه با شمارش پلاکتی به طور معناداری در روزهای سوم و پنجم کاهش یافت(001/0 p<). گفتنی است در روز پنجم، کیفیت فرآوردهها افت معناداری را هم نسبت به روز اول و هم نسبت به روز سوم نشان دادند(001/0 p<). در سال 2016 ، ماریا لوزاکورا و همکارانش فرآوردههای پلاکتی تولیدی به روش آفرزیس و بـافیکـوت را از لحـاظ pH بـه منظـور شناسایـی آلودگی
باکتریایی مورد بررسی قرار دادند. در این مطالعه، فرآوردههای پلاکتی را به 2 گروه کنترل و آزمایش تقسیم کرده و نمونه آزمایش را با یکی از 9 گونه باکتری شایع در آلودگی باکتریایی آلوده نمودند. فرآوردهها را به مدت 7 روز در دمای 24-20 درجه سانتیگراد با حرکت ملایم انکوبه کردند. پس از 7 روز مشاهده گردید میزان شدت کاهش در pH با تیتر باکتری رشد کرده رابطه مستقیم دارد. به طوری که شدت کاهش pH در فرآوردههای پلاکتی آلوده نسبت به گروه کنترل بالاتر بود(9).
با عنایت بر عدم وجود آلودگی باکتریایی و این مهم که مطابق استاندارد ملی ایران، pH فرآورده پلاکتی نباید از 2/6 کمتر شود که در این مطالعه نیز چنین بود، pH فرآوردههای پلاکتی مورد استفاده در همه روزهای پژوهش در محدوده قابل قبول قرار داشتند. فرآوردههای پلاکتی طی دوران نگهداری کاهش معناداری در شمارش لکوسیتی نشان دادند. دوران نگهداری، شمارش گلبولهای سفید را به طور معناداری تحت تاثیر قرار میدهد و باعث از بین رفتن گلبولهای سفید در فرآوردههای پلاکتی میگردد. افزایش معنادار میزان بیان مارکر سطحی CD62P که یک پروتئین غشایی وابسته به فعال شدن پلاکتهاست و CD63، طی دوران نگهداری نشاندهنده میزان فعال شدن و افت کیفیت پلاکتهای موجود در فرآوردههای پلاکتی تحت تاثیر نگهداری آنها در شرایط نگهداری پایگاه و مرکز درمانی میباشد. این تفاوتها و تغییرات به موازات هم در هر دو طرف مورد بررسی یعنی پایگاه و مرکز درمانی در مقایسه دادههای روزهای 1 با 3، 1 با 5 و 3 با 5 مشاهده شده ولیکن تفاوت معناداری بین یافتههای مرکز درمانی و پایگاه دیده نشد. این افزایش در میزان بیان مارکرهای فوق نشاندهنده افت کیفیت پلاکتها با افزایش زمان نگهداری میباشند. شرایط نگهداری و سایر عوامل مثل دما، افت pH و افزایش برخورد پلاکتها با گذشت زمان سبب فعال شدن پلاکتها و متعاقب آن افزایش بیان مارکرهای CD62P و CD63 میگردد. در مطالعهای دکتر پورفتح اله و همکاران با استفاده از 24 نمونه نشان دادند که با فعال شدن پلاکتها و افزایش بیان مولکولهای CD62P و CD63 ، توانایی عملکرد پلاکتها به صورت معناداری کاهش مییابد و باعث افت کارایی فرآوردههای پلاکتی در بیماران میشود(10).
هم چنین مطالعههای گذشته نشان دادهاند که با توجه به حجم کم پلاسمای فرآورده پلاکتی، احتمال برخورد پلاکتها با هم و شروع فرآیند فعال شدن و تجمع پلاکتی قبل از تزریق افزایش یافته، بنابراین باعث کاهش تعداد پلاکتها میگردد(11).
در ایران در سال 2015، قزلباش و همکارانش در مطالعهای مشابه تعداد 40 فرآورده پلاکتی تهیه شده به روش PRP در مراکز انتقال خون را به مدت 5 روز از لحاظ pH ، MPV ، بیان مارکر CD62P ، آلودگی باکتریایی و اگریگومتری مورد بررسی قرار دادند. نتایج حاصل نشانگر افت کیفیت پلاکتی بودند به طوری که pH فرآوردهها، مشابه مطالعه حاضر به صورت چشمگیری کاهش یافته بود. قزلباش و همکارانش نشان دادند که فرآوردههای پلاکتی تولیدی مراکز انتقال خون ایران طی مدت 5 روز نگهداری، سلامت خود را از لحاظ آلودگی باکتریایی حفظ میکنند که مشابه مطالعه حاضر میباشد (11). بیان مارکر CD62P طی مدت نگهداری در مطالعه قزلباش و همکاران با وجود اندکی افزایش مشابه یافتههای این مطالعه، تفاوت معناداری در روزهای مطالعه نسبت به هم برخلاف یافتههای مطالعه حاضر نشان نداد. افزایش بیان مارکر CD62P نشان دهنده فعال شدن پلاکتها در طی دوران نگهداری میباشد که متاثر از نحوه نگهداری، دما، شرایط حمل و نقل و بسیاری عوامل دیگر میباشد. به عبارتی میزان افزایش در بیان این مارکر رابطه مستقیمی با عوامل ذکر شده دارد. این میزان تفاوت در نتایج مطالعه قزلباش و همکاران با مطالعه حاضر نشان دهنده افت شرایط نگهداری و حمل و نقل فرآوردههای پلاکتی در پایگاه و مرکز درمانی میباشد که لزوم ارتقای شرایط موجود به منظور حصول معیارهای کیفیتی لازم در نگهداری طولانی مدت را بیش از پیش آشکار میسازد. حساسیت فرآورده پلاکتی به اندک تغییرات در شرایط لازم برای حفظ کیفیت مطلوب این فرآورده با افت فاحش و تغییرات غیر قابل جبران در کیفیت فرآورده پلاکتی روبروست. بنابراین میبایست در تامین و حفظ شرایط مطلوب نگهداری و حمل و نقل فرآورده پلاکتی نهایت دقت و حساسیت مبذول گردد. مطالعههای بعدی در مورد بهبود نحوه حمل و نقل و نگهداری فرآورده پلاکتی به منظور حفظ کیفیت آن توصیه میشود.
افزایش بیان مولکولهای CD62P و CD63 در مطالعه حاضر نشاندهنده فعال شدن پلاکتها طی دوران نگهداری و به موازات آن افت کیفیت فرآوردههای پلاکتی و کاهش بازده درمانی میباشد. در سال 2013 دکتر رحمان و همکارانش با بررسی کیفیت فرآوردههای پلاکتی طی دوران نگهداری به مدت 5 روز، با بررسی شمارش پلاکتی، شمارش گلبولهای سفید و pH، نشان دادند که تمامی پارامترها در روز اول، معیارهای استاندارد بینالمللی را دارند و این پارمترها طی دوران نگهداری به مدت 5 روز با کاهش معناداری مواجه گردیدند، لیکن این پارامترها در روز 5 نیز علیرغم این کاهش معنادار، در محدوده استاندارد بودند. این نتایج نشاندهنده این مطلب بود که شرایط نگهداری فرآوردههای پلاکتی در بیمارستان دانشگاه SAINS در مالزی به مدت 5 روز مناسب میباشد و در انتهای این مدت زمان نگهداری، همچنان محصول پلاکتی با کیفیت مناسب در دسترس است(7).
شرایط نگهداری پلاکتها با توجه به استانداردهای توصیه شده، در حفظ کیفیت و افزایش کارآیی درمانی این فرآوردهها حیاتی است؛ کاوش و بررسی دورهای و مداوم این عوامل در مراکز درمانی و پایگاههای تولید و نگهداری این فرآورده ضروری است.
پلاکتها طی دوران نگهداری از لحاظ متابولیسم فعال بوده و از دو مسیر گلیکولیز و فسفریلاسیون اکسیداتیو به منظور تولید ATP استفاده مینمایند. مسیر گلیکولیز منجر به تولید اسید لاکتیک و کاهش pH و بنابراین افت کیفیت پلاکتها میگردد لیکن مسیر فسفریلاسیون اکسیداتیو، اسید لاکتیک تولید نمیکند. از آن جایی که کیسههای امروزی مورد استفاده برای نگهداری پلاکتها به اکسیژن اجازه نفوذ میدهند، مسیر فسفریلاسیون اکسیداتیو تحریک شده و بنابراین ماندگاری پلاکتها طی دوران نگهداری افزایش مییابد(12). بدیهی است حفظ شرایط استاندارد نگهداری پلاکتها در مکان مناسب و استفاده از کیسههای پلاکتی نفوذپذیر به اکسیژن، باعث افزایش طول مدت نگهداری و هم چنین کیفیت فرآوردههای پلاکتی میشود. در این مطالعه با توجه به رعایت شرایط استاندارد نگهداری در هر دو مرکز درمانی و بیمارستان، تفاوت چندانی در نتایج حاصل از مقایسه این دو مکان دیده نشد.
با عنایت بر مدت مجاز نگهداری و تزریق فرآوردههای پلاکتی در ایران و پایگاه انتقال خون آذربایجان شرقی و بررسی مطالعههای مشابه و مقایسه پایداری کیفیت فرآوردههای پلاکتی میتوان نتیجهگیری کرد که شتاب افت کیفیتی فرآوردههای پلاکتی، در پایگاه انتقال خون آذربایجان شرقی اندکی بالاتر میباشد و این افت کیفیتی به نوبه خود منجر به افت بازده درمانی در بیماران نیز خواهد شد. در سازمانهای انتقال خون به منظور ارتقای کیفیت فرآوردههای پلاکتی و افزایش میزان پایداری آنها، اقدامات گستردهای هم چون مطالعه دکتر پورمختار در بررسی روشهای مختلف تهیه و هم در افزایش پایداری فرآوردههای پلاکتی مداخلاتی هم چون مطالعه دیهیم در بررسی تاثیر افزودن الکارنیتین به فرآوردههای پلاکتی و نیز بررسی وضعیت موجود تهیه و نگهداری آن مثل مطالعههای همدا انجام گرفته است(15-13). امید است در سازمان انتقال خون استان آذربایجان شرقی نیز با بهرهگیری از نتایج مطالعه حاضر در راستای پیگیری و بررسی
وضعیت موجود شرایط نگهداری فرآوردههای پلاکتی، کیفیت و پایداری فرآوردههای پلاکتی تولیدی این مرکز را بیش از پیش ارتقا داد.
نتیجهگیری
مطالعه کیفیت فرآوردههای پلاکتی تولیدی در پایگاه انتقال خون استان آذربایجان شرقی و شرایط نگهداری آنها در پایگاه و مرکز درمانی نشان داد که این فرآوردهها در روز تولید، تمامی استانداردهای لازم ملی را دارند و این کیفیت را تا روز سوم نگهداری حفظ میکنند و لیکن افت کیفیت فرآوردههای پلاکتی در شرایط نگهداری پایگاه و مرکز درمانی نسبتاً شتابنده است. به علاوه مشخص شد تغییرات کیفیت حاصل از شرایط نگهداری فرآوردههای پلاکتی در پایگاه انتقال خون و مرکز درمانی مشابه هم بوده و تفاوت معناداری در کیفیت فرآوردههای نگهداری شده در مرکز درمانی و پایگاه انتقال خون مشاهده نگردید.
تشکر و قدردانی
این مطالعه حاصل تلاش و همکاری ریاست محترم، پرسنل محترم بخش فرآورده و کنترل کیفی سازمان انتقال خون تبریز به ویژه خانمها محمدی، آهنگر و آقایان عبدی و عدالتخواه و هم چنین کمکهای صمیمانه و بیدریغ خانم صالح میباشد. بدینوسیله از این عزیزان و کلیه کارکنان سازمان انتقال خون تبریز تشکر و قدردانی به عمل میآید.
نوع مطالعه: پژوهشي |
موضوع مقاله:
انتقال خون
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |





