جلد 13، شماره 4 - ( زمستان 1395 )
جلد 13 شماره 4 صفحات 283-277 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Vossough Shirayeh F, Ahmadinejad M, Toogeh G, karimi K, Tabatabaei M. The results of two methods of factor VIII:C in patients with hemophilia A. bloodj 2016; 13 (4) :277-283
URL: http://bloodjournal.ir/article-1-1028-fa.html
URL: http://bloodjournal.ir/article-1-1028-fa.html
وثوق شیرایه فاطمه، احمدینژاد مینو، توگه غلامرضا، کریمی کتایون، طباطبایی محمدرضا، همایون ساناز. بررسی مقادیر فعالیت فاکتور 8 اندازهگیری شده به دو روش در بیماران هموفیلی A. فصلنامه پژوهشی خون. 1395; 13 (4) :277-283
فاطمه وثوق شیرایه 
 ، مینو احمدینژاد*
، مینو احمدینژاد* 
 ، غلامرضا توگه
، غلامرضا توگه 
 ، کتایون کریمی
، کتایون کریمی 
 ، محمدرضا طباطبایی
، محمدرضا طباطبایی 
 ، ساناز همایون
، ساناز همایون

 ، مینو احمدینژاد*
، مینو احمدینژاد* 
 ، غلامرضا توگه
، غلامرضا توگه 
 ، کتایون کریمی
، کتایون کریمی 
 ، محمدرضا طباطبایی
، محمدرضا طباطبایی 
 ، ساناز همایون
، ساناز همایون
تهران ـ ایران ـ صندوق پستی: 1157-14665
متن کامل [PDF 233 kb]
(4348 دریافت)
| چکیده (HTML) (5684 مشاهده)
مقدمه
هموفیلی A یک اختلال خونریزیدهنده وابسته به کروموزوم x مغلوب است که خصوصیت آن کاهش فعالیت انعقادی FVIII پلاسماست. تمایل به خونریزی در این بیماران با میزان فعالیت FVIII (FVIII:C) پلاسما متناسب است. شیوع هموفیلی، 1 در هر 5000 مرد گزارش شده است(3-1). طبق طبقهبندی متداول، بیماران هموفیلی A خفیف سطح FVIII بین IU/dL 40-5 ، بیماران هموفیلی A متوسط سطح FVIII بین IU/dL 5-1 و بیماران نوع شدید سطح FVIII کمتر از IU/dL 1 دارند(4). میانگین سطح FVIII در ناقلین نیز IU/dL 60 گزارش شده است. در مقایسه با بیماران نوع شدید، حوادث خونریزیدهنده در بیماران هموفیلی A خفیف شیوع کمتری دارد و به ندرت باعث همارتروزهای راجعه و در نتیجه آن آرتروپاتی میشود. نتایج اغلب آزمایشهای انعقادی غربالگری در هموفیلی A خفیف طبیعی هستند فقط احتمال دارد aPTT طولانی باشد. aPTT گاهاً طبیعی نیز خواهد شد. بنابراین هرگاه از لحاظ بالینی به هموفیلی A مشکوک باشیم حتی در صورت طولانی نبودن aPTT ، سنجش FVIII:C ضروری است(1). در حال حاضر سه روش برای اندازهگیری فعالیت FVIII پلاسما وجود دارد. روش یک مرحلهای مبتنی بر تشکیل لخته، روش دو مرحلهای مبتنی بر تشکیل لخته و روش دو مرحلهای کروموژنیک میباشد(5).
مقادیر FVIII:C اندازهگیری شده در اغلب بیماران هموفیلی A ، صرف نظر از روش سنجش به کار رفته یکسان است ولی طبق بسیاری از پژوهشهای پیشین، حدود 30% بیماران هموفیلی A خفیف و متوسط، اختلاف معناداری را در FVIII:C اندازهگیری شده با روشهای مختلف نشان میدهند(6). در این بیماران، اختلاف نتایج روش یک مرحلهای و کروموژنیک بیشتر یا مساوی دو برابر است. به این گروه از بیماران، «هموفیلی A دارای مغایرت» گفته میشود(7). موتاسیونهای ژنتیکی متعددی عنوان شده که با این مغایرتها مرتبطند. موتاسیونها باعث ایجاد پروتئینی با اختلال عملکرد میشوند(8).
اهمیــت بالینــی«مغایـرت» از آن لحـاظ اسـت کـه در
مبتلایان به هموفیلی Aدارای مغایرت ممکن است شدت بیماری به درستی تشخیص داده نشود؛ چون نتایج سنجش فعالیت FVIII آنها با روش یک مرحلهای، طبیعی یا نزدیک به محدوده طبیعی میباشد ولی در روش کروموژنیک کاهش یافته است(9). دو نوع مغایرت در نتایج وجود دارد؛ یک نوع میزان کمتر FVIII:C در روش کروموژنیک (یا دو مرحلهای) در مقایسه با روش یک مرحلهای است که بیماران الگوی خونریزی مطابق با نتایج روش کروموژنیک را نشان میدهند. نوع دیگر مغایرت، میزان کمتر FVIII:C در روش یک مرحلهای در مقایسه با روش کروموژنیک است که در این بیماران خونریزی اندکی گزارش شده است(5). مغایرت با مقادیر کمتر FVIII:C در روش کروموژنیک «مغایرت استاندارد» و مغایرت با مقادیر کمتر FVIII:C در روش یک مرحلهای، مغایرت معکوس نامیده میشود که شایعتر است(10).
با توجه به نبود گزارشی درباره میزان مغایرت در نتایج سنجش FVIII:C در بیماران هموفیلی Aخفیف/متوسط ایرانی و ضرورت تعیین دقیق FVIII:C ، در این بیماران به منظور تشخیص صحیح، پیشبینی خطر خونریزی و نیز ضرورت مدیریت استاندارد درمان این بیماران، هدف از مطالعه پیش رو تعیین میزان مغایرت در FVIII:C اندازهگیری شده به دو روش یک مرحلهای و کروموژنیک در بیماران هموفیلی A غیر شدید ایرانی بود. نتایج این مطالعه میتواند به عنوان گام ابتدایی در انتخاب و به کارگیری روشی مناسب جهت تعیین مقادیر FVIII:C در این بیماران به کار رود.
مواد و روشها
درمانگاه جامع هموفیلی مرکز تحقیقات ترومبوز و هموستاز دانشگاه علوم پزشکی تهران واقع در مجتمع بیمارستانی امام خمینی به جمعیتی بالغ بر 3234 بیمار هموفیلی خدمات درمانی ارائه میدهد که در این بین حدود 1600 بیمار ثبت نام شده، هموفیلی A نوع خفیف و متوسط هستند. بیماران هموفیلی A خفیف و متوسط ثبت شده در این مرکز، به عنوان جامعه آماری در این مطالعه توصیفی ـ مقطعی انتخاب شدند. اطلاعات بیماران از طریق بررسی آرشیو درمانگاه هموفیلی مرکز تحقیقات هموستاز و ترومبوز دانشگاه علوم پزشکی تهران جمعآوری شد. تمام بیماران با روش یک مرحلهای تشخیص داده شده بودند. با توجه به لزوم مراجعه بیماران به درمانگاه هموفیلی، از بیماران ساکن استانهای غیر از تهران و البرز به دلیل دوری مسافت، دعوت به همکاری نشد. به علاوه اطلاعات تعدادی از پروندهها نیز به روز نبود. از آن جایی که احتمال ریزش بیماران وجود داشت، 300 بیمار برای فراخوان انتخاب شدند و از تمام آنها جهت شرکت در مطالعه دعوت به عمل آمد.
85 بیمار جهت شرکت در این مطالعه اعلام آمادگی و رضایت نمودند. به بیماران توضیح داده شد که نباید از 10 روز قبل از جمعآوری نمونه خون، کنستانتره FVIII دریافت کرده باشند. علیرغم توضیحاتی که به بیماران داده شده بود؛ 7 بیمار طی 10 روز قبل از مراجعه کنستانتره FVIII دریافت کرده بودند و از مطالعه حذف شدند. بنابراین مطالعه بر روی 78 بیمار هموفیلی A غیرشدید با مقادیر FVIII بین 46%-1% (بر اساس اطلاعات موجود در پرونده) انجام شد. تمام آزمایشها با کسب مجوز اخلاق در پژوهش از معاونت پژوهشی دانشگاه علوم پزشکی تهران انجام شد. قبل از دریافت اطلاعات بالینی و نمونه خون، از تمام بیماران رضایتنامه کتبی آگاهانه جهت شرکت در این مطالعه دریافت شد.
آزمایشهای انعقادی:
آزمایشهای aPTT و mixed-aPTT بر روی تمام نمونهها با استفاده از آنالایزر تمام اتوماتیک STA-compact (دیاگنوستیکا، فرانسه) و با به کارگیری ریجنت DAPTTIN TC aPTT (تکنوکلون ـ آلمان) در همان روز نمونهگیری انجام شد. آزمایش سنجش مقدار فاکتور VIII به روش یک مرحلهای نیز با استفاده از آنالایزر فوق و همان ریجنت و پلاسمای فاقد فاکتور 8 (استاگو، فرانسه ، Immuno-depleted) برای تمام بیماران در دو رقت انجام شد. زمان انکوباسیون روش یک مرحلهای 4 دقیقه بود.
روش کـروموژنیـک سنجـش فاکتـور 8 نیـز برای تمام
بیماران با استفاده از آنالایزر تمام اتوماتیک STA-compact
(دیاگنوستیکا استاگو، فرانسه) و کیت FVIII:C TECHNOCHROM (تکنوکلون ـ آلمان) انجام شد. زمان انکوباسیون این روش 5 دقیقه بود.
تعریف مغایرت در نتایج:
بیماران در صورتی دارای مغایرت گفته میشوند که بین نتایج سنجش FVIII:C به روش یک مرحلهای و کروموژنیک اختلاف بیشتر یا مساوی دو برابر وجود داشته باشد.
آنالیز آماری:
به منظور آنالیز دادههای پژوهش از آزمون Paired t-test و نرمافزار 22 SPSS استفاده شد. p value کمتر از 05/0 معنادار در نظر گرفته شد.
یافتهها
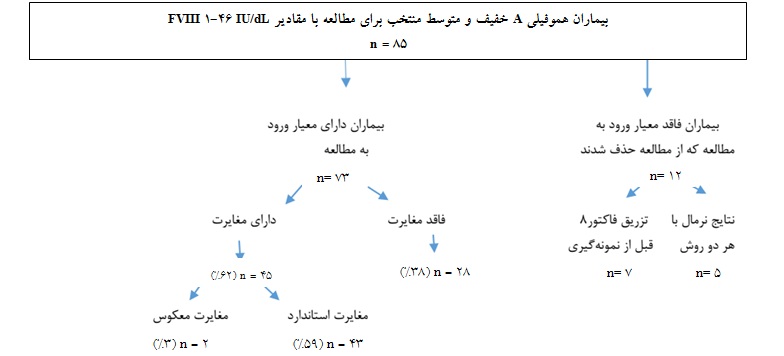
از 78 بیمار مورد مطالعه، 37 بیمار هموفیلی Aخفیف، 26 بیمار هموفیلی A متوسط و 15 زن ناقل علامتدار هموفیلی A در این مطالعه حضور داشتند. 5 بیمار با هر دو روش یک مرحلهای و کروموژنیک در این پژوهش مقادیر FVIII:C طبیعی داشتند و از مطالعه خارج شدند. بنابراین مطالعه بر روی 73 بیمار هموفیلی A خفیف و متوسط ادامه یافت. 45 بیمار(62٪) دارای مغایرت در نتایج بودند. از این تعداد در 43 بیمار(59٪) مقدار FVIII:C در روش کروموژنیک کمتر بود و تنها در 2 بیمار(3٪) مغایرت معکوس مشاهده شد. 28 بیمار نیز فاقد «مغایرت» بودند(شکل 1). دستهبندی بیماری از نظر شدت هموفیلی A در 25 بیمار(34%) تغییر کرد که از این تعداد 4 بیمار(5%) فاقد مغایرت در نتایج سنجش FVIII:C و 21 بیمار(29%) دارای «مغایرت» بودند. چگونگی تغییر شدت بیماری در این 25 بیمار به صورت زیر بود(جدول 2):
- در 20 بیمار، شدت بیماری با روش کروموژنیک از خفیف به متوسط تغییر یافت (FVIII:C کمتر در روش کروموژنیک).
- یـک بیـمار کـه بـا روش یـک مرحلهای در این پژوهش
FVIII:C طبیعی داشت، بـا روش کـروموژنیـک خفیـف
تشخیص داده شد.
جدول 2: تغییر دستهبندی بیماری از نظر شدت هموفیلی A بر اساس روش کروموژنیک
بحث
مغایرت در نتایج سنجش فعالیت FVIII با روشهای یک مرحلهای و کروموژنیک تاکنون در مطالعههای متعددی در حدود یک سوم بیماران هموفیلی A خفیف و متوسط گزارش شده است. در بررسی مطالعهها تا سال 2015، فقط سید و همکارانش میزان این مغایرت را تا 50% نیز گزارش کردهاند(11، 5). در این مطالعه مغایرت به صورت اختلاف دو برابر و یا بیشتر بین مقادیر FVIII:C اندازهگیری شده در روش یک مرحلهای و کروموژنیک تعریف شد. با این تعریف شیوع مغایرت در نتایج سنجش FVIII:C با این دو روش در جمعیت بیماران هموفیلی A خفیف و متوسط ایرانی 62% بود که قابل توجه بوده و بـه مراتب بیش از مطالعههای پیشین است.
شیوع مغایرت با مقادیر کمتر در روش کروموژنیک در این مطالعه 59%(45 بیمار) بود، که مانند اغلب مطالعههای پیشین، مؤید شیوع بیشتر این نوع مغایرت در مقایسه با مغایرت معکوس است(9). شیوع مغایرت معکوس در این مطالعه 3% (2 بیمار) بود. از بین مطالعههای بررسی شده درباره مغایرت، تنها دو مطالعه مخالف این پژوهش بودند. یک مورد، نتایج تروزرت و همکارانش در سال 2011 بود که میزان مغایرت معکوس را بیشتر اعلام کرده بودند؛ البته در آن مطالعه بایاس موجود در انتخاب جمعیت مورد مطالعه علت احتمالی شیوع بیشتر مغایرت معکوس عنوان شد و دیگری نتایج بویر و همکارانش در سال 2013 بود که میزان مغایرت معکوس را بیشتر گزارش کرده بودند(10، 6).
مغایـرت در بیمـاران همـوفیلـی A خفیـف و متوســط
زمانـی حائز اهمیت بالینی است که شدت بیماری، با توجه به روش سنجش به کار گرفته شده تغییر کند. در این مطالعه شدت بیماری در 25 بیمار(34%) با توجه به نتایج روش کروموژنیک تغییر یافت. مشابه همین اطلاعات در نتایج بویر و همکارانش در سال 2013 بیان شد(6). بویر و همکارانش نیز عنوان کردند، در 15% بیماران شدت بیماری بر اساس روش کروموژنیک تغییر یافته است. در سال 2014 نیز تروزرت و همکارانش بیان کردند اختلاف بین نتایج روشهای یک مرحلهای و کروموژنیک باعث تغییر شدت هموفیلی A خفیف در حدود 60% بیمارانشان شده است(12).
با توجه به کمتر بودن FVIII:C در روش کروموژنیک در 89% بیماران حاضر در این مطالعه و بر اساس نتایج سایرین، خطر تشخیص اشتباه برای برخی بیماران هموفیلی A خفیف که فقط با روش یک مرحلهای سنجش شدهاند وجود دارد. این بیماران ممکن است به اشتباه طبیعی گزارش شوند. این امر مانع پیگیریهای بعدی شده و بیمار را در خطر خونریزی قرار خواهد داد. در این مطالعه، فقط یک بیمار با شرایط فوق وجود داشت؛ که شاید به این دلیل باشد که تمام بیماران حاضر در این مطالعه، با روش یک مرحلهای تشخیص داده شده بودند. به منظور تشخیص صحیح چنین افرادی، مطالعههای گستردهتری نیاز است که در جمعیت مورد مطالعه هر دو روش یک مرحلهای و کروموژنیک جهت تشخیص به کار رفته باشد.
در این پژوهش، aPTT در 13 بیمار (18%) طولانی نشد. نتایج پژوهش حاضر مشابه نتایج بویر و همکارانش در سال 2013 است؛ که اعلام کرده بودند در 13% بیمارانشان aPTT طولانی نشد(6). بنابراین به aPTT نمیتوان به عنوان یک آزمایش غربالگری جهت تشخیص هموفیلی A اطمینان کرد.
نتیجهگیری
با توجه به شیوع بالای مغایرت(62%) در بیماران هموفیلی A خفیف و متوسط ایرانی و تغییر شدت بیماری در 34% بیماران با روش کروموژنیک، توصیه میشود جهت اطمینان از تشخیص کلیه موارد مبتلا به هموفیلی A خفیف یا متوسط و نیز تقسیمبندی صحیح شدت بیماری، سنجش فعالیت FVIII:C با هر دو روش الزامی شود.
از آن جایی که پدیده مغایرت اساس ژنتیکی دارد، لازم است ارتباط موتاسیونهای مسبب مغایرت با علائم بالینی
در مطالعه دیگری بررسی شود تا شاید بتوان به ارتباطی بین موتاسیونهای خاص با شدت علائم بالینی در بیماران دارای مغایرت دست یافت.
تشکر و قدردانی
این مطالعه با حمایتهای مالی مؤسسه عالی آموزشی و پژوهشی طب انتقال خون و هم چنین حمایت مالی مرکز تحقیقات ترومبوز و هموستاز دانشگاه علوم پزشکی تهران انجام شد که حمایتهای این مراکز را ارج مینهیم. هم چنین مؤلف مسئول مقاله سپاس ویژهای از آقای دکتر اتابک نجفی متخصص بیهوشی، دانشیار دانشگاه علوم پزشکی تهران برای همکاریهای بیدریغ ایشان در جریان انجام آزمایش ROTEM در این مطالعه دارد.
متن کامل: (13021 مشاهده)
بررسی مقادیر فعالیت فاکتور 8 اندازهگیری شده به دو روش
در بیماران هموفیلی A
فاطمه وثوق شیرایه1، مینو احمدی نژاد2، غلامرضا توگه3، کتایون کریمی4، محمدرضا طباطبایی5، ساناز همایون6
چکیده
سابقه و هدف
فعالیت (FVIII:C) FVIII در بیماران هموفیلی A با روشهای یک مرحلهای، دو مرحلهای مبتنی بر تشکیل لخته و کروموژنیک سنجش میشود. نتایج این سنجشها در اغلب بیماران هموفیلی A خفیف و متوسط مشابه است ولی در برخی بیماران اختلاف بارزی دارد که میتواند باعث عدم تشخیص یا تشخیص نادرست شدت بیماری شود. هدف مطالعه حاضر تعیین مقادیر فاکتور هشت به دو روش و میزان مغایرت در بیماران هموفیلی A است.
مواد و روشها
در یک مطالعه توصیفی مقطعی، FVIII:C با روشهای یک مرحلهای و کروموژنیک در 73 بیمار هموفیلی A شناخته شده سنجش شد. روش تحلیل دادهها آزمون t زوجی و نرمافزار 22 SPSS بود.
یافتهها
از 73 بیمار، FVIII:C به روش یک مرحلهای با محدود 4% تا 81% (میانگین 7/22% با انحراف معیار 8/14) و FVIII:C به روش دو مرحلهای کروموژنیک با محدوده 1% تا 123% (میانگین 5/16 و انحراف معیار 21) بود و در این بین 45 بیمار(62%) مغایرت در نتایج سنجش FVIII:C داشتند.
نتیجه گیری
جهت جلوگیری از عدم تشخیص یا تشخیص نادرست هموفیلی A و شدت بیماری سنجش FVIII:C با هر دو روش یک مرحلهای و دو مرحلهای کروموژنیک برای تشخیص بیماران مشکوک به هموفیلی خفیف یا متوسط اکیداً توصیه میشود.
کلمات کلیدی: هموفیلی A ، فاکتور VIII ، شیوع
تاریخ دریافت : 18/12/94
تاریخ پذیرش : 18/5 /95
1- کارشناس ارشد هماتولوژی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- مؤلف مسؤول: متخصص آسیبشناسی بالینی و تشریحی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران ـ صندوق پستی: 1157-14665
3- فوق تخصص هماتولوژی و انکولوژی بالغین ـ دانشیار مرکز تحقیقات ترومبوز و هموستاز دانشگاه علوم پزشکی تهران ـ تهران ـ ایران
4- پزشک عمومی ـ مرکز تحقیقات ترومبوز هموستاز دانشگاه علوم پزشکی تهران ـ تهران ـ ایران
5- کارشناس ارشد هماتولوژی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
6- کارشناس ارشد بیوشیمی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
در بیماران هموفیلی A
فاطمه وثوق شیرایه1، مینو احمدی نژاد2، غلامرضا توگه3، کتایون کریمی4، محمدرضا طباطبایی5، ساناز همایون6
چکیده
سابقه و هدف
فعالیت (FVIII:C) FVIII در بیماران هموفیلی A با روشهای یک مرحلهای، دو مرحلهای مبتنی بر تشکیل لخته و کروموژنیک سنجش میشود. نتایج این سنجشها در اغلب بیماران هموفیلی A خفیف و متوسط مشابه است ولی در برخی بیماران اختلاف بارزی دارد که میتواند باعث عدم تشخیص یا تشخیص نادرست شدت بیماری شود. هدف مطالعه حاضر تعیین مقادیر فاکتور هشت به دو روش و میزان مغایرت در بیماران هموفیلی A است.
مواد و روشها
در یک مطالعه توصیفی مقطعی، FVIII:C با روشهای یک مرحلهای و کروموژنیک در 73 بیمار هموفیلی A شناخته شده سنجش شد. روش تحلیل دادهها آزمون t زوجی و نرمافزار 22 SPSS بود.
یافتهها
از 73 بیمار، FVIII:C به روش یک مرحلهای با محدود 4% تا 81% (میانگین 7/22% با انحراف معیار 8/14) و FVIII:C به روش دو مرحلهای کروموژنیک با محدوده 1% تا 123% (میانگین 5/16 و انحراف معیار 21) بود و در این بین 45 بیمار(62%) مغایرت در نتایج سنجش FVIII:C داشتند.
نتیجه گیری
جهت جلوگیری از عدم تشخیص یا تشخیص نادرست هموفیلی A و شدت بیماری سنجش FVIII:C با هر دو روش یک مرحلهای و دو مرحلهای کروموژنیک برای تشخیص بیماران مشکوک به هموفیلی خفیف یا متوسط اکیداً توصیه میشود.
کلمات کلیدی: هموفیلی A ، فاکتور VIII ، شیوع
تاریخ دریافت : 18/12/94
تاریخ پذیرش : 18/5 /95
1- کارشناس ارشد هماتولوژی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
2- مؤلف مسؤول: متخصص آسیبشناسی بالینی و تشریحی ـ استادیار مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران ـ صندوق پستی: 1157-14665
3- فوق تخصص هماتولوژی و انکولوژی بالغین ـ دانشیار مرکز تحقیقات ترومبوز و هموستاز دانشگاه علوم پزشکی تهران ـ تهران ـ ایران
4- پزشک عمومی ـ مرکز تحقیقات ترومبوز هموستاز دانشگاه علوم پزشکی تهران ـ تهران ـ ایران
5- کارشناس ارشد هماتولوژی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
6- کارشناس ارشد بیوشیمی ـ مرکز تحقیقات انتقال خون ـ مؤسسه عالی آموزشی و پژوهشی طب انتقال خون ـ تهران ـ ایران
مقدمه
هموفیلی A یک اختلال خونریزیدهنده وابسته به کروموزوم x مغلوب است که خصوصیت آن کاهش فعالیت انعقادی FVIII پلاسماست. تمایل به خونریزی در این بیماران با میزان فعالیت FVIII (FVIII:C) پلاسما متناسب است. شیوع هموفیلی، 1 در هر 5000 مرد گزارش شده است(3-1). طبق طبقهبندی متداول، بیماران هموفیلی A خفیف سطح FVIII بین IU/dL 40-5 ، بیماران هموفیلی A متوسط سطح FVIII بین IU/dL 5-1 و بیماران نوع شدید سطح FVIII کمتر از IU/dL 1 دارند(4). میانگین سطح FVIII در ناقلین نیز IU/dL 60 گزارش شده است. در مقایسه با بیماران نوع شدید، حوادث خونریزیدهنده در بیماران هموفیلی A خفیف شیوع کمتری دارد و به ندرت باعث همارتروزهای راجعه و در نتیجه آن آرتروپاتی میشود. نتایج اغلب آزمایشهای انعقادی غربالگری در هموفیلی A خفیف طبیعی هستند فقط احتمال دارد aPTT طولانی باشد. aPTT گاهاً طبیعی نیز خواهد شد. بنابراین هرگاه از لحاظ بالینی به هموفیلی A مشکوک باشیم حتی در صورت طولانی نبودن aPTT ، سنجش FVIII:C ضروری است(1). در حال حاضر سه روش برای اندازهگیری فعالیت FVIII پلاسما وجود دارد. روش یک مرحلهای مبتنی بر تشکیل لخته، روش دو مرحلهای مبتنی بر تشکیل لخته و روش دو مرحلهای کروموژنیک میباشد(5).
مقادیر FVIII:C اندازهگیری شده در اغلب بیماران هموفیلی A ، صرف نظر از روش سنجش به کار رفته یکسان است ولی طبق بسیاری از پژوهشهای پیشین، حدود 30% بیماران هموفیلی A خفیف و متوسط، اختلاف معناداری را در FVIII:C اندازهگیری شده با روشهای مختلف نشان میدهند(6). در این بیماران، اختلاف نتایج روش یک مرحلهای و کروموژنیک بیشتر یا مساوی دو برابر است. به این گروه از بیماران، «هموفیلی A دارای مغایرت» گفته میشود(7). موتاسیونهای ژنتیکی متعددی عنوان شده که با این مغایرتها مرتبطند. موتاسیونها باعث ایجاد پروتئینی با اختلال عملکرد میشوند(8).
اهمیــت بالینــی«مغایـرت» از آن لحـاظ اسـت کـه در
مبتلایان به هموفیلی Aدارای مغایرت ممکن است شدت بیماری به درستی تشخیص داده نشود؛ چون نتایج سنجش فعالیت FVIII آنها با روش یک مرحلهای، طبیعی یا نزدیک به محدوده طبیعی میباشد ولی در روش کروموژنیک کاهش یافته است(9). دو نوع مغایرت در نتایج وجود دارد؛ یک نوع میزان کمتر FVIII:C در روش کروموژنیک (یا دو مرحلهای) در مقایسه با روش یک مرحلهای است که بیماران الگوی خونریزی مطابق با نتایج روش کروموژنیک را نشان میدهند. نوع دیگر مغایرت، میزان کمتر FVIII:C در روش یک مرحلهای در مقایسه با روش کروموژنیک است که در این بیماران خونریزی اندکی گزارش شده است(5). مغایرت با مقادیر کمتر FVIII:C در روش کروموژنیک «مغایرت استاندارد» و مغایرت با مقادیر کمتر FVIII:C در روش یک مرحلهای، مغایرت معکوس نامیده میشود که شایعتر است(10).
با توجه به نبود گزارشی درباره میزان مغایرت در نتایج سنجش FVIII:C در بیماران هموفیلی Aخفیف/متوسط ایرانی و ضرورت تعیین دقیق FVIII:C ، در این بیماران به منظور تشخیص صحیح، پیشبینی خطر خونریزی و نیز ضرورت مدیریت استاندارد درمان این بیماران، هدف از مطالعه پیش رو تعیین میزان مغایرت در FVIII:C اندازهگیری شده به دو روش یک مرحلهای و کروموژنیک در بیماران هموفیلی A غیر شدید ایرانی بود. نتایج این مطالعه میتواند به عنوان گام ابتدایی در انتخاب و به کارگیری روشی مناسب جهت تعیین مقادیر FVIII:C در این بیماران به کار رود.
مواد و روشها
درمانگاه جامع هموفیلی مرکز تحقیقات ترومبوز و هموستاز دانشگاه علوم پزشکی تهران واقع در مجتمع بیمارستانی امام خمینی به جمعیتی بالغ بر 3234 بیمار هموفیلی خدمات درمانی ارائه میدهد که در این بین حدود 1600 بیمار ثبت نام شده، هموفیلی A نوع خفیف و متوسط هستند. بیماران هموفیلی A خفیف و متوسط ثبت شده در این مرکز، به عنوان جامعه آماری در این مطالعه توصیفی ـ مقطعی انتخاب شدند. اطلاعات بیماران از طریق بررسی آرشیو درمانگاه هموفیلی مرکز تحقیقات هموستاز و ترومبوز دانشگاه علوم پزشکی تهران جمعآوری شد. تمام بیماران با روش یک مرحلهای تشخیص داده شده بودند. با توجه به لزوم مراجعه بیماران به درمانگاه هموفیلی، از بیماران ساکن استانهای غیر از تهران و البرز به دلیل دوری مسافت، دعوت به همکاری نشد. به علاوه اطلاعات تعدادی از پروندهها نیز به روز نبود. از آن جایی که احتمال ریزش بیماران وجود داشت، 300 بیمار برای فراخوان انتخاب شدند و از تمام آنها جهت شرکت در مطالعه دعوت به عمل آمد.
85 بیمار جهت شرکت در این مطالعه اعلام آمادگی و رضایت نمودند. به بیماران توضیح داده شد که نباید از 10 روز قبل از جمعآوری نمونه خون، کنستانتره FVIII دریافت کرده باشند. علیرغم توضیحاتی که به بیماران داده شده بود؛ 7 بیمار طی 10 روز قبل از مراجعه کنستانتره FVIII دریافت کرده بودند و از مطالعه حذف شدند. بنابراین مطالعه بر روی 78 بیمار هموفیلی A غیرشدید با مقادیر FVIII بین 46%-1% (بر اساس اطلاعات موجود در پرونده) انجام شد. تمام آزمایشها با کسب مجوز اخلاق در پژوهش از معاونت پژوهشی دانشگاه علوم پزشکی تهران انجام شد. قبل از دریافت اطلاعات بالینی و نمونه خون، از تمام بیماران رضایتنامه کتبی آگاهانه جهت شرکت در این مطالعه دریافت شد.
آزمایشهای انعقادی:
آزمایشهای aPTT و mixed-aPTT بر روی تمام نمونهها با استفاده از آنالایزر تمام اتوماتیک STA-compact (دیاگنوستیکا، فرانسه) و با به کارگیری ریجنت DAPTTIN TC aPTT (تکنوکلون ـ آلمان) در همان روز نمونهگیری انجام شد. آزمایش سنجش مقدار فاکتور VIII به روش یک مرحلهای نیز با استفاده از آنالایزر فوق و همان ریجنت و پلاسمای فاقد فاکتور 8 (استاگو، فرانسه ، Immuno-depleted) برای تمام بیماران در دو رقت انجام شد. زمان انکوباسیون روش یک مرحلهای 4 دقیقه بود.
روش کـروموژنیـک سنجـش فاکتـور 8 نیـز برای تمام
بیماران با استفاده از آنالایزر تمام اتوماتیک STA-compact
(دیاگنوستیکا استاگو، فرانسه) و کیت FVIII:C TECHNOCHROM (تکنوکلون ـ آلمان) انجام شد. زمان انکوباسیون این روش 5 دقیقه بود.
تعریف مغایرت در نتایج:
بیماران در صورتی دارای مغایرت گفته میشوند که بین نتایج سنجش FVIII:C به روش یک مرحلهای و کروموژنیک اختلاف بیشتر یا مساوی دو برابر وجود داشته باشد.
آنالیز آماری:
به منظور آنالیز دادههای پژوهش از آزمون Paired t-test و نرمافزار 22 SPSS استفاده شد. p value کمتر از 05/0 معنادار در نظر گرفته شد.
یافتهها
از 78 بیمار مورد مطالعه، 37 بیمار هموفیلی Aخفیف، 26 بیمار هموفیلی A متوسط و 15 زن ناقل علامتدار هموفیلی A در این مطالعه حضور داشتند. 5 بیمار با هر دو روش یک مرحلهای و کروموژنیک در این پژوهش مقادیر FVIII:C طبیعی داشتند و از مطالعه خارج شدند. بنابراین مطالعه بر روی 73 بیمار هموفیلی A خفیف و متوسط ادامه یافت. 45 بیمار(62٪) دارای مغایرت در نتایج بودند. از این تعداد در 43 بیمار(59٪) مقدار FVIII:C در روش کروموژنیک کمتر بود و تنها در 2 بیمار(3٪) مغایرت معکوس مشاهده شد. 28 بیمار نیز فاقد «مغایرت» بودند(شکل 1). دستهبندی بیماری از نظر شدت هموفیلی A در 25 بیمار(34%) تغییر کرد که از این تعداد 4 بیمار(5%) فاقد مغایرت در نتایج سنجش FVIII:C و 21 بیمار(29%) دارای «مغایرت» بودند. چگونگی تغییر شدت بیماری در این 25 بیمار به صورت زیر بود(جدول 2):
- در 20 بیمار، شدت بیماری با روش کروموژنیک از خفیف به متوسط تغییر یافت (FVIII:C کمتر در روش کروموژنیک).
- یـک بیـمار کـه بـا روش یـک مرحلهای در این پژوهش
FVIII:C طبیعی داشت، بـا روش کـروموژنیـک خفیـف
تشخیص داده شد.

شکل 1: نمودار گروههای حاضر در مطالعه به تفکیک تعداد: بیماران فاقد مغایرت، دارای مغایرت و دارای مغایرت معکوس
جدول 1: نتایج سنجش فعالیت فاکتور 8 گروههای حاضر در مطالعه به تفکیک تعداد بیماران فاقد مغایرت، دارای مغایرت و دارای مغایرت معکوس
جدول 1: نتایج سنجش فعالیت فاکتور 8 گروههای حاضر در مطالعه به تفکیک تعداد بیماران فاقد مغایرت، دارای مغایرت و دارای مغایرت معکوس
| فاقد مغایرت | دارای مغایرت با مقادیر کمتر در روش کروموژنیک | دارای مغایرت با مقادیر کمتر در روش یک مرحلهای | |
| تعداد بیماران | 28 | 43 | 2 |
| میانگین مقادیر FVIII:C1 | (81-7) 53/32 | (34-5) 6/15 | (46-30) 38 |
| میانگین مقادیر FVIII:CCR | (72-5) 39/27 | (16-1) 7/5 | (123-72) 5/97 |
| میانگین مقادیر FVIII:C1/ FVIII:CCR |
3/1 | 2/3 | 4/0 |
- فعالیت فاکتور 8 با روش یک مرحلهای: FVIII:C1 ، فعالیت فاکتور 8 با روش کروموژنیک: FVIII:CCR
- 4 بیمار که با روش یک مرحلهای خفیف تشخیص داده شده بودند(FVIII:C بین IU/dL 46-30)، در روش کروموژنیک مقادیر FVIII:C طبیعی داشتند. نتایج سنجش FVIII:C گروههای حاضر در مطالعه به تفکیک تعداد بیماران فاقد مغایرت، دارای مغایرت استاندارد و دارای مغایرت معکوس به هر دو روش یک مرحلهای و کروموژنیک در جدول 1 نشان داده شده است.
نتایج آزمایشهای aPTT و mixed-aPTT :
aPTT در 13 بیمار (18٪) از 73 بیمار مورد بررسی، با سطح FVIII:C1 بین IU/dL 81-23 و FVIII:CCR بین IU/dL 123-8 طولانی نشد و در محدوده طبیعی بود. از این تعداد، 2 بیمار دارای مغایرت و 11 بیمار فاقد مغایرت بودند. شایان ذکر است محدوده رفرانس در آزمایشگاه انعقاد سازمان انتقال خون با انجام آزمایش aPTT بر روی 25 نمونه طبیعی(7 زن و 18 مرد سالم) تعیین شد و محدوده آن بین 7/41- 4/30 محاسبه گردید. آزمایش mixed-aPTT نیز در 7٪ بیماران(4 بیمار نوع خفیف و 1 بیمار نوع متوسط) اصلاح نشد و بالاتر از محدوده طبیعی (7/41- 4/30) بود. در بررسیهای بعدی مشخص شد یک بیمار با آزمایش mixed-aPTT اصلاح نشده، مهارکننده علیه FVIII دارد.
نتایج آزمایشهای aPTT و mixed-aPTT :
aPTT در 13 بیمار (18٪) از 73 بیمار مورد بررسی، با سطح FVIII:C1 بین IU/dL 81-23 و FVIII:CCR بین IU/dL 123-8 طولانی نشد و در محدوده طبیعی بود. از این تعداد، 2 بیمار دارای مغایرت و 11 بیمار فاقد مغایرت بودند. شایان ذکر است محدوده رفرانس در آزمایشگاه انعقاد سازمان انتقال خون با انجام آزمایش aPTT بر روی 25 نمونه طبیعی(7 زن و 18 مرد سالم) تعیین شد و محدوده آن بین 7/41- 4/30 محاسبه گردید. آزمایش mixed-aPTT نیز در 7٪ بیماران(4 بیمار نوع خفیف و 1 بیمار نوع متوسط) اصلاح نشد و بالاتر از محدوده طبیعی (7/41- 4/30) بود. در بررسیهای بعدی مشخص شد یک بیمار با آزمایش mixed-aPTT اصلاح نشده، مهارکننده علیه FVIII دارد.
جدول 2: تغییر دستهبندی بیماری از نظر شدت هموفیلی A بر اساس روش کروموژنیک
| تغییر خفیف به متوسط | تغییر خفیف به طبیعی | تغییر طبیعی به خفیف | |||||
| دارای مغایرت | تعداد بیماران فاقد مغایرت | 20 | 4 | 1 | |||
| 19 | 1 | 2 | 2 | 0 | 1 | ||
| میانگین مقادیر FVIII:C1 | 11 (18-6) | 5/37 (46-30) | 81 | ||||
| میانگین مقادیر FVIII:CCR | 3 (5-1) | 83 (123-67) | 52 | ||||
| میانگین نسبت FVIII:C1/ FVIII:CCR |
7/3 | 46/0 | 5/1 | ||||
بحث
مغایرت در نتایج سنجش فعالیت FVIII با روشهای یک مرحلهای و کروموژنیک تاکنون در مطالعههای متعددی در حدود یک سوم بیماران هموفیلی A خفیف و متوسط گزارش شده است. در بررسی مطالعهها تا سال 2015، فقط سید و همکارانش میزان این مغایرت را تا 50% نیز گزارش کردهاند(11، 5). در این مطالعه مغایرت به صورت اختلاف دو برابر و یا بیشتر بین مقادیر FVIII:C اندازهگیری شده در روش یک مرحلهای و کروموژنیک تعریف شد. با این تعریف شیوع مغایرت در نتایج سنجش FVIII:C با این دو روش در جمعیت بیماران هموفیلی A خفیف و متوسط ایرانی 62% بود که قابل توجه بوده و بـه مراتب بیش از مطالعههای پیشین است.
شیوع مغایرت با مقادیر کمتر در روش کروموژنیک در این مطالعه 59%(45 بیمار) بود، که مانند اغلب مطالعههای پیشین، مؤید شیوع بیشتر این نوع مغایرت در مقایسه با مغایرت معکوس است(9). شیوع مغایرت معکوس در این مطالعه 3% (2 بیمار) بود. از بین مطالعههای بررسی شده درباره مغایرت، تنها دو مطالعه مخالف این پژوهش بودند. یک مورد، نتایج تروزرت و همکارانش در سال 2011 بود که میزان مغایرت معکوس را بیشتر اعلام کرده بودند؛ البته در آن مطالعه بایاس موجود در انتخاب جمعیت مورد مطالعه علت احتمالی شیوع بیشتر مغایرت معکوس عنوان شد و دیگری نتایج بویر و همکارانش در سال 2013 بود که میزان مغایرت معکوس را بیشتر گزارش کرده بودند(10، 6).
مغایـرت در بیمـاران همـوفیلـی A خفیـف و متوســط
زمانـی حائز اهمیت بالینی است که شدت بیماری، با توجه به روش سنجش به کار گرفته شده تغییر کند. در این مطالعه شدت بیماری در 25 بیمار(34%) با توجه به نتایج روش کروموژنیک تغییر یافت. مشابه همین اطلاعات در نتایج بویر و همکارانش در سال 2013 بیان شد(6). بویر و همکارانش نیز عنوان کردند، در 15% بیماران شدت بیماری بر اساس روش کروموژنیک تغییر یافته است. در سال 2014 نیز تروزرت و همکارانش بیان کردند اختلاف بین نتایج روشهای یک مرحلهای و کروموژنیک باعث تغییر شدت هموفیلی A خفیف در حدود 60% بیمارانشان شده است(12).
با توجه به کمتر بودن FVIII:C در روش کروموژنیک در 89% بیماران حاضر در این مطالعه و بر اساس نتایج سایرین، خطر تشخیص اشتباه برای برخی بیماران هموفیلی A خفیف که فقط با روش یک مرحلهای سنجش شدهاند وجود دارد. این بیماران ممکن است به اشتباه طبیعی گزارش شوند. این امر مانع پیگیریهای بعدی شده و بیمار را در خطر خونریزی قرار خواهد داد. در این مطالعه، فقط یک بیمار با شرایط فوق وجود داشت؛ که شاید به این دلیل باشد که تمام بیماران حاضر در این مطالعه، با روش یک مرحلهای تشخیص داده شده بودند. به منظور تشخیص صحیح چنین افرادی، مطالعههای گستردهتری نیاز است که در جمعیت مورد مطالعه هر دو روش یک مرحلهای و کروموژنیک جهت تشخیص به کار رفته باشد.
در این پژوهش، aPTT در 13 بیمار (18%) طولانی نشد. نتایج پژوهش حاضر مشابه نتایج بویر و همکارانش در سال 2013 است؛ که اعلام کرده بودند در 13% بیمارانشان aPTT طولانی نشد(6). بنابراین به aPTT نمیتوان به عنوان یک آزمایش غربالگری جهت تشخیص هموفیلی A اطمینان کرد.
نتیجهگیری
با توجه به شیوع بالای مغایرت(62%) در بیماران هموفیلی A خفیف و متوسط ایرانی و تغییر شدت بیماری در 34% بیماران با روش کروموژنیک، توصیه میشود جهت اطمینان از تشخیص کلیه موارد مبتلا به هموفیلی A خفیف یا متوسط و نیز تقسیمبندی صحیح شدت بیماری، سنجش فعالیت FVIII:C با هر دو روش الزامی شود.
از آن جایی که پدیده مغایرت اساس ژنتیکی دارد، لازم است ارتباط موتاسیونهای مسبب مغایرت با علائم بالینی
در مطالعه دیگری بررسی شود تا شاید بتوان به ارتباطی بین موتاسیونهای خاص با شدت علائم بالینی در بیماران دارای مغایرت دست یافت.
تشکر و قدردانی
این مطالعه با حمایتهای مالی مؤسسه عالی آموزشی و پژوهشی طب انتقال خون و هم چنین حمایت مالی مرکز تحقیقات ترومبوز و هموستاز دانشگاه علوم پزشکی تهران انجام شد که حمایتهای این مراکز را ارج مینهیم. هم چنین مؤلف مسئول مقاله سپاس ویژهای از آقای دکتر اتابک نجفی متخصص بیهوشی، دانشیار دانشگاه علوم پزشکی تهران برای همکاریهای بیدریغ ایشان در جریان انجام آزمایش ROTEM در این مطالعه دارد.
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |



