جلد 16، شماره 1 - ( بهار 1398 )
جلد 16 شماره 1 صفحات 31-24 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Yazdani Z, Mousavi Z, Ghasemi mehr N, Fatemi A, Farsinezhad A, Hassan Shahi G. Evaluation of alternations in the expression of CCR5 chemokine receptor in acute myeloid leukemia patients with monocytic differentiation after chemotherapy. Sci J Iran Blood Transfus Organ 2019; 16 (1) :24-31
URL: http://bloodjournal.ir/article-1-1217-fa.html
URL: http://bloodjournal.ir/article-1-1217-fa.html
یزدانی زینت، موسوی زهرا، قاسمی مهر نرگس، فاطمی احمد، فارسی نژاد علیرضا، حسن شاهی غلام حسین. تغییرات بیان گیرنده کموکاینی CCR5 در بیماران مبتلا به لوسمی میلوئیدی حاد با تمایز منوسیتی بعد از شیمی درمانی. فصلنامه پژوهشی خون. 1398; 16 (1) :24-31
استاد مرکز تحقیقات پزشکی مولکولی پژوهشکده علوم پایه، دانشگاه علوم پزشکی رفسنجان
متن کامل [PDF 551 kb]
(1287 دریافت)
| چکیده (HTML) (4308 مشاهده)
مقدمه
بیماری لوسمی میلوئیدی حاد(AML : Acute Myeloid Leukemia)، شایعترین لوسمی حاد دوران بزرگسالی است. اکثر بیماران مبتلا به AML میمیرند، حتی دوزهای بالای شیمی درمانی و پیوند سلولهای بنیادی آلوژنیک برای جلوگیری از عود این بیماری، اغلب موارد با شکست مواجه میشود(1).
همکاری کموکاینها و گیرندههای آنها؛ برای مهاجرت لکوسیتها به مناطق التهابی ضروری است (2). بنابراین منطقی است که نقش اساسی در شروع، پیشرفت، مهاجرت و بقای تومور داشته باشند(3). مطالعههای متعددی نشان داده است که سلولهای سرطانی، سیستم کموکاین را دستخوش تغییر مینمایند؛ در نتیجه سبب مقاومت به درمان، افزایش طول درمان AML ، افزایش عوارض مربوط به درمان و مطلوب نبودن نتایج درمان AML میشوند(4، 1).
عامل حضور بالای ماکروفاژهای وابسته به تومور (TAM: Tumor Associated Macrophage)، کموکاینهای CCL2 و CCL5 میباشد، این دو کموکاین در محیط تومور سبب افزایش بیان فاکتور آنژیوژنز(VEGF: Vascular endothelial growth factor) میشوند(6، 5). اکثر کموکاینها و رسپتورهای آنها در سرطان فعال میشوند، یکی از این کموکاینها و رسپتورهای آن CCL5 و گیرنده CCR5 است(7، 2). گیرنده CCR5 ، در پاتوژنز بیماریهای مختلف مثل آترواسکلروز و مالتیپل اسکلروزیس و بسیاری از بیماریهای دیگر نقش دارد(8).
گیرنده CCR5 عبور و مرور سلولهای لنفوئیدی مانند لنفوسیتهای اجرایی و خاطره Th1 و سلولهای رده میلوئیدی(مثل منوسیتها، ماکروفاژها،NK cells ، سلولهای نابالغ دندریتیک) را تنظیم میکند. همچنین سلولهای T تنظیمی این رسپتور را بیان میکنند(9، 1). گیرنده CCR5 نیز اثر غیر مستقیمی بر پیشرفت سرطان؛ توسط کنترل پاسخ ایمنی علیه تومور دارد. این گیرنده میتواند رشد تومور را تسریع و در متاستاز تومور نقش به سزایی ایفا کند. هم چنین اثبات شده است که آنتاگونیستهای گیرندهCCR5 رشد تومور را مهار میکنند(10، 9). بیان گیرنده CCR5 در سلولهای استرومال و سلولهای هماتوپوئتیک، در متاستاز تومور نقش دارند(2). از آن جا که CCL5 و گیرنده آن در سرطانزایی و پیشرفت تومورنقش دارند، بنابراین ممکن است این محور کموکاین ـ رسپتور هدفی برای توسعه ترکیبات ضد سرطان باشد(12، 11).
بنابراین با توجه به نقش شبکه کموکاینی در پاتوژنز AML، در تحقیق حاضر بر آن شدیم تا با بررسی گیرنده CCR5 در AML، با تکیه بر اندازهگیری سطح آن بر سطح گلبولهای سفید خون بیماران AML بعد از مرحله اول شیمی درمانی و این که بیان این گیرنده در پاسخ به شیمی درمانی تغییر میکند یا خیر، تا حدودی به بررسی نقش احتمالی این کموکاین رسپتور بپردازیم.
مواد و روشها
این مطالعه مورد ـ شاهدی، مقطعی در سال 1397-1396 در دانشگاه علوم پزشکی کرمان بر روی 25 بیمار با میانگین سنی 7/4 ± 45/41 سال که به بخش آنکولوژی بیمارستان شهید باهنر کرمان مراجعه کرده بودند و طبق یافتههای بالینی و آزمایشگاهی تشخیص AML داشتند، انجام شد. نمونههای تهیه شده از بیماران طبق طبقهبندی (FAB: French-American British) مورد ارزیابی ویژگیهای مورفولوژی، ایمونوفنوتایپینگ و رنگآمیزی سیتوشیمی قرار داده شدند و بر اساس این یافتهها، تشخیص AML و نوع آن داده شد. لام مغز استخوان بیماران قبل از شیمی درمانی و بعد از شیمی درمانی مرحله اول (هفته چهارم پس از شیمی درمانی)، بررسی شد و درصد بلاست تعیین گردید(جدول 1). بیمارانی که سیر شیمی درمانی متفاوت داشتند و علاوه بر روند مرسوم 3+7، داروی شیمی درمانی دیگری نیز دریافت کردند از این مطالعه حذف شدند. با اخذ رضایتنامه از بیماران، متعاقب شیمی درمانی مرحله اول(شیمی درمانی مرسوم 3+7)، در هفته چهارم پس از شیمی درمانی که شمارش گلبولهای سفید در خون محیطی به حد طبیعی رسیدند، 2 میلیلیتر خون در لوله حاوی ضد انعقادEDTA تهیه شد.
جدول 1: مشخصات دموگرافی و بررسیهای آزمایشگاهی گروه بیمار و گروه کنترل سالم
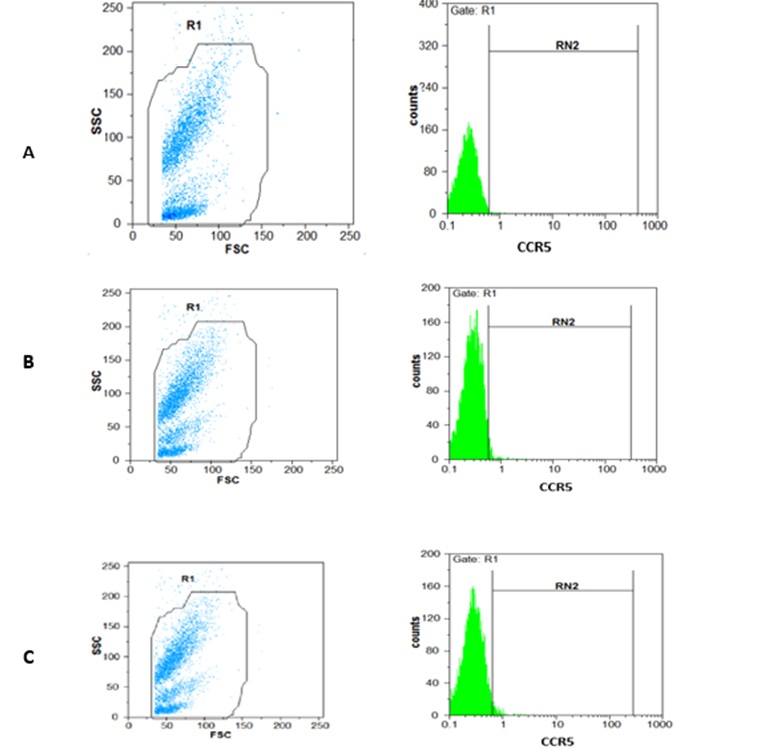
شکل 1: بیان گیرنده CCR5 توسط لکوسیتهای خون محیطی. سلولها با PE-conjugated MAb CCR5 رنگ آمیزی و توسط فلوسایتومتری تجزیه و تحلیل شدند. کل جمعیت لکوسیتها جداسازی شدند. هیستوگرام نشان دهنده فلورسانس PE است، با استفاده ازisotype-matched murine MAb به عنوان کنترل منفی (A)، نمونه یک کنترل سالم (B)، نمونه یک بیمار بعد از مرحله اول شیمی درمانی (هفته چهارم پس از شیمی درمانی)(C). منطقه R1 جمعیت لکوسیتها را نشان میدهد و RN2 منطقهی سلولهای بیان کننده گیرنده CCR5 را نشان میدهد.
جدول 2: بیان گیرنده CCR5 در گروه کنترل سالم و بیمار توسط فلوسیتومتری

نمودار 1: مقایسه میانگین میزان بیان گیرنده CCR-5در لکوسیتهای بیماران مبتلا به لوسمی میلوئیدی حاد با تمایز منوسیتی بعد از مرحله اول شیمی درمانی و گروه کنترل سالم. مقایسه بین دو گروه نشان داد که تفاوت معناداری بین آنها وجود ندارد.
بحث
نتایج این مطالعه نشان داد که بیماران مبتلا به لوسمی میلوئیدی حاد با تمایز منوسیتی، افزایش معناداری در بیان گیرندهCCR5 ، بعد از مرحله اول شیمی درمانی نشان ندادهاند و میزان بیان این گیرنده در بیماران پس از شیمی درمانی مرحله اول با گروه کنترل سالم مشابه بوده است. شاید این یک نتیجه مطلوب در شیمی درمانی میباشد و این که شیمی درمانی سبب میشود تا این گیرنده کموکاینی افزایش چندانی نداشته تا سبب بدخیم شدن بیماری شود. برخی از کموکاینها به همراه گیرنده خود در پاتوژنز بیماری AML نقش دارند(13). یکی از این کموکاینها و گیرنده آنها CCR5/CCL5 میباشد، این محور در سلولهای بلاست لوسمی بیماران مبتلا به AML افزایش مییابد(14).
 در تـلاشهـای اخیـر، نشـان داده شـــده اسـت که
در تـلاشهـای اخیـر، نشـان داده شـــده اسـت که
سلولهای سرکوبگر گرانولیسیتیک و مونوسیتیک مشتق میلوئیدی موشی مقدار بالایی از لیگاندهای CCR5 شامل؛ CCL3، CCL4 و CCL5 تولید میکنند، که همه آنها مسئول جمعآوری سلولهای T تنظیمی هستند. کمبود CCR5 باعث کاهش شدید آنها میشود، که بخش مهمی از CCR5 را در کنترل واکنشهای ایمنی ضد تومور نشان میدهد. بنابراین، مهاجرت سلولهای T تنظیمی به سمت ساختار ریز محیط تومور، در طی توسعه تومور توسط محور CCL5-CCR5 صورت میگیرد(9).
شاید بتوان سلولهای میلوئید سرکوب کننده ایمنی (IMC: Immunosuppressive myeloid cells) را به عنوان تنظیمگر منفی ایمنی علیه تومور تعریف کرد. محور CCL5/CCR5 در تومورژنسیس، پیشسازهای سلولی در مغز استخوان را به سمت سلولهای IMC رده گرانولوسیتی و مونوسیتی پیش میبرد و این سلولها خود سبب افزایش سلولهای T تنظیمی میشوند و متعاقباً سلولهای T تنظیمی، سلولهای TCD8+ را که نقش بالقوهای در مبارزه با سلولهای توموری بازی میکنند کاهش میدهند. اگر چه تاکنون مطالعهای بر روی نقش این محور کموکاین ـ رسپتوی در AML انجام نگردیده است ولی در راستای این قاعده در سال 2017، ییبان و همکارانش پژوهشی را بر روی بیماران مبتلا به سرطان سینه انجام دادند. این پژوهشگران توسط پارتیکلهایی که سبب خاموش شدن ژن CCL5 میشود، CCL5 در مغز استخوان را مورد هدف قرار دادند و هم چنین از آنتاگونیست Maraviroc به عنوان مهارکننده گیرنده CCR5 استفاده کردند که منجر به کاهش چشمگیر سلولهای IMC شد. بنابراین بر این اساس مطالعهها نشان داده است که هدف قرار دادن محور CCL5/CCR5، اثر درمانی بالقوهای در سرطان سینه دارد(14).
در مطالعهای دیگر در سال 2017، زی جی و همکاران اثر maraviroc بر روی سلولهای لوسمی لنفوئید حاد را مورد مطالعه قرار دادند. نتایج این پژوهش نشان داد که آنتاگونیست گیرندهCCR5 ، به طور چشمگیری رشد سلولهای لوسمی لنفوئید حاد رده سلولی SUP_B15 را مهار و سبب آپوپتوز این سلولها شد. این آنتاگونیست، سیگنالینگ فعال شده توسط CCR5، یعنی JAK1، JAK2 و STAT3 را مهار و در نتیجه سبب مهار رشد سلولهای توموری SUP_B15 که به موشهای فاقد تیموس پیوند زدهاند میشود. این مطالعه نشان داد که maraviroc به عنوان مهارگر گیرنده CCR5 میتواند یک راه درمانی برای بیماران مبتلا به لوسمی لنفوئید حاد باشد(10).
گیرنده CCR5 علاوه بر CCL5 به کموکاینهای CCL4 و CCL3 نیز متصل میشود(15). در طی مطالعهای کویچی تاکاهاشی و همکاران، مارکرهای CCL4 و CCL3 در بیماران مبتلا به لنفوم منتشر سلول B بزرگ(DLBCL : diffuse larg B cell lymphoma) را بعد از شیمی درمانی مورد بررسی قرار دادند. سطح سرمی CCL3 اکثر بیماران بعد از درمان کاهش یافت، در این بیماران پیشرفت بیماری مشاهده نشد و نیمی از بیماران کاهش CCL4 را نشان دادند. محققین در این مطالعه دست یافتند که غلظت بالای CCL4 و CCL3 مرتبط با پیشآگهی ضعیف در بیماران DLBCL میباشد(16). این مطالعه فقط بر روی کموکاینها و در بیماری DLBCL صورت گرفته است و گیرنده آنها را مورد بررسی قرار نداده است. در این مطالعه مشاهده کردیم که بیان گیرنده CCR5 بعد از شیمی درمانی، در بیماران مبتلا به AML ، همسان با گروه کنترل و دارای اثر مطلوبی میباشد و یافتهها همسان با یافتهها در مطالعه کویچی تاکاهاشی و همکاران است هر چند که تحقیق آنها در بیماری متفاوت و بر روی کموکاینها بوده است.
تاکنون تنها مطالعههای معدودی به بررسی ارتباط بین کموکاینها و ناهنجاریهای ایمونولوژیکی در بیماران مبتلا به لوسمی میلوئید حاد پرداختهاند. طبق بررسیهای انجام شده توسط ما تاکنون این مطالعهها بر روی مغز استخوان و سلولهای بلاست لوسمی این بیماران صورت گرفته است، حال که برخی از لکوسیتهای غیر لوسمی
نیزCCR5 را بیان میکنند و مطالعههایی در این زمینه بر روی لکوسیتها در خون محیطی صورت نگرفته است.
در نتیجه عدم افزایش بیان این گیرنده سبب میشود که سلولهای IMC که به عنوان تنظیمگر منفی ایمنی علیه تومور میباشند، افزایش پیدا نکنند که یک پیشآگهی خوب برای بیماران تلقی گردیده و احتمال عود بیماری را کاهش دهد.
نتیجهگیری
شیمی درمانی اثر نامطلوبی بر بیان گیرنده CCR5 که توسط لکوسیتهای خون محیطی بیان میشدند نداشته است و هم چنین سبب شده است که این گیرنده در حالت پایه خود در مقایسه با گروه کنترل سالم قرار بگیرد. با توجه به این مطالعه میتوان سایر محورهای کموکاین و گیرندههای آنها را مورد بررسی قرار داد که کدام محور کموکاینی نقش به سزایی در عود بیماران لوسمی میلوئید حاد خواهد داشت که شیمی درمانی روی آن محور کموکاینی تاثیری نخواهد داشت تا با مسدود کردن آن محور بتوان به نتایج مطلوبتری در شیمی درمانی دست یافت و از عود بیماری جلوگیری کرد.
از محدودیتهای این مطالعه نداشتن بودجه و زمان کافی بود. بهتر است این مطالعه در تک تک مراحل شیمی درمانی صورت گیرد و هم چنین دیگر محورهای کموکاینی و گیرندههای آنها نیز بررسی گردد.
تشکر و قدردانی
پژوهش حاضر با کمک مالی از دانشگاه علوم پزشکی کرمان صورت گرفت. ما هم چنین از تمام بیماران و همین طور افراد سالم که در این مطالعه شرکت کردهاند و هم چنین تمام کارکنان در مرکز درمانی بیمارستان شهید باهنر کرمان تشکر میکنیم که در این مطالعه همکاری لازم را داشتند.
متن کامل: (2386 مشاهده)
تغییرات بیان گیرنده کموکاینی CCR5 در بیماران مبتلا به لوسمی میلوئیدی حاد
با تمایز منوسیتی بعد از شیمی درمانی
زینت یزدانی1، زهرا موسوی2، نرگس قاسمی مهر1، احمد فاطمی3، علیرضا فارسی نژاد3، غلامحسین حسن شاهی4
چکیده
سابقه و هدف
لوسمی میلوئیدی حاد یک سرطان ناهمگن است که از طریق مکانیسمهای مختلف پاتولوژیک ایجاد میشود. سلولهای سرطانی، سیستم کموکاین را دستخوش تغییر مینمایند. گیرنده CCR5 ، اثر غیر مستقیمی بر پیشرفت سرطان توسط کنترل پاسخ ایمنی علیه تومور دارد. این گیرنده میتواند رشد تومور را تسریع و در متاستاز آن نقش به سزایی ایفا کند. در تحقیق حاضر برآن شدیم تا با بررسی گیرنده CCR5 در بیماران AML بعد از شیمی درمانی مرحله اول، تا حدودی به بررسی نقش احتمالی این رسپتور بپردازیم.
مواد و روشها
این مطالعه مورد ـ شاهدی در سال 1397-1396 در دانشگاه علوم پزشکی کرمان انجام شد. 25 بیمار مبتلا به AML با تمایز منوسیتی، پس از شیمی درمانی مرحله اول (هفته چهارم پس از شیمی درمانی) و بعد از بررسی لام خون محیطی و تائید عدم وجود بلاست، توسط فلوسیتومتری برای بیان گیرنده کموکاینی CCR5 بر جمعیت لکوسیتهای خون محیطی با گروه کنترل سالم مقایسه شدند. یافتهها توسط آزمون t دو نمونهای مستقل و 22 SPSS تجزیه و تحلیل شدند.
یافتهها
مطالعه حاضر نشان داد که میانگین بیان گیرنده CCR-5 در گروه بیماران بعد از شیمی درمانی(26/0 ± 04/1) مشابه با گروه کنترل سالم(16/0 ± 04/1) بوده است و تفاوت معناداری بین این دو گروه وجود نداشت.
نتیجه گیری
شیمی درمانی سبب شده است که بیان گیرنده CCR5 در حالت پایه خود در مقایسه با گروه کنترل سالم قرار گیرد. میتوان سایر محورهای کموکاین و گیرندههای آنها را مورد بررسی قرار داد تا پی ببریم کدام یک نقش به سزایی در عود بیماران خواهد داشت.
کلمات کلیدی: لوسمی میلوئید حاد، شیمی درمانی، منوسیتها، تومورها
تاریخ دریافت: 2 /5/97
تاریخ پذیرش: 17/6/97
1- کارشناس ارشد خونشناسی آزمایشگاهی و بانک خون ـ دانشکده پیراپزشکی دانشگاه علوم پزشکی کرمان ـ کرمان ـ ایران
2- کارشناس ارشد خونشناسی آزمایشگاهی و بانک خون ـ دانشکده پیراپزشکی دانشگاه علوم پزشکی کرمان و مربی دانشکده علوم پزشکی ایرانشهر ـ ایرانشهر ـ ایران
3- PhD خونشناسی آزمایشگاهی و بانک خون ـ استادیار دانشکده پیراپزشکی دانشگاه علوم پزشکی کرمان ـ کرمان ـ ایران
4- مؤلف مسئول: PhD خونشناسی آزمایشگاهی و بانک خون ـ استاد مرکز تحقیقات پزشکی مولکولی پژوهشکده علوم پایه، دانشگاه علوم پزشکی رفسنجان ـ بلوار امام علـی(ع) ـ رفسنجان ـ ایران ـ کدپستی: 7717933777
با تمایز منوسیتی بعد از شیمی درمانی
زینت یزدانی1، زهرا موسوی2، نرگس قاسمی مهر1، احمد فاطمی3، علیرضا فارسی نژاد3، غلامحسین حسن شاهی4
چکیده
سابقه و هدف
لوسمی میلوئیدی حاد یک سرطان ناهمگن است که از طریق مکانیسمهای مختلف پاتولوژیک ایجاد میشود. سلولهای سرطانی، سیستم کموکاین را دستخوش تغییر مینمایند. گیرنده CCR5 ، اثر غیر مستقیمی بر پیشرفت سرطان توسط کنترل پاسخ ایمنی علیه تومور دارد. این گیرنده میتواند رشد تومور را تسریع و در متاستاز آن نقش به سزایی ایفا کند. در تحقیق حاضر برآن شدیم تا با بررسی گیرنده CCR5 در بیماران AML بعد از شیمی درمانی مرحله اول، تا حدودی به بررسی نقش احتمالی این رسپتور بپردازیم.
مواد و روشها
این مطالعه مورد ـ شاهدی در سال 1397-1396 در دانشگاه علوم پزشکی کرمان انجام شد. 25 بیمار مبتلا به AML با تمایز منوسیتی، پس از شیمی درمانی مرحله اول (هفته چهارم پس از شیمی درمانی) و بعد از بررسی لام خون محیطی و تائید عدم وجود بلاست، توسط فلوسیتومتری برای بیان گیرنده کموکاینی CCR5 بر جمعیت لکوسیتهای خون محیطی با گروه کنترل سالم مقایسه شدند. یافتهها توسط آزمون t دو نمونهای مستقل و 22 SPSS تجزیه و تحلیل شدند.
یافتهها
مطالعه حاضر نشان داد که میانگین بیان گیرنده CCR-5 در گروه بیماران بعد از شیمی درمانی(26/0 ± 04/1) مشابه با گروه کنترل سالم(16/0 ± 04/1) بوده است و تفاوت معناداری بین این دو گروه وجود نداشت.
نتیجه گیری
شیمی درمانی سبب شده است که بیان گیرنده CCR5 در حالت پایه خود در مقایسه با گروه کنترل سالم قرار گیرد. میتوان سایر محورهای کموکاین و گیرندههای آنها را مورد بررسی قرار داد تا پی ببریم کدام یک نقش به سزایی در عود بیماران خواهد داشت.
کلمات کلیدی: لوسمی میلوئید حاد، شیمی درمانی، منوسیتها، تومورها
تاریخ دریافت: 2 /5/97
تاریخ پذیرش: 17/6/97
1- کارشناس ارشد خونشناسی آزمایشگاهی و بانک خون ـ دانشکده پیراپزشکی دانشگاه علوم پزشکی کرمان ـ کرمان ـ ایران
2- کارشناس ارشد خونشناسی آزمایشگاهی و بانک خون ـ دانشکده پیراپزشکی دانشگاه علوم پزشکی کرمان و مربی دانشکده علوم پزشکی ایرانشهر ـ ایرانشهر ـ ایران
3- PhD خونشناسی آزمایشگاهی و بانک خون ـ استادیار دانشکده پیراپزشکی دانشگاه علوم پزشکی کرمان ـ کرمان ـ ایران
4- مؤلف مسئول: PhD خونشناسی آزمایشگاهی و بانک خون ـ استاد مرکز تحقیقات پزشکی مولکولی پژوهشکده علوم پایه، دانشگاه علوم پزشکی رفسنجان ـ بلوار امام علـی(ع) ـ رفسنجان ـ ایران ـ کدپستی: 7717933777
مقدمه
بیماری لوسمی میلوئیدی حاد(AML : Acute Myeloid Leukemia)، شایعترین لوسمی حاد دوران بزرگسالی است. اکثر بیماران مبتلا به AML میمیرند، حتی دوزهای بالای شیمی درمانی و پیوند سلولهای بنیادی آلوژنیک برای جلوگیری از عود این بیماری، اغلب موارد با شکست مواجه میشود(1).
همکاری کموکاینها و گیرندههای آنها؛ برای مهاجرت لکوسیتها به مناطق التهابی ضروری است (2). بنابراین منطقی است که نقش اساسی در شروع، پیشرفت، مهاجرت و بقای تومور داشته باشند(3). مطالعههای متعددی نشان داده است که سلولهای سرطانی، سیستم کموکاین را دستخوش تغییر مینمایند؛ در نتیجه سبب مقاومت به درمان، افزایش طول درمان AML ، افزایش عوارض مربوط به درمان و مطلوب نبودن نتایج درمان AML میشوند(4، 1).
عامل حضور بالای ماکروفاژهای وابسته به تومور (TAM: Tumor Associated Macrophage)، کموکاینهای CCL2 و CCL5 میباشد، این دو کموکاین در محیط تومور سبب افزایش بیان فاکتور آنژیوژنز(VEGF: Vascular endothelial growth factor) میشوند(6، 5). اکثر کموکاینها و رسپتورهای آنها در سرطان فعال میشوند، یکی از این کموکاینها و رسپتورهای آن CCL5 و گیرنده CCR5 است(7، 2). گیرنده CCR5 ، در پاتوژنز بیماریهای مختلف مثل آترواسکلروز و مالتیپل اسکلروزیس و بسیاری از بیماریهای دیگر نقش دارد(8).
گیرنده CCR5 عبور و مرور سلولهای لنفوئیدی مانند لنفوسیتهای اجرایی و خاطره Th1 و سلولهای رده میلوئیدی(مثل منوسیتها، ماکروفاژها،NK cells ، سلولهای نابالغ دندریتیک) را تنظیم میکند. همچنین سلولهای T تنظیمی این رسپتور را بیان میکنند(9، 1). گیرنده CCR5 نیز اثر غیر مستقیمی بر پیشرفت سرطان؛ توسط کنترل پاسخ ایمنی علیه تومور دارد. این گیرنده میتواند رشد تومور را تسریع و در متاستاز تومور نقش به سزایی ایفا کند. هم چنین اثبات شده است که آنتاگونیستهای گیرندهCCR5 رشد تومور را مهار میکنند(10، 9). بیان گیرنده CCR5 در سلولهای استرومال و سلولهای هماتوپوئتیک، در متاستاز تومور نقش دارند(2). از آن جا که CCL5 و گیرنده آن در سرطانزایی و پیشرفت تومورنقش دارند، بنابراین ممکن است این محور کموکاین ـ رسپتور هدفی برای توسعه ترکیبات ضد سرطان باشد(12، 11).
بنابراین با توجه به نقش شبکه کموکاینی در پاتوژنز AML، در تحقیق حاضر بر آن شدیم تا با بررسی گیرنده CCR5 در AML، با تکیه بر اندازهگیری سطح آن بر سطح گلبولهای سفید خون بیماران AML بعد از مرحله اول شیمی درمانی و این که بیان این گیرنده در پاسخ به شیمی درمانی تغییر میکند یا خیر، تا حدودی به بررسی نقش احتمالی این کموکاین رسپتور بپردازیم.
مواد و روشها
این مطالعه مورد ـ شاهدی، مقطعی در سال 1397-1396 در دانشگاه علوم پزشکی کرمان بر روی 25 بیمار با میانگین سنی 7/4 ± 45/41 سال که به بخش آنکولوژی بیمارستان شهید باهنر کرمان مراجعه کرده بودند و طبق یافتههای بالینی و آزمایشگاهی تشخیص AML داشتند، انجام شد. نمونههای تهیه شده از بیماران طبق طبقهبندی (FAB: French-American British) مورد ارزیابی ویژگیهای مورفولوژی، ایمونوفنوتایپینگ و رنگآمیزی سیتوشیمی قرار داده شدند و بر اساس این یافتهها، تشخیص AML و نوع آن داده شد. لام مغز استخوان بیماران قبل از شیمی درمانی و بعد از شیمی درمانی مرحله اول (هفته چهارم پس از شیمی درمانی)، بررسی شد و درصد بلاست تعیین گردید(جدول 1). بیمارانی که سیر شیمی درمانی متفاوت داشتند و علاوه بر روند مرسوم 3+7، داروی شیمی درمانی دیگری نیز دریافت کردند از این مطالعه حذف شدند. با اخذ رضایتنامه از بیماران، متعاقب شیمی درمانی مرحله اول(شیمی درمانی مرسوم 3+7)، در هفته چهارم پس از شیمی درمانی که شمارش گلبولهای سفید در خون محیطی به حد طبیعی رسیدند، 2 میلیلیتر خون در لوله حاوی ضد انعقادEDTA تهیه شد.
جدول 1: مشخصات دموگرافی و بررسیهای آزمایشگاهی گروه بیمار و گروه کنترل سالم
| سن (Mean ± SEM) |
جنس | M4/M5 | درصد بلاست در مغز استخوانD (Mean ± SEM) |
درصد بلاست در مغز استخوان* (Mean ± SEM) |
شمارش گلبولهای سفید در خون محیطی (Mean ± SEM) |
|
| بیمار | 7/4 ± 45/41 | 12 مرد | 9/16 | 8/5 ± 47 | 2/1 ± 90/7 | 1158 ± 8360* |
| 13 زن | ||||||
| کنترل | 2/3 ± 40 | 10 مرد | - | - | - | 936 ± 8050 |
| سالم | 15 زن |
Δ قبل از شیمی درمانی
* بعد از شیمی درمانی مرحله اول ( هفته چهارم پس از شیمی درمانی)
لام خون محیطی برای هر بیمار تهیه شد و از نظر عدم وجود بلاست بررسی گردید. همچنین لام مغز استخوان بیماران در این مرحله بررسی و درصد بلاست تعیین شد. از 25 فرد سالم که از نظر سن و جنس با بیماران یکسانسازی شدند، به عنوان گروه کنترل نیز استفاده شد. نمونهگیری با رعایت موارد و اصول اخلاقی طبق اساسنامه دانشگاه و با اخذ رضایت از بیماران انجام شد. این پژوهش با شمارهIR.KMU.REC.1395.598 در کمیته اخلاق دانشگاه علوم پزشکی کرمان در پژوهش مورد تصویب قرار گرفته است.
بررسی مارکر سطح سلولی CCR5 با فلوسیتومتری:
آنتیبادی مورد مطالعه PE conjugated anti-CD195 (آمریکا، BD) خریداری شد.
نمونههای تهیه شده در ضدانعقاد EDTA به آزمایشگاه مغز استخوان بیمارستان باهنر انتقال داده شدند. مقدار 50 میکرولیتر از این خون با 5 میکرولیتر از Anti-CD195 (CCR5) کونژوگه شده با فیکواریترین(PE) مخلوط و به مدت نیم ساعت در دمای یخچال نگهداری شد و پس از آن برای لیز گلبولهای قرمز از محلول لیز، مارک داکو ساخت کشور هلند طبق دستورالعمل زیر انجام شد:
100 میکرولیتر محلول شمارهA (فیکساتور) ترکیب و به مدت 10 دقیقه در دمای اتاق و در تاریکی انکوبه شد و پس از آن با 1000 میکرولیتر از محلول شماره B (محلول لیز گلبولهای قرمز، حاوی آمونیوم کلراید، پتاسیم کربنات، اتیلن دیامین تترا استیک اسید) ترکیب و به مدت 20 دقیقه در دمای اتاق و در تاریکی انکوبه شد و پس از آن نمونهها با دستگاه فلوسایتومتری Partec مدل PAS ساخت کشور آلمان خوانده شد و بیان گیرندهCCR5 در 10000 سلول جمعیت کل گلبولهای سفید بررسی گردید. هم زمان از ایزوتایپ کنترل جهت حذف اتصالات غیر اختصاصی نیز استفاده شد و دادههای حاصل با نرمافزار فلومکس تحلیل گردیدند.
آنالیزهای آماری:
نتایج حاصل توسط نرمافزار SPSS ورژن 22 تجزیه و تحلیل شد. مبنای اصلی آنالیز دادهها بر اساس آزمون تی- دو نمونهای مستقل(two independent samples t-test) بود. در صورت 05/0 p< ، اختلاف بین گروههای مورد مقایسه معنادار در نظر گرفته شد.
یافتهها
در این مطالعه تعداد 25 بیمار مبتلا به AML با تمایز منوسیتی، مورد بررسی قرار گرفتند. میانگین سلولهای بلاست در خون محیطی این افراد در زمان تشخیص بیماری، 76/28 ± 45/46 بود و بعد از مرحله اول شیمی درمانی رایج(3+7)، هفته چهارم بعد از شیمی درمانی که شمارش سلولها به حالت طبیعی برمیگردد، با بررسی لام خون محیطی این افراد مشاهده شد که سلول بلاستی در خون محیطی آنها یافت نشده و جمعیت لکوسیتها طبیعی گردیده است. اگر بعد از شیمی درمانی کمتر از 5% بلاست در مغز استخوان بیماران یافت شود بیمار پاسخ کامل، اگر بین20% - 5% سلول بلاست مشاهده شود، پاسخ نسبی و اگر بیش از 20% سلول بلاست مشاهده شود، بدون پاسخ به درمان میباشد که بر این اساس کلیه بیماران مورد مطالعه در این تحقیق پاسخ نسبی به درمان داشتهاند.
نتایج مطالعه حاضر نشان داد که میانگین بیان گیرنده CCR-5 در گروه بیماران بعد از شیمی درمانی در مقایسه با گروه کنترل سالم تغییری نکرده است و تفاوت معناداری وجود نداشته است(شکل 1)(جدول 2)(نمودار 1).
* بعد از شیمی درمانی مرحله اول ( هفته چهارم پس از شیمی درمانی)
لام خون محیطی برای هر بیمار تهیه شد و از نظر عدم وجود بلاست بررسی گردید. همچنین لام مغز استخوان بیماران در این مرحله بررسی و درصد بلاست تعیین شد. از 25 فرد سالم که از نظر سن و جنس با بیماران یکسانسازی شدند، به عنوان گروه کنترل نیز استفاده شد. نمونهگیری با رعایت موارد و اصول اخلاقی طبق اساسنامه دانشگاه و با اخذ رضایت از بیماران انجام شد. این پژوهش با شمارهIR.KMU.REC.1395.598 در کمیته اخلاق دانشگاه علوم پزشکی کرمان در پژوهش مورد تصویب قرار گرفته است.
بررسی مارکر سطح سلولی CCR5 با فلوسیتومتری:
آنتیبادی مورد مطالعه PE conjugated anti-CD195 (آمریکا، BD) خریداری شد.
نمونههای تهیه شده در ضدانعقاد EDTA به آزمایشگاه مغز استخوان بیمارستان باهنر انتقال داده شدند. مقدار 50 میکرولیتر از این خون با 5 میکرولیتر از Anti-CD195 (CCR5) کونژوگه شده با فیکواریترین(PE) مخلوط و به مدت نیم ساعت در دمای یخچال نگهداری شد و پس از آن برای لیز گلبولهای قرمز از محلول لیز، مارک داکو ساخت کشور هلند طبق دستورالعمل زیر انجام شد:
100 میکرولیتر محلول شمارهA (فیکساتور) ترکیب و به مدت 10 دقیقه در دمای اتاق و در تاریکی انکوبه شد و پس از آن با 1000 میکرولیتر از محلول شماره B (محلول لیز گلبولهای قرمز، حاوی آمونیوم کلراید، پتاسیم کربنات، اتیلن دیامین تترا استیک اسید) ترکیب و به مدت 20 دقیقه در دمای اتاق و در تاریکی انکوبه شد و پس از آن نمونهها با دستگاه فلوسایتومتری Partec مدل PAS ساخت کشور آلمان خوانده شد و بیان گیرندهCCR5 در 10000 سلول جمعیت کل گلبولهای سفید بررسی گردید. هم زمان از ایزوتایپ کنترل جهت حذف اتصالات غیر اختصاصی نیز استفاده شد و دادههای حاصل با نرمافزار فلومکس تحلیل گردیدند.
آنالیزهای آماری:
نتایج حاصل توسط نرمافزار SPSS ورژن 22 تجزیه و تحلیل شد. مبنای اصلی آنالیز دادهها بر اساس آزمون تی- دو نمونهای مستقل(two independent samples t-test) بود. در صورت 05/0 p< ، اختلاف بین گروههای مورد مقایسه معنادار در نظر گرفته شد.
یافتهها
در این مطالعه تعداد 25 بیمار مبتلا به AML با تمایز منوسیتی، مورد بررسی قرار گرفتند. میانگین سلولهای بلاست در خون محیطی این افراد در زمان تشخیص بیماری، 76/28 ± 45/46 بود و بعد از مرحله اول شیمی درمانی رایج(3+7)، هفته چهارم بعد از شیمی درمانی که شمارش سلولها به حالت طبیعی برمیگردد، با بررسی لام خون محیطی این افراد مشاهده شد که سلول بلاستی در خون محیطی آنها یافت نشده و جمعیت لکوسیتها طبیعی گردیده است. اگر بعد از شیمی درمانی کمتر از 5% بلاست در مغز استخوان بیماران یافت شود بیمار پاسخ کامل، اگر بین20% - 5% سلول بلاست مشاهده شود، پاسخ نسبی و اگر بیش از 20% سلول بلاست مشاهده شود، بدون پاسخ به درمان میباشد که بر این اساس کلیه بیماران مورد مطالعه در این تحقیق پاسخ نسبی به درمان داشتهاند.
نتایج مطالعه حاضر نشان داد که میانگین بیان گیرنده CCR-5 در گروه بیماران بعد از شیمی درمانی در مقایسه با گروه کنترل سالم تغییری نکرده است و تفاوت معناداری وجود نداشته است(شکل 1)(جدول 2)(نمودار 1).

شکل 1: بیان گیرنده CCR5 توسط لکوسیتهای خون محیطی. سلولها با PE-conjugated MAb CCR5 رنگ آمیزی و توسط فلوسایتومتری تجزیه و تحلیل شدند. کل جمعیت لکوسیتها جداسازی شدند. هیستوگرام نشان دهنده فلورسانس PE است، با استفاده ازisotype-matched murine MAb به عنوان کنترل منفی (A)، نمونه یک کنترل سالم (B)، نمونه یک بیمار بعد از مرحله اول شیمی درمانی (هفته چهارم پس از شیمی درمانی)(C). منطقه R1 جمعیت لکوسیتها را نشان میدهد و RN2 منطقهی سلولهای بیان کننده گیرنده CCR5 را نشان میدهد.
جدول 2: بیان گیرنده CCR5 در گروه کنترل سالم و بیمار توسط فلوسیتومتری
| گروه مورد مطالعه | کنترل سالم | گره بیمار بعد از مرحله اول شیمی درمانی |
| حجم نمونه | 25 | 25 |
| بیان گیرنده CCR5 | 16/0 ± 04/1 | 26/0 ± 04/1 |

نمودار 1: مقایسه میانگین میزان بیان گیرنده CCR-5در لکوسیتهای بیماران مبتلا به لوسمی میلوئیدی حاد با تمایز منوسیتی بعد از مرحله اول شیمی درمانی و گروه کنترل سالم. مقایسه بین دو گروه نشان داد که تفاوت معناداری بین آنها وجود ندارد.
بحث
نتایج این مطالعه نشان داد که بیماران مبتلا به لوسمی میلوئیدی حاد با تمایز منوسیتی، افزایش معناداری در بیان گیرندهCCR5 ، بعد از مرحله اول شیمی درمانی نشان ندادهاند و میزان بیان این گیرنده در بیماران پس از شیمی درمانی مرحله اول با گروه کنترل سالم مشابه بوده است. شاید این یک نتیجه مطلوب در شیمی درمانی میباشد و این که شیمی درمانی سبب میشود تا این گیرنده کموکاینی افزایش چندانی نداشته تا سبب بدخیم شدن بیماری شود. برخی از کموکاینها به همراه گیرنده خود در پاتوژنز بیماری AML نقش دارند(13). یکی از این کموکاینها و گیرنده آنها CCR5/CCL5 میباشد، این محور در سلولهای بلاست لوسمی بیماران مبتلا به AML افزایش مییابد(14).
|
بیمار بعد از مرحله شیمی درمانی کنترل سالم
|
|
00/2
50/1 00/1 50/0 00/0 |
سلولهای سرکوبگر گرانولیسیتیک و مونوسیتیک مشتق میلوئیدی موشی مقدار بالایی از لیگاندهای CCR5 شامل؛ CCL3، CCL4 و CCL5 تولید میکنند، که همه آنها مسئول جمعآوری سلولهای T تنظیمی هستند. کمبود CCR5 باعث کاهش شدید آنها میشود، که بخش مهمی از CCR5 را در کنترل واکنشهای ایمنی ضد تومور نشان میدهد. بنابراین، مهاجرت سلولهای T تنظیمی به سمت ساختار ریز محیط تومور، در طی توسعه تومور توسط محور CCL5-CCR5 صورت میگیرد(9).
شاید بتوان سلولهای میلوئید سرکوب کننده ایمنی (IMC: Immunosuppressive myeloid cells) را به عنوان تنظیمگر منفی ایمنی علیه تومور تعریف کرد. محور CCL5/CCR5 در تومورژنسیس، پیشسازهای سلولی در مغز استخوان را به سمت سلولهای IMC رده گرانولوسیتی و مونوسیتی پیش میبرد و این سلولها خود سبب افزایش سلولهای T تنظیمی میشوند و متعاقباً سلولهای T تنظیمی، سلولهای TCD8+ را که نقش بالقوهای در مبارزه با سلولهای توموری بازی میکنند کاهش میدهند. اگر چه تاکنون مطالعهای بر روی نقش این محور کموکاین ـ رسپتوی در AML انجام نگردیده است ولی در راستای این قاعده در سال 2017، ییبان و همکارانش پژوهشی را بر روی بیماران مبتلا به سرطان سینه انجام دادند. این پژوهشگران توسط پارتیکلهایی که سبب خاموش شدن ژن CCL5 میشود، CCL5 در مغز استخوان را مورد هدف قرار دادند و هم چنین از آنتاگونیست Maraviroc به عنوان مهارکننده گیرنده CCR5 استفاده کردند که منجر به کاهش چشمگیر سلولهای IMC شد. بنابراین بر این اساس مطالعهها نشان داده است که هدف قرار دادن محور CCL5/CCR5، اثر درمانی بالقوهای در سرطان سینه دارد(14).
در مطالعهای دیگر در سال 2017، زی جی و همکاران اثر maraviroc بر روی سلولهای لوسمی لنفوئید حاد را مورد مطالعه قرار دادند. نتایج این پژوهش نشان داد که آنتاگونیست گیرندهCCR5 ، به طور چشمگیری رشد سلولهای لوسمی لنفوئید حاد رده سلولی SUP_B15 را مهار و سبب آپوپتوز این سلولها شد. این آنتاگونیست، سیگنالینگ فعال شده توسط CCR5، یعنی JAK1، JAK2 و STAT3 را مهار و در نتیجه سبب مهار رشد سلولهای توموری SUP_B15 که به موشهای فاقد تیموس پیوند زدهاند میشود. این مطالعه نشان داد که maraviroc به عنوان مهارگر گیرنده CCR5 میتواند یک راه درمانی برای بیماران مبتلا به لوسمی لنفوئید حاد باشد(10).
گیرنده CCR5 علاوه بر CCL5 به کموکاینهای CCL4 و CCL3 نیز متصل میشود(15). در طی مطالعهای کویچی تاکاهاشی و همکاران، مارکرهای CCL4 و CCL3 در بیماران مبتلا به لنفوم منتشر سلول B بزرگ(DLBCL : diffuse larg B cell lymphoma) را بعد از شیمی درمانی مورد بررسی قرار دادند. سطح سرمی CCL3 اکثر بیماران بعد از درمان کاهش یافت، در این بیماران پیشرفت بیماری مشاهده نشد و نیمی از بیماران کاهش CCL4 را نشان دادند. محققین در این مطالعه دست یافتند که غلظت بالای CCL4 و CCL3 مرتبط با پیشآگهی ضعیف در بیماران DLBCL میباشد(16). این مطالعه فقط بر روی کموکاینها و در بیماری DLBCL صورت گرفته است و گیرنده آنها را مورد بررسی قرار نداده است. در این مطالعه مشاهده کردیم که بیان گیرنده CCR5 بعد از شیمی درمانی، در بیماران مبتلا به AML ، همسان با گروه کنترل و دارای اثر مطلوبی میباشد و یافتهها همسان با یافتهها در مطالعه کویچی تاکاهاشی و همکاران است هر چند که تحقیق آنها در بیماری متفاوت و بر روی کموکاینها بوده است.
تاکنون تنها مطالعههای معدودی به بررسی ارتباط بین کموکاینها و ناهنجاریهای ایمونولوژیکی در بیماران مبتلا به لوسمی میلوئید حاد پرداختهاند. طبق بررسیهای انجام شده توسط ما تاکنون این مطالعهها بر روی مغز استخوان و سلولهای بلاست لوسمی این بیماران صورت گرفته است، حال که برخی از لکوسیتهای غیر لوسمی
نیزCCR5 را بیان میکنند و مطالعههایی در این زمینه بر روی لکوسیتها در خون محیطی صورت نگرفته است.
در نتیجه عدم افزایش بیان این گیرنده سبب میشود که سلولهای IMC که به عنوان تنظیمگر منفی ایمنی علیه تومور میباشند، افزایش پیدا نکنند که یک پیشآگهی خوب برای بیماران تلقی گردیده و احتمال عود بیماری را کاهش دهد.
نتیجهگیری
شیمی درمانی اثر نامطلوبی بر بیان گیرنده CCR5 که توسط لکوسیتهای خون محیطی بیان میشدند نداشته است و هم چنین سبب شده است که این گیرنده در حالت پایه خود در مقایسه با گروه کنترل سالم قرار بگیرد. با توجه به این مطالعه میتوان سایر محورهای کموکاین و گیرندههای آنها را مورد بررسی قرار داد که کدام محور کموکاینی نقش به سزایی در عود بیماران لوسمی میلوئید حاد خواهد داشت که شیمی درمانی روی آن محور کموکاینی تاثیری نخواهد داشت تا با مسدود کردن آن محور بتوان به نتایج مطلوبتری در شیمی درمانی دست یافت و از عود بیماری جلوگیری کرد.
از محدودیتهای این مطالعه نداشتن بودجه و زمان کافی بود. بهتر است این مطالعه در تک تک مراحل شیمی درمانی صورت گیرد و هم چنین دیگر محورهای کموکاینی و گیرندههای آنها نیز بررسی گردد.
تشکر و قدردانی
پژوهش حاضر با کمک مالی از دانشگاه علوم پزشکی کرمان صورت گرفت. ما هم چنین از تمام بیماران و همین طور افراد سالم که در این مطالعه شرکت کردهاند و هم چنین تمام کارکنان در مرکز درمانی بیمارستان شهید باهنر کرمان تشکر میکنیم که در این مطالعه همکاری لازم را داشتند.
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |






