جلد 16، شماره 1 - ( بهار 1398 )
جلد 16 شماره 1 صفحات 56-44 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Mohammadi Kian M, Mohammadi M, Tavallaie M, Sadeghi M, Nikbakht M. The impact of Arsenic trioxide and thalidomideon VEGF A gene expression in AML cell lines. Sci J Iran Blood Transfus Organ 2019; 16 (1) :44-56
URL: http://bloodjournal.ir/article-1-1198-fa.html
URL: http://bloodjournal.ir/article-1-1198-fa.html
محمدی کیان مهناز، محمدی سعید، تولایی محمود، صادقی مرتضی، نیکبخت محسن. اثر آرسنیک تریاکساید و تالیدوماید بر بیان ژن VEGF Aدر ردههای سلولی AML. فصلنامه پژوهشی خون. 1398; 16 (1) :44-56
مرکز تحقیقات ژنتیک انسانی دانشگاه علوم پزشکی بقیه اله
متن کامل [PDF 1060 kb]
(1813 دریافت)
| چکیده (HTML) (31424 مشاهده)
مقدمه
لوسمی میلوئیدی حاد(AML) یکی از شایعترین لوسمیها در بالغین محسوب میشود که از کشندگی زیادی نیز برخوردار است(1). پیشآگهی برای بالغین اغلب بد است به نحوی که بقای کلی بلند مدت(OS = Overall Survival) برای بیماران جوانتر حدود 40 تا 50 درصد بوده و برای بیماران در سنین بالاتر، به طور متوسط کمتر از یک سال است(2). فاکتور رشد VEGF (Vascular endothelial growth factor)، فاکتور به نسبت جدیدی است، که قابلیتهای بیولوژیک بسیار متنوعی را داراست. رگزایی در تومور به VEGF بستگی دارد، بسیاری از ردههای سلولی توموری در In vitro ، VEGF را ترشح میکنند(4، 3). تولید VEGF و رسپتورش به طور مستقیم میزان رگزایی در تومور را کنترل میکنند. با توجه به این که VEGF نقطه استراتژیکی در تنظیم رگزایی در تومور است، هدف مهمی در وقایع درمانی محسوب میگردد(6، 5). استفاده از آنتیبادی بر علیه VEGF و رسپتور آن و یا استفاده از مهارکنندههای تیروزین کیناز، نتایج مطلوبی در مطالعههای کلینیکی در ارتباط با درمان تومورها داشته است(7). داروها با اساس آرسنیک به عنوان عوامل شیمی درمانی مؤثر برای درمان بیماریهای مختلف و برخی از تومورها استفاده شده است. در سالهای اخیر As2O3 به عنوان یک ماده ضد لوسمی بسیار قوی به خصوص در برابر لوسمی پرومیلوسیتی حاد(APL) شناخته شده است(8). آرسنیک تریاکسید در دوزهای پایین به تنهایی نمیتواند موجب القای آپوپتوز شود و برای حذف سلولهای توموری با آن دوزهای بالا نیاز است، اما دوز بالا موجب عوارض جانبی بر روی بیماران APL میشود(9). به منظور کاهش دوز آرسنیک تریاکساید و دسترسی به افزایش اثرات شیمیدرمانی، روشهای درمانی به صورت استفاده ترکیبی از داروهایی که مکانیسم مشابهای برای جلوگیری از تکثیر و یا از بین بردن سلولهای سرطانی دارند؛ باید طراحی شوند، که از یک طرف موجب افزایش تاثیر درمان و از طرف دیگر موجب کاهش اثرات ناخواسته گردند(11، 10). تالیدوماید دارای خـواص ایمونومدولاتـوری، ضد التهابی و آنتیآنژیوژنیک
میباشد. تالیدوماید در سال۱95۶ اولین بار در آلمان تولید شد و به عنوان داروی بیخوابی و رفع تهوع صبحگاهی در خانمهای باردار به مصرف رسید ولی به دنبال داشتن عوارض تراتوژنیک مصرف آن متوقف گردید. با وجود عوارض جدی که متاسفانه این دارو ایجاد میکند، تحقیق در زمینه تاثیرات بالقوه این دارو جذابیت خاصی برای دانشمندان دارد و مشخص گردید که این دارو یک داروی بسیار مناسب بر علیه التهاب و سرطان است(12، 10). این دارو با اثر سرکوبکنندگی بر مرحله مهم تشکیل رگ یعنی خاموشی بیان اینتگرین به علت اثر سرکوبکنندگی بر TNF-α , INF-γ ایفای نقش میکند. دو رده سلولی KG-1 و U937 به عنوان دو مدل حساس و مقاوم به داروهای رایج در درمان AMLدر این مطالعه استفاده شدند. رده سلولی KG-1 از بیماری 59 ساله با لوسمی میلوژنی M0 استخراج شده است. سلول KG-1 به عنوان مدل LSCs (Leukemia Stem Cell) در مطالعههای تحقیقاتی استفاده میشود و دارای شباهت مورفولوژیکی و فیزیولوژیکی با سلولهای میلوئید بالغ و نابالغ (Dendritic cell) DC میباشد. این سلولها دارای مارکرهای متعدد توموری بوده و در مطالعههای تومورژنیسیتی و تمایز مورد استفاده قرار میگیرند. رده سلولی U937 نمونه AML بیمار 37 ساله با لوسمی میلوژنی M5 میباشد که بسیاری از خصوصیات مونوسیت را به نمایش میگذارد و مورد استفاده مطالعههای رفتاری و تمایزی مونوسیتها و نیز به عنوان مدلی برای نشان دادن تمایز ماکروفاژ/ مونوسیت، آزمایشهای ضد توموری و تومورژنیسیتی مورد استفاده قرار میگیرد. به طور معمول درمان(7+3) AML شامل ترکیبی ازcytarabine و یک anthracycline از قبیل (DNR) daunorubicin یا (mitoxantrone) anthracenedioneاست که در مطالعههای تحقیقاتی آزمایشگاهی استفاده میشوند(13). از مجموع آن چه گفته شد برآن شدیم که برای اولین بار به ارزیابی اثر ترکیبی دو داروی آرسنیک تریاکساید وتالیدوماید به عنوان یک ترکیب جدید با خاصیت ضد سرطانی منحصر به فرد بر روی بیان ژن A VEGF و بررسی آپوپتوز در محیط آزمایشگاهی بر روی سل لاینهای مقاوم و حساس
به داروهای متداول شیمیدرمانی AML بپردازیم.
مواد و روشها
کشت سلولی:
مطالعه انجام شده از نوع تجربی بود. دو رده سلولی KG-1 و U937 در محیط RPMI1640 با 10% سرم گاوی (Fetal Bovin Serum) برای U937 و 20% سرم گاوی برای KG-1 ، همراه با U/mL ۱۰۰ پنیسیلین و μg/mL ۱۰۰ استرپتومایسین کشت و نگهداری میشود. سلولها در انکوباتور با دمای ۳۷ درجه سانتیگراد، رطوبت و ۵% دیاکسید کربن، انکوبه خواهند شد.
Microculture Tetrazolium Test (MTT) :
برای اندازهگیری اثر مهاری تالیدوماید(سانتاکروز) و آرسنیک تری اکساید(سینا دارو) برروی فعالیت متابولیکی سلولهایU937 و KG-1 به روش MTT Assay ]برای ساخت محلولMTT ، 5 میلی گرم پودر MTT را در 1 میلیلیتر محیط RPMI 1640 بدون FBS حل کرده (این پودر به سختی حل میشود) تا محلول mg/mL 5 ساخته شود. سپس با محیط RPMI آن را به حجم 10 میلیلیتر رسانده تا استوک mg/mL 5/0 ساخته شود(این محلول به صورت تازه استفاده میشود)[. در 24 ، 48 و 72 ساعت از پودرMTT (مشتق از نمکهای تیازول) و محلول DMSO (دیمتیل سولفواکساید) استفاده خواهد شد. محلول MTT (mg/mL 5/0) به مقدار 50 میکرولیتر به سلولها اضافه میشود و سلولها به مدت چهار ساعت در 37 درجه سانتیگراد انکوبه خواهند شد تا این محلول را متابولیزه کنند. رسوب فرمازان تشکیل شده با 100 میکرولیتر DMSO حل خواهد شد و محلول بنفش رنگی
ایجاد میشود. این مراحل باید به سرعت انجام گیرد(بین 1 تا 2 دقیقه بعد از ریختن محلول DMSO ، سلولها باید در دستگاه ELISA Reader قرار بگیرند) زیراDMSO در صورت تماس طولانی مدت با سلولها برای آنها سمی است و سپس جذب نوری با دستگاه الایزا ریدر در طول موج ۵۷۸ نانومتر خوانده خواهد شد. سلولها با غلظتهای µmol 100-5 تالیدوماید و µmol 5-4/0 آرسنیک به مدت 24 ، 48 و 72 ساعت تیمار میشوند.
سنجش میزان آپوپتوزسلولی به روش فلوسیتومتری:
بدین منظور 24 و 48 ساعت پس ازتیمار نمودن ردههای سلولی KG-1 و U937 توسط آرسنیک تریاکساید و تالیدوماید و نیز ترکیب آرسنیک تریاکساید با تالیدوماید که در پلیتهای 24 خانه کشت داده شده بودند، با استفاده از کیت رنگی دوگانه Annexin/PI سلولها جهت بررسی میزان آپوپتوز رنگآمیزی شدند.در این روش سلولهای تیمار شده با بافر شسته شد و سوسپانسیون سلولی تهیه گردید(106× 1 در هر میلیلیتر). ابتدا سلولها جمعآوری شده و با دور G 600 در دمای اتاق به مدت 5 دقیقه سانتریفوژ شدند. سلولها 1 بار توسط PBS 1X شسته شدند. به هر لوله ۱۰۰ میکرو لیتر از Binding buffer 1X که به آن ۱ میکرولیتر از رنگ آنکسین با غلظت استوک mg/mL ۵/۰ و µL۱ از PI با غلظت استوک mg/mL ۱/۰ اضافه شده بود، افزوده و لولهها به آرامی ورتکس شدند. لولهها به مدت 15-10 دقیقه در تاریکی و در دمای اتاق قرار داده شدند و سپس بلافاصله توسط فلوسیتومتری آنالیز شدند. نتایج دستگاه فلوسیتومتری توسط نرمافزار FlowJO باversion (7.6.1) تجزیه و تحلیل شدند.
استخراج RNA ، ساخت cDNA و بررسی بیان ژن توسط Real Time quantitative PCR :
برای استخراج RNA سلولها TriPure (رُوش) مورد استفاده قرار گرفت.
برای اندازه گیری غلظت RNA نمونهها از دستگاه نانو دراپ(آلمان، NanoDrop) استفاده گردید. با استفاده از کیت cDNA سنتاز (Takara Bio) از RNAها ، cDNA ساخته شد و تغییرات در سطح mRNA به روش Real-time PCR انجام شد. روش Real-time PCR با دستگاه light cycler instrument (دیاگنوستیک، رُوش، آلمان) انجام شد. برای انجام PCR برای هر نمونه مقدار 10 میکرو لیترSYBR Green master mix ، 2 میکرولیتر cDNA ، 1 میکرولیتر آغازگر معکوس و1 میکرولیتر آغازگر جلوبرنده(10 پیکومول) و 6 میکرولیتر آب با هم ادغام گردید(جدول 1).
برنامه دمایی PCR برای مرحله فعالسازی اولیه در 95 درجه سانتیگراد به مدت 30 ثانیه، مرحله دناتوراسیون در 95 درجه سانتیگراد به مدت 5 ثانیه و برای مرحله آنیلینگ/اکستنشن در 60 درجه سانتیگراد به مدت20 ثانیه و تعداد چرخههای دمایی 40 بار خواهد بود.
به منظور تکثیر هر قطعهی ژنی، یک جفت آغازگر اختصاصی برای هر ژن انتخاب شد که شامل آغازگر جلوبرنده و معکوس بود. اختصاصیت تمامی آغازگرها با نرمافزار آنلاین Primer-BLAST (وب سایتNCBI) تأیید شده است.
یافتهها
بررسیهای MTT در رده سلولی KG-1 :
نتایج حاکی از آن است که در رده سلولی KG-1 اثر آرسنیک تریاکساید در دوزهای ۶۱۸/۱ (اگر چه مقدار دوز آرسنیک تریاکساید در رده سلولی KG-1 یک مقدار عددی میباشد و یک نسبت نیست؛ با این وجود این دوز نتایج مؤثرتری نسبت به دوزهای بالا و پایینتر خود نشان داده است. اخیراً استفاده از این نسبت در پروژههای مربوط بهDrug discovery بررسی شده است) تا ۵ میکرومولار و اثر تالیدوماید در دوزهای ۶۰ تا ۱۰۰ میکرومول قابل توجه بوده است(نمودار 1)(14). هم چنین اثر ترکیبی این دو دارو نشان میدهد ۶۱۸/۱ میکرومولار آرسنیک تریاکساید و۸۰ میکرومولار تالیدوماید میتوانند کشندگی بیشتری به دنبال داشته باشند(نمودار 1).
بررسیهای MTT در رده سلولی U937 :
نتایج حاکی از آن است که در رده سلولی U937 اثر آرسنیک تریاکساید در دوزهای ۱ تا ۵ میکرومولار و اثر تالیدوماید در دوزهای ۶۰ تا ۱۰۰ میکرومولار قابل توجه بوده است(نمودار 2). هم چنین اثر ترکیبی این دو دارو نشان میدهد ۱ میکرومولار آرسنیک تریاکساید و۶۰ میکرومولار تالیدوماید میتوانند کشندگی بیشتری به دنبال داشته باشند(نمودار 2).
همان طور که نتایج نمودارهای فوق نشان میدهد درصد بقای سلولهای تیمار شده با آرسنیک تریاکساید و تالیدوماید در یک روند وابسته به دوز و زمان نسبت به گروه کنترل کاهش مییابد.
در ادامه جهت تایید نتایج بقا حاصل از آزمایش MTT، به منظور ارزیابی اثر القایی آرسنیک تریاکساید به تنهایی یا در ترکیب با تالیدوماید بر فعالیت کشندگی و مهار رشد سلولی و مشخص شدن این که این اثر با واسطه آپوپتوز و یا با واسطه نکروز سلولی است، رنگآمیزی Annexin/PI انجام شد و درصد سلولهای آپوپتوتیک تعیین گردید. نتایج Annexin/PI مؤید این مسئله است که آرسنیک تریاکساید و تالیدوماید دارای اثرات کشندگی در هر دو رده سلولی در یک روند وابسته به دوز است.
بررسیها به منظور تعیین اثرات تیمار هم زمان ترکیبی آرسنیک تریاکساید و تالیدوماید بر بقا و رشد دو رده سلولی KG-1 و U937 در یک بازه زمانی 48 ساعتی صورت گرفت.
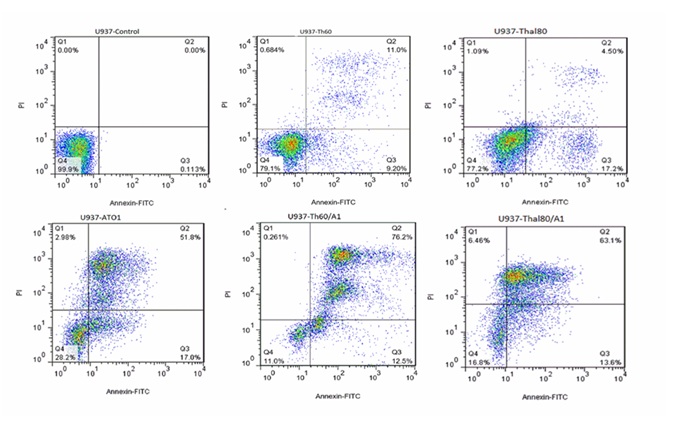
در این آزمایش تنها جمعیتهایی که Annexin+ و یا Annexin+/PI+ باشند حائز اهمیت بوده و جمعیتهای PI+ به تنهایی حاکی از نکروز سلولی بوده که فاقد اهمیت میباشند(شکلهای 1 و 2).

نمودار 1 : A) نمودار ستونی اثر مهاری غلظتهای مختلف(µM 5-4/0) آرسنیک تریاکساید بر رشد سلولها و بقا. B : نمودار ستونی اثر مهاری غلظتهای مختلف(µM 100- 5) تالیدوماید بر رشد سلولها و بقا. C : نمودار ستونی اثر مهاری غلظتهای مختلف آرسنیک تریاکساید و تالیدوماید و همچنین اثر ترکیبی آنها بر رشد سلولها و بقا. رده سلولی KG-1 در بازه زمانی 24، 48 و 72 ساعت با استفاده از روش MTT .
با سه بار تکرار به صورت SD±mean نمایش داده شده و تفاوت آماری معنادار در مقایسه با گروه کنترل به صورت 05/0 p< * و 01/0 p< ** تعریف شده است.
نمودار 2 : A) نمودار ستونی اثر مهاری غلظتهای مختلف(µM 4-5/0) آرسنیک تریاکساید بر رشد سلولها و بقا. B) نمودار ستونی اثر مهاری غلظتهای مختلف(µM 100- 5) تالیدوماید بر رشد سلولها و بقا. C) نمودار ستونی اثر مهاری غلظتهای مختلف آرسنیک تریاکساید و تالیدوماید و هم چنین اثر ترکیبی آنها بر رشد سلولها و بقا. رده سلولی U937 در بازه زمانی24، 48 و 72 ساعت با استفاده از روش MTT . با سه بار تکرار به صورت mean ± SD نمایش داده شده و تفاوت آماری معنادار در مقایسه با گروه کنترل به صورت 05/0 p< *، 01/0 p< ** و 001/0 p< *** تعریف شده است.

شکل 1: بررسی آپوپتوز با داروهای آرسنیک تریاکساید و تالیدوماید بر روی KG-1

شکل 2: بررسی آپوپتوز با داروهای آرسنیک تریاکساید و تالیدوماید بر روی U937

نمودار 3 : نتایج بررسی آپوپتوز سلولی حاصل از رنگ آمیزی Annexin/PI در رده سلولی KG-1 در بازه زمانی 48 ساعت به دنبال تیمارسازی با غلظتهای(µM۶۱۸/۱) آرسنیک تریاکساید و غلظت(Mµ 60 و80) تالیدوماید و مقادیر ترکیبی آنها را نشان میدهد.

نمودار 4: نتایج بررسی آپوپتوز سلولی حاصل از رنگآمیزی Annexin/PI در رده سلولی U937 در بازه زمانی 48 ساعت به دنبال تیمارسازی با غلظتهای (µM 1) آرسنیک تریاکساید و غلظت(µM 60 و80) تالیدوماید و مقادیر ترکیبی آنها را نشان میدهد.

نمودار 5: نتایج تیمار سلولها با آرسنیک تریاکساید(µM ۶۱۸/۱) و تالیدوماید(µM 60 و80) و ترکیب آرسنیک و تالیدوماید بر روی بیان VEGF A. در یک بازه زمانی 48 ساعتی. نمونهها با سه بار تکرار به صورت SD ± mean نمایش داده شدهاند و تفاوت آماری معنادار در مقایسه با گروه کنترل به صورت 05/0 p< * ، 01/0 p< ** و 001/0 p< *** تعریف شده است.

نمودار 6 : نتایج تیمار سلولها با آرسنیک تریاکساید(µM 1) و تالیدومایدµM) ۶۰ و۸۰) و ترکیب آرسنیک و تالیدوماید بر روی بیان VEGF A. در یک بازه زمانی 48 ساعته. نمونهها با سه بار تکرار به صورت SD ± mean نمایش داده شدهاند و تفاوت آماری معنادار در مقایسه با گروه کنترل به صورت 05/0 p< * ، 01/0 p<** و 001/0 p< *** تعریف شده است.
نتایج برسی Annexin/PI در رده سلولی KG-1 و :U937
نتایج نشان داد که سلولهای KG-1 و U937 تیمار شده با دوزهای ترکیبی آرسنیک تریاکساید و تالیدوماید، یک افزایش آپوپتوتیک قابل توجهی را نسبت به دوزهای آرسنیک تری اکساید و تالیدوماید به تنهایی، نشان میدهد(نمودارهای 3 و 4).
نتایج بررسی اثر آرسنیک تریاکساید و تالیدوماید بر روی بیـان ژن A VEGF در سطـح mRNA در ردهی سلولی KG-1 :
نتایج بررسی میزان بیان ژن VEGF A در رده سلولی KG-1 نشان میدهد میزان بیان در دوزهای ۶۰ و۸۰ میکرومولار تالیدوماید کاهشی و در دوز ۶۱۸/۱ آرسنیک تریاکساید افزایشی بوده و هم چنین اثر ترکیبی این دو دارو میزان بیان را به نسبت کنترل کاهش میدهد، این کاهش بیان در دوز ۸۰ میکرومولار تالیدوماید و ۶۱۸/۱ آرسنیـک تـریاکساید بیشتر نشان داده شده است (نمودار
5).
نتایج بررسی اثر آرسنیک تریاکساید و تالیدوماید بر روی بیان ژن A VEGFدر سطح mRNA در ردهی سلولیU937:
نتایج بررسی میزان بیان ژن VEGF A در رده سلولی U937 نشان میدهد میزان بیان در دوزهای ۶۰ و۸۰ میکرومولار تالیدوماید کاهشی بوده و در دوز ۱ میکرومولار آرسنیک تریاکساید نیز کاهشی بوده و هم چنین اثر ترکیبی این دو دارو میزان بیان را به نسبت کنترل کاهش میدهد، این کاهش بیان در دوز ۶۰ میکرومولار تالیدوماید و ۱ آرسنیک تری اکساید بیشتر نشان داده شده است(نمودار 6).
بحث
لوسمی میلوئیدی حاد یکی از شایعترین اختلالات هماتولوژیک است. اگر چه بیش از 80 درصد بیماران مبتلا به AML با داروهای رایج امروزی به مرحله خاموشی کامل میرسند، ولی میزان بقای 5 ساله تنها بین 40 -50 درصد میباشد و شانس بقای طولانی مدت بسیار پائین است، که این خود حاکی از ناکارآمد بودن درمانهای رایج میباشد(15). داروها با اساس آرسنیک به عنوان عوامل شیمیدرمانی مؤثر برای درمان بیماریهای مختلف و برخی از تومورها استفاده شده است(14). در مطالعهها نشان داده شده که این ترکیب سبب توقف چرخه سلولی و القای آپوپتوز درسلولهای APL وnon-APL میشود. بنابراین تصمیم گرفتیم برای اولین بار به ارزیابی اثر ترکیبی تالیدوماید و آرسنیک تریاکساید بر روی بیان ژن VEGF A در سللاینهای U937 و KG-1 بپردازیم.
در این مطالعه ارزیابی اولیه توسط MTT به منظور تعیین اثرات توکسیک آرسنیک تریاکساید و تالیدوماید در بازه زمانی مختلف در دو ردهی سلولی KG-1 و U937 صورت گرفت. دوز انتخابی توسط این آزمایش ۶۱۸/۱ میکرومولار برای آرسنیک تریاکساید و ۶۰ و۸۰ میکرو مولار بـرای تالیدومایـد و هم چنیـن دوز ترکیبی(µMT80 µMA- ۶۱۸/۱) برای ردهی سلولی KG-1 در نظر گرفته شد. هم چنین دوزهای انتخابی توسط آزمایش µM 1 برای آرسنیک تریاکساید و µM 60 و80 برای تالیدوماید در رده سلولی U937 در نظر گرفته شد. هم چنین دوز ترکیبی) µM T۶0µM A - ۱) برای ردهی سلولی U937 در نظر گرفته شد. برای تعیین میزان آپوپتوز و نکروز توسط این دوزها، آزمایش فلوسایتومتری انجام شد. نتایج حاکی از آن بود که این دوزهای آرسنیک و تالیدوماید و اثر ترکیبی آنها قادر به القای درصد قابل توجهی از آپوپتوز میباشد. علاوه بر آن که مطالعههای گذشته بیانگر آن هستند که دوز استاندارد برای القای آپوپتوز توسط آرسنیک تریاکساید در محدوده غلظتی 2-5/0 میکرو مولار است. بنابراین دوزهای اصلی برای این مطالعه برای آرسنیک ۶۱۸/۱ میکرومولار و ۱ میکرومولار به ترتیب در رده سلولی KG-1 وU937 انتخاب شد. بر اساس نتایج حاضر، آرسنیک تریاکساید و تالیدوماید در مهار رشد و القای آپوپتوز در رده سلولی KG-1 و U937 به صورت وابسته به دوز و زمان عمل کرده است.
در مطالعهها مشخص شده است که VEGF (VEGF A) فاکتور رشد اختصاصی برای آنژیوژنز میباشد. VEGF ترشح شده توسط سلول لوسمی با گیرندههای مربوطه در سطح سلولهای اندوتلیال در ارتباط است و سلولهای اندوتلیال را برای تولید فاکتورهای رشد که بر روی سلولهای لوسمیک قرار دارند؛ تحریک میکند در نتیجه فعالیت تکثیری و مقاومت دارویی افزایش مییابد(16). بنابراین درمان ضد آنژیوژنز بر اساس مهار فعالیت فیزیولوژیکی VEGF یک استراتژی جدید برای درمان هدفمند است. در مطالعههای اخیر بیان VEGF و VEGF-R در بیماران AML مشاهده شده است.
آرسنیک تریاکساید به عنوان یک داروی چند هدفی(Multi target) شناخته شده است. آرسنیک تریاکساید قادر به فعال کردن JNKs میباشد. JNKs یک پروتئین کیناز فعال شده میتوژنی است که با فعال کردن ROS و به دنبال آن فعال شدن Cyt P450 و P38 MAPK منجر به القای آپوپتوز و هم چنین باعث مهار مسیر PI3K-Akt-mTOR شده و از سوی دیگر، JNKs سبب افزایش بیان PTEN که یک سرکوبگر تومور است؛ میشود که منجر به مهار PI3K-Akt-mTOR خواهد شد. از آن جایی که مسیر PI3K-Akt-mTOR مسیر حفظ حیات سلول شناخته میشود؛ مهار این مسیر میتواند مرگ سلولی را افزایش دهد. هم چنین در مطالعههای گذشته نشان دادهاند که آرسنیک تریاکساید باعث فعال شدن سیتوکروم C و فعال شدن مسیر آبشاری کاسپازها و درنهایت آپوپتوز میشود(17).
تالیدوماید با اثر بر روی ژنهای مسیر رگزایی میتواند از توسعه سرطان پیشگیری کند. تالیدوماید اثر مهاری خود را بر روی رگزایی توسط مهار β-FGF در rabbit cornea و توسط مهار VEGF در murine model نشان داد(19، 18).
تالیدوماید به علت ویژگی ضد رگزایی خود روی
چندین نوع از تومورها تحت ارزیابی قرار گرفته است، مثل بدخیمیهای هماتولوژیک، میلوم مالتیپل و تومورهای جامد. در این مطالعهها نشان داده شده است که تالیدوماید موجب کاهش بیان عوامل مؤثر در رگزایی میشود(24-20).
استینز و همکاران در سال ۲۰۰۲ در مطالعه خود نتایج مشابهی را گزارش کردند که تالیدوماید با پایین آوردن سطح FGF-2 و VEGF باعث آنتی آنژیوژنز میشوند(25).
روبوز در سال 2000 نشان داد که آرسنیک تریاکساید با مهار VEGF منجر به القای آپوپتوز در لوسمی میشود. هم چنین آنها نشان دادند که این دارو PML/RAR-α را تخریب میکند(18).
چن و همکارانش با بررسیهایی بر روی NB4 و آرسنیک تریاکساید افزایش آپوپتوز را به واسطه کنترل کردن bcl-2 و PML/RAR-α نشان دادند(26).
یانگ و همکارانش در مطالعهای بر روی سرطان ریه در سال 2014 نشان دادند که آرسنیک تریاکساید با مهار فاکتورهایی از قبیل VEGF-A، VEGFR-2، HIF-1α و Notch-1 مسیر آنژیوژنز را مهار میکند(27).
نتیجهگیری
اثر ترکیبی این دارو سبب افزایش آپوپتوز سلولی و کاهش میزان بیان ژن اصلی در رگزایی (VEGF A) میشود. با توجه به نتایج حاصل از این مطالعه و نتایج مطالعههای گذشته این دو دارو به صورت ترکیبی میتوانند اثرات مؤثری در درمان سرطان خون ایفا کنند.
تشکر و قدردانی
ﺑﺪﻳﻦ ﻭﺳﻴﻠﻪ ﺍﺯ ﻣﺮﮐﺰ تحقیقات هماتولوژی، آنکولوژی و پیوند مغز استخوان بیمارستان شریعتی ﺑﻪ ﺧﺎﻃر ﺗـﺎﻣﻴﻦ ﺑﻮﺩﺟـﻪ ﻃـﺮﺡ ﻗـﺪﺭﺩﺍﻧﻲ ﻣﻲﮔﺮﺩﺩ.
متن کامل: (4608 مشاهده)
اثر آرسنیک تریاکساید و تالیدوماید بر بیان ژن VEGF A
در ردههای سلولی AML
مهناز محمدی کیان1، سعید محمدی2، محمود تولایی3، مرتضی صادقی4، محسن نیکبخت5
چکیده
سابقه و هدف
آرسنیک تریاکساید اثرات ضد سرطانی روی طیف گستردهای از سرطانها داشته است و عمدتاً با راه انداختن آپوپتوز در سلولهای سرطانی عمل میکنـد. تالیدوماید به عنوان مهارکننده رگزایی مانع افزایش حیات در سلولها میشود. هدف اصلی در این مطالعه، بررسی اثر ترکیبی آرسنیک تریاکساید و تالیدوماید بر روی سطح بیان ژن VEGF A بود.
مواد و روشها
در این مطالعـه تجربی، آزمایش MTTبرای بررسی اثر آرسنیک تریاکساید و تالیدوماید بر مهار رشـد سـلولهـای KG-1 و U937 استفاده شد. دوزهای آرسنیک تریاکساید و تالیدوماید به صورت تک و در ترکیب با هم در زمانهای متفاوت بررسی شدند. بررسی آپوپتوز سلولی از طریق فلوسیتومتری انجام شد و بعد از آن اثر این دو دارو بر بیان ژن VEGF A از طریق Real Time PCR صورت گرفت. از آزمون آماری student-t test، ANOVA و نرمافزار 17 SPSS برای تجزیه و تحلیل اطلاعات استفاده شد.
یافتهها
دوز انتخابی آرسنیک تری اکساید در رده سلولی KG-1 و U937 به ترتیب برابر باμM ۶۱۸/۱ و μM ۱ و دوز انتخابی تالیدوماید در رده سلولی KG-1 و U937 به ترتیب برابر با μM ۸۰ و μM ۶۰ به دست آمد. همراهی دوزهای انتخابی این دو دارو با هم اثر کشندگی بیشتری بر هر دو رده سلولی نشان داد. از طرفی بیان ژن VEGF A در زمان اثردهی هر دو دارو کاهش قابل توجهی داشت.
نتیجه گیری
مطالعه حاضر نشان داد که بیان ژن VEGF A در رده سلولی 1-KG و U937 کاهش یافته و اثر این دو دارو بر روی سلولها باعث القای آپوپتوز شده است. برای تایید این نتایج، بررسی بیشتر در سطح پروتئین لازم است.
کلمات کلیدی
آرسنیک، تالیدوماید، لوسمی میلوئیدی حاد
تاریخ دریافت: 10/2/97
تاریخ پذیرش: 1 /7/97
1- کارشناس ارشد ژنتیک پزشکی ـ مرکز تحقیقات ژنتیک انسانی دانشگاه علوم پزشکی بقیهاله(عج) ـ تهران ـ ایران
2- دکترای تخصصی هماتولوژی ـ استادیار مرکز تحقیقات خون، انکولوژی و پیوند سلولهای بنیادی دانشگاه علوم پزشکی تهران ـ تهران ـ ایران
3- دکترای تخصصی بیوتکنولوژی پزشکی ـ استاد مرکز تحقیقات ژنتیک انسانی دانشگاه علوم پزشکی بقیهاله(عج) ـ تهران ـ ایران
4- دکترای تخصصی ژنتیک ـ استادیار مرکز تحقیقات ژنتیک انسانی دانشگاه علوم پزشکی بقیهاله(عج) ـ تهران ـ ایران
5- مؤلف مسئول: دکترای تخصصی بیوتکنولوژی پزشکی ـ دانشیار مرکز تحقیقات خون، انکولوژی و پیوند سلولهای بنیادی دانشگاه علوم پزشکی تهران ـ تهران ـ خیابان کارگر شمالی ـ بیمارستان شریعتی ـ ایران ـ کدپستی: 1411713131
در ردههای سلولی AML
مهناز محمدی کیان1، سعید محمدی2، محمود تولایی3، مرتضی صادقی4، محسن نیکبخت5
چکیده
سابقه و هدف
آرسنیک تریاکساید اثرات ضد سرطانی روی طیف گستردهای از سرطانها داشته است و عمدتاً با راه انداختن آپوپتوز در سلولهای سرطانی عمل میکنـد. تالیدوماید به عنوان مهارکننده رگزایی مانع افزایش حیات در سلولها میشود. هدف اصلی در این مطالعه، بررسی اثر ترکیبی آرسنیک تریاکساید و تالیدوماید بر روی سطح بیان ژن VEGF A بود.
مواد و روشها
در این مطالعـه تجربی، آزمایش MTTبرای بررسی اثر آرسنیک تریاکساید و تالیدوماید بر مهار رشـد سـلولهـای KG-1 و U937 استفاده شد. دوزهای آرسنیک تریاکساید و تالیدوماید به صورت تک و در ترکیب با هم در زمانهای متفاوت بررسی شدند. بررسی آپوپتوز سلولی از طریق فلوسیتومتری انجام شد و بعد از آن اثر این دو دارو بر بیان ژن VEGF A از طریق Real Time PCR صورت گرفت. از آزمون آماری student-t test، ANOVA و نرمافزار 17 SPSS برای تجزیه و تحلیل اطلاعات استفاده شد.
یافتهها
دوز انتخابی آرسنیک تری اکساید در رده سلولی KG-1 و U937 به ترتیب برابر باμM ۶۱۸/۱ و μM ۱ و دوز انتخابی تالیدوماید در رده سلولی KG-1 و U937 به ترتیب برابر با μM ۸۰ و μM ۶۰ به دست آمد. همراهی دوزهای انتخابی این دو دارو با هم اثر کشندگی بیشتری بر هر دو رده سلولی نشان داد. از طرفی بیان ژن VEGF A در زمان اثردهی هر دو دارو کاهش قابل توجهی داشت.
نتیجه گیری
مطالعه حاضر نشان داد که بیان ژن VEGF A در رده سلولی 1-KG و U937 کاهش یافته و اثر این دو دارو بر روی سلولها باعث القای آپوپتوز شده است. برای تایید این نتایج، بررسی بیشتر در سطح پروتئین لازم است.
کلمات کلیدی
آرسنیک، تالیدوماید، لوسمی میلوئیدی حاد
تاریخ دریافت: 10/2/97
تاریخ پذیرش: 1 /7/97
1- کارشناس ارشد ژنتیک پزشکی ـ مرکز تحقیقات ژنتیک انسانی دانشگاه علوم پزشکی بقیهاله(عج) ـ تهران ـ ایران
2- دکترای تخصصی هماتولوژی ـ استادیار مرکز تحقیقات خون، انکولوژی و پیوند سلولهای بنیادی دانشگاه علوم پزشکی تهران ـ تهران ـ ایران
3- دکترای تخصصی بیوتکنولوژی پزشکی ـ استاد مرکز تحقیقات ژنتیک انسانی دانشگاه علوم پزشکی بقیهاله(عج) ـ تهران ـ ایران
4- دکترای تخصصی ژنتیک ـ استادیار مرکز تحقیقات ژنتیک انسانی دانشگاه علوم پزشکی بقیهاله(عج) ـ تهران ـ ایران
5- مؤلف مسئول: دکترای تخصصی بیوتکنولوژی پزشکی ـ دانشیار مرکز تحقیقات خون، انکولوژی و پیوند سلولهای بنیادی دانشگاه علوم پزشکی تهران ـ تهران ـ خیابان کارگر شمالی ـ بیمارستان شریعتی ـ ایران ـ کدپستی: 1411713131
مقدمه
لوسمی میلوئیدی حاد(AML) یکی از شایعترین لوسمیها در بالغین محسوب میشود که از کشندگی زیادی نیز برخوردار است(1). پیشآگهی برای بالغین اغلب بد است به نحوی که بقای کلی بلند مدت(OS = Overall Survival) برای بیماران جوانتر حدود 40 تا 50 درصد بوده و برای بیماران در سنین بالاتر، به طور متوسط کمتر از یک سال است(2). فاکتور رشد VEGF (Vascular endothelial growth factor)، فاکتور به نسبت جدیدی است، که قابلیتهای بیولوژیک بسیار متنوعی را داراست. رگزایی در تومور به VEGF بستگی دارد، بسیاری از ردههای سلولی توموری در In vitro ، VEGF را ترشح میکنند(4، 3). تولید VEGF و رسپتورش به طور مستقیم میزان رگزایی در تومور را کنترل میکنند. با توجه به این که VEGF نقطه استراتژیکی در تنظیم رگزایی در تومور است، هدف مهمی در وقایع درمانی محسوب میگردد(6، 5). استفاده از آنتیبادی بر علیه VEGF و رسپتور آن و یا استفاده از مهارکنندههای تیروزین کیناز، نتایج مطلوبی در مطالعههای کلینیکی در ارتباط با درمان تومورها داشته است(7). داروها با اساس آرسنیک به عنوان عوامل شیمی درمانی مؤثر برای درمان بیماریهای مختلف و برخی از تومورها استفاده شده است. در سالهای اخیر As2O3 به عنوان یک ماده ضد لوسمی بسیار قوی به خصوص در برابر لوسمی پرومیلوسیتی حاد(APL) شناخته شده است(8). آرسنیک تریاکسید در دوزهای پایین به تنهایی نمیتواند موجب القای آپوپتوز شود و برای حذف سلولهای توموری با آن دوزهای بالا نیاز است، اما دوز بالا موجب عوارض جانبی بر روی بیماران APL میشود(9). به منظور کاهش دوز آرسنیک تریاکساید و دسترسی به افزایش اثرات شیمیدرمانی، روشهای درمانی به صورت استفاده ترکیبی از داروهایی که مکانیسم مشابهای برای جلوگیری از تکثیر و یا از بین بردن سلولهای سرطانی دارند؛ باید طراحی شوند، که از یک طرف موجب افزایش تاثیر درمان و از طرف دیگر موجب کاهش اثرات ناخواسته گردند(11، 10). تالیدوماید دارای خـواص ایمونومدولاتـوری، ضد التهابی و آنتیآنژیوژنیک
میباشد. تالیدوماید در سال۱95۶ اولین بار در آلمان تولید شد و به عنوان داروی بیخوابی و رفع تهوع صبحگاهی در خانمهای باردار به مصرف رسید ولی به دنبال داشتن عوارض تراتوژنیک مصرف آن متوقف گردید. با وجود عوارض جدی که متاسفانه این دارو ایجاد میکند، تحقیق در زمینه تاثیرات بالقوه این دارو جذابیت خاصی برای دانشمندان دارد و مشخص گردید که این دارو یک داروی بسیار مناسب بر علیه التهاب و سرطان است(12، 10). این دارو با اثر سرکوبکنندگی بر مرحله مهم تشکیل رگ یعنی خاموشی بیان اینتگرین به علت اثر سرکوبکنندگی بر TNF-α , INF-γ ایفای نقش میکند. دو رده سلولی KG-1 و U937 به عنوان دو مدل حساس و مقاوم به داروهای رایج در درمان AMLدر این مطالعه استفاده شدند. رده سلولی KG-1 از بیماری 59 ساله با لوسمی میلوژنی M0 استخراج شده است. سلول KG-1 به عنوان مدل LSCs (Leukemia Stem Cell) در مطالعههای تحقیقاتی استفاده میشود و دارای شباهت مورفولوژیکی و فیزیولوژیکی با سلولهای میلوئید بالغ و نابالغ (Dendritic cell) DC میباشد. این سلولها دارای مارکرهای متعدد توموری بوده و در مطالعههای تومورژنیسیتی و تمایز مورد استفاده قرار میگیرند. رده سلولی U937 نمونه AML بیمار 37 ساله با لوسمی میلوژنی M5 میباشد که بسیاری از خصوصیات مونوسیت را به نمایش میگذارد و مورد استفاده مطالعههای رفتاری و تمایزی مونوسیتها و نیز به عنوان مدلی برای نشان دادن تمایز ماکروفاژ/ مونوسیت، آزمایشهای ضد توموری و تومورژنیسیتی مورد استفاده قرار میگیرد. به طور معمول درمان(7+3) AML شامل ترکیبی ازcytarabine و یک anthracycline از قبیل (DNR) daunorubicin یا (mitoxantrone) anthracenedioneاست که در مطالعههای تحقیقاتی آزمایشگاهی استفاده میشوند(13). از مجموع آن چه گفته شد برآن شدیم که برای اولین بار به ارزیابی اثر ترکیبی دو داروی آرسنیک تریاکساید وتالیدوماید به عنوان یک ترکیب جدید با خاصیت ضد سرطانی منحصر به فرد بر روی بیان ژن A VEGF و بررسی آپوپتوز در محیط آزمایشگاهی بر روی سل لاینهای مقاوم و حساس
به داروهای متداول شیمیدرمانی AML بپردازیم.
مواد و روشها
کشت سلولی:
مطالعه انجام شده از نوع تجربی بود. دو رده سلولی KG-1 و U937 در محیط RPMI1640 با 10% سرم گاوی (Fetal Bovin Serum) برای U937 و 20% سرم گاوی برای KG-1 ، همراه با U/mL ۱۰۰ پنیسیلین و μg/mL ۱۰۰ استرپتومایسین کشت و نگهداری میشود. سلولها در انکوباتور با دمای ۳۷ درجه سانتیگراد، رطوبت و ۵% دیاکسید کربن، انکوبه خواهند شد.
Microculture Tetrazolium Test (MTT) :
برای اندازهگیری اثر مهاری تالیدوماید(سانتاکروز) و آرسنیک تری اکساید(سینا دارو) برروی فعالیت متابولیکی سلولهایU937 و KG-1 به روش MTT Assay ]برای ساخت محلولMTT ، 5 میلی گرم پودر MTT را در 1 میلیلیتر محیط RPMI 1640 بدون FBS حل کرده (این پودر به سختی حل میشود) تا محلول mg/mL 5 ساخته شود. سپس با محیط RPMI آن را به حجم 10 میلیلیتر رسانده تا استوک mg/mL 5/0 ساخته شود(این محلول به صورت تازه استفاده میشود)[. در 24 ، 48 و 72 ساعت از پودرMTT (مشتق از نمکهای تیازول) و محلول DMSO (دیمتیل سولفواکساید) استفاده خواهد شد. محلول MTT (mg/mL 5/0) به مقدار 50 میکرولیتر به سلولها اضافه میشود و سلولها به مدت چهار ساعت در 37 درجه سانتیگراد انکوبه خواهند شد تا این محلول را متابولیزه کنند. رسوب فرمازان تشکیل شده با 100 میکرولیتر DMSO حل خواهد شد و محلول بنفش رنگی
ایجاد میشود. این مراحل باید به سرعت انجام گیرد(بین 1 تا 2 دقیقه بعد از ریختن محلول DMSO ، سلولها باید در دستگاه ELISA Reader قرار بگیرند) زیراDMSO در صورت تماس طولانی مدت با سلولها برای آنها سمی است و سپس جذب نوری با دستگاه الایزا ریدر در طول موج ۵۷۸ نانومتر خوانده خواهد شد. سلولها با غلظتهای µmol 100-5 تالیدوماید و µmol 5-4/0 آرسنیک به مدت 24 ، 48 و 72 ساعت تیمار میشوند.
سنجش میزان آپوپتوزسلولی به روش فلوسیتومتری:
بدین منظور 24 و 48 ساعت پس ازتیمار نمودن ردههای سلولی KG-1 و U937 توسط آرسنیک تریاکساید و تالیدوماید و نیز ترکیب آرسنیک تریاکساید با تالیدوماید که در پلیتهای 24 خانه کشت داده شده بودند، با استفاده از کیت رنگی دوگانه Annexin/PI سلولها جهت بررسی میزان آپوپتوز رنگآمیزی شدند.در این روش سلولهای تیمار شده با بافر شسته شد و سوسپانسیون سلولی تهیه گردید(106× 1 در هر میلیلیتر). ابتدا سلولها جمعآوری شده و با دور G 600 در دمای اتاق به مدت 5 دقیقه سانتریفوژ شدند. سلولها 1 بار توسط PBS 1X شسته شدند. به هر لوله ۱۰۰ میکرو لیتر از Binding buffer 1X که به آن ۱ میکرولیتر از رنگ آنکسین با غلظت استوک mg/mL ۵/۰ و µL۱ از PI با غلظت استوک mg/mL ۱/۰ اضافه شده بود، افزوده و لولهها به آرامی ورتکس شدند. لولهها به مدت 15-10 دقیقه در تاریکی و در دمای اتاق قرار داده شدند و سپس بلافاصله توسط فلوسیتومتری آنالیز شدند. نتایج دستگاه فلوسیتومتری توسط نرمافزار FlowJO باversion (7.6.1) تجزیه و تحلیل شدند.
جدول 1: توالی آغازگرهای جلوبرنده و معکوس
| ژن | آغازگر رفت(5¢-3¢) | آغازگر برگشت(5¢-3¢) | اندازه (bp) | منابع |
| HPRT | GCTATAAATTCTTTGCTGACCTGCTG | AATTACTTTTATGTCCCCTGTTGACTG | 26 | (13) |
| VEGF-A | AGGGCAGAATCATCACGAAGT | AGGGTCTCGATTGGATGGCA | 21 | (14) |
استخراج RNA ، ساخت cDNA و بررسی بیان ژن توسط Real Time quantitative PCR :
برای استخراج RNA سلولها TriPure (رُوش) مورد استفاده قرار گرفت.
برای اندازه گیری غلظت RNA نمونهها از دستگاه نانو دراپ(آلمان، NanoDrop) استفاده گردید. با استفاده از کیت cDNA سنتاز (Takara Bio) از RNAها ، cDNA ساخته شد و تغییرات در سطح mRNA به روش Real-time PCR انجام شد. روش Real-time PCR با دستگاه light cycler instrument (دیاگنوستیک، رُوش، آلمان) انجام شد. برای انجام PCR برای هر نمونه مقدار 10 میکرو لیترSYBR Green master mix ، 2 میکرولیتر cDNA ، 1 میکرولیتر آغازگر معکوس و1 میکرولیتر آغازگر جلوبرنده(10 پیکومول) و 6 میکرولیتر آب با هم ادغام گردید(جدول 1).
برنامه دمایی PCR برای مرحله فعالسازی اولیه در 95 درجه سانتیگراد به مدت 30 ثانیه، مرحله دناتوراسیون در 95 درجه سانتیگراد به مدت 5 ثانیه و برای مرحله آنیلینگ/اکستنشن در 60 درجه سانتیگراد به مدت20 ثانیه و تعداد چرخههای دمایی 40 بار خواهد بود.
به منظور تکثیر هر قطعهی ژنی، یک جفت آغازگر اختصاصی برای هر ژن انتخاب شد که شامل آغازگر جلوبرنده و معکوس بود. اختصاصیت تمامی آغازگرها با نرمافزار آنلاین Primer-BLAST (وب سایتNCBI) تأیید شده است.
یافتهها
بررسیهای MTT در رده سلولی KG-1 :
نتایج حاکی از آن است که در رده سلولی KG-1 اثر آرسنیک تریاکساید در دوزهای ۶۱۸/۱ (اگر چه مقدار دوز آرسنیک تریاکساید در رده سلولی KG-1 یک مقدار عددی میباشد و یک نسبت نیست؛ با این وجود این دوز نتایج مؤثرتری نسبت به دوزهای بالا و پایینتر خود نشان داده است. اخیراً استفاده از این نسبت در پروژههای مربوط بهDrug discovery بررسی شده است) تا ۵ میکرومولار و اثر تالیدوماید در دوزهای ۶۰ تا ۱۰۰ میکرومول قابل توجه بوده است(نمودار 1)(14). هم چنین اثر ترکیبی این دو دارو نشان میدهد ۶۱۸/۱ میکرومولار آرسنیک تریاکساید و۸۰ میکرومولار تالیدوماید میتوانند کشندگی بیشتری به دنبال داشته باشند(نمودار 1).
بررسیهای MTT در رده سلولی U937 :
نتایج حاکی از آن است که در رده سلولی U937 اثر آرسنیک تریاکساید در دوزهای ۱ تا ۵ میکرومولار و اثر تالیدوماید در دوزهای ۶۰ تا ۱۰۰ میکرومولار قابل توجه بوده است(نمودار 2). هم چنین اثر ترکیبی این دو دارو نشان میدهد ۱ میکرومولار آرسنیک تریاکساید و۶۰ میکرومولار تالیدوماید میتوانند کشندگی بیشتری به دنبال داشته باشند(نمودار 2).
همان طور که نتایج نمودارهای فوق نشان میدهد درصد بقای سلولهای تیمار شده با آرسنیک تریاکساید و تالیدوماید در یک روند وابسته به دوز و زمان نسبت به گروه کنترل کاهش مییابد.
در ادامه جهت تایید نتایج بقا حاصل از آزمایش MTT، به منظور ارزیابی اثر القایی آرسنیک تریاکساید به تنهایی یا در ترکیب با تالیدوماید بر فعالیت کشندگی و مهار رشد سلولی و مشخص شدن این که این اثر با واسطه آپوپتوز و یا با واسطه نکروز سلولی است، رنگآمیزی Annexin/PI انجام شد و درصد سلولهای آپوپتوتیک تعیین گردید. نتایج Annexin/PI مؤید این مسئله است که آرسنیک تریاکساید و تالیدوماید دارای اثرات کشندگی در هر دو رده سلولی در یک روند وابسته به دوز است.
بررسیها به منظور تعیین اثرات تیمار هم زمان ترکیبی آرسنیک تریاکساید و تالیدوماید بر بقا و رشد دو رده سلولی KG-1 و U937 در یک بازه زمانی 48 ساعتی صورت گرفت.
در این آزمایش تنها جمعیتهایی که Annexin+ و یا Annexin+/PI+ باشند حائز اهمیت بوده و جمعیتهای PI+ به تنهایی حاکی از نکروز سلولی بوده که فاقد اهمیت میباشند(شکلهای 1 و 2).

نمودار 1 : A) نمودار ستونی اثر مهاری غلظتهای مختلف(µM 5-4/0) آرسنیک تریاکساید بر رشد سلولها و بقا. B : نمودار ستونی اثر مهاری غلظتهای مختلف(µM 100- 5) تالیدوماید بر رشد سلولها و بقا. C : نمودار ستونی اثر مهاری غلظتهای مختلف آرسنیک تریاکساید و تالیدوماید و همچنین اثر ترکیبی آنها بر رشد سلولها و بقا. رده سلولی KG-1 در بازه زمانی 24، 48 و 72 ساعت با استفاده از روش MTT .
با سه بار تکرار به صورت SD±mean نمایش داده شده و تفاوت آماری معنادار در مقایسه با گروه کنترل به صورت 05/0 p< * و 01/0 p< ** تعریف شده است.

نمودار 2 : A) نمودار ستونی اثر مهاری غلظتهای مختلف(µM 4-5/0) آرسنیک تریاکساید بر رشد سلولها و بقا. B) نمودار ستونی اثر مهاری غلظتهای مختلف(µM 100- 5) تالیدوماید بر رشد سلولها و بقا. C) نمودار ستونی اثر مهاری غلظتهای مختلف آرسنیک تریاکساید و تالیدوماید و هم چنین اثر ترکیبی آنها بر رشد سلولها و بقا. رده سلولی U937 در بازه زمانی24، 48 و 72 ساعت با استفاده از روش MTT . با سه بار تکرار به صورت mean ± SD نمایش داده شده و تفاوت آماری معنادار در مقایسه با گروه کنترل به صورت 05/0 p< *، 01/0 p< ** و 001/0 p< *** تعریف شده است.

شکل 1: بررسی آپوپتوز با داروهای آرسنیک تریاکساید و تالیدوماید بر روی KG-1

شکل 2: بررسی آپوپتوز با داروهای آرسنیک تریاکساید و تالیدوماید بر روی U937

نمودار 3 : نتایج بررسی آپوپتوز سلولی حاصل از رنگ آمیزی Annexin/PI در رده سلولی KG-1 در بازه زمانی 48 ساعت به دنبال تیمارسازی با غلظتهای(µM۶۱۸/۱) آرسنیک تریاکساید و غلظت(Mµ 60 و80) تالیدوماید و مقادیر ترکیبی آنها را نشان میدهد.

نمودار 4: نتایج بررسی آپوپتوز سلولی حاصل از رنگآمیزی Annexin/PI در رده سلولی U937 در بازه زمانی 48 ساعت به دنبال تیمارسازی با غلظتهای (µM 1) آرسنیک تریاکساید و غلظت(µM 60 و80) تالیدوماید و مقادیر ترکیبی آنها را نشان میدهد.

نمودار 5: نتایج تیمار سلولها با آرسنیک تریاکساید(µM ۶۱۸/۱) و تالیدوماید(µM 60 و80) و ترکیب آرسنیک و تالیدوماید بر روی بیان VEGF A. در یک بازه زمانی 48 ساعتی. نمونهها با سه بار تکرار به صورت SD ± mean نمایش داده شدهاند و تفاوت آماری معنادار در مقایسه با گروه کنترل به صورت 05/0 p< * ، 01/0 p< ** و 001/0 p< *** تعریف شده است.

نمودار 6 : نتایج تیمار سلولها با آرسنیک تریاکساید(µM 1) و تالیدومایدµM) ۶۰ و۸۰) و ترکیب آرسنیک و تالیدوماید بر روی بیان VEGF A. در یک بازه زمانی 48 ساعته. نمونهها با سه بار تکرار به صورت SD ± mean نمایش داده شدهاند و تفاوت آماری معنادار در مقایسه با گروه کنترل به صورت 05/0 p< * ، 01/0 p<** و 001/0 p< *** تعریف شده است.
نتایج برسی Annexin/PI در رده سلولی KG-1 و :U937
نتایج نشان داد که سلولهای KG-1 و U937 تیمار شده با دوزهای ترکیبی آرسنیک تریاکساید و تالیدوماید، یک افزایش آپوپتوتیک قابل توجهی را نسبت به دوزهای آرسنیک تری اکساید و تالیدوماید به تنهایی، نشان میدهد(نمودارهای 3 و 4).
نتایج بررسی اثر آرسنیک تریاکساید و تالیدوماید بر روی بیـان ژن A VEGF در سطـح mRNA در ردهی سلولی KG-1 :
نتایج بررسی میزان بیان ژن VEGF A در رده سلولی KG-1 نشان میدهد میزان بیان در دوزهای ۶۰ و۸۰ میکرومولار تالیدوماید کاهشی و در دوز ۶۱۸/۱ آرسنیک تریاکساید افزایشی بوده و هم چنین اثر ترکیبی این دو دارو میزان بیان را به نسبت کنترل کاهش میدهد، این کاهش بیان در دوز ۸۰ میکرومولار تالیدوماید و ۶۱۸/۱ آرسنیـک تـریاکساید بیشتر نشان داده شده است (نمودار
5).
نتایج بررسی اثر آرسنیک تریاکساید و تالیدوماید بر روی بیان ژن A VEGFدر سطح mRNA در ردهی سلولیU937:
نتایج بررسی میزان بیان ژن VEGF A در رده سلولی U937 نشان میدهد میزان بیان در دوزهای ۶۰ و۸۰ میکرومولار تالیدوماید کاهشی بوده و در دوز ۱ میکرومولار آرسنیک تریاکساید نیز کاهشی بوده و هم چنین اثر ترکیبی این دو دارو میزان بیان را به نسبت کنترل کاهش میدهد، این کاهش بیان در دوز ۶۰ میکرومولار تالیدوماید و ۱ آرسنیک تری اکساید بیشتر نشان داده شده است(نمودار 6).
بحث
لوسمی میلوئیدی حاد یکی از شایعترین اختلالات هماتولوژیک است. اگر چه بیش از 80 درصد بیماران مبتلا به AML با داروهای رایج امروزی به مرحله خاموشی کامل میرسند، ولی میزان بقای 5 ساله تنها بین 40 -50 درصد میباشد و شانس بقای طولانی مدت بسیار پائین است، که این خود حاکی از ناکارآمد بودن درمانهای رایج میباشد(15). داروها با اساس آرسنیک به عنوان عوامل شیمیدرمانی مؤثر برای درمان بیماریهای مختلف و برخی از تومورها استفاده شده است(14). در مطالعهها نشان داده شده که این ترکیب سبب توقف چرخه سلولی و القای آپوپتوز درسلولهای APL وnon-APL میشود. بنابراین تصمیم گرفتیم برای اولین بار به ارزیابی اثر ترکیبی تالیدوماید و آرسنیک تریاکساید بر روی بیان ژن VEGF A در سللاینهای U937 و KG-1 بپردازیم.
در این مطالعه ارزیابی اولیه توسط MTT به منظور تعیین اثرات توکسیک آرسنیک تریاکساید و تالیدوماید در بازه زمانی مختلف در دو ردهی سلولی KG-1 و U937 صورت گرفت. دوز انتخابی توسط این آزمایش ۶۱۸/۱ میکرومولار برای آرسنیک تریاکساید و ۶۰ و۸۰ میکرو مولار بـرای تالیدومایـد و هم چنیـن دوز ترکیبی(µMT80 µMA- ۶۱۸/۱) برای ردهی سلولی KG-1 در نظر گرفته شد. هم چنین دوزهای انتخابی توسط آزمایش µM 1 برای آرسنیک تریاکساید و µM 60 و80 برای تالیدوماید در رده سلولی U937 در نظر گرفته شد. هم چنین دوز ترکیبی) µM T۶0µM A - ۱) برای ردهی سلولی U937 در نظر گرفته شد. برای تعیین میزان آپوپتوز و نکروز توسط این دوزها، آزمایش فلوسایتومتری انجام شد. نتایج حاکی از آن بود که این دوزهای آرسنیک و تالیدوماید و اثر ترکیبی آنها قادر به القای درصد قابل توجهی از آپوپتوز میباشد. علاوه بر آن که مطالعههای گذشته بیانگر آن هستند که دوز استاندارد برای القای آپوپتوز توسط آرسنیک تریاکساید در محدوده غلظتی 2-5/0 میکرو مولار است. بنابراین دوزهای اصلی برای این مطالعه برای آرسنیک ۶۱۸/۱ میکرومولار و ۱ میکرومولار به ترتیب در رده سلولی KG-1 وU937 انتخاب شد. بر اساس نتایج حاضر، آرسنیک تریاکساید و تالیدوماید در مهار رشد و القای آپوپتوز در رده سلولی KG-1 و U937 به صورت وابسته به دوز و زمان عمل کرده است.
در مطالعهها مشخص شده است که VEGF (VEGF A) فاکتور رشد اختصاصی برای آنژیوژنز میباشد. VEGF ترشح شده توسط سلول لوسمی با گیرندههای مربوطه در سطح سلولهای اندوتلیال در ارتباط است و سلولهای اندوتلیال را برای تولید فاکتورهای رشد که بر روی سلولهای لوسمیک قرار دارند؛ تحریک میکند در نتیجه فعالیت تکثیری و مقاومت دارویی افزایش مییابد(16). بنابراین درمان ضد آنژیوژنز بر اساس مهار فعالیت فیزیولوژیکی VEGF یک استراتژی جدید برای درمان هدفمند است. در مطالعههای اخیر بیان VEGF و VEGF-R در بیماران AML مشاهده شده است.
آرسنیک تریاکساید به عنوان یک داروی چند هدفی(Multi target) شناخته شده است. آرسنیک تریاکساید قادر به فعال کردن JNKs میباشد. JNKs یک پروتئین کیناز فعال شده میتوژنی است که با فعال کردن ROS و به دنبال آن فعال شدن Cyt P450 و P38 MAPK منجر به القای آپوپتوز و هم چنین باعث مهار مسیر PI3K-Akt-mTOR شده و از سوی دیگر، JNKs سبب افزایش بیان PTEN که یک سرکوبگر تومور است؛ میشود که منجر به مهار PI3K-Akt-mTOR خواهد شد. از آن جایی که مسیر PI3K-Akt-mTOR مسیر حفظ حیات سلول شناخته میشود؛ مهار این مسیر میتواند مرگ سلولی را افزایش دهد. هم چنین در مطالعههای گذشته نشان دادهاند که آرسنیک تریاکساید باعث فعال شدن سیتوکروم C و فعال شدن مسیر آبشاری کاسپازها و درنهایت آپوپتوز میشود(17).
تالیدوماید با اثر بر روی ژنهای مسیر رگزایی میتواند از توسعه سرطان پیشگیری کند. تالیدوماید اثر مهاری خود را بر روی رگزایی توسط مهار β-FGF در rabbit cornea و توسط مهار VEGF در murine model نشان داد(19، 18).
تالیدوماید به علت ویژگی ضد رگزایی خود روی
چندین نوع از تومورها تحت ارزیابی قرار گرفته است، مثل بدخیمیهای هماتولوژیک، میلوم مالتیپل و تومورهای جامد. در این مطالعهها نشان داده شده است که تالیدوماید موجب کاهش بیان عوامل مؤثر در رگزایی میشود(24-20).
استینز و همکاران در سال ۲۰۰۲ در مطالعه خود نتایج مشابهی را گزارش کردند که تالیدوماید با پایین آوردن سطح FGF-2 و VEGF باعث آنتی آنژیوژنز میشوند(25).
روبوز در سال 2000 نشان داد که آرسنیک تریاکساید با مهار VEGF منجر به القای آپوپتوز در لوسمی میشود. هم چنین آنها نشان دادند که این دارو PML/RAR-α را تخریب میکند(18).
چن و همکارانش با بررسیهایی بر روی NB4 و آرسنیک تریاکساید افزایش آپوپتوز را به واسطه کنترل کردن bcl-2 و PML/RAR-α نشان دادند(26).
یانگ و همکارانش در مطالعهای بر روی سرطان ریه در سال 2014 نشان دادند که آرسنیک تریاکساید با مهار فاکتورهایی از قبیل VEGF-A، VEGFR-2، HIF-1α و Notch-1 مسیر آنژیوژنز را مهار میکند(27).
نتیجهگیری
اثر ترکیبی این دارو سبب افزایش آپوپتوز سلولی و کاهش میزان بیان ژن اصلی در رگزایی (VEGF A) میشود. با توجه به نتایج حاصل از این مطالعه و نتایج مطالعههای گذشته این دو دارو به صورت ترکیبی میتوانند اثرات مؤثری در درمان سرطان خون ایفا کنند.
تشکر و قدردانی
ﺑﺪﻳﻦ ﻭﺳﻴﻠﻪ ﺍﺯ ﻣﺮﮐﺰ تحقیقات هماتولوژی، آنکولوژی و پیوند مغز استخوان بیمارستان شریعتی ﺑﻪ ﺧﺎﻃر ﺗـﺎﻣﻴﻦ ﺑﻮﺩﺟـﻪ ﻃـﺮﺡ ﻗـﺪﺭﺩﺍﻧﻲ ﻣﻲﮔﺮﺩﺩ.
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |






